Рак желчного пузыря (РЖП) — злокачественная опухоль, исходящая из эпителия желчного пузыря, характеризующаяся местной и сосудистой инвазией, обширным регионарным лимфогенным и гематогенным метастазированием[1]. РЖП встречается достаточно редко, но среди всех видов рака желчевыводящих путей эта злокачественная опухоль является самой распространенной[2]. Данное новообразование отличается высокой злокачественностью с 5-летней выживаемостью < 10%[3].
Бессимптомный характер начального развития РЖП, нечетко выраженная клиническая симптоматика, анатомическая особенность желчного пузыря в виде отсутствующей серозной оболочки и склонность к раннему и быстрому метастатическому распространению приводят к поздней диагностике большинства случаев РЖП и неблагоприятному прогнозу заболевания[4]. Актуальность проблемы связана еще и с тем, что в международных рекомендациях РЖП рассматривается как естественная стадия течения билиарной патологии: дискинезия — холецистит — желчнокаменная болезнь (ЖКБ) — РЖП[5].
ЗАБОЛЕВАЕМОСТЬ И ФАКТОРЫ РИСКА РАКА ЖЕЛЧНОГО ПУЗЫРЯ
Точные данные о заболеваемости РЖП во всем мире трудно получить из-за проблематичности его своевременного выявления, а также в связи с тем, что в структуре заболеваемости и смертности его часто оценивают совместно с другими видами билиарного рака — внутрипеченочной холангиокарциномой и ампулярным раком внепеченочных желчных протоков.
Необходимо подчеркнуть, что в глобальном масштабе эпидемиологические тенденции заболеваемости РЖП существенно различаются в разных географических регионах в зависимости от этнической принадлежности, степени экономического развития, образа жизни и различных социальных факторов. Так, по данным из 290 онкологических регистров, охватывающих 424 группы населения в 6 странах на пяти континентах за период с 2003 по 2007 г., наиболее значительные показатели заболеваемости РЖП регистрируются в Азии, Индии, среди коренного населения Америки[6] и в Корее[7]. Самая высокая частота РЖП с поправкой на возраст наблюдается в Чили (27/100 000), где это заболевание является четвертой по распространенности причиной смерти от рака. За Чили следуют северная Индия (21,5/100 000)[8], Польша (14/100 000)[9] и Корея (14/100 000)[7], южный Пакистан (11,3/100 000)[10], Япония (7/100 000) и Израиль (5/100 000)[9].
В России, по данным Федеральной службы государственной статистики (Росстат, 2020 г.), заболеваемость РЖП в 2019 г. составила среди мужчин 1,4 на 100 000 мужского, а среди женщин — 2,5 на 100 000 женского населения1.
РЖП — один из немногих типов рака, которые ассоциируются с гендерной принадлежностью: у женщин РЖП может встречаться в среднем в 3 раза чаще, чем у мужчин, в зависимости от региона и численности населения, особенно в возрасте 70–80 лет. Так, соотношение женщины/мужчины варьирует от 1/1–2/1 в Восточной Азии до 5/1 и более в Испании и Колумбии[10]. В Китае среди пациентов с РЖП 73% составляют женщины[11]. В северной Индии, согласно данным ракового регистра, заболеваемость РЖП — 4,5/100 000 у мужчин и 10,1/100 000 у женщин[12].
Тенденция к увеличению частоты РЖП с возрастом также является общей для всех популяций. Более двух третей больных, у которых диагностирован РЖП, старше 65 лет, при этом средний возраст установления диагноза составляет 72 года[12]. Так, в России, по данным за 2019 г., средний возраст заболевших мужчин — 66 лет, женщин — 70,1 года2.
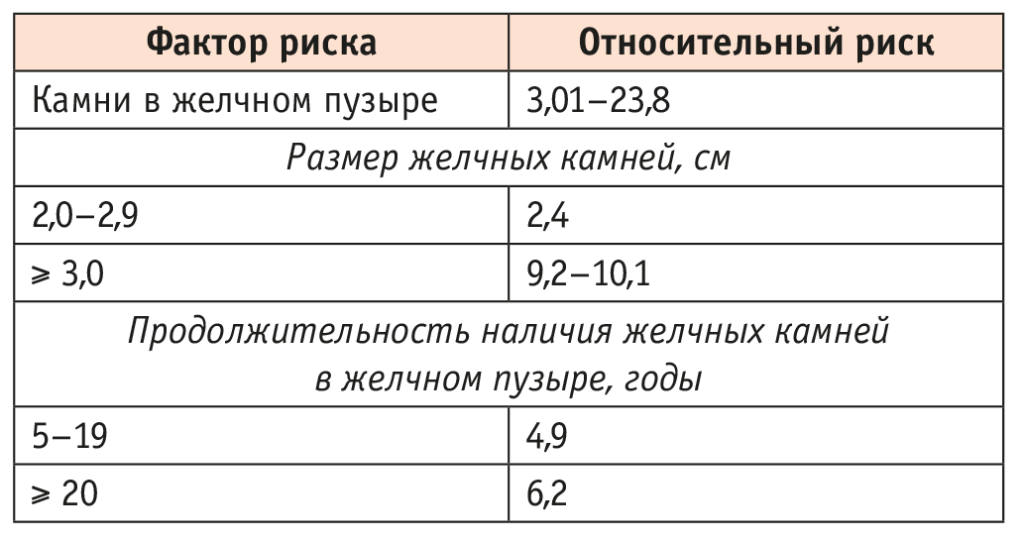
Роль ЖКБ в развитии РЖП определяется в качестве одного из пяти наиболее значимых факторов риска. Относительный риск РЖП при ЖКБ может достигать 23,8 в зависимости от размера камней, их вида и продолжительности течения холелитиаза (табл.)[13].
Таблица. Факторы риска рака желчного пузыря[13]
При этом надо отметить, что остальные четыре ведущих фактора риска РЖП — этническая принадлежность, генетическая предрасположенность, факторы образа жизни (избыточная масса) и инфекции желчевыводящих путей[10] — являются общими и для пациентов с ЖКБ[14]. Так, у лиц с избыточной массой и индексом массы тела 30,0–34,9 кг/м2 риск РЖП повышен до 1,8 у мужчин и до 2,3 у женщин[15], а инфицирование желчевыводящих путей, например Helicobacter bilis, увеличивает его до 2,6–6,5[16].
ПАТОГЕНЕЗ РАКА ЖЕЛЧНОГО ПУЗЫРЯ
Канцерогенные механизмы при РЖП изучены недостаточно, но сейчас решающее значение придается длительным воспалительным изменениям в эпителии вследствие механической травматизации слизистой оболочки желчного пузыря конкрементами[4]. Предполагается, что пролонгированное повреждение эпителиоцитов наряду с вероятным увеличением доли вторичных желчных кислот в желчи обладают мутагенным потенциалом[17], стимулируют развитие дисплазии и формирование злокачественных изменений[13].
ДИАГНОСТИКА РАКА ЖЕЛЧНОГО ПУЗЫРЯ
Современные Доказательные клинические рекомендации по ведению больных с раком желчевыводящих путей, опубликованные в 2021 г., были созданы Японским обществом гепато-билиарно-панкреатической хирургии. Мы сочли необходимым представить ниже резюме некоторых рекомендаций из этого руководства[18].
Необходима ли профилактическая холецистэктомия при бессимптомных камнях в желчном пузыре? Профилактическая холецистэктомия (ХЭ) не рекомендуется в принципе (степень 2, уровень доказательности C).
Симптомы. Типичные симптомы, указывающие на РЖП, — боли в верхней правой области живота, желтуха, тошнота, рвота и потеря массы. У значительного числа пациентов рак обнаруживают случайно при ультразвуковом исследовании (УЗИ) органов брюшной полости или во время ХЭ по поводу ЖКБ.
Первый шаг диагностики. Первый этап диагностики — проведение исследования крови (биохимия) и УЗИ. УЗИ обладает высокими специфичностью и чувствительностью и должно быть выполнено в качестве первого шага у пациентов с подозрением на рак желчевыводящих путей. Это достаточно эффективно для выявления РЖП.
Второй и третий шаги. В качестве второго шага в диагностике РЖП полезна компьютерная томография (КТ) для оценки локализации и распространения опухоли. Необходима многофазная усиленная КТ. Однако чувствительность КТ-исследования при опухолях Т1 относительно низкая. Магнитно-резонансная томография, включая магнитно-резонансную холангиопанкреатографию, также помогает оценить распространение опухоли на пузырный проток и общий желчный проток.
В качестве третьего шага для обнаружения утолщенной части желчного пузыря более полезно эндоскопическое УЗИ, обладающее более высокими чувствительностью, специфичностью и точностью, чем УЗИ брюшной полости и КТ. Эндоскопическое УЗИ повышает качество диагностики, позволяя точнее определить местоположение и степень вертикального распространения опухоли. Прямая холангиография: эндоскопическая ретроградная холангиопанкреатография и наблюдение с помощью пероральной холангиоскопии помогают оценить распространение опухоли на пузырный проток и общий желчный проток. Позитронная эмиссионная томография и позитронная эмиссионная КТ полезны для обнаружения лимфатических узлов, отдаленных метастазов и рецидивов.
Поскольку важным предиктором РЖП являются полипы желчного пузыря, мы сочли возможным представить в рамках данной статьи современные рекомендации по ведению пациентов с полипозом желчного пузыря, разработанные коллегиально Европейским обществом желудочно-кишечной и абдоминальной радиологии (European Society of Gastrointestinal and Abdominal Radiology), Европейской ассоциацией эндоскопической хирургии и других интервенционных методов (European Association of Endoscopic Surgery), Международным обществом пищеварения Европейской федерации хирургии (European Federation International Society for Digestive Surgery) и Европейского общества эндоскопистов по желудочно-кишечным заболеваниям (European Society of Gastrointestinal Endoscopy), опубликованные в 2022 г., которые обновляют европейские рекомендации от 2017 г.[19].
Основные рекомендации European Society of Gastrointestinal and Abdominal Radiology, European Association of Endoscopic Surgery, European Federation International Society for Digestive Surgery, European Society of Gastrointestinal Endoscopy по ведению пациентов с полипозом желчного пузыря[19]
1. Первичное исследование полипозных поражений желчного пузыря должно проводиться с помощью УЗИ органов брюшной полости. Рутинное использование других методов визуализации в настоящее время не рекомендуется. В центрах с соответствующим опытом и ресурсами альтернативные методы визуализации (например, контрастное и эндоскопическое УЗИ) могут быть полезны для облегчения принятия решений в сложных случаях (сильная рекомендация, низкое-среднее качество доказательств).
2. ХЭ рекомендуется больным с полиповидным поражением желчного пузыря размером 10 мм или более при условии, что пациент не имеет соматических противопоказаний к операции и согласен на нее. Междисциплинарное обсуждение можно провести для оценки предполагаемого индивидуального риска малигнизации (сильная рекомендация, низкое качество доказательств).
3. ХЭ показана больным с полиповидным поражением и клинической симптоматикой, потенциально связанной с желчным пузырем, если не выявлена никакая другая ее причина, в случае, если симптомы у пациента ярко выражены, пациент не имеет соматических противопоказаний к операции и согласен на нее. Больной должен быть проинформирован о пользе ХЭ и о риске, которому он подвергнется, продолжая жить с сохраняющимися стойкими симптомами (сильная рекомендация, доказательства низкого качества).
4. При наличии у больного полипозного поражения желчного пузыря диаметром 6–9 мм и одного или нескольких факторов риска злокачественных новообразований ХЭ также рекомендуется, если пациент подходит для операции и соглашается на нее. Эти факторы риска следующие: возраст старше 60 лет, наличие в анамнезе первичного склерозирующего холангита, азиатская этническая принадлежность, полиповидное поражение на широком основании (в том числе очаговое утолщение стенки желчного пузыря > 4 мм) (сильная рекомендация, доказательства низкого-умеренного качества).
5. Если у больного полиповидное образование желчного пузыря диаметром 6–9 мм и нет факторов риска малигнизации либо если у него есть факторы риска малигнизации, но диаметр полипозного поражения желчного пузыря 5 мм и менее, рекомендуется контрольное УЗИ желчного пузыря через 6 мес., 1 и 2 года. Последующее наблюдение следует прекратить через 2 года при отсутствии роста полипа (рекомендация средней силы, доказательства среднего качества).
6. Если у пациента нет факторов риска злокачественного новообразования и имеется полиповидное поражение желчного пузыря размером 5 мм и менее, последующее наблюдение не требуется (сильная рекомендация, доказательства среднего качества).
7. Если за время наблюдения полиповидное образование желчного пузыря разрастается до 10 мм, то рекомендуется ХЭ. Если полиповидное поражение вырастает на 2 мм или более в течение 2-летнего периода наблюдения, следует учитывать текущий размер полиповидного поражения наряду с факторами риска у пациента. Междисциплинарное обсуждение может быть проведено для принятия решения о необходимости продолжения наблюдения или ХЭ (рекомендация средней силы, доказательства среднего качества).
ЗАКЛЮЧЕНИЕ
Мы обращаем внимание практических врачей на то, что РЖП в настоящее время рассматривается как возможная и естественная стадия течения холелитиаза. Риск возникновения РЖП значительно возрастает у пациентов с размерами камней больше 2 см и длительностью патологии больше 5 лет. Другой существенный фактор риска РЖП — полипы желчного пузыря. Больных с размерами полипов от 6 до 9 мм необходимо тщательно обследовать для определения тактики лечения. Больным с полипом желчного пузыря более 10 мм рекомендуется ХЭ.
С учетом вышесказанного диагностика возможных осложнений у пожилых пациентов с холециститом, ЖКБ должна включать тщательное клиническое, лабораторное и инструментальное обследование. Среди профилактических мероприятий у лиц с факторами риска РЖП должны быть оптимизация диеты, снижение массы тела, по возможности усиление двигательной активности. Прием препаратов урсодезоксихолевой кислоты способствует снижению содержания гидрофобных желчных кислот в желчи и уменьшает вероятность осложнений билиарной патологии[20].
Поступила: 11.01.2024
Принята к публикации: 19.02.2024
________
1 Смелов П.А., Глотко О.Л., Иванова А.М., Игнатова Н.В. и др. Женщины и мужчины России. 2020. М.: Росстат; 2020. 239 с.
2 Там же.








