ВВЕДЕНИЕ
Послеродовое кровотечение (ПРК) продолжает оставаться одной из основных причин материнской заболеваемости и смертности[1]. В то же время большая часть случаев материнской смертности, обусловленных кровотечением, предотвратима[2].
Проблема ПРК представляется хорошо изученной. Четко определено понятие ПРК, под которым понимают кровопотерю ≥ 500 мл во время родов через естественные родовые пути (вагинальные роды — ВР) и ≥ 1000 мл при операции кесарева сечения (КС) или любой клинически значимый объем кровопотери, возникающий на протяжении 42 дней после родов. Принято разделять раннее (первичное) ПРК, возникшее в течение ≤ 24 ч после родов и позднее (вторичное) ПРК, возникшее > 24 ч и ≤ 42 дней послеродового периода[3–5].
Определены и сгруппированы основные причины ранних ПРК — правило «4Т»: нарушение сокращения матки (tonus) обусловливает 70% случаев ПРК, задержка частей плаценты в полости матки (tissue) — 20%, травма родовых путей, разрыв матки (trauma) — 10%, нарушения свертывающей системы крови (thrombin) — 1%[2]. Основными причинами поздних ПРК являются остатки плацентарной ткани, субинволюция матки, послеродовая инфекция, наследственные дефекты гемостаза[2].
Разработан алгоритм действий при раннем ПРК, в основе которого — организация помощи по принципу работы мультидисциплинарной бригады с четким распределением обязанностей[6]. Основным методом терапии ПР является утеротоническая терапия[7, 8]. Утеротоники применяются как самостоятельный метод, так и в комбинации с компрессионным швом[9] или управляемой баллонной тампонадой матки (УБТ)[10–12].
Общепризнанными факторами риска ПРК являются анемия, преэклампсия, многоплодная беременность, многоводие, хориоамнионит, индуцированные или усиленные роды, затянувшийся второй период родов, пролонгирование третьего периода родов, предыдущие роды путем КС[13–15]. Однако практика показывает, что значительная часть пациенток с акушерскими кровотечениями не имеет факторов риска. Поэтому разработка алгоритма прогнозирования ПРК на основе клинико-анамнестических и лабораторных исследований, рутинно применяющихся в клинической практике, остается актуальной.
Цель исследования — оценить частоту послеродовых кровотечений в стационаре III группы и провести сравнительную оценку клинико-анамнестических и лабораторных особенностей пациенток, перенесших ПРК, и эффективность локального алгоритма действия при послеродовых кровотечениях после ВР и КС.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено ретроспективное сплошное исследование. Исследование одобрено этическим комитетом ГБОУ ВО «Кемеровский государственный медицинский университет» МЗ РФ (протокол №309/к от 14.06.2023). Частота ПРК оценивалась у 15 480 пациенток, родоразрешенных в 2019–2022 гг. в Перинатальном центре Кузбасской областной клинической больницы им. С.В. Беляева. Критерием включения в исследование было наличие раннего ПРК после вагинальных или абдоминальных родов. Диагноз ПРК устанавливался при наличии кровопотери 500 мл и более при вагинальных родах или 1000 мл и более при КС или при любом другом клинически значимом объеме кровопотери, возникшей после рождения плода за 24 ч после родов. Критерием невключения в исследование было позднее (вторичное) ПРК, возникшее позже 24 ч послеродового периода.
Локальный алгоритм действия при ПРК после ВР включал внутривенное введение утеротонического препарата окситоцина 10 МЕ при помощи инфузомата со скоростью 125 мл/мин; проведение УБТ с установкой двухбаллонного внутриматочного и влагалищного катетеров Жуковского; лапаротомию, двустороннюю перевязку маточных сосудов, наложение двустороннего кисетного шва в нижнем маточном сегменте (патент на изобретение № 2797734, дата регистрации 08.06.2023)[16].
Локальный алгоритм действия при КС включал внутривенное введение утеротонического препарата окситоцина 10 МЕ при помощи инфузомата со скоростью 125 мл/мин; проведение УБТ с установкой двухбаллонного внутриматочного и влагалищного катетеров Жуковского; наложение двустороннего кисетного шва в нижнем маточном сегменте (патент на изобретение № 2797734, дата регистрации 08.06.2023)[16], ректальное введение 800 мкг мизопростола; введение в мышцу матки в место разреза терлипрессина в дозе до 0,4 мг, разведенных до 10 мл 0,9% раствором NaCl; двустороннюю перевязку маточных сосудов.
Анамнестические сведения, данные об объеме кровопотери, мероприятиях для остановки ПРК, длительности пребывания в отделении реанимации и интенсивной терапии и послеродовом отделении, а также лабораторных показателях были получены путем выкопировки из историй родов. Уровень гемоглобина, тромбоцитов и гематокрит определяли на гематологическом анализаторе Mindray BC-6800 Рlus на основе технологии SF Cube, уровень фибриногена и активированного частичного тромбопластинового времени — на автоматическом анализаторе гемостаза SYSMEX CS-1600 на основе технологии мультиволнового анализа. Объем кровопотери оценивали гравиметрическим методом путем взвешивания перевязочного материала и использования градуированных емкостей.
Статистическую обработку результатов проводили с использованием лицензионного пакета программ Statistica 6.1 (StatSoft; лицензия № ВХХR006BO92218 FAN11) с определением средней арифметической величин (М), ошибки средней величины (m), относительных (%) величин, p-критерия, критерия соответствия χ2.
РЕЗУЛЬТАТЫ
За 2019–2022 гг. в Перинатальном центре КОКБ им. С.В. Беляева родоразрешены 15 480 пациенток, через естественные родовые пути — 9708 (62,7%), путем операции КС — 5772 (37,3%). У 104 (0,67%) пациенток было диагностировано раннее ПРК, в том числе у 63 (0,65%) женщин — после ВР и у 41 (0,71%) — после операции КС.
Средний возраст менархе пациенток с ПРК составил 13,11 ± 1,20 года, продолжительность менструального цикла — 29,49 ± 3,73 дней, продолжительность менструации — 4,89 ± 0,82 дня.
У большинства пациенток настоящая беременность была повторной. Число беременностей у каждой женщины составило 1,96 ± 2,25, число родов — 1,26 ± 1,68. Почти у каждой пятой — 19 (18,3%) в анамнезе было КС. Кровотечение при предыдущих родах имели 6 (5,8%) женщин.
Гинекологические заболевания (миома матки, эндометриоз, гиперпластические процессы эндометрия) зарегистрированы у 12 (11,5%) пациенток. Сопутствующие экстрагенитальные заболевания встречались более чем у половины исследуемых — у 62 (59,6%). В структуре экстрагенитальных заболеваний доминировали сердечно-сосудистые заболевания — 29 (27,9%), анемия — 26 (25,0%), сахарный диабет — 20 (19,3%), другие заболевания эндокринной системы — 23 (22,1%), заболевания мочевыводящих путей — 11 (10,6%), желудочно-кишечного тракта — 8 (7,7%), органов дыхания — 6 (5,8%), 3 (2,9%) пациентки имели ВИЧ. Каждая четвертая пациентка — 28 (26,9%) имела избыточную массу тела, каждая десятая — 14 (13,5%) страдала ожирением. Нормальную массу тела имели 58 (55,8%) исследуемых, а 4 (3,8%) женщины страдали дефицитом массы тела. Наиболее значимые факторы риска ПРК представлены на рис. 1.
Рис. 1. Частота наиболее значимых факторов риска у женщин с ПРК
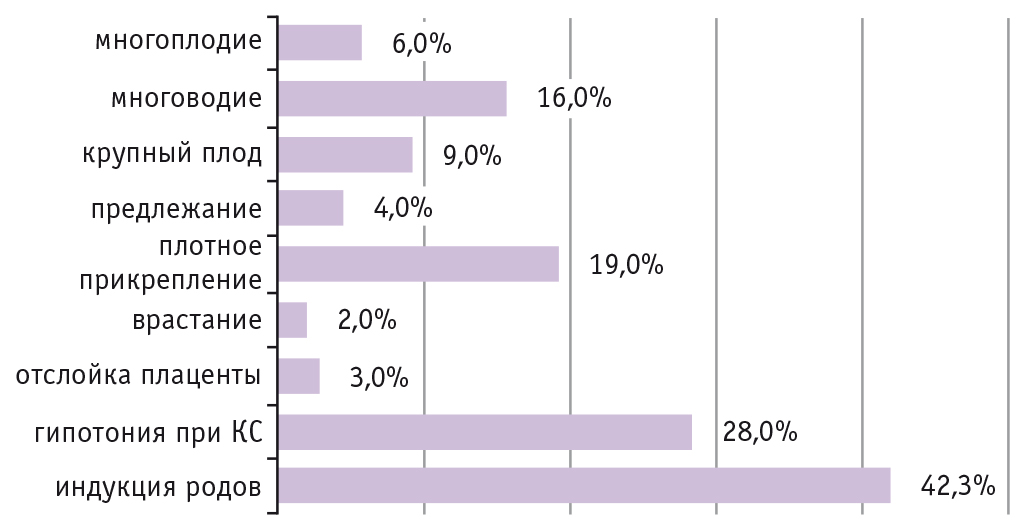
У 70 (67,3%) пациенток с ПРК выявлены значимые факторы риска ПРК: плотное прикрепление плаценты — у 19 (18,3%), рубец на матке после КС — у 19 (18,3%), многоводие — у 16 (15,4%), гипотония матки во время операции КС — у 14 (13,5%), крупный плод — у 9 (8,7%). Предлежание плаценты зарегистрировано у 4 (3,8%) пациенток, многоплодная беременность — у 3 (2,9%), преждевременная отслойка нормально расположенной плаценты — у 3 (2,9%), врастание плаценты — у 2 (1,9%). Следует обратить внимание на то, что у 34 (32,7%) пациенток явных факторов риска ПРК не установлено. Индукция родов проводилась только при ВР и имела место у 44 женщин, что составило 42,3% от всех женщин с ПРК или 69,8% от женщин с ВР. Нейроаксиальная аналгезия проводилась в 80 (76,9%) случаях: при ВР — у 47 (74,6%), при КС — у 33 (80,5%) (χ2 = 0,500; р = 0,738).
Оценка лабораторных показателей у обследованных пациенток накануне родоразрешения и после остановки кровотечения, несмотря на проводимые мероприятия, выявила достоверное снижение уровня гемоглобина, тромбоцитов, фибриногена, гематокрита. При этом значение активированного частичного тромбопластинового времени статистически значимо не изменялось (табл. 1).
Таблица 1
Динамика лабораторных показателей до и после родоразрешения у пациенток с ПРК
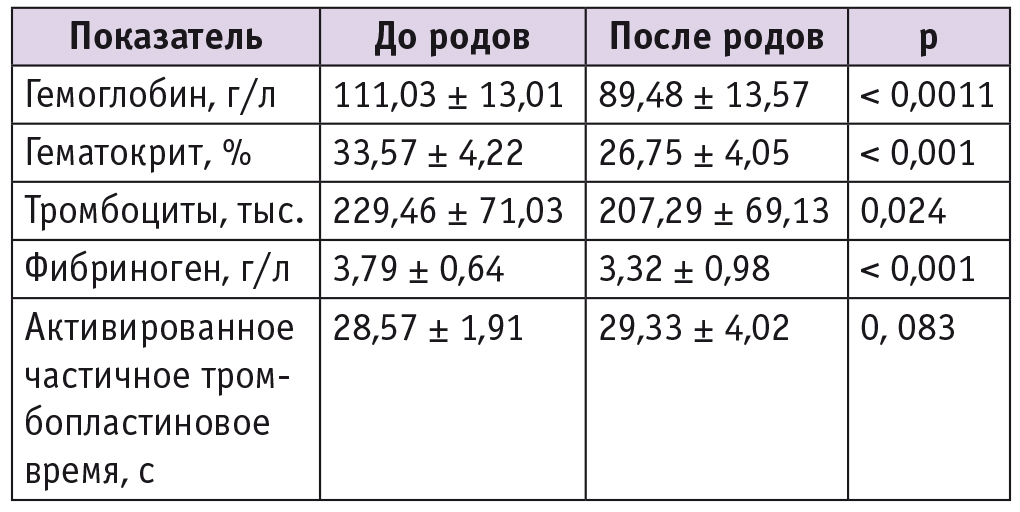
Объем кровопотери у пациенток с ПРК после КС составил 1218,29 ± 728,15 мл, что было достоверно больше, чем при ПРК после ВР — 784,12 ± 304,44 мл (р < 0,001).
Частота применения отдельных методов остановки ПРК у пациенток после ВР и КС представлена в табл. 2. У пациенток после ВР утеротоническая терапия ПРК была ограничена использованием только окситоцина, в то время как после КС дополнительно к окситоцину вводили мизопростол у 26 (63,4%) пациенток (χ2 = 55,3; р < 0,0001) и терлипрессин — у 13 (12,5%) (χ2 = 22,8; р < 0,001). Частота использования УБТ составила 28 (44,4%) случаев после ВР и 27 (65,9%) — после КС (χ2 = 4,600; р = 0,142). Наложение компрессионных швов на матку проводилось у 12 (29,3%) пациенток после КС и у 3 (2,9%) родильниц после ВР (χ2 = 2,800; р = 0,001). Перевязка маточных сосудов проведена у 14 (34,1%) пациенток с ПРК после КС. Гистерэктомия проведена только у 4 (9,8%) родильниц после КС и отсутствовала у пациенток с ПРК после ВР.
Таблица 2
Частота применения отдельных методов остановки ПРК, n (%)

Длительность пребывания в отделении реанимации и интенсивной терапии пациенток после ВР была достоверно меньше, чем после КС, — 1,19 ± 0,53 и 1,46 ± 0,73 дня (р = 0,031), а продолжительность пребывания в послеродовом отделении не имела статистически значимых отличий — 3,80 ± 1,33 и 3,87 ± 2,52 дня соответственно (р = 0,854).
ОБСУЖДЕНИЕ
Результаты проведенного исследования показали, что частота послеродовых кровотечений в стационаре III группы значительно меньше общепопуляционных показателей и составляет 0,67%. По данным систематического обзора S. Feduniw и соавт. (2020), распространенность ПРК в различных популяциях составляет от 1,2% до 12,5%[17].
Нами было выявлено, что пациентки с ПРК имели высокую частоту экстрагенитальных заболеваний, среди которых значимое место занимали избыток массы тела и ожирение (44,2%) и анемия (25%). Анемия является общепризнанным фактором риска ПРК. По данным ретроспективного исследования D.B. Ehrenthal и соавт., которое включало 59 282 пациенток, установлено, что риск ПРК возрастает с увеличением степени тяжести анемии[18]. По данным метаанализа H.B. Ende и соавт., наличие ожирения не ассоциировано с увеличением риска ПРК[19]. Большая доля тучных женщин среди пациенток с ПРК лишь отражает общепопуляционную распространенность ожирения. В США, по данным C.B. Paredes и соавт., 50% беременных имеют избыток массы тела или ожирение[20].
Такие факторы риска, как предлежание и врастание плаценты, многоплодная беременность, в нашем исследовании наблюдались в единичных случаях, в то время как в других более ранних исследованиях, например, M.S. Kramer и соавт.[21], их вклад был более значим. Данный факт может быть обусловлен обязательной стратификацией факторов риска у пациенток, поступающих в стационар высокого риска, и проведением соответствующих профилактических мероприятий.
По нашим данным, доля преждевременных родов у пациенток с ПРК была незначительной и преждевременно были родоразрешены только 9 (8,7%) пациенток с ПРК. Г.В. Каменских и соавт. показали, что преждевременные роды сопряжены с риском кровотечения[22]. Доминирующими причинами массивной кровопотери при очень ранних и ранних преждевременных родах являются предлежание плаценты с аномалией ее инвазии и гипотония матки, что оставляет ресурс для выбора превентивных и лечебных мер. В нашем исследовании у пациенток с преждевременными родами причинами ПРК явились преждевременная отслойка нормально расположенной плаценты — 2 случая, врастание плаценты — 1, гипотония матки во время КС — 2. В 4 случаях у пациенток с преждевременными родами явных факторов риска не выявлено.
Наиболее значимым фактором риска ПРК при ВР в нашем наблюдении явилась индукция родов, проведенная более чем у половины пациенток. В исследовании В.Е. Радзинского и соавт. было отмечено, что использование мифепристона повышает вероятность клинически значимой кровопотери[23]. Следует признать, что строгий отбор пациенток и тщательное определение показаний к индукции можно считать резервом снижения частоты ПРК.
Особого внимания заслуживает тот факт, что у каждой третьей пациентки явных факторов риска ПРК не установлено, что подтверждает тезис о том, что акушерские кровотечения часто происходят не у тех пациенток, у которых мы их ожидаем, и свидетельствует о необходимости дальнейшего поиска факторов риска ПРК.
Достоверное снижение после родов уровня гемоглобина, тромбоцитов, фибриногена, показателя гематокрита логично объясняется кровопотерей. Отсутствие статистически значимых изменений наиболее чувствительного показателя свертываемости крови — активированного частичного тромбопластинового времени — может свидетельствовать о своевременном и адекватном восполнении кровопотери.
УБТ применялась почти у половины женщин с ПРК после ВР и у 2/3 пациенток с ПРК после КС. УБТ считается одной из современных технологий для контроля ПРК и предотвращения гистерэктомии[24], регламентирована клиническими рекомендациями многих профессиональных мировых сообществ, в том числе российскими клиническими рекомендациями[8, 25].
Проведенное исследование наглядно продемонстрировало, что применение существующего локального пошагового алгоритма остановки ПРК после ВР, основанного на внутривенном введении окситоцина и проведении УБТ двухбаллонным катетером Жуковского, позволяет в 95,2% случаев избежать лапаротомии. При неудаче этого подхода проведение лапаротомии с последующей перевязкой маточных сосудов и наложением компрессионного шва на матку позволяет избежать гистерэктомии в 100% случаев.
Применение локального пошагового алгоритма остановки ПРК при КС, который включал внутривенное введение окситоцина, УБТ двухбаллонным катетером Жуковского, ректальное введение мизопростола, внутриматочное введение терлипрессина и комплексный хирургический гемостаз: перевязку маточных сосудов и компрессионный шов на матку по авторской методике, позволяет в 90,2% случаев избежать гистерэктомии.
Систематический обзор и метаанализ, проведенные S. Suarez и соавт., включавшие 91 исследование и 4729 женщин, продемонстрировали несколько меньшую эффективность тампонады матки — 85,9% (95% ДИ 83,9–87,9%): при КС — 81,7%, при ВР — 87,0%, возможно, обусловленную изолированным применением этого метода или использованием только маточного модуля[24].
По данным нашего исследования, ПРК после КС в сравнении с ВР отличает больший объем кровопотери и в связи с этим более частое применение утеротоников резерва (мизопростола и терлипрессина). В многоцентровом когортном исследовании Terli-Bleed убедительно продемонстрированы преимущества локального применения терлипрессина, вводимого в толщу миометрия, для снижения объема интраоперационной кровопотери при отсутствии влияния на систему гемостаза[26, 27].
ЗАКЛЮЧЕНИЕ
Результаты проведенного исследования показали, что частота ПРК в стационаре III уровня составляет 0,67% и значимо не различается при ВР и КС. Наиболее значимым фактором риска ПРК является индукция родов, но более трети женщин не имеют значимых факторов риска. Разработанные локальные пошаговые алгоритмы остановки ПРК высокоэффективны и позволяют избежать гистерэктомии при ВР в 100% случаев, при КС — в 90,2%.
Поступила: 22.06.2023
Принята к публикации: 04.08.2023








