Хологенная диарея — секреторная диарея, возникающая в результате избыточного поступления желчных кислот (ЖК) в ободочную кишку вследствие нарушения их обратной реабсорбции в подвздошной кишке. Секреторный эффект ЖК в толстой кишке осуществляется через передаточный механизм — циклический аденозинмонофосфат, под влиянием которого ингибируется всасывание и усиливается секреция воды и электролитов в толстой кишке, что является причиной диареи.
Как известно, ЖК в качестве основного компонента желчи участвуют в расщеплении и абсорбции липидов и жирорастворимых витаминов. Правильное соотношение ЖК и холестерина в желчи предотвращает осаждение холестерина и образование отложений в желчном пузыре. Потеря ЖК повышает риск желчнокаменной болезни. Кроме того, ЖК действуют как сигнальные молекулы, которые регулируют активность метаболических путей липидов и глюкозы[1]. Известно их значительное влияние на двигательные, сенсорные и секреторные функции толстой кишки, а также на состав микрофлоры кишечника[2]. Поскольку механизмы действия ЖК очень сложны, они могут играть важную роль не только в патогенезе желудочнокишечных заболеваний, но и в регуляции многих метаболических процессов.
За последние годы в литературе появилось много работ, освещающих механизмы всасывания ЖК и их мальабсорбцию, результатом которой является диарея.
Выделяют три типа мальабсорбции ЖК. Тип 1 исследован давно и встречается при резекции или воспалении подвздошной кишки (болезни Крона и др.)[3, 4]. В условиях физиологической нормы 95% ЖК реабсорбируются в подвздошной кишке и транспортируются обратно в печень. При поражении подвздошной кишки нарушается всасывание ЖК, и они в избытке поступают в толстую кишку, вызывая хологенную диарею.
Обследование 298 пациентов с хронической водянистой диареей показало наличие положительных тестов, характерных для мальабсорбции ЖК, у 15 (51,7%) из 29 человек с болезнью Крона, у 40 (93,0%) из 43 больных после резекции подвздошной кишки, у всех 12 (100%) пациентов после резекции тонкой кишки и у 2 (66,7%) из 3 человек после лучевого поражения тонкой кишки[5].
Наблюдается зависимость выраженности диарейного синдрома от объема резекции тонкой кишки[6]. Избыток ЖК, вторично возникающий вследствие поражения места их всасывания, послужил основанием для названия данного типа хологенной диареи — вторичная. Этот тип наиболее часто встречается и хорошо изучен.
Тип 2 (идиопатический, или первичный) впервые описан E. H Thaysen и L. Pedersen в 1976 г. и получил свое название изза отсутствия патогистологических признаков поражения подвздошной кишки[7]. Он длительное время считался редким. Однако последние исследования указывают на то, что малое количество больных с данным типом хологенной диареи было обусловлено сложностью ее диагностики. Результаты последних исследований показывают, что среди пациентов с синдромом раздраженного кишечника (СРК) с диареей более 30% страдают хологенной диареей и ее распространенность может достигать 1% среди жителей Западной Европы[8].
Этиология идиопатической хологенной диареи до настоящего времени остается неясной. Рассматривается несколько ее патофизиологических механизмов. Появились данные, что идиопатический вариант мальабсорбции ЖК связан с быстрым транзитом кишечного содержимого[9, 10]. Другие исследователи считают причиной генетические дефекты регуляции транспорта и синтеза ЖК или молекулярных механизмов, ответственных за эти процессы[11].
Тип 3 — смешанный, включает в себя состояния, при которых также возможно возникновение хологенной диареи: например, перенесенную холецистэктомию, синдром избыточного бактериального роста, панкреатит, микроскопический колит, целиакию и др.[12, 13].
В последние годы активно исследуется и влияние приема гипогликемического препарата метформина на нарушение реабсорбции ЖК вследствие повышения секреции глюкагоноподобного пептида 1, однако эти данные весьма противоречивы, и механизмы такого влияния не до конца изучены[14]. Таким образом, центральным звеном патогенеза хологенной диареи является нарушение энтерогепатической циркуляции ЖК вследствие различных причин.
Известно, что синтез первичных ЖК (холевой и хенодезоксихолевой) происходит в печени из холестерина. Он обеспечивается ферментом 7αгидроксилазой, представляющей собой одну из форм цитохрома Р450 (P450 7A1 или CYP7A1). В процессе конъюгирования — присоединения ионизированных молекул глицина или таурина к карбоксильной группе ЖК — образуются глициновые и тауриновые конъюгаты ЖК. Выведение ЖК в желчные капилляры в основном происходит с помощью транспортного белка, обозначаемого как насос выведения ЖК (bile salt export pump). Часть ЖК в кишечнике подвергается действию ферментов бактерий, которые отщепляют глицин и таурин, а также гидроксильную группу ЖК, образуя вторичные ЖК. Вторичные ЖК: дезоксихолевая, образующаяся из холевой, и литохолевая, образующаяся из хенодезоксихолевой, — хуже растворяются и медленнее всасываются в кишечнике, чем первичные. В норме небольшая часть не всосавшихся в подвздошной кишке ЖК (около 0,3–0,6 г/сут) выводится из организма с калом. При повышении количества вторичных ЖК в толстой кишке усиливается секреция натрия и воды, и возникает хологенная диарея.
Всасывание в терминальном отделе подвздошной кишки и поступление ЖК в клетки тонкой кишки происходит с помощью как пассивной диффузии, так и апикального натрийзависимого транспортера ЖК — белка ASBT (apical sodium bile acid transporter), расположенного на энтероците; а в систему воротной вены доставка ЖК осуществляется так называемым органическим переносчиком растворенного вещества (organic solute transporter α/β). В гепатоциты ЖК проникают при участии натрийзависимого таурохолатного транспортного белка (sodium taurocholate cotransporting polypeptide, NTCP) и белковтранспортеров органических анионов (organic anion transporting polypeptide, OATP)[15]. Эти транспортеры позволяют переносить ЖК из крови в гепатоциты против высокого градиента концентрации и электрического потенциала.
Обеспечение баланса между синтезом, поглощением и экскрецией гепатобилиарных транспортеров жестко регулируется ядерными рецепторами. В энтероцитах и гепатоцитах имеется рецептор (FXR), стимуляция которого в энтероцитах ЖК индуцирует транскрипцию гормона — фактора роста фибробластов 19 (fibroblast growth factor 19, FGF19)[16, 17]. Данный процесс запускается всеми ЖК, хотя более интенсивно это происходит с помощью хенодезоксихолевой и гликохенодезоксихолевой кислоты. В последующем, высвобождаясь из энтероцита и циркулируя в системе воротной вены, FGF19 взаимодействует с рецептором FGF4 на мембране гепатоцитов через косвенную регуляцию постоянного белка эндоплазматического ретикулума klothoβ[18]. В результате этого процесса через белки так называемых малых гетеродимерных партнеров (small heterodimer partner) происходят ингибирование CYP7A1 и подавление синтеза новых ЖК[19]. Одновременно снижаются экспрессия транспортных белков NTCP и OATP в гепатоцитах и активное поглощение ЖК из системы воротной вены.
Нарушения, возникающие на различных этапах регуляции, реабсорбции, синтеза и транспорта ЖК в системе энтерогепатической циркуляции ЖК, могут приводить к возникновению хологенной диареи.
Одним из таких нарушений является дефицит FGF19, впервые обнаруженный G. R. Walters и соавт. у больных с идиопатическим типом хологенной диареи. Недостаток этого гормона по механизму обратной связи приводит к активации синтеза новых ЖК в печени, увеличению их количества в тонкой кишке и возникновению хологенной диареи[12]. Редким нарушением, приводящим к идиопатической хологенной диарее, считается генетический дефект в белке ASBT, результатом которого становится нарушение реабсорбции ЖК из просвета кишечника в энтероцит[20].
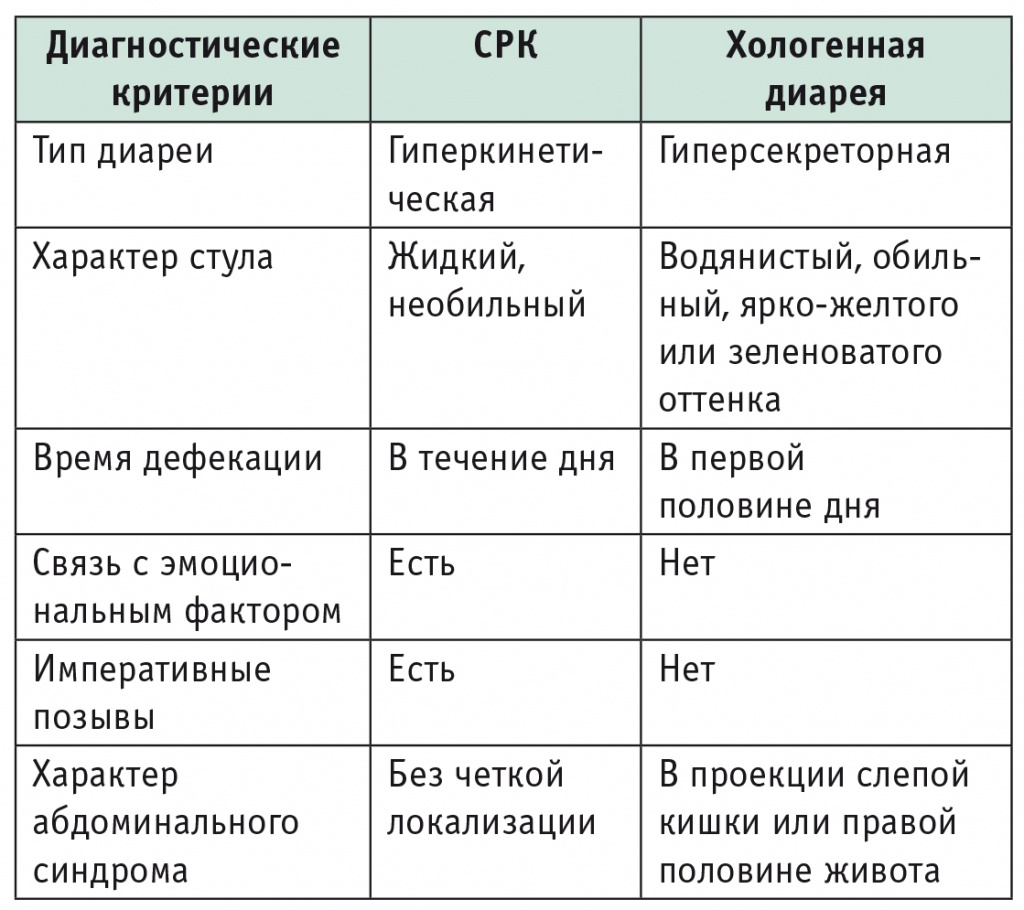
Клиническая картина хологенной диареи характеризуется частым водянистым стулом, сочетается с болью в правых отделах живота, часто в проекции слепой кишки, а также жжением в прямой кишке и заднем проходе[21, 22]. Отсутствие клинических симптомов прогрессирования заболевания, несмотря на его длительность, нередко приводит к ошибочному диагнозу СРК. В таблице показаны дифференциальнодиагностические признаки хологенной диареи и диареи при СРК.
Таблица
Дифференциально-диагностические признаки хологенной диареи и диареи при синдроме раздраженного кишечника (СРК)
Для диагностики хологенной диареи разработаны методы выявления мальабсорции ЖК, но имеются трудности в их воспроизведении, и они не всегда общедоступны[23]. Количественная оценка ЖК в фекалиях трудоемка и требует наличия специально оборудованной лаборатории.
Диагностика мальабсорбции ЖК может производиться с помощью теста SeHCAT, который основан на использовании аналога конъюгированной ЖК (75Seгомохолилтаурина), проходящего все этапы энтерогепатической циркуляции, потери которого фиксируют через 7 дней после перорального приема данного вещества с помощью γкамеры. Сохранение SeHCAT в организме через 7 дней после перорального приема менее 15–10% от исходного указывает на наличие мальабсорбции ЖК. Однако ввиду использования специального дорогостоящего оборудования этот метод не всегда является доступным.
C помощью жидкостной хроматографии высокого разрешения возможно измерение уровня в сыворотке крови предшественника ЖК — 7αгидрокси4холестен31 (С4), повышение которого также указывает на усиленный синтез ЖК, характерный для хологенной диареи[13]. Уровень C4 значительно возрастает у пациентов с хологенной диареей с чувствительностью и специфичностью 90% и 79% соответственно. При этом содержание C4 хорошо коррелирует с показателем SeHCAT. С учетом простоты и экономичности исследование уровня C4 является более привлекательным в качестве скринингового теста для диагностики хологенной диареи[24].
Определение концентрации FGF19 в сыворотке крови иммуноферментным методом может также использоваться как тест для диагностики мальабсорбции ЖК[25]. Ранее проведенные исследования показали, что медианные уровни FGF19 значительно ниже в группе больных с идиопатической хологенной диареей, чем в контрольной группе (120 пг/мл против 231 пг/мл), а уровень C4 натощак значительно выше, чем в контроле (51 нг/мл против 18 нг/мл), что подтверждает дефицит ингибирования обратной связи гормоном FGF19, вследствие которого возникают перепроизводство ЖК и хологенная диарея[12].
Для количественного определения ЖК в кале применяется спектрофотометрический ферментный метод. В спиртовом экстракте из образцов кала весом 1–1,5 г ферментным методом определяют концентрацию ЖК с последующим расчетом их суточной экскреции с учетом количества каловых масс в сутки. По данным Л. М. Крумс и соавт., у здоровых лиц потеря ЖК с фекалиями составляет от 100–200 мг/сут. У больных, перенесших резекцию более 100 см подвздошной кишки, средние потери ЖК — 2250,7 ± 685,3 мг/сут. В группе перенесших холецистэктомию среднее содержание ЖК в кале также превышало норму и составляло в среднем 786,4 ± 103,7 мг/сут[21].
В рекомендациях Британского общества гастроэнтерологов и Американской ассоциации гастроэнтерологов в качестве теста на наличие мальабсорбции ЖК предложено эмпирическое назначение секвестранта ЖК холестирамина. Положительный клинический эффект от его применения может свидетельствовать о мальабсорбции[26].
Холестирамин представляет собой синтетическую анионообменную смолу, используемую для абсорбции ЖК в просвете тонкой кишки. Так же, как и в случае применения углеродных энтеросорбентов, выведение ЖК из энтерогепатической циркуляции приводит к усилению их печеночного синтеза, следовательно, к снижению концентрации холестерина в плазме крови. Холестирамин представляет собой мелкий порошок сильноосновной смолы в хлорформе, назначаемый в виде болтушки с фруктовым соком или молоком и имеющий выраженный неприятный вкус. Это обстоятельство, а также частое возникновение запоров на фоне приема данного препарата заставили разработать ряд других синтетических смол для удаления ЖК, в частности холестипол, колесевелам. Последний энтеросорбент обладает в 4–6 раз бо́льшим, чем холестирамин, сродством к ЖК и, являясь набухающим гидрогелем, практически не оказывает констипационное действие[27].
Несмотря на выраженные положительные терапевтические свойства, препараты, связывающие ЖК, обладают рядом отрицательных эффектов. К ним относятся абсорбция лекарственных средств, поглощение жирорастворимых витаминов и др. Это требует мониторинга уровня витаминов при длительном применении данных препаратов[28]. Помимо полимерных ионообменных сорбентов для лечения хологенной диареи, возможно применение природных пищевых волокон, энтеросорбентов на основе хитозана и углеродных адсорбентов, но их терапевтическое действие несколько ниже, чем у холестирамина, поэтому они не всегда эффективны.
К экспериментальным препаратам, применяемым в настоящее время для лечения хологенной диареи, можно отнести обетихолевую кислоту. Имеются данные об увеличении сывороточного уровня FGF19 у пациентов с идиопатической хологенной диареей и с экономной (менее 45 см) резекцией подвздошной кишки после использования обетихолевой кислоты[29]. Обетихолевая кислота (также известная как INT747 и 6αэтилCDCA) является мощным агонистом рецептора FXR и может стимулировать продуцирование FGF19 дозозависимым образом[30].
ЗАКЛЮЧЕНИЕ
Хологенная диарея является нозологической формой, которую обнаруживают более чем у 30% пациентов с диагнозом функциональной диареи или синдрома раздраженного кишечника.
Наиболее чувствительный и специфичный метод диагностики мальабсорбции желчнных кислот — тест SeHCAT.
Одновременное применение других диагностических методов (измерение уровня 7α-гидрокси-4-холестен-3-1 или фактора роста фибробластов 19) и дальнейшее изучение патогенеза различных типов хологенной диареи позволят более точно установить диагноз и назначить адекватное лечение.
Основными терапевтическими средствами при хологенной диарее являются холестирамин и другие энтеросорбенты.








