Гендерные различия в распространенности рака различных отделов ЖКТ хорошо известны. При одних заболеваниях доминируют женщины (желчнокаменная болезнь и первичный билиарный цирроз), при других — мужчины (пищевод Барретта и рак толстой кишки) [15, 21, 26]. Во всем мире рак пищевода у мужчин наблюдается в 3–4 раза чаще, чем у женщин [12], этот гендерный уклон сопровождается мужским доминированием в основных группах риска: среди курящих и потребляющих алкоголь [17]. Причины увеличения частоты рака пищевода у мужчин не изучены в деталях, но некоторые исследователи связывают его с половыми гормонами как факторами риска [14]. В ткани рака пищевода обнаружены также андрогенные рецепторы [3, 19, 25]. Показано, что в развитии аденокарциномы пищевода значимую роль играют эстрогенные рецепторы [24, 28]. У пациентов с пищеводом Барретта определены высокие уровни циркулирующего тестостерона и дигидротестостерона [6]. Несмотря на простоту функций пищевода, гендерные различия существуют и при нормальном функционировании органа, и при его болезни. Некоторые компоненты функций пищевода зависят от половой принадлежности, и это необходимо учитывать при интерпретации результатов функционального тестирования. При заболеваниях пищевода, в частности в случаях гастроэзофагеальной рефлюксной болезни, пищевода Барретта, рака пищевода, существуют половые и гендерные различия в патофизиологии и реакции на лечение [23].
Во многих исследованиях доказано, что эстрогены обладают ангиогенным эффектом [5]. A. R. Gagliardi и соавт. описали антиангиогенное действие антиэстрогенов, вызванное непосредственным ингибированием как фактора роста эндотелия сосудов (англ. vascular endothelial growth factor — VEGF) типа A, так и основного фактора роста фибробластов (англ. fibroblast growth factor — FGF) [9]. Интерес вызывают исследования системы факторов роста, обусловливающих активацию неоангиогенеза при раке различной локализации. Особое значение имеют VEGF, FGF и трансформирующие факторы роста (англ. transforming growth factor — TGF) альфа и бета, которые известны как факторы запуска ангиогенеза [8].
Факторы роста являются основными переносчиками митогенного сигнала, осуществляют контроль клеточного роста, дифференцировки и регулируют такие функциональные состояния гладких мышечных клеток, как секреция компонентов экстрацеллюлярного матрикса, сократительная активность ткани, экспрессия различных рецепторов, межклеточные контакты, а также ангио- и лимфангиогенез [1].
Целью настоящего исследования явилось изучение уровней некоторых факторов роста в тканях плоскоклеточного рака пищевода (ПРП), его перифокальной зоны (ПЗ) и в ткани по линии резекции (ЛР) у мужчин и женщин.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось в течение 2014–2015 гг. на базе торакоабдоминального отдела ФГБУ «Ростовский научно-исследовательский онкологический институт» Минздрава России (руководитель — д. м. н., профессор О. И. Кит). Дизайн был одобрен этическим комитетом института. Получено информированное добровольное согласие всех больных на участие в исследовании.
Изучали образцы тканей, взятых от 32 больных ПРП, поступивших на оперативное лечение: 21 мужчины и 11 женщин. Возраст мужчин составлял от 38 до 74 лет (62,3 ± 5,8 года), женщин — от 53 до 74 лет (66,7 ± 5,9 года); все женщины были в менопаузе в течение 3–5 лет. У 30 из 32 больных признаков ожирения не обнаружено.
Все пациенты имели II стадию опухолевого процесса (G2, рTNM). Метастазы в лимфатические узлы были только у 46,7% мужчин. Гистологический контроль осуществляли во всех случаях. В ходе операции производили удаление злокачественных образований пищевода с последующим биохимическим исследованием образцов тканей: опухоли, ее ПЗ, а также ЛР в 3–5 см от края опухолевой ткани.
В 10%-ных цитозольных фракциях ткани, приготовленных на калий-фосфатном буфере рН 7,4, содержавшем 0,1%-ный Твин-20 и 1%-ный раствор бычьего сывороточного альбумина, методом ИФА с использованием стандартных тест-систем определяли уровни VEGF-А и его рецептора VEGF-R1 (Bender MedSystems, Австрия), VEGF-С и его рецептора VEGF-R3 (Bender MedSystems, Австрия), а также эпидермального фактора роста (англ. epidermal growth factor — EGF) (Biosource, США), инсулиноподобных факторов роста (англ. insulin-like growth factor — IGF) 1 и 2 (Mediagnost, США), TGF-β1 (Bender MedSystems, Австрия).
Статистика: пакет программ Microsoft Excel (Windows XP). Данные таблиц представляли в виде M ± m, где M — среднее значение, а m — стандартная ошибка среднего. Различия оценивали по Т-критерию Стьюдента и считали достоверными при р < 0,05. Корреляции между параметрами анализировали с помощью коэффициента линейной корреляции Пирсона (r), достоверность констатировали при р < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Данные, полученные при изучении содержания факторов роста в тканях у мужчин и женщин при ПРП, показаны в таблице.
Таблица
Показатели факторов роста в тканях у мужчин и женщин при плоскоклеточном раке пищевода
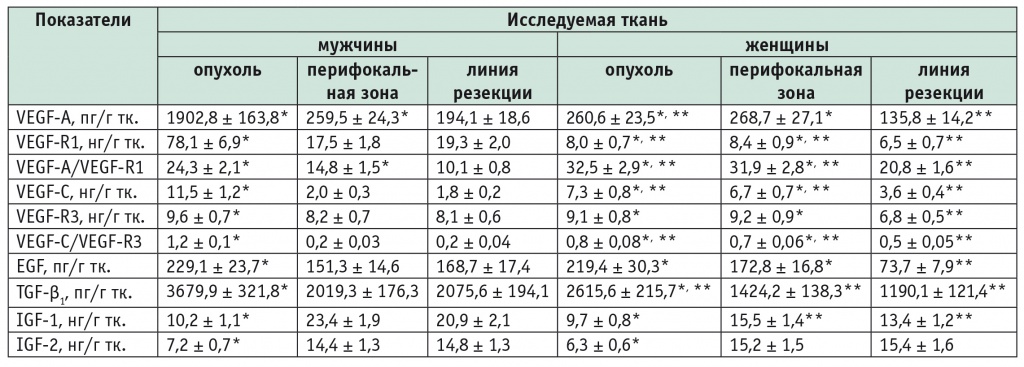
Примечания.
1. EGF — эпидермальный фактор роста; IGF-1, -2 — инсулиноподобные факторы роста 1, 2; TGF-β1 — трансформирующий фактор роста бета 1; VEGF-A, -C — факторы роста эндотелия сосудов типов A, C; VEGF-R1, -R3 — рецепторы VEGF-A, -C.
2. Знаком (*) отмечены статистически значимые различия (p < 0,05): (*) — с условно интактной тканью по линии резекции; (**) — с соответствующей тканью мужчин.
В первую очередь были определены уровни факторов роста в ткани по ЛР, т. е. условно интактной ткани. Такое исследование может дать информацию о фоне, на котором развивается и растет злокачественная опухоль.
Установлено, что уровни VEGF-А и VEGF-R1 в ткани по ЛР у мужчин выше, чем у женщин, в 1,4 и 3,0 раза соответственно, а соотношение VEGF-А/VEGF-R1, характеризующее уровень свободного VEGF-А, в ткани по ЛР у мужчин, напротив, было в 2,1 раза ниже (р < 0,05 во всех случаях, см. табл.). Содержание VEGF-С в ткани по ЛР у мужчин было в 2,0 раза ниже, чем в соответствующих образцах у женщин, а уровень VEGF-R3 — в 1,2 раза выше, и поэтому соотношение VEGF-С/VEGF-R3 оказалось в 2,5 раза выше в ткани по ЛР у женщин (р < 0,05 во всех случаях).
Уровни EGF, TGF-β1 и IGF-1 в ткани по ЛР у мужчин в 2,3; 1,7 и 1,6 раза соответственно превосходили показатели у женщин (р < 0,05 во всех случаях), и только значения IGF-2 не имели достоверных различий.
В ткани опухоли у мужчин уровни VEGF-А и VEGF-R1 превышали показатели у женщин в 7,3 и 9,8 раза соответственно, а соотношение VEGF-А/VEGF-R1 оказалось в 1,3 раза выше у женщин (р < 0,05 во всех случаях, см. табл.). В этой же ткани содержание VEGF-С у мужчин превосходило аналогичный показатель у женщин в 1,6 раза (р < 0,05), значения VEGF-R3 не имели достоверных различий и, соответственно, соотношение VEGF-С/VEGF-R3 у мужчин было в 1,5 раза выше (р < 0,05). Показатели EGF, IGF-1, IGF-2 у мужчин и женщин достоверно не различались. Уровень TGF-β1 в ткани опухоли у мужчин был выше, чем у женщин, в 1,4 раза (р < 0,05).
В ткани ПЗ опухоли у мужчин достоверные (р < 0,05) различия с женщинами обнаружены по показателям VEGF-R1, VEGF-А/VEGF-R1, VEGF-С, VEGF-С/VEGF-R3, TGF-β1 и IGF-1 (см. табл.). Причем выше, чем у женщин, были уровни VEGF-R1 (в 2,1 раза), TGF-β1 (в 1,4 раза) и IGF-1 (в 1,5 раза), а ниже — значения VEGF-А/VEGF-R1 (в 2,2 раза), VEGF-С (в 3,4 раза) и VEGF-С/VEGF-R3 (в 3,5 раза). Содержание VEGF-A, EGF и IGF-2 не имело достоверных отличий от аналогичных показателей у женщин.
Далее было изучено изменение содержания факторов роста в тканях от ЛР до опухоли, включая ее ПЗ, отдельно для мужчин и женщин.
У мужчин в ткани опухоли уровни VEGF-А и VEGF-R1 превосходили показатели в ткани по ЛР в 9,8 и 4,0 раза соответственно, а соотношение VEGF-А/VEGF-R1 — в 2,4 раза (см. табл.). Содержание VEGF-С и VEGF-R3 в ткани опухоли было повышено в 6,4 и 1,2 раза соответственно, а показатель VEGF-С/VEGF-R3 — в 6,0 раза. Уровни EGF и TGF-β1 в ткани опухоли превышали значения в ткани по ЛР в 1,4 и 1,8 раза соответственно, а содержание IGF-1 и IGF-2, напротив, оказалось в среднем вдвое ниже (р < 0,05 для всех изучаемых показателей).
Уровень VEGF-А и соотношение VEGF-А/VEGF-R1 в ПЗ опухоли у мужчин были увеличены относительно таковых в ткани по ЛР в 1,3 и 1,5 раза соответственно, но оставались ниже, чем в ткани опухоли, в 7,3 и 1,6 раза (р < 0,05 во всех случаях). Остальные исследуемые показатели в ПЗ опухоли у мужчин не имели достоверных отличий от показателей в ткани по ЛР.
У женщин уровни VEGF-А и VEGF-R1 в ткани опухоли в сравнении с показателями в ткани по ЛР были выше в 1,9 и 1,2 раза соответственно, а соотношение VEGF-А/VEGF-R1 — в 1,6 раза (см. табл.). Значения VEGF-С, VEGF-R3 и показатель VEGF-С/VEGF-R3 превосходили таковые в ткани по ЛР в 2,0; 1,3 и 1,6 раза соответственно. Уровни EGF и TGF-β1 были выше в 3,0 и 2,2 раза соответственно. Так же как у мужчин, содержание IGF-1 и IGF-2 в ткани опухоли у женщин оказалось ниже, чем в ткани по ЛР, — в 1,4 и 2,4 раза соответственно (р < 0,05 для всех изучаемых показателей).
В ткани ПЗ опухоли у женщин, в отличие от соответствующей ткани у мужчин, многие показатели достоверно отличались от таковых в ткани по ЛР и не имели достоверных отличий от значений в ткани опухоли. В их число входили факторы ангиогенеза (VEGF-А, VEGF-R1, VEGF-А/VEGF-R1), лимфангиогенеза (VEGF-С, VEGF-R3, VEGF-С/VEGF-R3) и эпидермальный фактор роста (EGF). Содержание TGF-β1, IGF-1 и IGF-2 в ткани ПЗ опухоли и в ткани по ЛР у женщин достоверно не различалось.
Таким образом, выявлены различия в уровнях факторов роста в условно нормальной и злокачественной тканях пищевода у мужчин и женщин. Прежде всего, обращают на себя внимание результаты исследования условно интактной ткани по ЛР. Очевидно, что в непораженной ткани пищевода у мужчин уровни большинства изученных факторов роста и их рецепторов выше, чем у женщин; исключение составило только содержание VEGF-С и IGF-2. Можно предположить, что этот факт связан с разной насыщенностью тканей половыми гормонами — андрогенами и эстрогенами — у мужчин и женщин. Для VEGF-А, VEGF-R1, TGF-β1 отмеченная закономерность сохраняется и в ткани опухоли.
Представляют интерес факторы роста эндотелия кровеносных и лимфатических сосудов — VEGF-А, VEGF-С. В ткани пищевода по ЛР у мужчин уровни VEGF-А и VEGF-R1 выше, чем в такой же ткани у женщин. Известно, что для всех членов VEGF-семейства характерна специализация связывания со своими рецепторами. VEGF-A взаимодействует с VEGF-R1 и VEGF-R2. Несмотря на то что VEGF-R1 взаимодействует с VEGF-А с наивысшей аффинностью, предполагают, что этот рецептор функционирует главным образом в качестве ловушки, связывая VEGF и тем самым ингибируя VEGF-опосредованную сигнализацию. Предполагают также, что таким образом происходит регуляция взаимодействия VEGF с VEGF-R2, который считают главным рецептором сигнального пути VEGF [8]. Учитывая изложенное, а также величину соотношения VEGF-А/VEGF-R1, определенную в непораженной ткани пищевода, можно говорить о том, что взаимодействие VEGF с VEGF-R2 выше именно у женщин и нарастает в тканях ПЗ и самой опухоли. Связывание VEGF с VEGF-R2 приводит к димеризации и аутофосфорилированию каталитического домена рецептора, запускающего сигнальный путь Akt — главный сигнальный путь выживания клеток. В результате запускаются экспрессия антиапоптотических белков, активация циклинов и циклинзависимых протеинкиназ, что обусловливает выход эндотелиоцитов из G0-фазы и вступление в клеточный цикл; происходит активация интегринов, стимулирующих клеточную адгезию, миграцию и рост эндотелиальных клеток [10].
Имеются исследования, показывающие, что экспрессия VEGF в тканях ПРП с глубокой инфильтрацией значительно выше, чем в тканях только с поверхностной инфильтрацией, а экспрессия VEGF в злокачественных тканях существенно повышается при наличии метастазов в лимфатические узлы [30]. Метастазы в лимфатические узлы были обнаружены только у 46,7% мужчин. При сравнительном изучении уровней VEGF-А, VEGF-R1 и соотношения VEGF-А/VEGF-R1 в ткани опухоли у мужчин с метастазами в лимфатические узлы и без таковых оказалось, что содержание VEGF-А в ткани опухоли у больных с метастазами в 3,2 раза выше, чем у больных без метастазов (3165,2 ± 411,9 против 990,7 ± 75,2 пг/г тк., р < 0,05). Уровни VEGF-R1 не имели достоверных различий, поэтому показатель VEGF-А/VEGF-R1 при метастазах в лимфатические узлы также был в 3,2 раза выше.
VEGF-C связывается с VEGF-R3, запуская лимфангиогенез, в меньшей степени — с VEGF-R2. Известно, что VEGF-C синтезируется в виде пропептида, впоследствии пропептид подвергается протеолизу и происходит его созревание. Короткие незрелые формы связываются с VEGF-R3, а созревшие — с VEGF-R2. Следовательно, соотношение VEGF-С/VEGF-R3 может косвенно указывать на уровень зрелых форм VEGF-С, обеспечивающих плотность лимфатических сосудов [2]. В ткани пищевода по ЛР и в ткани ПЗ опухоли у женщин при ПРП соотношение VEGF-С/VEGF-R3 было выше, чем у мужчин (р < 0,05), однако в ткани опухоли этот показатель оказался более высоким у мужчин (р < 0,05). В ходе сравнительного изучения уровней VEGF-С, VEGF-R3 и соотношения VEGF-С/VEGF-R3 в ткани опухоли у мужчин с метастазами в лимфатические узлы и без таковых обнаружено, что уровень VEGF-С у больных мужчин с метастазами в 1,6 раза выше (12,6 ± 1,9 против 8,1 ± 1,1 нг/г тк., р < 0,05). Уровни VEGF-R3 не имели достоверных различий, соответственно, соотношение VEGF-С/VEGF-R3 также было выше в 1,5 раза.
Полученные результаты согласуются с данными исследований, которые показали значение повышения уровня VEGF-С в ткани ПРП для плохого прогноза и метастазирования в лимфатические узлы [11, 29].
EGF является сильным митогеном для различных клеток эндо-, экто- и мезодермального происхождения. Он регулирует дифференцировку, апоптоз, пролиферацию, подвижность и выживаемость как нормальных, так и опухолевых клеток; рецепторы семейства EGF регулируют ангиогенез. Различия в содержании EGF в интактной ткани у мужчин и женщин в настоящем исследовании, скорее всего, связаны с гендерными особенностями строения пищевода. L. P. Rocha и соавт. при иммуногистохимическом и гистологическом исследовании эпителия пищевода на аутопсийном материале показали, что хотя толщина эпителиального слоя одинакова у больных обоего пола, в образцах ткани, взятых у женщин, имеется больше эпителиальных слоев, клетки которых значительно меньшего размера по сравнению с образцами, взятыми у мужчин [22]. С другой стороны, низкий уровень EGF в ткани по ЛР у женщин может быть маркером более редкой малигнизации органа. Показано, что в эпителии пищевода здоровых женщин в 4 раза больше IgA-, IgG- и IgM-положительных клеток, а также имеется значительно большее количество антигенпредставляющих клеток Лангерганса по сравнению с аналогичной тканью здоровых мужчин, что подтверждает различия защиты слизистых оболочек пищевода у больных разного пола [22]. Известно также, что мужчины более чувствительны к перфузии кислотой при эзофагеальном рефлюксе, чем женщины [20].
Вместе с тем, как показано в нашем исследовании, содержание EGF в тканях опухоли и ее ПЗ не имеет гендерных различий.
Семейство EGF, кроме самого EGF, включает TGF-β. Сигнальный путь TGF-β имеет большое значение для эпителиального гомеостаза и часто тормозится во время прогрессирования ПРП. G. F. Le Bras и соавт. показали, что потеря передачи сигналов TGF-β способствует инвазии фибробластов в эпителий [16]. Используя иммортализованные кератиноциты пищевода, авторы продемонстрировали, что лечение ингибиторами TGF-β-сигнализации усиливает инвазию эпителиальных клеток в фибробласты встраиваемой матрицы матригель/коллаген I. Это вторжение связано с увеличением экспрессии провоспалительных цитокинов IL-1 и EGF-R-лигандов — EGF и TGF-α, изменяет эпителиально-фибробластные взаимодействия, подавляя маркеры активированных фибробластов. Данные результаты свидетельствуют о том, что ингибирование передачи сигналов TGF-β модулирует множество путей, сочетанное действие которых способствует опухолевой инвазии.
В настоящем исследовании отмечено синхронное изменение содержания TGF-β и EGF. В ткани по ЛР у женщин показатель TGF был ниже, чем у мужчин. В ткани опухоли и у женщин, и у мужчин уровень TGF-β возрастал, как и уровень EGF. Вероятно, TGF-β можно рассматривать как фактор, компенсирующий EGF. Однако существуют исследования, показывающие, что избыточная экспрессия TGF и ЕGF в пищеводном эпителии и стромальных фибробластах способствует прогрессированию предраковых поражений пищевода через пролиферацию эпителиальных клеток и кровеносных сосудов, а также повышенную регуляцию VEGF [16, 27].
Особое внимание необходимо уделить результатам изучения IGF. Имеются исследования, указывающие на участие оси IGF в прогрессировании рака пищевода. Компоненты оси включают родственные пептиды IGF-1, IGF-2, мРНК-связывающие белки (IGF2BPs) и связывающие белки (IGFBPs), которые регулируют факторы роста посттранскрипционно и постпоступательно, а также рецепторы IGF-1R и IGF-2R [4]. В обзоре M. K. Kashyap указывается, что ось «IGF — IGF-R — IGFBP» задействована в развитии рака органов ЖКТ, в том числе ПРП [13]. W. Ma и соавт. [18] выявили более высокую экспрессию IGF-1R в опухолевых тканях ПРП по сравнению с соседними нормальными тканями, а также обнаружили, что она связана с прогрессией опухоли. Н. Yang и соавт. продемонстрировали связь между генетическими вариантами IGFBP-3 (rs2270628) и риском развития ПРП [28]. S. L. Doyle и соавт. показали, что ось «IGF — IGF-R — IGFBP» играет ключевую роль в прогрессировании рака пищевода и представляет собой вероятный механизм, посредством которого висцеральное ожирение воздействует на риск возникновения аденокарциномы и биологию опухоли [7].
Однако мы не обнаружили повышенных уровней IGF-1 и IGF-2 в ткани ПРП — напротив, их содержание было снижено как у мужчин, так и у женщин. Более того, при наличии метастазов у мужчин показатели уменьшались: IGF-1 — 15,9 ± 1,2 нг/г тк. в опухоли у больных без метастазов и 8,4 ± 1,1 нг/г тк. в опухоли у больных с метастазами (p ˂ 0,05); IGF-2 — 7,9 ± 0,8 и 5,7 ± 1,0 нг/г тк. соответственно (p ˂ 0,05). Возможно, это было связано с отсутствием ожирения у обследованных больных или с другими особенностями, очевидно, что этот вопрос требует дальнейшего изучения.
Выводы
1. У мужчин в ткани пищевода, не пораженной раковым процессом (из области ЛР), уровни большинства изученных факторов роста и их рецепторов были выше, чем у женщин. Исключение составили VEGF-С и IGF-2.
2. В ткани ПРП и мужчин, и женщин значения большинства изученных факторов роста были повышены относительно соответствующих показателей области ЛР. Исключение составили IGF-1 и IGF-2.
3. В ткани ПЗ опухоли у мужчин значения всех изученных факторов роста, кроме VEGF-А, были сходны с соответствующими показателями в ткани по ЛР, тогда как у женщин уровни большинства факторов роста в ткани ПЗ не имели достоверных различий с таковыми в ткани опухоли. Исключение составили IGF-1, IGF-2 и TGF-β1, содержание которых в ткани ПЗ и области ЛР у женщин достоверно не различалось.
ЗАКЛЮЧЕНИЕ
Обнаруженные гендерные различия в содержании изученных факторов роста и рецепторов VEGF в тканях пищевода в большей степени относятся к их уровням в условно интактной ткани из области линии резекции (ЛР). Количественные их изменения в ткани плоскоклеточного рака пищевода синхронны, однонаправлены и зависят от исходного уровня в ткани по ЛР. Привлекает внимание ткань перифокальной зоны: в отличие от мужчин, большинство показателей у женщин в этой ткани было повышено и не имело достоверных отличий от значений в ткани злокачественной опухоли.








