Одной из важных междисциплинарных медицинских проблем считается развитие венозных тромбоэмболических осложнений (ВТЭО). По данным статистических отчетов Министерства здравоохранения Российской Федерации, у нас в стране ежегодно регистрируются около 80 000 новых случаев этого заболевания[1]. К ним относят тромбоз глубоких вен (ТГВ), тромбоэмболию легочных артерий (ТЭЛА). Актуальность проблемы ВТЭО связана с их чрезвычайно сильным влиянием на здоровье и жизнь пациентов[2].
С клинических позиций тромботическое поражение венозного русла нижних конечностей наиболее опасно в виде поражения глубоких вен. В пожилом и старческом возрасте частота ТГВ увеличивается в несколько раз и достигает 200 случаев на 100 000 человек в год. Легочную эмболию регистрируют ежегодно с частотой 35–40 на 100 000 человек.
Следует сказать, что сам по себе тромбоз вен нижних конечностей (глубоких и тем более подкожных) не представляет опасности для жизни пациента (синяя флегмазия или венозная гангрена встречаются крайне редко). Непосредственная угроза жизни больного связана с ТЭЛА. Даже при своевременном выявлении ТГВ от легочной эмболии умирают 6% пациентов, в то время как частота ТЭЛА может быть и больше, поскольку не всегда диагноз ТГВ ставится вовремя в связи с нечеткой клинической картиной заболевания[3]. В таких случаях ТЭЛА может быть первым проявлением ВТЭО.
Но даже благополучный исход острого периода не означает разрешения проблемы. В отдаленном периоде после ТГВ формируется посттромботическая болезнь нижних конечностей или хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ). В первом случае происходит глубокая дезорганизация работы венозной системы нижних конечностей с высокой вероятностью развития трофических язв и рецидива венозного тромбоза, а при ХТЭЛГ формируется правожелудочковая недостаточность, напрямую связанная с массивностью поражения легочного русла[4]. Тяжелая ХТЭЛГ в течение 5 лет приводит к смерти 10–15% больных, перенесших массивную ТЭЛА.
Одной из причин развития ВТЭО следует считать прием гормональных контрацептивов и в меньшей степени средств менопаузальной гормональной терапии (МГТ). МГТ применяется для предупреждения ряда симптомов, беспокоящих многих женщин в период менопаузы, например приливов и ночной потливости. Кроме того, доказана значительная положительная роль МГТ в профилактике остеопороза, при терапии генитоуринарного синдрома; обсуждается польза ее раннего назначения для предотвращения атеросклероза, СД и АГ, что особенно актуально ввиду доминирования сердечно-сосудистых заболеваний среди причин женской смертности.
Риск развития ВТЭО при приеме гормональных препаратов в первую очередь связан с эстрогенами. Обусловлено это тем, что они обладают вазодилатирующим эффектом, приводят к замедлению кровотока в венах[5]. Показано также, что эстрогены увеличивают концентрацию VIII фактора, снижают уровень естественного ингибитора коагуляции — антитромбина III, собственного тромболитического компонента протеина C[6] и усиливают образование тромбина, что отражается в увеличении эндогенного тромбинового потенциала[7, 8]. Однако и гестагены оказывают существенное влияние на риск венозного тромбоза. Одни из них усугубляют тромботическую активность эстрогенов, другие в этом плане более инертны. Следует сказать, что наиболее безопасными препаратами принято считать те, которые содержат минимальную дозу эстрогенов и максимально безопасный гестаген (табл. 1)[9].
Таблица 1
Риск развития венозных тромбоэмболических осложнений в зависимости от концентрации эстрогенов и вида гестагена
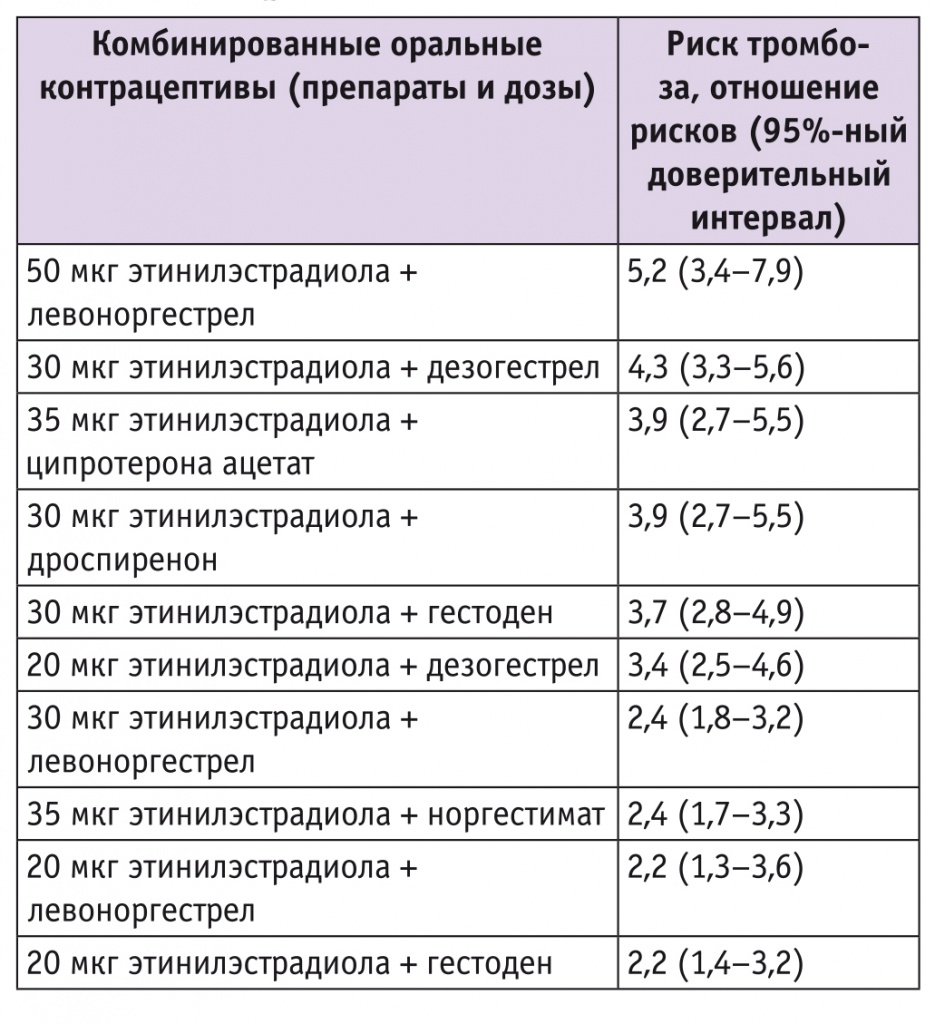
В 2015 г. Национальный институт здравоохранения и совершенствования медицинской помощи Великобритании (National Institute for Health and Care Excellence) опубликовал первые рекомендации по диагностике и лечению симптомов менопаузы в Соединенном Королевстве. Ключевым моментом была необходимость информирования женщин о рисках и преимуществах МГТ с тем, чтобы они могли сделать соответствующий выбор терапии; однако эти рекомендации относятся к применению МГТ в целом, оцениваются различия только между пероральными и трансдермальными формами препаратов[10]. В рекомендациях отмечается необходимость дальнейшего изучения рисков препаратов МГТ, содержащих разные типы прогестагенов в сочетании с эстрогенами.
Подобные рекомендации выпустили и другие организации: Международное общество по менопаузе (2016)[11], Североамериканское общество по менопаузе (2017)[12], Российское общество акушеров-гинекологов (2015)[13]. Они содержат аналогичные положения и подтверждают важность изучения рисков препаратов для МГТ. Рекомендации, вероятно, приведут к росту частоты применения МГТ у женщин с симптомами менопаузы, что повысит потребность в подробных исследованиях отдаленных рисков различных схем МГТ.
Препараты МГТ для приема внутрь могут содержать только эстроген (монотерапия), например конъюгированный лошадиный эстроген или эстрадиол, или эстроген в сочетании с прогестагеном (комбинированная терапия). Из прогестагенов в состав комбинированных препаратов входят медроксипрогестерона ацетат или более новые вещества, такие как норгестрел, дидрогестерон или дроспиренон. Предыдущие исследования, в которых оценивался риск ВТЭО, сопряженный с использованием различных средств МГТ, либо не делали различий между типами эстрогенов и прогестагенов, либо их мощности хватало только для анализа самых распространенных препаратов[14, 15].
Результаты рандомизированных контролируемых исследований, обобщенные в Кокрейновском систематическом обзоре[14], основывались главным образом на исследовании Women's Health Initiative, включавшем женщин без хронических соматических заболеваний[16]. В обзоре сказано, что повышенный риск венозных тромбозов сопряжен с приемом пероральных препаратов, содержащих только эстроген, и комбинированных препаратов для приема внутрь с конъюгированным лошадиным эстрогеном и медроксипрогестерона ацетатом.
За прошедшие 20 лет и в других странах появились новые препараты, однако в наблюдательных исследованиях этих препаратов, включенных в метаанализ, применялись различные определения исхода, и мощности этих исследований не хватало для изучения отдельных типов МГТ[15]. Таким образом, информации о риске ВТЭО, сопряженном с конкретными препаратами для МГТ, недостаточно, чтобы сделать информированный выбор препарата для лечения симптомов менопаузы.
В 2019 г. опубликованы интересные данные крупного наблюдательного исследования с участием общей женской популяции Великобритании[17]. В его основе лежал анализ сведений о 80 396 женщинах в возрасте от 40 до 79 лет, зарегистрированных в общеврачебных базах и получавших c 1997 по 2017 г. различные виды МГТ. В данном исследовании, помимо прочего, оценивались риски ВТЭО на фоне приема тех или иных гормональных препаратов.
Благодаря большому числу участниц удалось проанализировать множество моментов, ранее не известных в связи со слабой мощностью предыдущих исследований. В частности, показано, что вероятность развития венозных тромбозов ниже при применении трансдермальных форм, чем пероральных. Правда, здесь необходимо остановиться на нескольких моментах.
Во-первых, при назначении МГТ женщинам с расстройствами, обусловленными дефицитом эстрогенов, либо для профилактики остеопороза в первую очередь руководствуются не столько безопасностью, сколько эффективностью препаратов. При этом нужно учитывать, что МГТ, помимо купирования симптомов, при наличии показаний к назначению снижает смертность от ИБС и общую смертность. Иметь в виду эти дополнительные эффекты крайне важно, т.к. именно сердечно-сосудистые заболевания являются основной причиной инвалидизации и смертности женщин в постменопаузе[11, 18]. Выявлено также, что ранняя менопауза увеличивает риск АГ и инфаркта миокарда в 2 раза, а овариэктомия до 50 лет повышает частоту сердечно-сосудистых заболеваний в 4,55 раза[19].
Снижение смертности от ИБС и профилактика сердечно-сосудистых заболеваний обусловлены влиянием МГТ на липидный спектр крови и зависят от типа гормонов (эстрогена и прогестерона), дозы и пути введения. Доказано, что оральные эстрогены оказывают более выраженное положительное влияние на липидный спектр крови, т.к. при первичном прохождении через печень кривая концентрации гормонов в 4–5 раз выше, чем при парентеральном пути введения. В итоге проявляется это тем, что повышается элиминация из крови атерогенных ЛПНП, снижается индекс атерогенности и тормозится развитие атеросклероза за счет индуцированного эстрогенами увеличения на поверхности гепатоцитов количества рецепторов к ЛПНП[20].
С этих позиций крайне интересны выпущенные в 2018 г. новые рекомендации по менопаузе и СД, в которых говорится, что МГТ дает положительный эффект на гликемический профиль у женщин без СД и с СД 2 типа. Кроме того, отмечается, что своевременно начатая МГТ может отсрочить развитие СД у женщин в постменопаузе.
Наиболее важным представляется то, что именно пероральная МГТ предпочтительна для профилактики развития СД, а из доступных и максимально исследованных гестагенов в составе пероральной МГТ наиболее оправдано использование прогестерона и дидрогестерона[21].
Возвращаясь к ВТЭО, следует сказать, что, несмотря на выводы ряда исследований о большей безопасности трансдермальных форм препаратов, многие авторы отмечают, что пероральные формы тоже существенно различаются между собой в зависимости от вида эстрогена, его дозировки, а также выбора гестагена. В целом прием препаратов, содержащих конъюгированный лошадиный эстроген, сопряжен с более высоким риском по сравнению с таковым препаратов с эстрадиолом (Е2). Наибольший риск развития ВТЭО связан с применением конъюгированного лошадиного эстрогена с медроксипрогестерона ацетатом (рис. 1).
Рис. 1. Риск развития венозных тромбоэмболических осложнений в зависимости от вида эстрогена и гестагена[17], отношение шансов (95%-ный доверительный интервал).
Примечание. Здесь и в рисунках 3, 4: КЛЭ — конъюгированный лошадиный эстроген
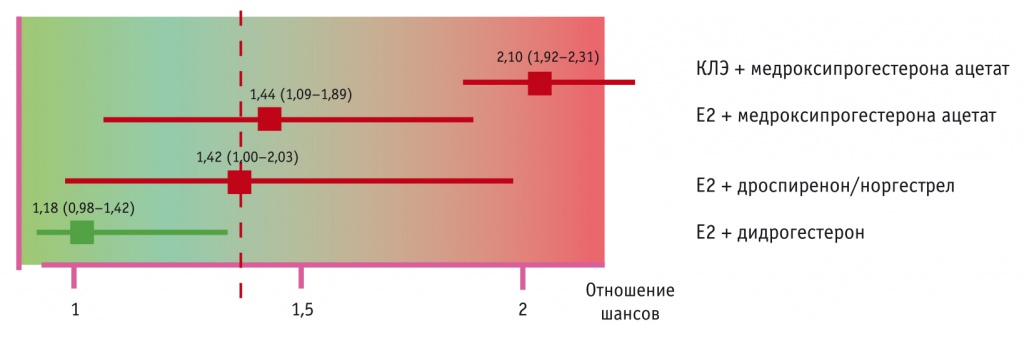
С другой стороны, комбинация эстрадиола с дидрогестероном характеризовалась минимальным риском венозных тромбозов, статистически значимо не отличавшимся от риска при использовании трансдермальных форм. Сочетания эстрадиола с дроспереноном или норгестрелом отнесли в одну группу, поскольку пациенток, принимавших МГТ с этими гестагенами, было недостаточно для отдельного статистического анализа. Авторы замечают, что в Великобритании менее 1% женщин принимают эти препараты из-за с высокого риска тромботических осложнений[17].
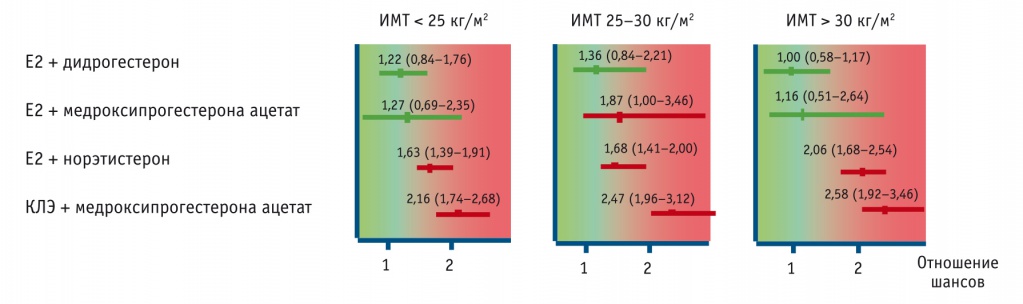
Был отмечен еще один важный момент. При применении эстрадиола с дидрогестероном риск венозных тромбозов не возрастал ни при изменении режима терапии (циклический или непрерывный), ни при увеличении возраста пациенток, ни при повышении их ИМТ (рис. 2–4).
2. Риск венозных тромбоэмболических осложнений в зависимости от режима терапии и дозировки эстрадиола с дидрогестероном[17], отношение шансов (95%-ный доверительный интервал)
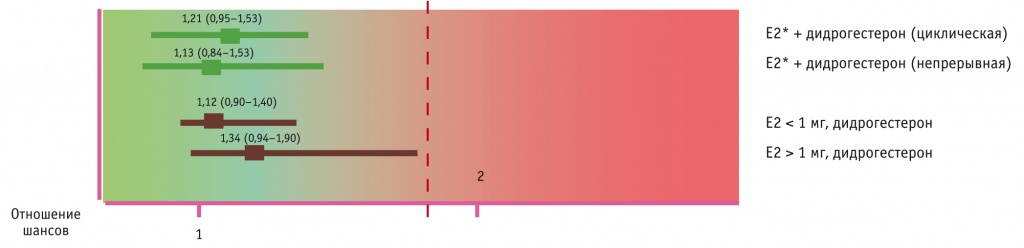
Рис. 3. Риск венозных тромбоэмболических осложнений в зависимости от возраста пациенток[17], отношение шансов (95%-ный доверительный интервал)
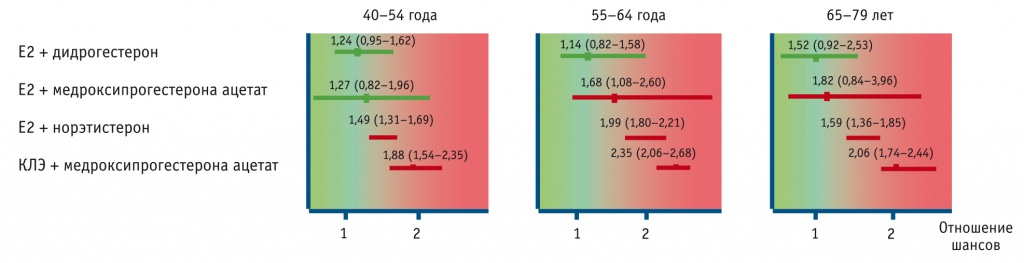
Рис. 4. Риск венозных тромбоэмболических осложнений в зависимости от индекса массы тела (ИМТ)[17], отношение шансов (95%-ный доверительный интервал)
Последнее особенно актуально, поскольку пожилой возраст и избыточная масса тела сами по себе являются отдельными независимыми и усиливающими друг друга тромбофилическими состояниями, существенно повышающими риск развития ВТЭО.
Тромбофилии могут быть как врожденными (табл. 2), так и приобретенными.
Таблица 2
Современная классификация тромбофилий. Врожденные (семейные и первичные) тромбофилии
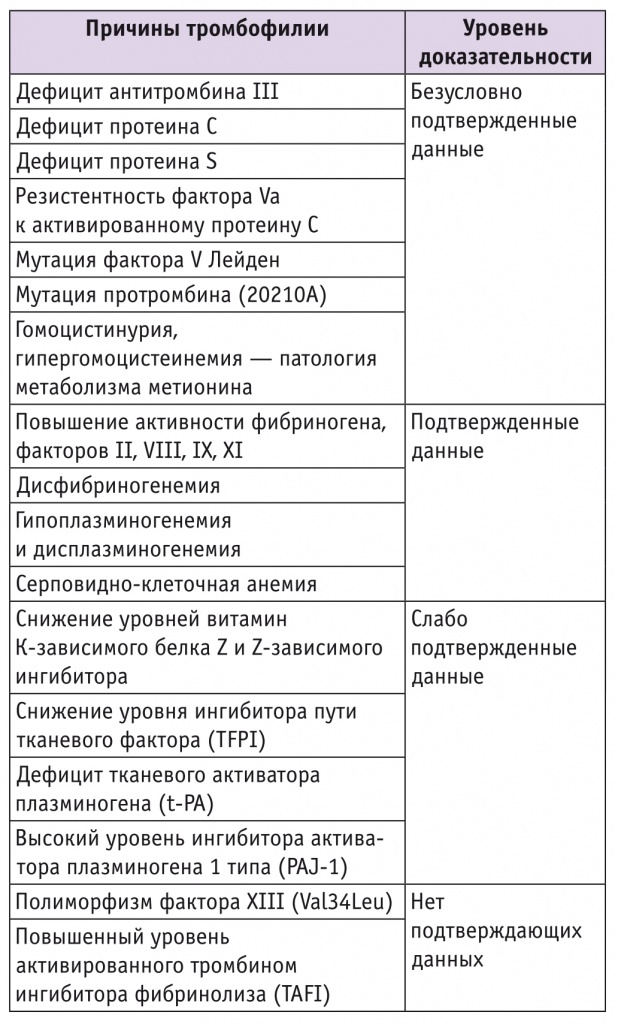
Приобретенные или вторичные тромбофилии:
- активный рак (включая миелопролиферативные и миелодиспластические заболевания);
- наличие антифосфолипидных антител в достаточном титре (волчаночных, антикардиолипиновых, анти-β2 и др.);
- аутоиммунные нарушения;
- гепарин-индуцированная тромбоцитопения;
- ночная пароксизмальная гемоглобинурия;
- инфекция (пневмония, сепсис, инфекция мочевых путей, ВИЧ);
- гипергомоцистеинемии;
- тромботическая тромбоцитопеническая пурпура;
- дислипидемия, ожирение;
- микроальбуминурия, нефротический синдром;
- обезвоживание;
- синдром диссеминированного внутрисосудистого свертывания;
- беременность, послеродовой период;
- химиотерапия;
- терапия эстрогенами или прогестероном;
- прием селективных модуляторов рецепторов эстрогена (тамоксифена и ралоксифена).
Среди врожденных тромбофилий[22] выделяют семь наиболее злокачественных (см. табл. 2). Однако если еще несколько лет назад сам по себе термин «тромбофилия» вызывал чрезмерную озабоченность клиницистов, приводящую к необоснованному длительному, а часто пожизненному, назначению антикоагулянтов, то в настоящее время подход значительно изменился. Кроме того, только гомозиготные врожденные тромбофилии несут существенный риск тромботических осложнений, а при гетерозиготных риск практически не отличается от среднестатистического в популяции.
Тем не менее следует признать, что нет возможности каким-либо образом повлиять на врожденные тромбофилии, и приходится в какой-то степени с ними «мириться». Сложнее дело обстоит с некоторыми приобретенными тромбофилиями, которые могут протекать скрыто и накапливаться в течение жизни. С другой стороны, при правильном подходе можно минимизировать или полностью устранить риск ВТЭО, обусловленный приобретенными тромбофилическими состояниями.
Одной из таких тромбофилий, помимо возраста и избыточной массы тела, является обезвоживание. В некоторых комбинированных пероральных препаратах, помимо эстрогенов, содержатся гестагены, обладающие выраженным тромбогенным эффектом, — медроксипрогестерона ацетат[19] и дроспиренон[23, 24]. Последний усиливает агрегацию тромбоцитов, что может быть причиной выраженного тромбогенного эффекта[25]. Дидрогестерон в этом плане представляется инертным, что выделяет его из всех гестагенов как препарат с минимальным риском развития ВТЭО.
Более того, некоторые авторы отмечают, что ультранизкодозированная МГТ с дидрогестероном в своем составе (0,5 мг 17β-эстрадиола + 2,5 мг дидрогестерона) приводит даже к снижению риска ВТЭО по сравнению с отсутствием МГТ за счет статистически значимого уменьшения на 16% содержания антигена ингибитора активатора плазминогена 1 и торможения тем самым тромбогенной активности[26].
ЗАКЛЮЧЕНИЕ
В настоящее время практически всеми специалистами признается важнейшая роль менопаузальной гормональной терапии (МГТ) не только в купировании симптомов дефицита эстрогенов у женщин в постенопаузе, но и в профилактике грозных осложнений у этих женщин при назначении МГТ по показаниям. Чаще всего подобные осложнения связаны с сердечно-сосудистыми заболеваниями, представляющими наибольшую опасность для жизни женщин в этом возрастном периоде. Однако осложнения, которые могут быть связаны с приемом половых гормонов, в первую очередь венозные тромбозы, нередко ограничивают применение заместительной терапии. В связи с этим ведутся исследования, направленные на снижение риска венозных тромбоэмболических осложнений (ВТЭО) при использовании различных препаратов МГТ, и достаточно часто появляются суждения, что трансдермальные формы гораздо безопаснее.
Однако и эффективность этих препаратов в профилактике СД и атеросклероза значительно ниже, чем пероральных форм. При этом соотношение пользы и риска при применении оральных препаратов во многом зависит от дозировки и вида эстрогена, а также гестагеновой составляющей.
Наибольший риск развития ВТЭО связан с использованием конъюгированного лошадиного эстрогена и более высоких доз эстрадиола. Целый ряд гестагенов, входящих в комбинированные препараты, может дополнительно стимулировать эту тромбогенную активность, что и вызывает негативное суждение о пероральной МГТ.
Но прием комбинации эстрадиола с дидрогестероном, обладающей выраженной защитной функцией от сердечно-сосудистых заболеваний, сопровождается минимальным риском ВТЭО, сравнимым с риском трансдермальных форм гормональных препаратов. Кроме того, риск развития ВТЭО может снижать ультранизкодозированная комбинация данных компонентов.
Следует признать, что правильный выбор МГТ может способствовать более широкому ее применению, позволяющему максимально снизить вероятность грозных сердечно-сосудистых событий при минимальных рисках ВТЭО.








