Эндометриоз — гормонально- и иммунозависимое, генетически обусловленное заболевание, характеризующееся доброкачественным разрастанием ткани, по морфологическому строению сходной с эндометрием, но находящейся за пределами полости матки [1–3].
Эндометриоз встречается у 6–10% женщин репродуктивного возраста [4], в основном у женщин с бесплодием — в среднем у 38% (20–50%) [5] — и с хроническими тазовыми болями (71–87%) [6]. Частота обнаружения эндометриоза при лапароскопии, в том числе проводимой с целью уточнения характера бесплодия, составляет 20–55%. Именно поэтому эндометриоз называют «упущенным» заболеванием, так как в среднем проходит от 7 до 8 лет от момента появления первых симптомов до постановки диагноза [7].
Тазовая боль, ассоциированная с эндометриозом, преимущественно включает такие типы, как дисменорея, диспареуния, дизурия, дисхезия и хроническая тазовая боль [8]. Тазовые боли по своему происхождению (сенсорному разграничению) подразделяются на соматические, висцеральные, нейрогенные. Они возникают вследствие механического или физико-химического раздражения биологически активными веществами (продуктами воспаления и повреждения тканей) болевых рецепторов внутренних органов, нервных, соматических структур и/или покрывающей их брюшины [9].
Глубокий инфильтративный эндометриоз — это специфическое состояние, характеризующееся инвазией более 5 мм эндометриоидных гетеротопий в подлежащие и рядом расположенные ткани [10, 11]. Глубокий инфильтративный эндометриоз преимущественно затрагивает Дугласово пространство, крестцово-маточные связки, ректовагинальную перегородку и сигмовидную кишку, и описанные локализации непосредственно связаны с симптомами эндометриоз-ассоциированной боли [12, 13].
Хирургическая тактика лечения должна быть в первую очередь направлена на снижение болевого синдрома, повышение качества жизни пациентки, на реализацию ее репродуктивных планов в дальнейшем.
Хирургическое иссечение очагов глубокого инфильтративного эндометриоза является эффективным вариантом лечения с целью снижения болей и повышения качества жизни [14, 15], оно рекомендовано гайдлайнами и консенсусами по эндометриозу [16, 17]. Несмотря на доказанную эффективность и значимое уменьшение болей урогенитального тракта и кишечника (дисменореи, диспареунии, дисхезии, хронической тазовой боли), полное иссечение очагов глубокого инфильтративного эндометриоза может вызывать определенные осложнения, в том числе дисфункцию мочевого пузыря, кишечника, различные сексуальные нарушения, которые иногда имеют необратимый характер [18–20]. Вышеописанные осложнения связаны с непреднамеренным повреждением нервных волокон вегетативной нервной системы, преимущественно ветвей nn. hypogastricus, которые обеспечивает иннервацию тазовых органов [15].
Зарубежные исследования показали, что нерв-сберегающая методика хирургического лечения инфильтративных форм эндометриоза, при которой выделяются и сохраняются ветви nn. hypogastricus, иннервирующие мочевой пузырь, кишечник и влагалище, может уменьшить риск послеоперационной дисфункции тазовых органов без снижения эффективности операции [21, 22].
Данный подход был впервые описан в онкологии при радикальном хирургическом лечении рака прямой кишки и шейки матки [23–25] и успешно адаптирован M. Ceccaroni для лапароскопического иссечения очагов глубокого инфильтративного эндометриоза, при его использовании меньше число висцеральных функциональных осложнений, и наблюдаются долгосрочное симптоматическое улучшение и повышение качества жизни [21, 22, 26–28].
В настоящее время в современной российской научной литературе достаточно мало данных о результатах нерв-сберегающих операций при глубоком инфильтративном эндометриозе, что послужило поводом к выполнению нашего исследования.
Цель исследования: оценка эффективности хирургического лечения нерв-сберегающим лапароскопическим методом глубокого инфильтративного эндометриоза.
Задачи исследования:
1) описать клинико-анамнестические характеристики пациенток с тяжелым инфильтративным эндометриозом;
2) представить этапы проведения лапароскопической нерв-сберегающей операции при ретроцервикальном эндометриозе;
3) сравнить результаты лапароскопического хирургического лечения глубокого инфильтративного эндометриоза нерв-сберегающим и классическим методами.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проведено в период с сентября 2016 г. по апрель 2019 г. в отделении онкогинекологии № 7 Клиники акушерства и гинекологии ФГБОУ ВО «ПСПбГМУ им. акад. И.П. Павлова» Минздрава России на базе кафедры акушерства, гинекологии и неонатологии (заведующий кафедрой — д. м. н., профессор В.Ф. Беженарь), в отделении оперативной гинекологии ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии им. Д.О. Отта» (заведующая отделением оперативной гинекологии — к. м. н. А.А. Цыпурдеева). Морфологическое и иммуногистохимическое исследования проведены на кафедре патологической анатомии с патолого-анатомическим отделением ФГБОУ ВО «ПСПбГМУ им. акад. И.П. Павлова» Минздрава России (заведующая кафедрой — д. м. н., профессор М.Г. Рыбакова).
Исследование было обсервационным продольным (лонгитюдным) проспективным в сочетании с ретроспективным.
В исследование включили 118 женщин, из них 71 составила основную группу (группу А) и 47 — контрольную группу (группу Б). Пациентки основной группы прооперированы по модифицированной нерв-сберегающей методике хирургического лечения эндометриоза, предложенной M. Ceccaroni [22], а участницы контрольной группы — классическим способом, также при лапароскопии. Согласно критериям включения, в обе группы были отобраны пациентки с IV стадией эндометриоза (по классификации эндометриоза R-AFS).
На 1-м этапе получено одобрение протокола исследования локальным этическим комитетом, у всех участниц взято информированное согласие на исследование и догоспитальное анкетирование: сбор жалоб, анамнеза, клинико-инструментальное обследование, хирургическое лечение. Интраоперационно выполнялось стадирование эндометриоза согласно классификации R-AFS, у всех пациенток диагноз подтвержден гистологически.
На 2-м этапе оценивали течение послеоперационного периода: через 6 месяцев повторно оценивали жалобы на нарушения мочеиспускания и дефекации, динамику жалоб пациенток на боли различных типов, ранние (первые сутки после операции) и отдаленные (12 месяцев) эпизоды нарушения функции мочевого пузыря и кишечника.
Этапы модификации нерв-сберегающей методики хирургического лечения ретроцервикального инфильтративного эндометриоза
Подготовка к операции обязательно включала подготовку кишечника — прием накануне пероральных слабительных препаратов. Лапароскопия выполнялась с помощью комплекта оборудования Karl Storz (Германия), в который входит интегрированный операционный комплекс с SCB управлением и HD эндокамерой.
Операции производились под эндотрахеальным наркозом. При этом выполнялась катетеризация мочевого пузыря катетером Фоллея, в шейке матки устанавливали гистерограф или манипулятор TINTARA (Karl Storz), чтобы манипулировать маткой в различных направлениях и провести хромогидротубацию маточных труб.
1-й этап. Наложение карбоксиперитонеума. Устанавливали 4 троакара в типичных местах. Первый троакар (10 мм) для оптической системы вводился в область пупка, два 5 мм троакара — в подвздошных областях, один 5 мм — над лоном.
2-й этап. Разделение спаечных сращений между органами брюшной полости и передней брюшной стенкой для лучшей визуализации. Производили разделение спаечных и физиологических сращений ректосигмоидного отдела кишечника для максимальной мобильности кишечника и временную фиксацию яичников и ректосигмоидного отдела кишечника за жировые подвески.
3-й этап. Двусторонний сальпингоовариолизис. Временная двусторонняя овариопексия.
4-й этап. Определение проекции мочеточника на стороне поражения брюшины эндометриозом. Мочеточник выделяли путем вскрытия брюшины в месте, отстоящем на 1,5–2 см от края инфильтративных изменений брюшины. Также выделяли и сохраняли симпатические волокна заднелатерального параметрия и мезоректума (нижние подчревные нервы и проксимальная часть нижнего подчревного или тазового сплетения). Уретеролизис выполняли на значительном протяжении, до перекреста мочеточника с маточной артерией.
5-й этап. Вскрытие пресакрального пространства, выделение и сохранение тазовых симпатических волокон нижнего брыжеечного сплетения, верхнего подчревного сплетения и пояснично-крестцового симпатического ствола. Этот этап начинается со вскрытия брюшины на уровне крестцового мыса. Затем, ориентируясь на брыжейку ректосигмоидного отдела кишечника, производят диссекцию, при которой кишечник смещается медиально, а нервные волокна и мышечно-фасциальные структуры крестцово-маточной связки — латерально. Далее после вскрытия верхнего параректального пространства и этапа точного определения проекции кишечника, крестцово-маточных связок и нервных волокон выполняется скелетирование нижнего гипогастрального сплетения, затем гипогастрального нерва до уровня неизмененных тканей.
6-й этап. Диссекции в латерокаудальном направлении в основании крестцово-маточных связок, выделение и сохранение каудальной части нижнего подчревного сплетения, висцеральных афферентных и эфферентных волокон матки, влагалища и мочевого пузыря.
7-й этап. Иссечение эндометриоидного инфильтрата ректосигмоидного отдела толстой кишки методом shaving.
8-й этап. Проба Мишлен (на герметичность прямой кишки).
9-й этап. Цистэктомия методом stripping.
10-й этап. Иссечение инфильтративных, поверхностных очагов эндометриоза малого таза.
11-й этап. Хромогидротубация.
12-й этап. Ревизия и санация брюшной полости.
13-й этап. Применение противоспаечного барьера.
14-й этап. Дренирование малого таза.
Статистическая обработка данных производилась в статистической программе SAS.
Для описания разных значений категориальных данных считали абсолютные частоты и проценты от количества наблюдений в группе. Обработка категориальных данных проведена с использованием таблиц частот, таблиц сопряженности, критерия χ2 или точного критерия Фишера (в случае малого числа наблюдений).
Для количественных данных выполнялась проверка распределения на нормальность с помощью критерия Колмогорова — Смирнова. Количественные нормально распределенные переменные описаны через среднее значение и стандартное отклонение; переменные, имеющие распределение, отличное от нормального, — при помощи медианы и 25-го и 75-го квантилей.
Для сравнения влияния методов лечения (в группах) по нормально распределенным данным использованы критерии ANOVA (однофакторный дисперсионный анализ), для данных, распределение которых отличается от нормального, — критерий Манна — Уитни.
Динамика для нормально распределенных данных по нескольким временны́м точкам исследована при помощи критерия АNOVA Repeated, для данных, распределение которых отличается от нормального, применялся непараметрический критерий Вилкоксона. Динамика исследовалась в каждой группе по отдельности.
Различия считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
Пациентки групп А и Б по клиническим характеристикам (возрасту, ИМТ), содержанию в венозной крови СА-125 и антимюллерова гормона, количеству предыдущих операций по поводу эндометриоза, интенсивности эндометриоз-ассоциированных болей различных типов, оцененных по визуальной аналоговой шкале (ВАШ), существенно не различались (p > 0,05, табл. 1). Отмечено значимое повышение уровня маркера СА-125, который, по данным литературы [1], не являясь чувствительным при эндометриозе (20–50%), может быть достаточно специфичным при III и IV стадии болезни (до 80%).
Таблица 1
Клинические характеристики пациенток групп А и Б
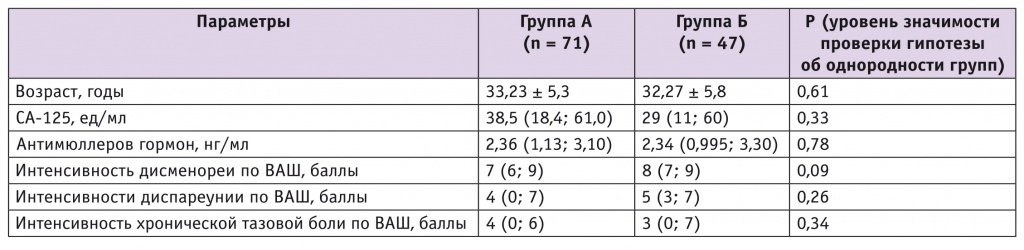
Примечание. Здесь и в таблице 3: ВАШ — визуальная аналоговая шкала.
Основной жалобой пациенток обеих групп был болевой синдром: дисменорея — у всех обследованных, диспареуния — у 50 (70,4%) женщин группы А и у 36 (76,6%) из группы Б, хроническая тазовая боль — у 47 (66,2%) и 25 (53,2%) соответственно. Нарушение менструальной функции по типу гиперполименореи встречалось у 52 (73,2%) пациенток группы А и у 33 (70,2%) группы Б, нарушение репродуктивной функции — у 34 (47,9%) и 22 (46,8%) пациенток, нарушение мочеиспускания (в дни менструации: боль, примесь крови в моче) — у 6 (8,4%) и 8 (17,0%), нарушение дефекации (преимущественно в дни менструации: кровь в стуле, боль при дефекации, жидкий, «карандашевидный» стул) — у 16 (22,5%) и 20 (42,5%) соответственно.
Группы были однородны по всем показателям, кроме нарушения дефекации до оперативного лечения: в группе Б их было значимо больше (p = 0,0006). Давность дебюта жалоб в группе А — 4 (2; 6) года, в группе Б — 7 (4; 12) лет (p = 0,002). Соотношение количества женщин, которые были прооперированы впервые или повторно по поводу эндометриоза, в группах не различалось (p = 0,13).
На догоспитальном этапе всем женщинам исследуемых групп выполнялись УЗИ органов малого таза; МРТ органов малого таза с контрастированием — 34 (47,9%) и 19 (40,4%), колоноскопия — 18 (25,3%) и 7 (15,0%) пациенткам групп А и Б соответственно. По данным УЗИ органов малого таза, инфильтративная форма эндометриоза диагностирована лишь у 3 (4,2%) и 2 (4,2%) женщин, УЗИ без патологии было у 5 (7,0%) и 5 (10,6%) участниц групп А и Б соответственно.
Преимущественно на УЗИ обнаруживались признаки аденомиоза и эндометриом яичников. По заключению МРТ органов малого таза значимо чаще (p < 0,05) были описаны инфильтративные формы эндометриоза: у 26 (76,5%) и 15 (78,9%) пациенток групп А и Б соответственно. При колоноскопии только у 3 участниц группы А были найдены косвенные признаки эндометриоза ректосигмоидного отдела толстой кишки, о чем можно было судить по наличию сдавления кишки извне.
Объем хирургического вмешательства у участниц обеих групп представлен в таблице 2.
Таблица 2
Объем хирургического вмешательства, n (%)
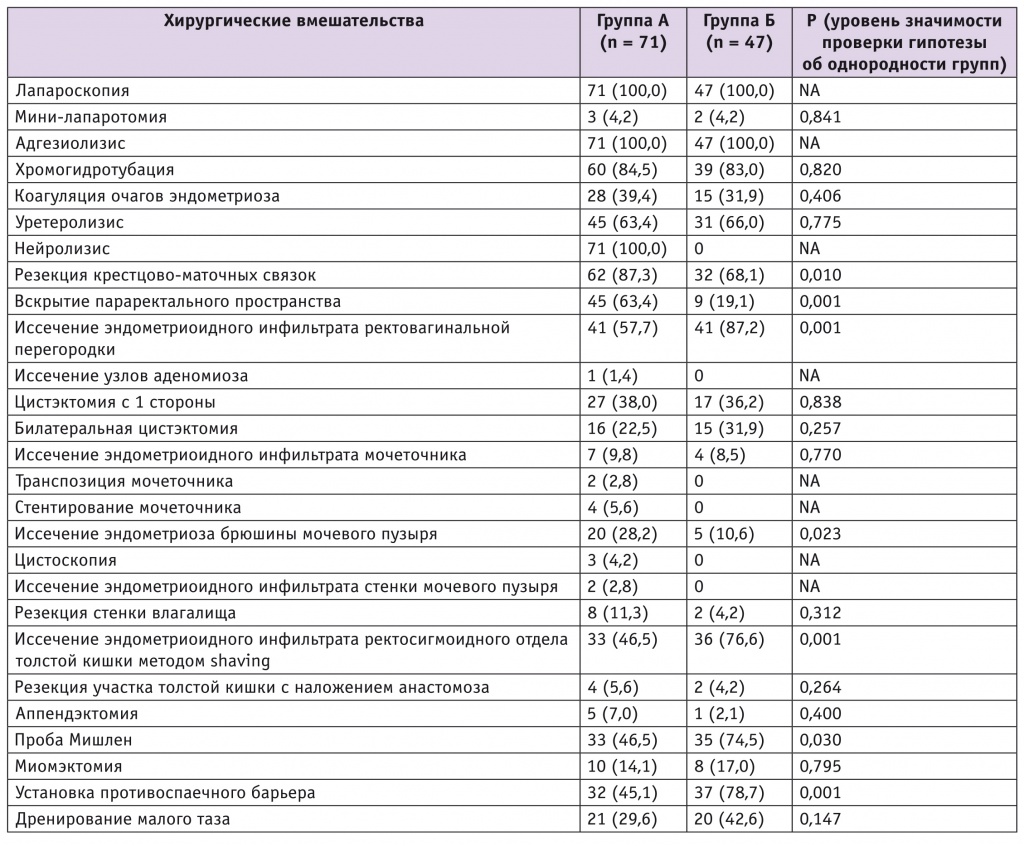
В послеоперационном периоде в каждой группе оказалось по две пациентки с послеоперационным осложнением, потребовавшим повторного оперативного вмешательства.
В группе А по сравнению с группой Б отмечены значимо меньшая кровопотеря (p = 0,012): 100 (50; 100) мл против 100 (100; 150) мл соответственно; высокозначимо меньшая продолжительность операции (p = 0,0002): 120 (85; 100) минут против 160 (147; 182) минут; а также высокозначимо меньшая длительность госпитализации (p = 00002): 7 (6; 9) против 11 (8; 12,5) койко-дней соответственно.
В послеоперационном периоде особое внимание уделялось функции мочеиспускания и дефекации, в связи с тем что при непреднамеренном пересечении ветвей сплетения nn. hypogastricus возможны эпизоды неполного опорожнения мочевого пузыря, атонии мочевого пузыря, отсутствие позывов на мочеиспускание или дефекацию.
Так, в группе А было 8 (11,3%) случаев нарушения мочеиспускания после операции (различная степень атонии мочевого пузыря), в группе Б — 14 (29,8%) (p = 0,016, точный двусторонний критерий Фишера). Нарушения дефекации после операции (отсутствие позывов на дефекацию) имели место у 9 (12,7%) пациенток группы А и у 11 (23,4%) из группы Б (p = 0,14, точный двусторонний критерий Фишера).
Длительность динамического наблюдения за пациентками составила 12 месяцев. Через 6 месяцев повторно оценивали жалобы на нарушения мочеиспускания и дефекации. В группе А у 3 (4,2%) женщин сохранялись жалобы на изменение мочеиспускания (неполное опорожнение мочевого пузыря, эпизоды отсутствия позывов к мочеиспусканию), в группе Б — у 7 (14,9%) (наблюдалась тенденция к значимому различию, p = 0,086, точный двусторонний критерий Фишера). Жалобы на отсутствие позывов к дефекации в группе А оставались у 3 (4,2%) пациенток, в группе Б — у 8 (17,0%) (p = 0,042, точный двусторонний критерий Фишера).
Через 12 месяцев после хирургического лечения производилась оценка динамики болей, ассоциированных с эндометриозом, с применением ВАШ. В обеих группах отмечалось высокозначимое снижение дисменореи, диспареунии и хронической тазовой боли (табл. 3). Однако группы А и Б не различались между собой по интенсивности снижения боли (p > 0,05).
Таблица 3
Динамика снижения эндометриоз-ассоциированной боли в группах А и Б по визуальной аналоговой шкале, баллы
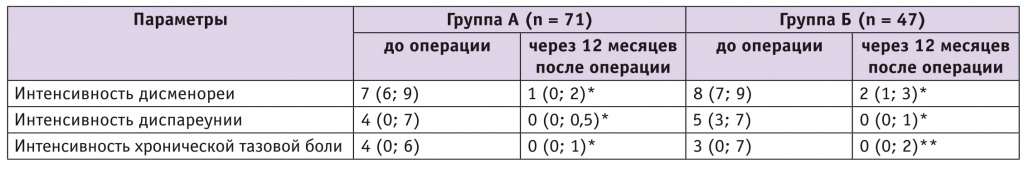
Примечание. Отличия от исходного показателя статистически значимы: (*) — р < 0,0001; (**) — р = 0,001.
ОБСУЖДЕНИЕ
Проведенное исследование показывает, что основные клинические проявления наружного генитального эндометриоза разнообразны. Высокая частота болевого синдрома и нарушения репродуктивной функции у женщин с распространенными формами эндометриоза должны быть важными критериями в дифференциальной диагностике и принятии решения об оперативном лечении.
В связи с высокой частотой экстрагенитального эндометриоза хирургическое лечение распространенных форм инфильтративного эндометриоза следует осуществлять в специализированных центрах, где также есть возможность проведения симультантной операции совместно с урологами, абдоминальными хирургами. На этапе предоперационной подготовки необходимо выполнять МРТ органов малого таза с контрастированием, при наличии показаний — колоноскопию, цистоскопию и другие дополнительные исследования ввиду их большей информативности в сравнении со стандартным УЗИ органов малого таза.
Результаты исследования говорят и о том, что хирургическое лечение инфильтративных форм эндометриоза значимо снижает интенсивность эндометриоз-ассоциированных болей и повышает качество жизни. Однако при выполнении операции по нерв-сберегающей методике отмечаются значимо меньшая частота дисфункции мочеиспускания и дефекации, связанной с пересечением ветвей nn. hypogastricus, а также более гладкое течение послеоперационного периода и меньшее количество дней пребывания в стационаре.
ЗАКЛЮЧЕНИЕ
Применение нерв-сберегающей методики хирургического лечения инфильтративных форм ретроцервикального эндометриоза позволяет улучшить течение послеоперационного периода и уменьшить количество послеоперационных осложнений на фоне значимого снижения болевого синдрома и улучшения качества жизни. Кроме того, полученные результаты позволяют рекомендовать нерв-сберегающую методику лапароскопического вмешательства как предпочтительную при выборе стратегии хирургического лечения глубокого инфильтративного эндометриоза.








