Злокачественные трофобластические опухоли (ЗТО) относятся к редким заболеваниям, составляют 1% от всей онкогинекологической патологии. Опухоли трофобласта преимущественно поражают женщин репродуктивного возраста и всегда ассоциированы с беременностью. ЗТО характеризуются чрезвычайно высокой злокачественностью, быстрым ростом и отдаленным метастазированием, частыми некрозами и кровотечением. Трофобластические опухоли высокочувствительны к противоопухолевой лекарственной терапии, являясь моделью для химиотерапии.
К настоящему времени в клинической онкологии достигнуты большие успехи в лечении пациенток с ЗТО. Так, выживаемость больных ЗТО, получивших лечение в специализированном трофобластическом центре, достигает 95–98%[1–3].
ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННЫХ ТРОФОБЛАСТИЧЕСКИХ ОПУХОЛЕЙ
В настоящее время стандартом лечения больных ЗТО является химиотерапия. Планирование химиотерапии I линии осуществляется для всех пациенток в соответствии с группой риска развития резистентности опухоли по шкале International Federation of Gynecology and Obstetrics (FIGO).
Лечение ЗТО основано на оценке факторов риска по шкале FIGO (табл.)[4]. Женщинам с низким риском (0–6 баллов) в качестве средства I линии назначается монохимиотерапия. Метотрексат или дактиномицин применяются наиболее часто. Показательно, что химиотерапия метотрексатом или дактиномицином вызывает ремиссию у 50–90% таких пациенток[5–7].
Таблица
Классификация трофобластических опухолей International Federation of Gynecology and Obstetrics и Всемирной организации здравоохранения 2003 г.[4]
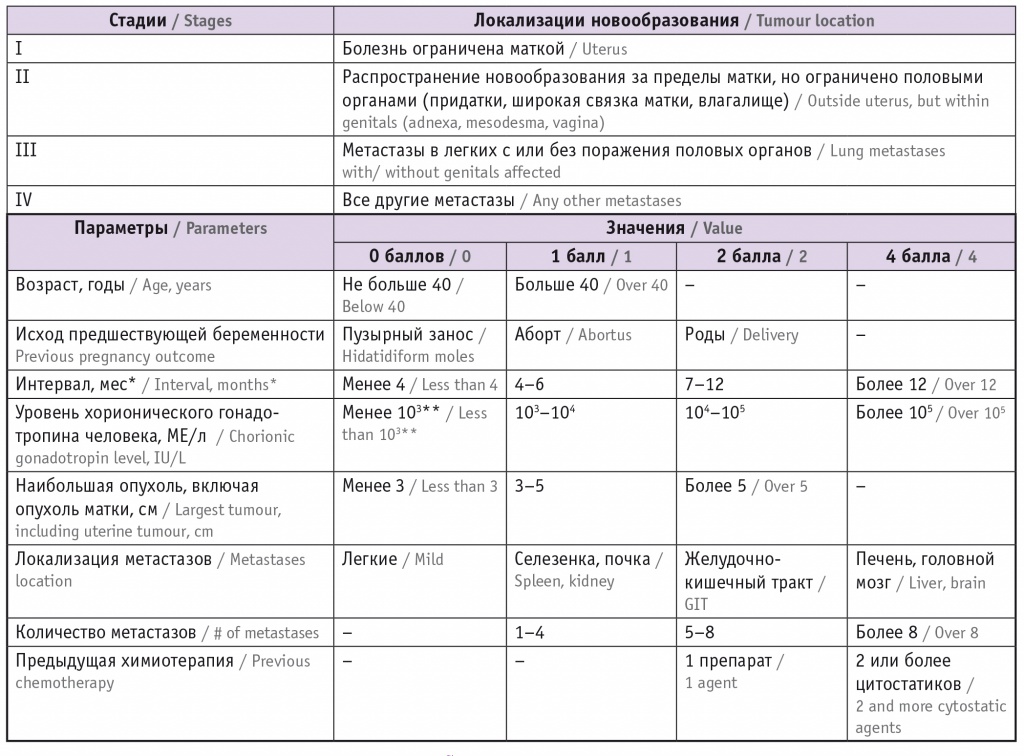
* Интервал между окончанием предыдущей беременности и началом химиотерапии.
** Низкий уровень хорионического гонадотропина человека может быть при трофобластической опухоли на месте плаценты.
Примечание. При сумме баллов 6 и менее риск развития резистентности опухоли низкий, 7 и более баллов — высокий.
Несмотря на обширный опыт лечения больных ЗТО с низким риском резистентности, накопленный за последние 50 лет, и на существование более 14 различных режимов, нет единого мнения относительно оптимальной терапии I линии. В отсутствие значительных данных, демонстрирующих явное превосходство одного метода, различия в лечении произвольно используются разными центрами.
Три основных режима, которые применяются наиболее широко:
- внутримышечное введение метотрексата в низкой дозе в течение 1 недели[8];
- импульсные дозы дактиномицина каждые 2 недели до нормализации маркера[9];
- несколько других режимов дозирования для одноразового введения метотрексата одновременно с фолиевой кислотой (кальция фолинат) и без нее[10].
Недавнее рандомизированное исследование Gynecologic Oncology Group показало, что двухнедельное внутривенное введение дактиномицина в дозе 1,25 мг/м статистически значимо превосходило по эффективности недельное внутримышечное введение метотрексата (30 мг/м) в группе с низким риском по оценке ВОЗ (0–4 балла): полный ответ был у 70% против 53%[11]. Однако оба режима оказались менее эффективными, если риск превышал 5 или 6 баллов, а также у больных с хориокарциномой[12].
Сравнивая затраты на различные схемы, N.T. Shah и соавт. создали модель дерева решений, описанную в Руководстве по анализу затрат Национального информационного центра по исследованиям в области медицинских услуг и технологий здравоохранения. Авторы пришли к выводу, что 8-дневный режим введения метотрексата/Fa по сравнению с еженедельным введением метотрексата или импульсным введением дактиномицина является наименее затратным[13].
Эффективность использования метотрексата/кальция фолината у больных с низким риском резистентности, по данным различных авторов, варьирует от 75% до 90%[2, 3].
Резистентность трофобластических опухолей подразумевает лекарственную устойчивость опухоли к стандартной химиотерапии I линии. Самые ранние критерии резистентности ЗТО: плато или снижение уровня ХГЧ менее 10%, зафиксированное при трех последовательных исследованиях в течение 10 дней; увеличение уровня ХГЧ во время или по окончании химиотерапии (до 6 месяцев), зафиксированное при трех последовательных исследованиях в течение 10 дней.
По мнению ряда авторов[14, 15], пациентки с низким риском и резистентностью к монохимиотерапии обычно могут достичь ремиссии в результате применения комбинированной химиотерапии либо режима MAC (метотрексат, дактиномицин и циклофосфамид) или EMA-CO (этопозид, метотрексат, дактиномицин, циклофосфамид и винкристин). MAC предпочтительнее в качестве исходной комбинированной химиотерапии, так как этопозид повышает риск возникновения вторичных опухолей, в частности его использование ассоциировано с 1%-ным риском развития лейкемии[14, 15].
Относительный риск лейкемии, меланомы, рака толстой кишки и рака молочной железы был увеличен на 16,6%, 3,4%, 4,6% и 5,8% соответственно у пациенток, получавших этопозид в дозировке более 2 г/м2[16].
Известно, что резистентность к лекарственным средствам и рецидив чаще встречаются у пациенток с высоким риском[16]. Недавние исследования показали, что количество консолидирующих курсов, исходный уровень ХГЧ, стадия заболевания и более высокий риск по шкале ВОЗ, как представляется, предрасполагают к рецидиву и лекарственной устойчивости[17, 18]. Среди пациенток с низким уровнем риска, получавших 3 консолидирующих курса метотрексата, рецидивов ЗТО были значительно меньше, чем у женщин, получивших 2 курса (4,0% против 8,3% случаев)[18].
В настоящее время принято считать основным клиническим признаком эффективности лечения трофобластических опухолей прогрессивное снижение сывороточного уровня β-ХГ. Плато или увеличение концентрации ХГЧ в процессе химиотерапии свидетельствует о развитии резистентности трофобластической опухоли.
Ведущую роль в лечении больных трофобластическими опухолями играет химиотерапия I линии, в результате которой излечивается большинство пациенток. Пятидесятилетний опыт применения современных стандартных режимов химиотерапии I линии в мире показал прекрасные результаты: приближающуюся к 100% выживаемость больных с низким риском резистентности опухоли и более 90% больных с высоким риском. Однако до сих пор существует проблема резистентности трофобластических опухолей. Ее частота, по данным разных зарубежных клиник, варьирует от 11% до 32%[19].
Лечение резистентной опухоли с помощью современных режимов химиотерапии у пациенток с низким риском в настоящее время является высокоэффективным. Достижение полного выздоровления женщин с высоким риском и развившейся резистентностью опухоли до сих пор остается серьезной проблемой и требует поиска новых эффективных комбинаций химиотерапии, оптимизации с помощью дополнительного хирургического лечения[19].
Пациентки с суммой баллов 7 и более по шкале FIGO относятся к группе высокого риска. В качестве режима I линии у них применяется схема ЕМА-СО.
Режим MAC неприменим в качестве I линии при наличии метастазов у пациенток с высоким риском, он приводит к ремиссии только у 50%[22, 23]. M. Bower и соавт. указывают, что EMA-CO индуцирует полную ремиссию у 86% пациенток с метастазами, а G. Bolis и соавт. — у 76%[22, 23].
У таких женщин выше риск развития резистентности, поэтому им требуется комбинированная химиотерапия для достижения ремиссии. Ранее для лечения ЗТО у больных с высоким риском использовались различные комбинации:
- режим ЕМА/СО применялся еженедельно, чаще, чем все остальные;
- ЕМА (метотрексат, этопозид, дактиномицин) имеет сравнительные показатели эффективности, но более низкую токсичность, чем режим ЕМА-СО;
- MAC или комбинация метотрексата, дактиномицина и хлорамбуцила;
- FA (5-фторурацил, дактиномицин) или FAV (5-фторурацил, дактиномицин, винкристин) обычно используются в Китае;
- MEF (метотрексат, этопозид, 5-фторурацил);
- EMA/EP (этопозид, метотрексат, дактиномицин/этопозид, цисплатин), при этом EMA и EP чередуются еженедельно;
- CHAMOCA (метотрексат, дактиномицин, циклофосфамид, доксорубицин, мелфалан, гидроксимочевина, винкристин) является более токсичным и менее эффективным, чем MAC, и его заменили на EMA/CO[24].
Редкие трофобластические опухоли: опухоль плацентарного ложа и эпителиоидная трофобластическая опухоль — оказались менее чувствительны к стандартной химиотерапии, чем инвазивный пузырный занос или хориокарцинома, поэтому они чаще рецидивируют.
На первом этапе лечения опухоли плацентарного ложа A.N. Gordon и соавт. рекомендуют выполнение гистерэктомии с селективной тазовой лимфодиссекцией и последующим применением адъювантной химиотерапии у женщин с метастатическими очагами[24].
J.R. Lurain и B. Nejad провели систематический обзор литературы о применении химиотерапии при ЗТО у женщин с высоким риском и не смогли сформулировать никаких выводов о наилучшем режиме I линии химиотерапии (EMA/CO
по сравнению с CHAMOCA). EMA/CO — наиболее широко применяемая схема в качестве I линии химиотерапии ЗТО с высоким риском, однако у 30–40% женщин развивается резистентность или рецидивы после ремиссии, в связи с чем они нуждаются в химиотерапии спасения[25].
Химиотерапия спасения при ЗТО и высоком риске резистентности представляет собой гораздо более сложный клинический сценарий, чем химиотерапия спасения при ЗТО низкого риска.
Факторы риска резистентности к лечению в группе высокого риска включают количество и локализацию метастазов (метастазы в головном мозге, печени и ЖКТ ухудшают прогноз), предшествующую химиотерапию, хирургическое лечение и возраст пациентки. Есть высокая вероятность, что больным, подвергшимся нестандартному лечению, не поможет химиотерапия спасения. Поэтому гистерэктомия и другие вспомогательные методы играют важную роль в лечении этих женщин. В литературе[11] сообщается о нескольких режимах спасения, в основном в небольших сериях исследований, в том числе:
- EMA/EP;
- BEP (блеомицин, этопозид, цисплатин);
- VBP или PVB (цисплатин или карбоплатин, винбластин, блеомицин);
- VIP или ICE (ифосфамид, этопозид, цисплатин);
- EP (этопозид, цисплатин);
- TP/TE (паклитаксел, цисплатин/паклитаксел, этопозид), ТР и ТЕ чередуются еженедельно;
- FAEV (флоксуридин, дактиномицин, этопозид, винкристин) каждый 21 день.
Приблизительно у 90% пациенток с высоким риском, первоначально получавших EMA/CO, а затем спасительную химиотерапию с комбинацией цисплатина и этопозида, выживаемость лучше, чем у больных, не получавших данные схемы[11].
В трех сериях исследований эффективность режима EMA/EP после EMA/CO составляет 75% (9 из 12 пациенток), 66,7% (12 из 18 женщин) и 84,6% (11 из 13 женщин). Однако применение режима EMA/EP было связано со значительной миелосупрессией и гепатотоксичностью, приводящей к задержкам в лечении и коррекции дозы вводимых препаратов. Миелосупрессия может быть минимизирована путем введения гранулоцитарно-колониестимулирующего фактора (G-CSF)[2].
Установлено, что схема TP/TE сравнима с ЕМА/ЕР по эффективности (70% из 10 пациенток, которые не получили предшествующее лечение в режиме ЕР, были излечены), но имеет относительно небольшую токсичность, поэтому при ней отсутствуют задержки или редукция дозы[7].
В некоторых регионах Китая предпочтение отдается режимам с включением 5-фторурацила. S. Yingna и соавт. рассмотрели 222 пациенток и выявили, что 5-фторурацил эффективен в первичном лечении женщин с ЗТО низкого и высокого риска (с ремиссиями у 99% и 84% участниц соответственно), за исключением пациенток со множественными метастазами[26].
5-фторурацил также использовался как средство терапии спасения в японском исследовании. Показано, что он хорошо переносится и способствует излечению 8 из 10 пациенток (80%) в течение одного года; но в 2 из 8 наблюдений впоследствии развились рецидивы; эти больные были излечены с помощью режима MEA[26].
Режим BEP используется как спасительная терапия при резистентности ЗТО к 5-фторурацилу, и сообщается о частоте ремиссии 80% (10 из 12) при высоком риске.
В одном из обзоров, включавшем 91 пациентку с резистентными или рецидивирующими ЗТО и с высоким риском, которые получили лечение до начала химиотерапии спасения, сообщалось об эффективности применения режима FAEV в 60,4% случаев и о 75%-ной трехлетней общей выживаемости. Сообщенная миелосупрессия при режиме FAEV была ниже, чем при EMA/EP и TP/TE. Характеристики пациенток в данных сериях исследований широко варьируют в зависимости от типа и количества предыдущих режимов химиотерапии (FAEV, EMA-CO, EP) показателей риска и других факторов (см. табл.), поэтому прямые сравнения их результатов не дают убедительных данных относительного эффекта[3].
Для небольшой группы пациенток с резистентностью к режиму EMA/CO нет общепринятой схемы лечения.
Гистерэктомия может быть эффективной для уменьшения числа курсов химиотерапии, и хирургическая резекция метастатических очагов поможет достичь ремиссии, если обнаружено одно метастатическое поражение[27].
В ретроспективном анализе S.J. Kim и соавт. сравнили применение четырех режимов у пациенток со множественной лекарственной устойчивостью: MFA (метотрексат, кальция фолинат, дактиномицин), MAC, CHAMOCA (метотрексат, дактиномицин, циклофосфамид, доксорубицин, мелфалан, гидроксикарбамид и винкристин) и EMA-CO — и обнаружили, что частота ремиссии составила 63%, 68%, 71% и 91% соответственно [8].
Пациенток с ЗТО, устойчивой к режиму ЕМА-СО, можно лечить, заменяя цисплатин и этопозид в 8-й день лечения (EMA-EP)[23, 26] и проводя EMA в 1-й день. Этопозид и дактиномицин во 2-й день повторно не вводили. Благодаря применению режима EMA-EP в сочетании с хирургическим вмешательством была достигнута индуцированная ремиссия у 16 из 21 (76,2%) пациентки с резистентностью к режиму ЕМА-СО[23].
Комбинированную химиотерапию проводят с перерывом в 2–3 недели, не допуская токсичность, до нормализации уровня ХГЧ при трех последовательных измерениях[9, 23]. После нормализации концентрации ХГЧ проводятся 3–4 дополнительных курса химиотерапии для снижения риска рецидива. Другие режимы были также эффективны при лечении резистентных ЗТО высокого риска, включая ВЕР (блеомицин, этопозид, цисплатин), ICE (ифосфамид, цисплатин, этопозид) и VIP (этопозид, ифосфамид, цисплатин)[28–31].
Хирургическое вмешательство при ЗТО применяется для лечения осложнений основного заболевания либо для удаления резистентных к химиотерапии очагов болезни[32]. R.M. Clark и соавт.[33] сообщили о результатах лечения 98 пациенток, перенесших гистерэктомию при ЗТО. Двадцать пять (76%) из 33 пациенток, которым выполнялась гистерэктомия для лечения резистентных опухолей, достигли полной ремиссии[33].
С.В. Hammond и соавт.[34] сообщили, что у пациенток, перенесших гистерэктомию, были меньше сроки госпитализации и химиотерапии, чем у тех, кому гистерэктомию не производили.
S. Yingna и соавт.[26] пишут, что у 18 (35,3%) из 51 пациентки с вагинальными метастазами развилось кровотечение. Кровотечение контролировалось тампонированием влагалища у 16 пациенток и ангиографической эмболизацией у двух. K.Y. Tse и соавт.[35] в 20-летнем ретроспективном исследовании подтвердили, что ангиографическая эмболизация, по-видимому, была перспективной альтернативой гистерэктомии и перевязки маточных артерий.
Торакотомия играет ограниченную, но важную роль в лечении резистентных ЗТО III стадии. Торакотомия (торакоскопия) должна выполняться при сомнительном диагнозе. Кроме того, если у больной есть резистентный метастаз в легком, ей показана резекция легкого с лечебной целью[36]. Однако необходимо провести комплексное обследование, чтобы исключить другие резистентные очаги опухоли. Важно подчеркнуть, что фиброзные узелки могут длительно сохраняться на рентгенограмме грудной клетки после нормализации уровня ХГЧ[37]. Если на рентгенограмме постоянно выявляются метастатические очаги, которые вызывают сомнение, нужно выполнить ПЭТ-КТ. Данное исследование также может быть полезно для выявления отдаленных метастазов[38].
Y. Tomoda и соавт.[39] рассмотрели свой опыт легочной резекции у 19 пациенток с резистентной к химиотерапии ЗТО. Они предложили следующие критерии успешной резекции: соматический статус не отягощен, течение ЗТО контролируется, нет других метастатческих очагов, уровень ХГЧ менее 1000 мМЕ/мл. Полная ремиссия достигнута у 14 из 15 пациенток, которые соответствовали всем пяти критериям.
Аналогично E.L. Fleming и соавт.[14] сообщили, что 10 (90,9%) из 11 тщательно отобранных пациенток с резистентными легочными очагами достигли ремиссии после их резекции. По данным нескольких исследователей, нормализация уровня ХГЧ в течение 1–2 недель после резекции одиночного легочного узла достаточна для благоприятного исхода[39–45].
Пациентки с IV стадией заболевания являются группой крайне высокого риска при прогрессировании ЗТО. Этим больным требуются высокодозная комбинированная химиотерапия с локальным облучением и хирургическое вмешательство. По данным NETDC[46], до 1975 года выжили только 30% пациенток с IV стадией. После 1975 года применение ранней интенсивной комбинированной химиотерапии способствовало значительному улучшению выживаемости. В настоящее время 80% женщин с IV стадией заболевания достигают полной стойкой ремиссии.
У всех пациенток с IV стадией ЗТО проводится первичная комбинированная химиотерапия в режиме EMA-CO. Когда присутствуют метастазы в ЦНС, доза однодневного введения метотрексата увеличивается до 1 г/м2[46, 47]. Если обнаружены церебральные метастазы, по мнению K. Brace, следует немедленно проводить облучение (NETDC). Одиночные церебральные очаги можно облучить локально или удалить, если они расположены по периферии. Однако наличие множественных очагов требует облучения всего мозга. Риск спонтанного кровоизлияния в мозг снижается при одновременном применении химиотерапии и облучении головного мозга[48].
E.L. Yordan Jr и соавт.[49] отметили, что из 25 пациенток, получавших только химиотерапию, вследствие вовлечения ЦНС умерли 11 (44%), а из 18 женщин, проходивших облучение мозга и химиотерапию, не умерла ни одна.
Но есть данные больницы Чаринг-Кросс в Лондоне о превосходных показателях ремиссии у больных с метастазами в головном мозге, которые лечились только химиотерапией[46].
Тридцать (85,7%) из 35 пациенток с церебральными поражениями достигли стойкой ремиссии с помощью интенсивной комбинированной химиотерапии, включавшей внутривенное и интратекальное введение метотрексата в высокой дозе, без облучения мозга.
Редко метастазы в головном мозге, которые оказываются резистентными к химиотерапии, могут поддаваться резекции. C.M. Feltmate и соавт.[50] пишут о полной ремиссии у 3 из 4 пациенток, которые подверглись краниотомии с целью уменьшить внутричерепное давление, а также у 2 из 3 женщин, которым делали краниотомию для резекции резистентного очага. А. Athanassiou и соавт.[51] тоже свидетельствуют, что 4 из 5 пациенток, подвергшихся краниотомии при острых внутричерепных осложнениях, были в итоге излечены без остаточного неврологического дефицита.
Лечение метастазов в печени является особенно важным и сложным. Резекция печени может потребоваться для контроля кровотечения из опухоли или резистентности к проводимой химиотерапии. F.C. Grumbine и соавт.[21] описывают выполнение избирательной окклюзии печеночной артерии с одновременной комбинированной химиотерапией у пациентки с кровоточащими метастазами в печени, которая впоследствии достигла ремиссии. С.М. Wаng и соавт.[3] отмечают, что 9 из 10 больных с вовлечением печени достигли полной ремиссии при помощи первичной интенсивной комбинированной химиотерапии. Y.N. Bakri и соавт.[52] также сообщили, что 5 (62,5%) из 8 женщин с метастазами в печени, которые получали комбинированную химиотерапию, достигли полной ремиссии.
По данным НМИЦ онкологии им. Н.Н. Блохина[4], из 342 больных, получавших химиотерапию I линии современными стандартными режимами, у 40 (11,7%) развилась резистентность опухоли. Из 260 больных с низким риском резистентности у 20 (7,7%) все же возникла резистентность к химиотерапии I линии: 18 пациенток исходно имели единственную локализацию опухоли в полости матки, у 1 больной был метастаз во влагалище, у 1 пациентки — множественные мелкие метастазы в легких.
Химиотерапию II линии все 20 женщин получали в следующем режиме: дактиномицин 500 мкг в/в струйно в 1–5-й дни с повторением курсов с 15-го дня. В результате у 16 (80%) женщин достигнута полная маркерная ремиссия. Для ее достижения потребовалось от 1 до 6 курсов (в среднем 3 курса). Дополнительное лечение пациентки не получали. Общая продолжительность терапии данных больных варьировала от 3,5 до 6 месяцев, составляя в среднем 4,5 месяца. Все пациентки излечены только с помощью химиотерапии.
При выявлении резистентности первичной опухоли и пересчете суммы баллов по шкале FIGO 1 пациентке назначена химиотерапия в режиме ЕМА-СО. Больная излечена.
В 3 наблюдениях при резистентности первичной опухоли матки для достижения ремиссии потребовалось проведение химиотерапии III линии в режиме ЕМА-СО, а у одной из них дополнительно удалена остаточная опухоль матки (гистерорезектоскопия).
Таким образом, все пациентки группы низкого риска с развившейся резистентностью опухоли, излечены.
В группе высокого риска резистентности у 20 (24,4%) из 82 больных развилась резистентность опухоли к химиотерапии I линии. Следует отметить, что 16 (80%) из 20 женщин с развившейся резистентностью опухоли ранее (в других лечебных учреждениях) подверглись нестандартному лечению (химиотерапия от 1 до 10 курсов и различные оперативные вмешательства). У всех 20 пациенток по поводу резистентности опухоли начата химиотерапия II линии: 16 — режим ЕМА-ЕР, 4 — различные другие режимы: PVB, ЕР, ТР/ТЕ.
Только с помощью химиотерапии удалось вылечить лишь 3 больных. Остальным 17 женщинам с резистентностью потребовалось комбинированное лечение. В качестве дополнительного лечения удалена опухоль у 11 больных (матка, придатки, легкое, стенка двенадцатиперстной кишки), лучевая терапия проведена 5 и более двух линий химиотерапии — 5 больным.
Следует отметить, что данная группа из 17 пациенток характеризуется самым неблагоприятным прогнозом. Впервые были использованы новые высокоэффективные режимы химиотерапии (FAMtx, TP/TE и др.), стереотаксическое облучение резистентных метастазов опухоли, эндоскопическая операция при удалении резистентных очагов в легких, органосохраняющая гистеротомия, стереотаксическая радиохирургия резистентных метастазов в головном мозге (гамма-нож). В результате из 17 больных у 13 (76,5%) с помощью комбинированного лечения достигнута полная ремиссия.
Таким образом, в результате лечения пациенток группы высокого риска с резистентностью к стандартной химиотерапии выздоровели 16 (80%) из них.
Частота рецидивов трофобластических опухолей варьирует от 3% до 8%, у больных группы высокого риска резистентности — до 20%.
По данным отечественных авторов[1, 4], из 345 больных, получивших лечение в НМИЦ онкологии им. Н.Н. Блохина в 1996–2013 гг., рецидивы заболевания диагностированы у 16 (4,6%).
Среди 260 больных группы исходно низкого риска резистентности после достижения маркерной ремиссии и консолидирующих курсов химиотерапии у 5 (1,9%) пациенток диагностирован рецидив болезни. Их возраст варьировал от 25 до 42 лет, составляя в среднем 34 года. Предшествующая беременность завершилась пузырным заносом в 3 наблюдениях, инвазивным пузырным заносом — в 1 наблюдении, самопроизвольным абортом — в 1 случае. Исходный уровень ХГЧ у 4 больных был в диапазоне от 25 000 до 82 000 мМЕ/мл, у 1 пациентки — 600 мМе/мл. У всех больных опухоль локализовалась только в матке, размеры опухоли — от 2 до 3,5 см. Все пациентки в качестве химиотерапии I линии получали метотрексат/кальция фолинат (Лейковорин). Все рецидивы излечены с помощью химиотерапии II линии дактиномицином[4].
Из 85 больных группы высокого риска развития резистентности (средний возраст — 34 года) у 11 (13%) также диагностирован рецидив болезни. Чаще всего исходом предшествующей беременности были роды. У 7 из 11 пациенток зафиксированы редкие морфологические формы опухоли. В 90% наблюдений исходно диагностирован распространенный опухолевый процесс. Только 1 пациентка с рецидивом ЗТО излечена с помощью химиотерапии. Всем остальным больным потребовалось дополнительное лечение: удаление рецидивной опухоли, лучевая терапия или радиохирургия. Несмотря на потенциально плохой прогноз в данной группе больных, нам удалось достичь излечения 9 (81,8%) из 11 пациенток. У 3 больных впервые в клинической практике достигнута ремиссия при метастазировании резистентной трофобластической опухоли в головной мозг благодаря дополнительной радиохирургии (гамма-нож)[4].
D.G. Mutch и соавт. сообщили о рецидивах после первоначальной ремиссии у 2% пациенток с неметастатическими ЗТО, у 4% с метастатическими ЗТО с хорошим прогнозом и у 13% женщин с плохим прогнозом[18]. Рецидивы развивались в течение 3 (85%) и 18 месяцев (50%).
По данным NETDC, рецидив после начальной ремиссии наблюдался у 2,9% пациенток на I стадии, у 8,3% на II стадии, у 4,2% на III стадии и у 9,1% на IV стадии[53]. Все пациентки с I, II и III стадией ЗТО, у которых развился рецидив, впоследствии были излечены, тогда как две пациентки на IV стадии с рецидивами умерли.
N.Y. Ngan и соавт.[46], описывая свой 20-летний опыт лечения ЗТО в Гонконге, заметили, что средний интервал от ремиссии до рецидива составил 6,5 месяцев. Они пришли к выводу, что наиболее важные факторы риска рецидива имели место у пациенток, которые не соблюдали режим лечения или наблюдения, а также у тех, у кого был диссеминированный опухолевый процесс.
ЗАКЛЮЧЕНИЕ
Недостаточно успешное лечение пациенток с резистентными формами трофобластической опухоли диктует необходимость оптимизации ранней топической диагностики, внедрения в практику новых эффективных режимов химиотерапии, иммунотерапии, радиохирургии.
Поступила: 20.12.2019
Принята к публикации: 23.12.2019








