Ишемическая болезнь сердца (ИБС) является главной причиной преждевременной смерти и утраты трудоспособности в экономически развитых странах, в том числе в Российской Федерации (Росстат, 2017) [1]. Основными задачами при лечении ИБС являются устранение симптомов заболевания (эпизодов ишемии миокарда в виде приступов стенокардии или ее эквивалентов) и замедление прогрессирования атеросклеротического процесса с целью профилактики грозных осложнений — инфаркта миокарда (ИМ), недостаточности кровообращения и внезапной сердечной смерти [2–4].
Эффективность и необходимость комбинированной медикаментозной терапии (МТ) в решении этих задач не вызывают сомнений. Для профилактики прогрессирования атеросклероза и снижения риска осложнений назначают антиагреганты (ацетилсалициловую кислоту или клопидогрел, в ряде случаев комбинацию антиагрегантов), статины, при необходимости с присоединением эзетимиба или ингибиторов проконвертазы 9, для достижения целевого уровня холестерина липопротеидов низкой плотности, а также препараты, блокирующие активность ренин-ангиотензинной системы, — ингибиторы ангиотензинпревращающего фермента, а при их непереносимости блокаторы ангиотензинных рецепторов [2, 3]. Терапия, направленная на устранение ишемических проявлений заболевания (стенокардии и/или безболевой ишемии миокарда), включает применение бета-блокаторов, блокаторов кальциевых каналов, пролонгированных нитратов, ингибитора If-каналов клеток синусового узла (ивабрадин), цитопротективных препаратов (триметазидин), ингибитора позднего натриевого тока (ранолазин) и активатора калиевых каналов (никорандил), в том числе в различных комбинациях.
При недостаточной эффективности антиангинальной терапии рекомендуются инвазивные методы лечения. Представления о роли чрескожного коронарного вмешательства (ЧКВ) и подход к отбору пациентов для интервенционного лечения изменяются по мере совершенствования техники вмешательства и появления новых данных. Современное понимание вопросов, связанных с эндоваскулярным лечением ИБС, отражено в обновленных клинических рекомендациях по реваскуляризации миокарда (КРМ-2018) Европейского кардиологического общества (англ. European Society of Cardiology, ESC) и Европейской ассоциации кардиоторакальной хирургии (англ. European Association for Cardio-Thoracic Surgery, EACTS) [5].
Целью обзора является освещение основных положений обновленных клинических рекомендаций по реваскуляризации миокарда, касающихся чрескожных коронарных вмешательств при стабильной ишемической болезни сердца.
Важной позицией КРМ-2018 является расширение показаний к выполнению ЧКВ: в соответствии с современными представлениями эндоваскулярное лечение способно улучшить прогноз у большего числа пациентов со стабильной ИБС, чем предполагалось ранее (рис. и раздел «Показания к чрескожному коронарному вмешательству: улучшение прогноза»).
Рис. Новые позиции в рекомендациях по реваскуляризации миокарда по классам доказательности [5].
Примечание. ИБС — ишемическая болезнь сердца; ЛКА — левая коронарная артерия; ОКС — острый коронарный синдром; ФВ ЛЖ — фракция выброса левого желудочка; ЧКВ — чрескожное коронарное вмешательство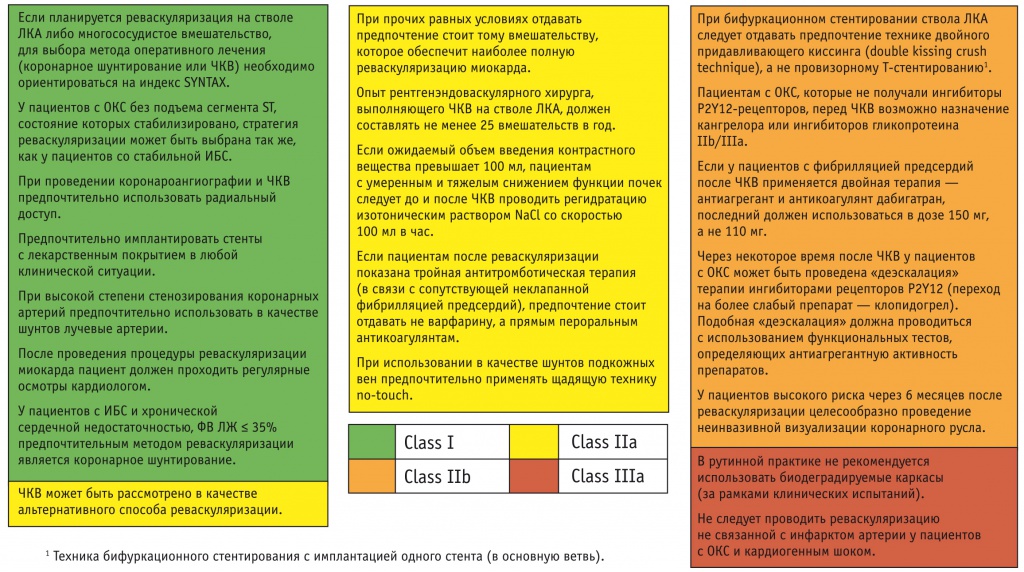
Выбор тактики ведения должен осуществляться кардиокомандой и учитывать мнение пациента. Основными ориентирами в определении способа лечения являются полнота достигаемой реваскуляризации и расчетный индекс по шкале SYNTAX.
Другие изменения затрагивают аспекты, связанные с подготовкой пациента к ЧКВ, с МТ после процедуры, техникой вмешательства: при проведении коронарной ангиографии и ЧКВ рекомендуется использовать радиальный доступ, при бифуркационном поражении предпочтительным признается провизорное стентирование (метод бифуркационного стентирования с имплантацией одного стента) и пр.
ПОКАЗАНИЯ К ЧРЕСКОЖНОМУ КОРОНАРНОМУ ВМЕШАТЕЛЬСТВУ: УЛУЧШЕНИЕ ПРОГНОЗА
В ранних (до 2010 г.) исследованиях по изучению влияния инвазивного лечения на прогноз при стабильной ИБС (COURAGE, MASS, MASS II, RITA 2, BARI-2D, OAT и др.) улучшение прогноза в результате реваскуляризации было показано у пациентов с поражением ствола левой коронарной артерии; при трехсосудистом поражении коронарного русла, особенно со снижением глобальной сократимости миокарда; при двухсосудистом поражении коронарного русла, если одно из поражений включает проксимальный отдел передней нисходящей артерии (ПНА); при проксимальном поражении ПНА; при значительной зоне ишемизированного миокарда, выявляемой в ходе нагрузочного тестирования (> 10% миокарда). В соответствии с КРМ-2018 в случаях однососудистого поражения, а также двух- и трехсосудистого поражения коронарного русла при риске по шкале SYNTAX в пределах 22 баллов выполнение ЧКВ сохраняет класс рекомендаций I.
В остальных случаях до недавнего времени достоверных прогностических преимуществ устранения преходящей ишемии при стабильной ИБС выявлено не было. Подобные результаты объяснялись тем, что ЧКВ не оказывает непосредственного влияния на субстрат острого коронарного синдрома (ОКС): точка приложения ЧКВ при стабильной ИБС — гемодинамически значимая, преимущественно стабильная атеросклеротическая бляшка, а морфологический субстрат развития ОКС — нестабильная атеросклеротическая бляшка, в значительном числе случаев не имеющая гемодинамической значимости и не способная вызывать ишемию миокарда, стенокардию.
Однако некоторые предпосылки для отрицательного результата могут быть обнаружены в особенностях методологии этих исследований. Так, в аналитическом обзоре 10 рандомизированных клинических исследований (ACME 1, ACME 2, RITA 1, RITA 2, MASS I, MASS II, AVERT, ACIP, COURAGE, FAME 2), проводившихся до 2011 г. (196 433 пациента), показано, что 30% больных с верифицированной ишемией миокарда были исключены по ангиографическим критериям, у 20% включенных пациентов с гемодинамически значимыми стенозами коронарной артерии не было подтвержденной преходящей ишемии [6]. Вместе с тем в КРМ-2018 подчеркивается значимость инструментально подтвержденной преходящей ишемии миокарда и полной реваскуляризации (при многососудистом поражении коронарного русла) для улучшения клинической симптоматики и прогноза при проведении ЧКВ.
Связь полной реваскуляризации с улучшением прогноза показана в ряде исследований последних лет. По данным ретроспективного анализа результатов исследования SYNTAX (2647 пациентов после эндоваскулярного и хирургического лечения ИБС), через 5 лет наблюдения в группе пациентов с полной реваскуляризацией констатировано статистически значимо меньше осложнений, чем у больных, у которых не были скорректированы все имевшиеся на момент включения ангиографически выявленные стенозы (> 50% поперечного сечения в любой проекции) коронарных артерий (> 1,5 мм) [7]. Наличие резидуальных стенозов, оценивавшихся по шкале SYNTAX от 0 до 8 баллов, приводило к увеличению числа повторных ЧКВ; превышение 8 баллов по SYNTAX ассоциировалось также со статистически значимым увеличением смертности и количества сердечно-сосудистых и цереброваскулярных осложнений.
В метаанализе результатов рандомизированных и обсервационных клинических исследований (89 883 пациента) отмечено уменьшение риска отдаленных неблагоприятных исходов: смерти (ОР = 0,71; 95%-й ДИ [0,65–0,77]; p < 0,001), ИМ (ОР = 0,78; 95%-й ДИ [0,68–0,90]; p = 0,001), повторных ЧКВ (ОР = 0,74; 95%-й ДИ [0,65–0,83]; p < 0,001) — среди больных, у которых была достигнута полная реваскуляризация [8].
Более того, в метаанализе 2015 г., включившем 25 наблюдательных исследований, показано, что реваскуляризация хронических тотальных окклюзий может приводить к улучшению не только клинической симптоматики, но и прогноза при наблюдении в течение 3 лет [9].
В отсутствие верификации ишемии миокарда при проведении неинвазивной нагрузочной пробы для определения показаний к ЧКВ могут быть применены методы оценки функциональной значимости стеноза коронарных артерий, измерение фракционного резерва кровотока (ФРК), моментального резерва кровотока, а также неинвазивно определяемого КТ-ФРК (класс рекомендаций I при ангиографически пограничном стенозе и IIа при многососудистом поражении коронарного русла) [5].
В исследовании FAME 2 пациенты с однососудистым поражением коронарного русла и стенокардией напряжения (n = 888) были рандомизированы в группы МТ и МТ + ЧКВ с имплантацией стента с лекарственным покрытием (СЛП) при ФРК ≤ 0,80. Улучшение клинических исходов (уменьшение количества неотложных ЧКВ, смертности, числа ИМ, событий комбинированной конечной точки) в группе ЧКВ было показано на различных сроках наблюдения — от 7 месяцев (4,3% против 12,7%; ОР = 0,32; 95%-й ДИ [0,19–0,53]; p < 0,001) до 5 лет (13,9% против 27,0%; ОР = 0,46; 95%-й ДИ [0,34–0,63]; p < 0,001) [10].
Выполнение ЧКВ при стабильной ИБС с однососудистым поражением коронарного русла при ФРК ≤ 0,80 с целью улучшения прогноза имеет в КРМ-2018 класс рекомендаций I.
Большое значение в дальнейшей судьбе пациента после ЧКВ имеет тип имплантированного стента. В течение последнего десятилетия широко применяются СЛП, значительно повысилась эффективность МТ, сопровождающей ЧКВ, а также направленной на коррекцию факторов риска (появились новые антиагрегантные препараты, мощные статины, к которым при необходимости могут быть присоединены эзетимиб или ингибиторы проконвертазы 9), пересмотрены целевые значения показателей артериального давления, липидного профиля и т. д. Совершенствование технологии эндоваскулярного лечения и прогресс в лечении ИБС в целом способствуют повышению эффективности ЧКВ не только в устранении стенокардии, но и в улучшении прогноза у пациентов.
По результатам метаанализа S. Windecker и соавт. (2014), включившего 95 исследований (93 553 пациента, 262 090 пациенто-лет), ЧКВ в дополнение к МТ с применением СЛП второго поколения при стабильной ИБС способствует достоверному улучшению показателей выживаемости по сравнению с МТ (эверолимус: ОШ = 0,75; 95%-й ДИ [0,59–0,96]; зотаролимус: ОШ = 0,65; 95%-й ДИ [0,42–1,00]) [11].
Кроме того, с целью снижения риска осложнений, связанных с имплантацией СЛП, в долгосрочном прогнозе предпринимались попытки создания биодеградируемых каркасов (БДК). Существует два типа БДК: с биорастворимым полимером (период растворения до 3–4 лет) и с биорастворимым металлическим (магниевым) остовом без полимера (растворение в течение 1 года). В рандомизированных исследованиях изучен только стент с биорастворимым полимером Absorb (Abbott Vascular), уступающий современным СЛП в отношении как эффективности, так и безопасности. Показано, что в сравнении с СЛП имплантация стента Absorb сопровождается увеличением риска повторной реваскуляризации и тромбоза (последний происходит у каждого 40–60-го пациента) [12, 13]. Применение стентов Absorb было остановлено в 2017 г. Результаты использования магниевых БДК, полученные в небольших обсервационных исследованиях, представляются обнадеживающими; необходимо их дальнейшее изучение на большем массиве данных.
В соответствии с КРМ-2018 БДК не должны применяться вне контролируемых клинических исследований; у пациентов, которым БДК были установлены ранее, может быть обоснованным назначение двойной антиагрегантной терапии в течение 3 и более лет. СЛП имеют приоритет в любых клинических ситуациях, включая необходимость сокращения сроков двойной антитромботической терапии.
ПОКАЗАНИЯ К ЧРЕСКОЖНОМУ КОРОНАРНОМУ ВМЕШАТЕЛЬСТВУ: УСТРАНЕНИЕ СИМПТОМОВ
Согласно КРМ-2018 лимитирующая стенокардия напряжения на фоне оптимальной антиангинальной МТ остается в числе основных показаний к проведению ЧКВ при стабильной ИБС [2, 3].
Преимущество МТ в сочетании с ЧКВ перед МТ в устранении преходящей ишемии миокарда (стенокардии) показано в большинстве исследований, как в самых ранних, когда в качестве основного метода эндоваскулярного лечения применялась транслюминальная баллонная коронарная ангиопластика с имплантацией голометаллических стентов (RITA 2, TIME, SWISSI II, ACIP, BARI, MASS II, COURAGE и др.), так и в относительно недавних, проведенных во время, когда широкое распространение получили СЛП (FAME 2, SYNTAX, FREEDOM, EXCEL). Бóльшая эффективность ЧКВ в сравнении с консервативной тактикой в отношении устранения или значительного уменьшения частоты ангинозных приступов отмечалась при разной продолжительности наблюдения (до 10–15 лет), различных локализации стенозов, распространенности поражения коронарного русла, а также степени реваскуляризации (табл.) [3].
Таблица
Исследования по сравнению эффективности чрескожного коронарного вмешательства и медикаментозной терапии [3]
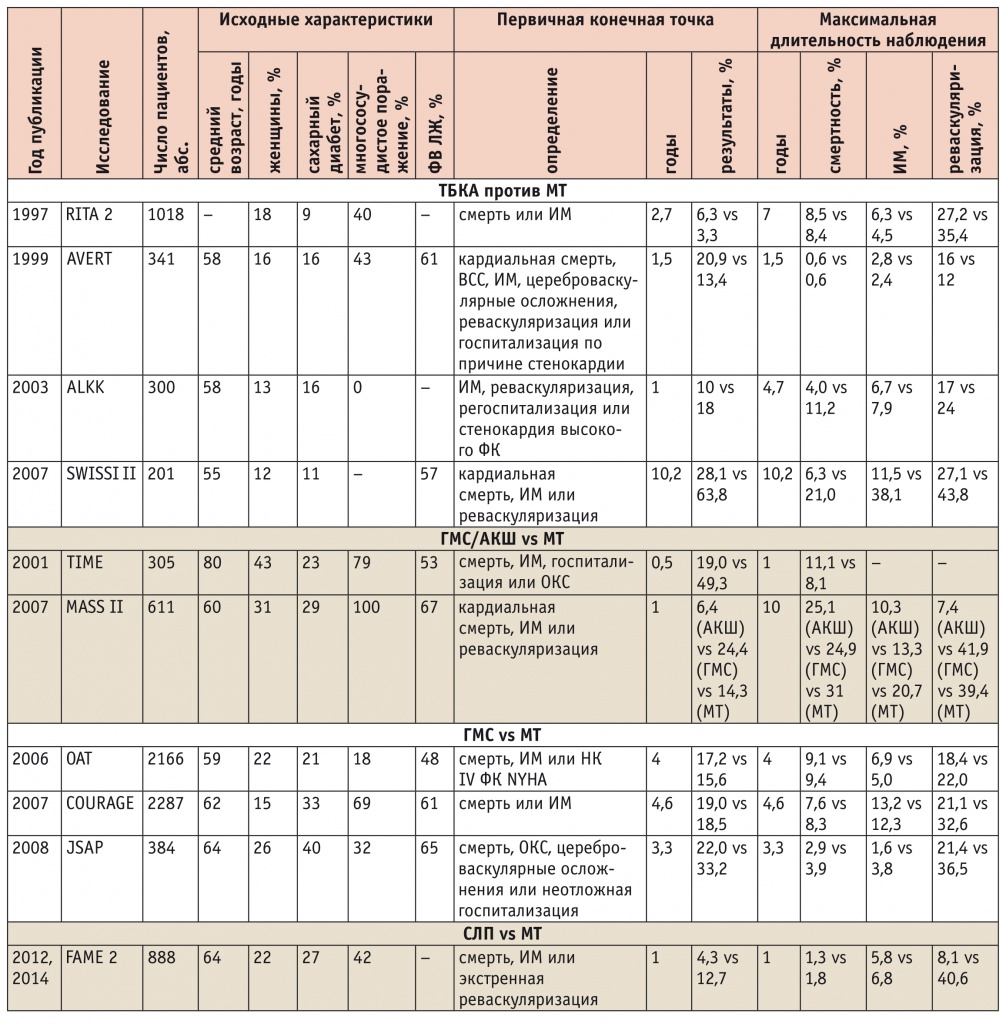
Примечание. АКШ — аортокоронарное шунтирование; ВСС — внезапная сердечная смерть; ГМС — голометаллические стенты; ИМ — инфаркт миокарда; МТ — медикаментозная терапия; НК — недостаточность кровообращения; ОКС — острый коронарный синдром; СЛП — стенты с лекарственным покрытием; ТБКА — транслюминальная баллонная коронарная ангиопластика; ФВ ЛЖ — фракция выброса левого желудочка; ФК — функциональный класс; NYHA — New York Heart Association (Нью-Йоркская кардиологическая ассоциация).
Вместе с тем степень антиангинальной эффективности ЧКВ при стабильной ИБС была предметом дискуссий.
В 2017 г. были опубликованы результаты многоцентрового (5 центров в Великобритании) исследования ORBITA, включившего 230 больных стабильной стенокардией с однососудистым поражением коронарного русла [14]. Важной особенностью этого первого в истории ЧКВ плацебо-контролируемого исследования стала рандомизация в группы ЧКВ и имитации процедуры для исключения возможного плацебо-эффекта эндоваскулярного лечения ИБС. Оценивались (клинически и инструментально) преимущества процедуры ЧКВ на фоне оптимальной МТ (в среднем каждому пациенту были назначены два антиангинальных препарата), коррекция МТ проводилась в течение 6 недель до вмешательства. Перед рандомизацией во всех случаях выполнялось определение ФРК, однако этот показатель не был учтен при распределении в группы инвазивного и консервативного лечения. Через 6 недель после вмешательства (или его имитации) статистически значимые различия между группами эндоваскулярного лечения и плацебо были отмечены только при проведении добутаминовой стресс-Эхо-КГ: после ЧКВ индекс сократимости миокарда улучшился в статистически значимо большей степени, чем при плацебо-вмешательстве, разница в изменении функционального класса, а также показателей тредмил-теста носила характер выраженной тенденции.
Ценность данного исследования заключается в том, что его авторами впервые обсуждается необходимость рандомизированных исследований с помощью двойного слепого метода для оценки эффективности ЧКВ. Эта концепция получила развитие в недавнем обзоре плацебо-контролируемых исследований по изучению различных вмешательств при стабильной стенокардии напряжения (лигирование внутренней грудной артерии, трансмиокардиальная лазерная реваскуляризация при хронический окклюзии, перкутанная миокардиальная лазерная реваскуляризация, имплантация устройств в коронарный синус с целью повышения коронарной перфузии) [15]. Кроме того, из результатов исследования ORBITA может быть сделан вывод о целесообразности не только ангиографической, но и функциональной оценки значимости стенозов.
ВЫБОР СПОСОБА РЕВАСКУЛЯРИЗАЦИИ, ИЛИ РОЛЬ КАРДИОКОМАНДЫ
Выбор способа реваскуляризации должен осуществляться кардиокомандой, или консилиумом в составе кардиолога, эндоваскулярного хирурга и кардиохирурга, с учетом мнения пациента и основываться на оценке соотношения потенциальной пользы и риска возможных осложнений.
Польза от реваскуляризации напрямую зависит от ее полноты и, в меньшей степени, от способа реваскуляризации. Так, анализ данных Нью-Йоркского регистра (9223 сопоставимых пары пациентов, подвергавшихся либо хирургическому лечению, либо ЧКВ с имплантацией СЛП нового поколения) не показал статистически значимых различий по влиянию на прогноз ЧКВ и аортокоронарного шунтирования (АКШ) при полной реваскуляризации [16]. Сходные результаты получены в метаанализе исследований SYNTAX, BEST и PRECOMBAT (3212 пациентов в общей сложности) [17].
Вместе с тем при анализе исходов у пациентов по критерию наличия сахарного диабета (n = 7040; период наблюдения — 5 лет) показатели общей смертности в группе АКШ оказались ниже, чем при выполнении ЧКВ (10,0% против 15,5%; ОР = 1,48; 95%-й ДИ [1,19–1,84]; p = 0,0004; p для взаимодействия = 0,045) [18]. В метаанализе исследований SYNTAX и BEST (1275 пациентов, период наблюдения — 5 лет) более благоприятный отдаленный прогноз в отношении смертности, ИМ, повторных реваскуляризаций при хирургической тактике, чем при ЧКВ (7,1% vs 11,6%; p = 0,02), отмечен и у пациентов со сложным поражением коронарного русла при суммарном балле по шкале SYNTAX более 22–23 [19].
Риск хирургического лечения может быть оценен с помощью STS — Шкалы оценки хирургического риска, связанного с АКШ (класс I), и EuroSCORE II — Шкалы оценки риска при кардиохирургических вмешательствах (класс IIb), однако существенное их ограничение заключается в отсутствии установленных значений, превышение которых соответствует низкой смертности. Риск осложнений при проведении ЧКВ для всех пациентов, подвергаемых коронарной ангиографии, в КРМ-2018 предлагается оценивать по шкале SYNTAX.
Шкала SYNTAX (http://www.syntaxscore.com) создана в ходе проспективного наблюдения за пациентами одноименного исследования для оценки анатомической сложности поражения коронарного русла у больных с вовлечением ствола или многососудистым стенозированием коронарных артерий. В исследовании SYNTAX, а также других валидирующих исследованиях суммарный балл по шкале SYNTAX являлся независимым предиктором развития серьезных кардиальных и цереброваскулярных осложнений и смерти у пациентов в группе ЧКВ при длительном наблюдении [20].
В исследовании SYNTAX нижний и средний терцили распределения баллов соответствовали пациентам с сопоставимыми результатами ЧКВ и АКШ, верхний терциль — пациентам, для которых прогностически более благоприятно выполнение АКШ [21]. В последующих рандомизированных клинических исследованиях эти результаты не имели статически значимого характера. Однако в недавнем метаанализе, включившем 11 518 пациентов, уровень значимости различий (p) составил 0,0011 [22]. Необходимо учитывать и ограничения шкалы SYNTAX: значительную вариабельность экспертных заключений (ситуация может быть улучшена при регулярном применении шкалы), а также снижение предсказующей ценности в отношении риска смерти и других сосудистых осложнений у пациентов промежуточного и низкого риска и при выборе тактики лечения у пациентов с сахарным диабетом.
В соответствии с КРМ-2018 аргументами в пользу проведения ЧКВ являются пожилой возраст пациента, низкая ожидаемая продолжительность жизни, наличие коморбидных заболеваний, которые не учитываются в шкалах для оценки риска хирургических осложнений, но ухудшают прогноз или осложняют процесс реабилитации, а также повышают сложность и риск АКШ («фарфоровая аорта», состояние после облучения грудной клетки).
Преимущество АКШ показано у пациентов с сахарным диабетом, а также при высоком риске эндоваскулярного лечения (SYNTAX > 23 баллов, выраженный кальциноз); выбор хирургического лечения может быть обоснован наличием противопоказаний к приему двойной антиагрегантной терапии, необходимостью одномоментного выполнения кардиохирургической операции, выраженным снижением насосной функции сердца (фракция выброса < 35%).
В целом проведение ЧКВ сопровождается более быстрым восстановлением и меньшим риском осложнений (в том числе острого нарушения мозгового кровообращения) на ранних сроках; АКШ ассоциируется с улучшением долгосрочного прогноза, уменьшением риска ИМ и повторных реваскуляризаций.
ЗАКЛЮЧЕНИЕ
В обновленных клинических рекомендациях по реваскуляризации миокарда Европейского кардиологического общества и Европейской ассоциации кардиоторакальной хирургии сформулированы основные критерии отбора пациентов для инвазивного лечения. Совершенствование техники эндоваскулярного лечения ишемической болезни сердца (ИБС) и расширение арсенала средств медикаментозной терапии способствуют повышению эффективности чрескожного коронарного вмешательства (ЧКВ) и расширению показаний к нему. Все шире применяются методы оценки функциональной значимости стеноза, методы внутрисосудистой визуализации. При стентировании рекомендовано применение только стентов с лекарственным покрытием. Показано, что с помощью ЧКВ можно не только устранять приступы стенокардии, но и улучшать прогноз у многих пациентов со стабильной ИБС.








