Вальпроевая кислота (ВК) и ее производные являются эффективными лекарственными средствами первого ряда для лечения различных форм эпилепсии [1]. Частота назначения препаратов ВК в Красноярском крае составляет 60,85%, что статистически значимо (р < 0,05) выше этого показателя по другим противоэпилептическим препаратам (ПЭП)[2, 3]. Повышение эффективности и безопасности лечения эпилепсии препаратами ВК представляет актуальную задачу реальной клинической практики. Нежелательные реакции (НР), индуцированные приемом препаратов ВК, могут развиваться со стороны различных органов и систем[4]. По данным Неврологического центра эпилептологии, нейрогенетики и исследования мозга Университетской клиники (НЦ УК) Красноярского государственного медицинского университета имени профессора В.Ф. Войно-Ясенецкого, наиболее часто наблюдаются НР со стороны желудочно-кишечного тракта и ожирение (у 15,25% и 13,49% пациентов соответственно). НР со стороны ЦНС отмечены суммарно у 15,10% пациентов; такие НР представлены энцефалопатией (5,28%), аггравацией приступов (5,13%), когнитивными нарушениями (3,23%), сонливостью (1,47%), тремором кистей рук (7,48%). НР со стороны психоэмоциональной сферы — раздражительность, агрессия (1,76%) и эмоциональные расстройства, депрессия (1,32%). Повысить безопасность терапии эпилепсии за счет снижения частоты развития НР ПЭП возможно на основании результатов терапевтического лекарственного мониторинга (ТЛМ) вальпроатов и учета носительства полиморфизмов гена СYР2С9, ассоциированных с изменением скорости метаболизма ВК в печени. Такой подход лежит в основе персонализированного применения препаратов ВК в реальной клинической практике[5, 6]. Достижение запланированного положительного результата лечения требует выполнения определенной хронологической последовательности действий, но словесное описание такой последовательности часто бывает нечетким, имеет смысловую перегруженность и приводит к дефектам оказания специализированной неврологической помощи рассматриваемой категории пациентов. Избежать этого позволяет использование алгоритмов в виде наглядных блок-схем на основе общепризнанных визуальных алгоритмических языков[7, 8].
Цель исследования: разработать алгоритм персонализированного назначения препаратов вальпроевой кислоты пациентам, страдающим эпилепсией, и его графическую визуализацию.
МАТЕРИАЛЫ И МЕТОДЫ
Проведен анализ безопасности лечения в случайной выборке из 263 пациентов, страдающих эпилепсией и получающих ВК в виде монотерапии или в составе комбинированного медикаментозного лечения в дозе не более 1250 мг/сут.
Пациенты составили две группы без статистически значимых межгрупповых различий (р > 0,05). В контрольную группу были включены 96 больных, которым препараты ВК назначались по стандартной схеме без проведения ТЛМ и фармакогенетического тестирования. Все они имели ВК-индуцированные НР, доза ВК корректировалась эмпирически. В основную группу вошли 167 пациентов. Всем участникам этой группы были проведены обследование на носительство однонуклеотидных полиморфизмов (ОНП) CYP2C9*2 и CYP2C9*3, ассоциированных с замедлением метаболизма ВК в печени, а также ТЛМ ВК и оценка НР. Основная группа была разделена на две подгруппы в зависимости от наличия или отсутствия НР: в первой подгруппе (n = 99; 59,28%) были выявлены НР на фоне приема ВК; во второй (n = 68; 40,72%) НР не регистрировались. В обеих подгруппах дозу ВК снижали при развитии НР либо обнаружении токсических концентраций ВК в крови; скорость титрования дозы ВК зависела от носительства ОНП CYP2C9*2 и CYP2C9*3 гена CYP2C9, результатов ТЛМ ВК. Блок-схемы алгоритмов построены в программе Microsoft Visio 2013 по ГОСТ 19.701-90 [7]. ТЛМ ВК в крови проводили на базе центральной научно-исследовательской лаборатории (ЦНИЛ) КрасГМУ им. проф. В.Ф. Войно-Ясенецкого, в лаборатории НИИ медицинских проблем Севера (г. Красноярск). Концентрацию ВК в плазме крови определяли методом высокоэффективной жидкостной хроматографии. Референсные значения этого показателя составляли 50–100 мкг/мл. Молекулярно-генетические исследования выполнены на базе межкафедральной лаборатории медицинской генетики кафедры медицинской генетики и клинической нейрофизиологии Института последипломного образования и ЦНИЛ КрасГМУ им. проф. В.Ф. Войно-Ясенецкого. Методом полимеразной цепной реакции в режиме реального времени исследовали следующие ОНП гена CYP2C9 на хромосоме 10q24.1–24.3: распространенный полиморфизм (дикий тип) CYP2C9*1; минорные ОНП (мутантного типа) CYP2C9*2 (R144C, c.430 С>Т), CYP2C9*3 (I359L, c.1075 А>С). После этого в зависимости от генотипа уточняли тип метаболизма ВК: CYP2C9*1/*1 — экстенсивный метаболизатор; CYP2C9*1/*2, CYP2C9*1/*3 — медленный метаболизатор; CYP2C9*2/*2, CYP2C9*3/*3 и CYP2C9*2/*3 — сверхмедленный метаболизатор. Тип метаболизма определяет скорость биотрансформации ВК в печени: у экстенсивных метаболизаторов этот показатель находится в пределах нормы, у медленных метаболизаторов он снижен на 25–30%, а у сверхмедленных — на 50% и более. Статистическая обработка данных проведена с помощью программы Statistica v. 6.1 (StatSoft, США). Для сравнения и оценки выявленных различий использовали непараметрический критерий хи-квадрат Пирсона (χ2) с процедурой попарного сравнения (Мараскуило). Различия расценивали как статистически значимые при p < 0,05. Отношение шансов (ОШ) рассчитывали по формуле:
ОШ = (a/c)/(b/d) = a × d/b × c,
где:
a — число лиц, находившихся под воздействием изучаемого фактора, у которых развились НР;
b — число лиц, находившихся под воздействием изучаемого фактора, у которых не развились НР;
c — число лиц, не находившихся под воздействием изучаемого фактора, у которых развились НР;
d — число лиц, не находившихся под воздействием изучаемого фактора, у которых не развились НР.
ОШ > 1 свидетельствовало о прямой связи фактора с вероятностью наступления исхода; ОШ < 1 — об обратной связи.
РЕЗУЛЬТАТЫ
Установлено, что среди 99 пациентов основной группы с ВК-индуцированными НР (подгруппа 1) медленные и сверхмедленные метаболизаторы встречаются статистически значимо чаще, чем экстенсивные (62,63% и 37,37% соответственно; р < 0,05), так же как и количество пациентов, имеющих токсические концентрации ВК в крови, больше количества пациентов с концентрациями ВК в рамках терапевтического коридора (64,65% и 35,35%; р < 0,05). У больных без НР (подгруппа 2) токсические концентрации ВК в крови регистрировались статистически значимо реже, чем у пациентов с НР (23,53% и 64,65% соответственно; р < 0,05). Частота встречаемости медленных и сверхмедленных метаболизаторов во второй подгруппе составила 32,35% против 62,63% в первой подгруппе (р < 0,05). Расчет ОШ продемонстрировал, что как наличие токсической концентрации ВК в крови пациента, так и отнесение пациента к группе медленных и сверхмедленных метаболизаторов по носительству СYР2С9*2 и/или СYР2С9*3 имеет прямую ассоциативную связь с вероятностью развития НР: ОШ = 5,94 и 4,27 соответственно. Частота проведения ТЛМ зависела от типа метаболизма: у экстенсивных метаболизаторов (CYP2C9*1/*1) ТЛМ ВК проводился 2 раза в год; у медленных метаболизаторов (CYP2C9*1/*2 или CYP2C9*1/*3) — 4 раза в год; у сверхмедленных метаболизаторов (CYP2C9*2/*2, CYP2C9*3/*3, CYP2C9*2/*3) — 6 раз в год. На основании полученных результатов корректировали применение ВК: уменьшали суточную дозу при развитии токсических концентраций, снижали темп ее наращивания у медленных и сверхмедленных метаболизаторов. Подбор доз ВК на основании данных ТЛМ привел к тому, что у экстенсивных метаболизаторов средняя доза ВК составила 1250 ± 105 мг/сут, у медленных метаболизаторов — 900 ± 84 мг/сут, у сверхмедленных — 600 ± 55 мг/сут. В контрольной группе все пациенты получали ВК в среднем в дозе 1250 ± 124 мг/сут. Оценка частоты регистрации НР через 12 месяцев от начала исследования в основной группе (персонализированный подбор дозы) показала, что доля пациентов с НР сократилась с 59,28% (99/167) до 10,78% (18/167). Это статистически значимо ниже (χ2 = 16,78; р < 0,05), чем в контрольной группе, где при эмпирической тактике дозирования ВК доля пациентов с НР снизилась со 100% (96/96) до 37,50% (36/96). Полученные данные о более высокой безопасности тактики ведения пациентов с эпилепсией с использованием нового подхода, основанного на результатах фармакогенетического тестирования и ТЛМ, явились основанием для разработки в НЦ УК КрасГМУ им. проф. В.Ф. Войно-Ясенецкого алгоритма персонализированного назначения препаратов ВК. Графическая визуализация этого алгоритма представлена на рисунках 1–4.
Рис. 1. Алгоритм персонализированного назначения препаратов вальпроевой кислоты (начало).
Примечание. На рис. 1–4: ВК — вальпроевая кислота; ЛП — лекарственный препарат; НР — нежелательная реакция; ОНП — однонуклеотидный полиморфизм; ПЭП — противоэпилептический препарат; УДХК — урсодезоксихолевая кислота
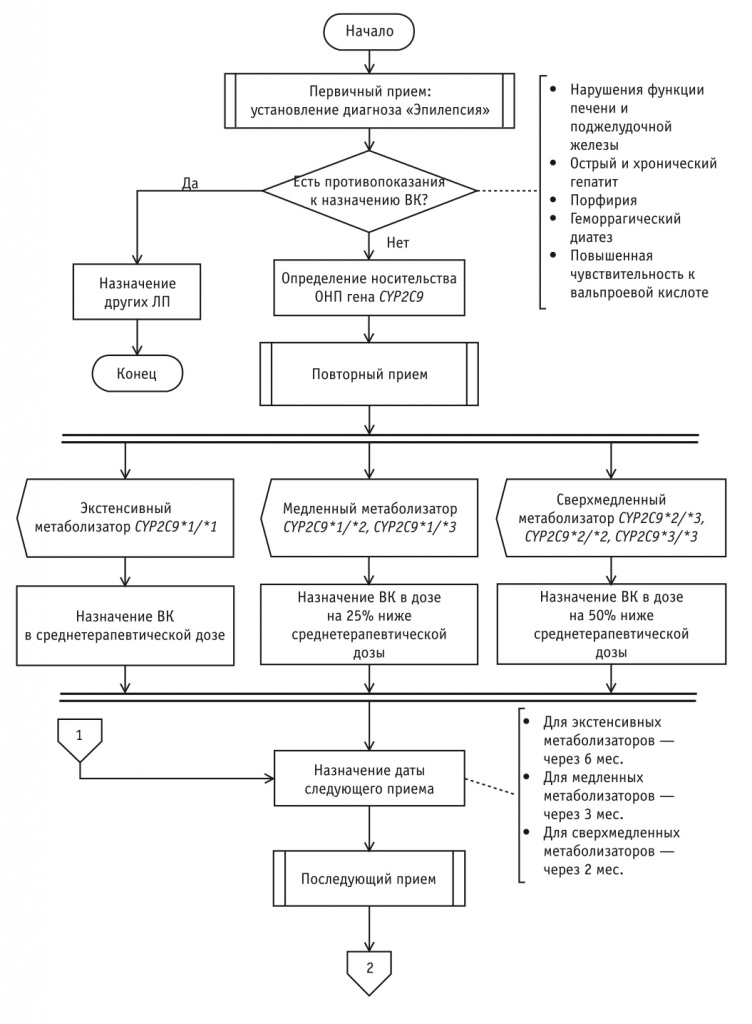
Рис. 2. Алгоритм персонализированного назначения препаратов вальпроевой кислоты (продолжение)
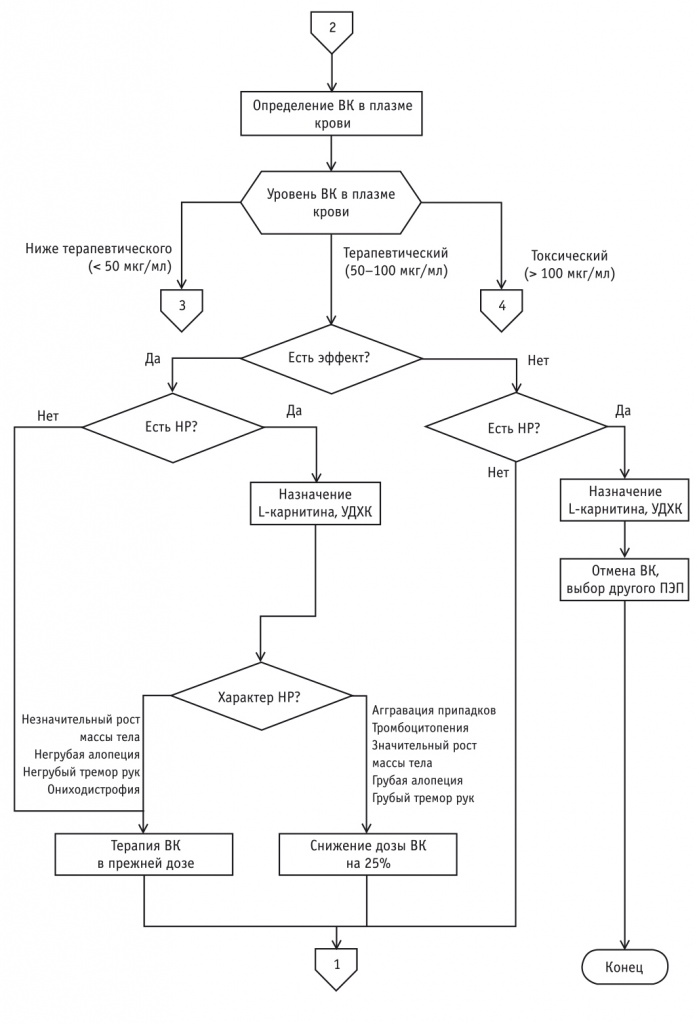
Рис. 3. Алгоритм персонализированного назначения препаратов вальпроевой кислоты (при уровне вальпроевой кислоты в плазме крови < 50 мкг/мл)
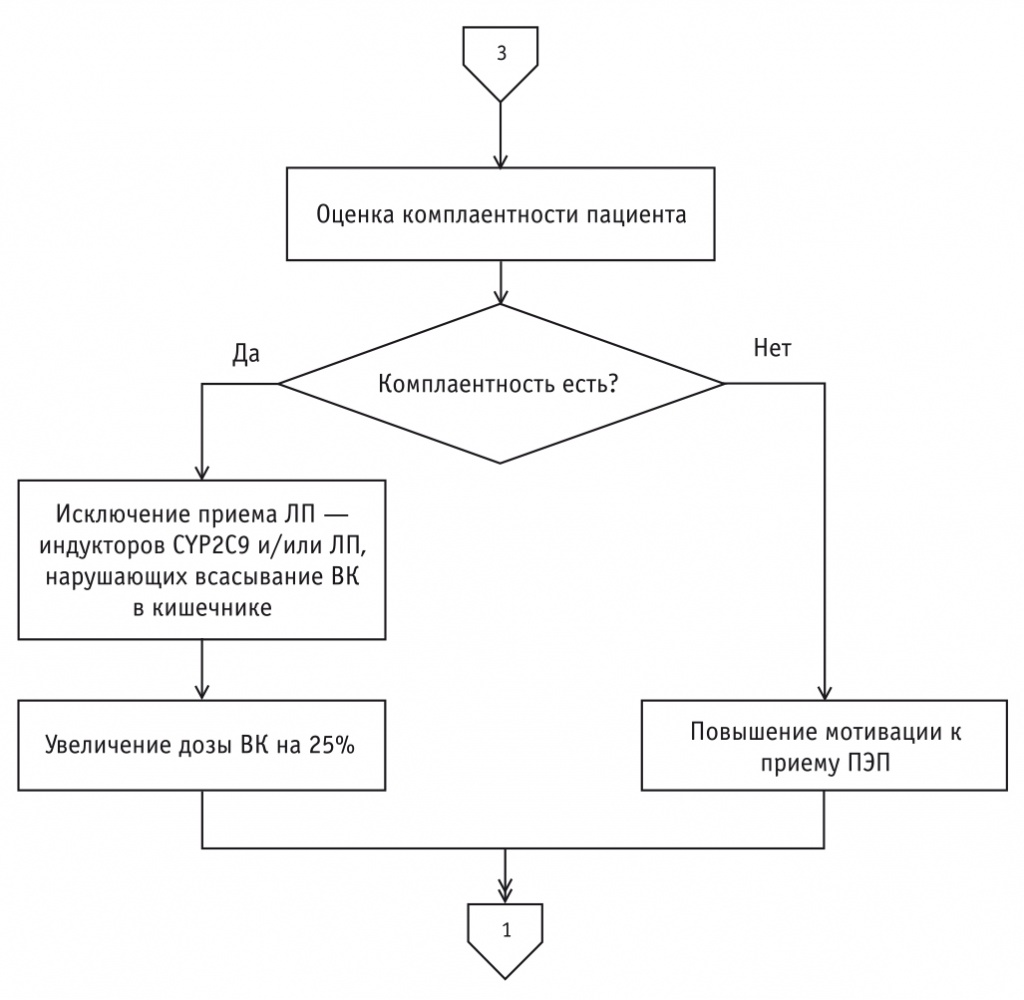
Рис. 4. Алгоритм персонализированного назначения препаратов вальпроевой кислоты (при уровне вальпроевой кислоты в плазме крови > 100 мкг/мл)
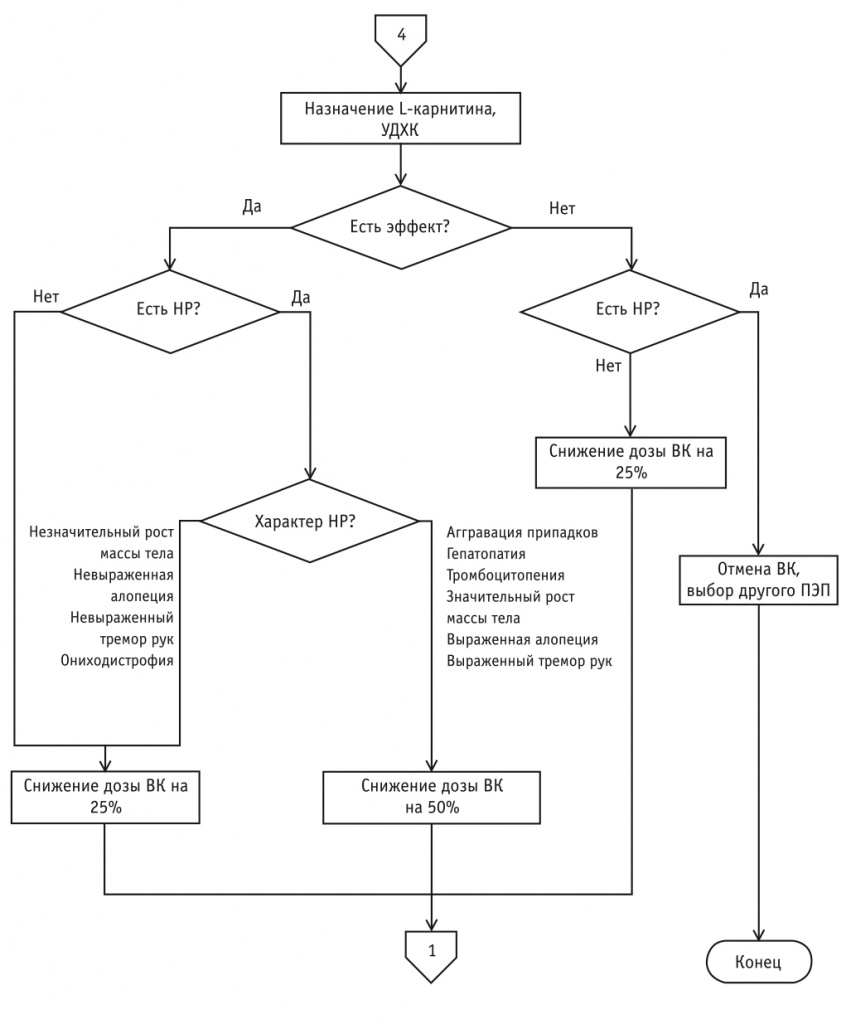
Началом работы по алгоритму (см. рис. 1) являются установление диагноза эпилепсии на первичном приеме врача-невролога и исключение противопоказаний для назначения препаратов ВК. К числу противопоказаний относятся, в частности: повышенная чувствительность к вальпроату, дивальпроату, вальпромиду или какому-либо из компонентов вальпроатов; острый и хронический гепатит; тяжелые нарушения функции печени или поджелудочной железы; печеночная порфирия; митохондриальные заболевания, вызванные мутациями ядерного гена POLG, кодирующего митохондриальный фермент γ-полимеразу; нарушения цикла мочевины; прием мефлохина или препаратов зверобоя продырявленного[9]; применение лекарственных препаратов (ЛП), повышающих ферментативную активность печени или нарушающих всасывание ПЭП в кишечнике. После установления диагноза эпилепсии и принятия решения о назначении ВК всех пациентов обследуют на носительство ОНП CYP2C9*2 и CYP2C9*3.
На повторном приеме проводится интерпретация полученного результата и назначаются препараты ВК, стартовая доза которых зависит от гомо- или гетерозиготного носительства выявленных ОНП гена CYP2C9: экстенсивным метаболизаторам (генотип CYP2C9*1/*1) назначается среднетерапевтическая доза ВК; медленным метаболизаторам (гетерозиготные генотипы CYP2C9*1/*2, CYP2C9*1/*3) — ВК в дозе на 25% ниже среднетерапевтической; у сверхмедленных метаболизаторов (гомозиготные генотипы CYP2C9*2/*2, CYP2C9*3/*3 или компаунд-гетерозиготный генотип CYP2C9*2/*3) доза ВК должна быть снижена на 50%. Темп титрования суточной дозы ВК также зависит от выявленных ОНП гена CYP2C9: у экстенсивных метаболизаторов — 1 раз в 3 дня, у медленных — 1 раз в неделю, у сверхмедленных метаболизаторов — 1 раз в 2 недели. Пациентам устанавливается дата следующего (повторного) приема: экстенсивным метаболизаторам — через 6 месяцев, медленным — через 3 месяца, а сверхмедленным метаболизаторам — через 2 месяца. Все пациенты перед визитом к врачу должны пройти ТЛМ ВК.
Дальнейшая тактика ведения больного зависит от результатов ТЛМ, клинической эффективности и ситуации с НР на фоне лечения препаратами ВК за прошедший период. Выбор ЛП для коррекции НР ВК основан на том, что одним из патогенетических механизмов их развития является вальпроат-индуцированное снижение синтеза L-карнитина в митохондриях гепатоцитов. Данное снижение происходит за счет соединения ВК с L-карнитином с образованием вальпроилкарнитина, который свободно выделяется с мочой, и снижением почечной реабсорбции свободного карнитина и ацилкарнитина, что приводит к дефициту L-карнитина и, как следствие, к развитию гипераммониемии[10]. С другой стороны, известно, что прием препаратов ВК часто приводит к развитию холестаза. При этом проведение курса гепатопротекторной терапии возможно без отмены препаратов ВК[4]. Назначение препаратов L-карнитина и урсодезоксихолевой кислоты (УДХК) позволяет устранить дефицит L-карнитина и обеспечить гепатопротективный эффект.
У пациентов с результатом ТЛМ ВК в пределах терапевтического коридора (50–100 мкг/мл) (см. рис. 2):
- при развитии положительной клинико-электроэнцефалографической динамики на фоне лечения и отсутствии НР применение ВК продолжается в прежней дозе;
- при развитии положительной клинико-электроэнцефалографической динамики на фоне лечения и формировании НР назначаются препараты L-карнитина и УДХК на 1 месяц. У пациентов с такими НР, как аггравация припадков, тромбоцитопения, гепатопатия, выраженные алопеция и тремор рук, значительный рост массы тела, доза ВК снижается на 25%; при таких НР, как ониходистрофия, негрубый тремор рук и негрубая алопеция, незначительный рост массы тела, терапия ВК продолжается в прежней дозе по согласованию с пациентами;
- при отсутствии клинико-электроэнцефалографического эффекта лечения вальпроатами и развитии НР производятся отмена ВК и выбор другого ПЭП. Всем пациентам этой группы назначаются препараты L-карнитина и УДХК на 1 месяц;
- в случае неэффективности лечения ВК и при отсутствии НР по согласованию с пациентами терапия может быть продолжена с повышением дозы ВК на 25% и сохранением темпа титрования дозы в зависимости от индивидуального фармакогенетического профиля пациента. Пациентам с уровнем ВК ниже терапевтического (< 50 мкг/мл) по результатам ТЛМ проводится оценка комплаентности в части соблюдения режима дозирования и схемы приема ПЭП (см. рис. 3). В случае отсутствия комплаентности проводится повышение мотивации к приему ПЭП, прием ВК продолжается в прежней дозе. В случае соблюдения рекомендаций по приему ВК исключается прием ЛП, повышающих ферментативную активность печени или нарушающих всасывание ВК в кишечнике, решается вопрос о дополнительном фармакогенетическом обследовании для исключения профиля «быстрый метаболизатор», доза ВК увеличивается на 25% с сохранением темпа титрования дозы в зависимости от индивидуального фармакогенетического профиля пациента. Пациентам с токсическим уровнем ВК (> 100 мкг/мл) по результатам ТЛМ назначаются препараты L-карнитина и УДХК на 1 месяц (см. рис. 4). В случае положительной клинико-электроэнцефалографической динамики на фоне лечения и при отсутствии НР доза ВК снижается на 25%. В случае положительной клинико-электроэнцефалографической динамики на фоне лечения и при развитии НР терапия ВК корректируется в зависимости от НР: у пациентов с такими НР, как аггравация эпилептических припадков, тромбоцитопения, гепатопатия, выраженные алопеция и тремор рук, значительный рост массы тела, доза ВК снижается на 50%; у пациентов с НР в виде ониходистрофии, негрубого тремора рук и негрубой алопеции, незначительного роста массы тела терапия ВК продолжается в дозе на 25% ниже, чем первоначальная. При отсутствии клинико-электроэнцефалографического эффекта лечения ВК и развитии НР производятся отмена ВК и выбор другого ПЭП. Если отсутствует клинико-электроэнцефалографический эффект лечения ВК и не развиваются НР, по согласованию с пациентами терапия ВК может быть продолжена в дозе на 25% ниже, чем первоначальная. Пациентам назначается дата следующего (повторного) приема: экстенсивным метаболизаторам — через 6 месяцев, медленным — через 3 месяца, а сверхмедленным метаболизаторам — через 2 месяца. Всем пациентам перед визитом к врачу должен быть выполнен ТЛМ ВК.
ЗАКЛЮЧЕНИЕ
Применение предложенного алгоритма персонализированного назначения препаратов вальпроевой кислоты (ВК) позволит врачам-неврологам, психиатрам, врачам общей практики при подборе стартовой и поддерживающей дозы препаратов ВК учитывать индивидуальный фармакогенетический профиль пациента и тем самым существенно повысить безопасность фармакотерапии эпилепсии. Графическая визуализация алгоритма делает процесс наглядным и удобным в применении. Утверждение Министерством здравоохранения Российской Федерации в апреле 2018 г. Концепции предиктивной, превентивной и персонализированной медицины, направленной на развитие индивидуальных подходов к пациенту, в том числе до развития у него заболеваний[11], подтверждает необходимость трансляции достижений фармакогенетических исследований в реальную клиническую практику.








