Пандемия COVID-19, вызванная новым коронавирусом SARS-CoV-2, оказала беспрецедентное влияние на здоровье населения Земли. Хотя симптомы коронавируса могут быстро проходить у большинства людей, некоторые страдают от долгосрочных последствий заболевания. После эпидемий коронавирусных инфекций, с которыми ранее сталкивалось человечество, также были описаны их отдаленные последствия. У выживших после перенесенных ранее коронавирусных инфекций, включая атипичную пневмонию (2003) и ближневосточный респираторный синдром (2012), наблюдалась аналогичная совокупность устойчивых симптомов, что усиливает настороженность в отношении клинически значимых последствий COVID-19[1, 2].
Накопившиеся к настоящему времени факты свидетельствуют, что пост-COVID-состояния — это широкий спектр новых, возвращающихся или продолжающихся проблем со здоровьем, с которыми люди могут столкнуться более чем через 4 недели после первого заражения вирусом SARS-CoV-2. Даже люди, у которых отсутствовали симптомы, когда они были инфицированы, могут иметь пост-COVID-19 состояния. Им свойственны разные типы и комбинации клинических симптомов в различные временны́е периоды.
В отношении острого COVID-19 существует общепризнанная категоризация болезни, основанная на тяжести заболевания. Острый COVID-19 включает бессимптомное, легкое, умеренное, тяжелое и критическое течение. Напротив, категоризация отдаленных последствий COVID-19 находится в стадии активного обсуждения. В настоящее время не существует общепринятой временно’й границы, определяющей начало болезни. Большинство исследователей согласны, что пролонгация болезни для COVID-19 начинается через 3 недели после появления симптомов.
Оценка временно́го периода острой фазы в 3–4 недели базируется на клинической картине, способности вируса к репликации в течение 10 (максимум 20) дней от момента появления первых симптомов1 и средней продолжительности положительной ПЦР в течение 24 дней у пациентов с симптомами[3].
Предлагается «хронический COVID-19» рассматривать как стойкую симптоматику, продолжающуюся более 12 недель после появления первых симптомов[4]. Наблюдение за большим количеством больных с последствиями COVID-19 позволило выделить несколько этапов коронавирусной инфекции.
- Острый COVID-19 включает признаки и симптомы до 4 недель после начала заболевания.
- Продолжающийся симптоматический COVID-19: симптомы в период от 4 до 12 недель после начала заболевания.
- Синдром пост-COVID-19: признаки и симптомы, которые развиваются во время или после инфекции, продолжаются более 12 недель и не объясняются другим диагнозом.
- Хронический COVID/Long COVID-19, который включает как продолжающийся симптоматический COVID-19 (от 4 до 12 недель), так и синдром пост-COVID-19 (12 недель и более).
Результаты больших эпидемиологических исследований последствий коронавирусной инфекции пока недоступны, но в большинстве национальных исследований распространенность соответствует данным, приведенным в обсервационном когортном исследовании V. Chopra и соавт. Авторы показали, что у 32,6% пациентов наблюдались стойкие симптомы, из них у 18,9% имелись новые или ухудшившиеся симптомы[5]. Совсем недавно Long COVID-19 (постковидный синдром) признан ВОЗ всемирной проблемой здравоохранения и зарегистрирован в МКБ-10 и МКБ-11 как отдельная нозологическая единица под кодом «для экстренного использования» (U09.9 Post-COVID-19).
ПАТОФИЗИОЛОГИЯ COVID-19
Основные патофизиологические механизмы острого COVID-19 включают прямую вирусную токсичность, повреждение эндотелия и микрососудов, нарушение регуляции иммунной системы с формированием системного воспалительного ответа, гиперкоагуляцию с последующим тромбозом in situ и макротромбозом и дисфункцию пути ангиотензин-превращающего фермента 2 с активацией классической прооксидантной оси ангиотензин-рениновой системой и развитием окислительного стресса.
Возможные механизмы, влияющие на патофизиологию хронического COVID-19, включают вирус-специфические патофизиологические изменения, иммунологические аберрации и воспалительное повреждение в ответ на острую инфекцию и ожидаемые последствия посткритического заболевания. Патофизиология синдрома после интенсивной терапии многофакторна и включает микрососудистую ишемию, неподвижность и метаболические изменения во время критического периода заболевания[6].
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ LONG COVID-19
Как правило, исследователи выделяют две основные группы симптомов Long COVID-19. Первая группа — это в основном респираторные симптомы, такие как кашель и чувство одышки, но также включает усталость и головные боли. Наши собственные предварительные данные, основанные на опросе врачей-терапевтов, показали, что респираторные симптомы беспокоят каждого десятого пациента. Вторая группа — полисистемные симптомы, свидетельствующие о поражении/дисфункции многих систем организма, включая ЦНС, сердце, мозг и кишечник, усиливающиеся после физических или умственных нагрузок:
- усталость;
- одышка или затрудненное дыхание;
- кашель;
- боли в суставах;
- боль в грудной клетке;
- проблемы с памятью, концентрацией внимания («мозговой туман») или сном;
- боль в мышцах или головная боль;
- учащенное сердцебиение;
- потеря чувства запаха или вкуса;
- депрессия или тревога;
- ощущение жара;
- головокружение при вставании, ортостатическая интолерантность.
Согласно нашим данным, доминирующим симптомом является чувство усталости и/или общей слабости, о котором сообщали 24,7% пациентов, называя усталость/слабость в качестве главного негативного симптома.
ЛЕГОЧНЫЕ ПОСЛЕДСТВИЯ COVID-19
Как и при других респираторных инфекциях, кашель — ключевой симптом COVID-19 в острой фазе, который сохраняется и в постинфекционной фазе. Кашель не только беспокоит пациента, но и стигматизирует его как источник инфекции, что приводит к социальной изоляции. В отличие от кашля, который сохраняется после простуды или гриппа, хронический кашель при пост-COVID-синдроме обычно сопровождается другими мультисистемными проявлениями, которые могут указывать либо на многофакторный патогенез, либо на общие механизмы, лежащие в основе этих симптомов. Сопутствующие усталость, одышка, боль и кашель могут свидетельствовать о нарушениях в ЦНС.
Снижение диффузионной способности легких является наиболее частым патогенетическим нарушением при пост-COVID-синдроме, напрямую связанным с тяжестью острого заболевания[7, 8].
Дополнительно рассматриваются нейрогенные механизмы гиперчувствительности. Предполагается, что SARS-CoV-2 через взаимодействие нейровоспалительных и нейроиммунных механизмов поражает чувствительные нервы, опосредующие кашель. Кроме того, нейрогенные механизмы могут объяснить другие сопутствующие симптомы пост-COVID-синдрома.
Не исключено, что в целом пост-COVID-синдром становится результатом общей гиперчувствительности, которая лежит в основе множества симптомов, связанных с этим состоянием. Ключевые симптомы пост-COVID-синдрома (одышка, боль и кашель) имеют сходство в отношении контроля и периферической сенсибилизации соответствующих афферентных путей[9].
Функциональные МРТ-исследования показали, что островковая и поясная кора являются ключевыми областями, которые активируются как болевыми ощущениями, так и кашлем[9, 10]. ПЭТ-изображение головного мозга демонстрирует гипометаболизм в обонятельной извилине и связанных лимбических и паралимбических областях, распространяющихся на ствол мозга. Частично эти находки объясняют биологическую связь между респираторными симптомами пост-COVID-синдрома и респираторными паническими атаками (РПА), которые мы наблюдаем у пациентов, перенесших COVID-19.
РПА, или гипервентиляционными кризами, называют панические атаки с преобладанием дыхательных расстройств в картине пароксизма, в которых дисфункциональное дыхание играет решающую роль в формировании многочисленных клинических проявлений.
В настоящее время большинство исследователей достигли консенсуса в отношении рассмотрения респираторной паники как отдельной клинической единицы, отличающейся клинической феноменологией, приводящей к социальной дезадаптации пациента, но, возможно, поддающейся терапии.
Нарушенное дыхание является причиной гипервентиляции и респираторного алкалоза, которые вызывают различные соматические симптомы. Согласно гипотезе РПА, предполагается существование ложных приступов удушья, которые вызывают спонтанные приступы паники (при условии, что мозг ошибочно воспринимает отсутствие кислорода и активирует неадекватные вегетативные ответы на удушье). Неправильная интерпретация этих симптомов усиливает страх и активизирует вегетативную нервную систему, тем самым увеличивая частоту дыхания, что приводит к дальнейшему снижению концентрации CO2 и усиливает гипокапнические симптомы. Это создает положительную обратную связь, усиливая страх и увеличивая вероятность приступа паники.
Считается, что хемочувствительные области ЦНС, отвечающие за паническую реакцию, распространены на несколько ядер ствола мозга, в том числе ядра солитарного тракта, голубого пятна и ядра шва, при этом все они находятся в пределах дыхательного центра ствола мозга. Дисфункциональное дыхание, включая кашель, одышку, в острый и хронический периоды COVID-19 является важным предраспологающим фактором развития РПА. Одно из наших клинических наблюдений демонстрирует эту взаимосвязь.
Клиническое наблюдение
Пациент — мужчина 29 лет, специалист в медиасфере. Четыре месяца назад он перенес коронавирусную инфекцию COVID-19 (подтвержденную) среднетяжелой степени, внебольничную двустороннюю пневмонию (КТ2). В период долечивания испытывал выраженную общую слабость, приступы кашля. Не мог носить защитную маску, т. к. маска способствовала приступам кашля. Через 2 месяца после регресса симптомов инфекционного заболевания состояние пациента ухудшилось. Он стал вновь испытывать приступы затрудненного дыхания, ощущения нехватки воздуха, кома в горле, сухость во рту. В момент приступа на него «накатывал» страх задохнуться, он открывал окна, чтобы дышать кислородом.
Пациент был осмотрен пульмонологом, дополнительно ему проведено КТ легких. Данные о новой респираторной патологии отсутствовали. У больного был диагностирован синдром дисфункционального дыхания (гипервентиляционный синдром).
С больным провели длительную беседу и объяснили, что его симптомы неопасны и имеют благоприятный прогноз. Пациент согласился с доводами врача, но у него продолжали сохраняться опасения о своем здоровье. Дополнительное беспокойство вызывали сердцебиение, ощущение «зажатия» в области сердца во время приступов удушья. Он потерял 4 кг веса без диеты, потому что ему не хотелось есть. У него сохранялись проблемы с засыпанием, и он просыпался в 3 часа ночи несколько раз в неделю.
Несмотря на то что больной значительно снизил профессиональную нагрузку, он плохо справлялся с работой. Он чувствовал, что ему не хватает энергии, тревожность за свое состояние мешает сосредоточиться и у него все меньше возможностей выполнять работу. Он начал делать профессиональные ошибки и думал про себя: «Я глупец, я не могу хорошо работать, я болен».
После того как его мать забеспокоилась и спросила у него о психическом состоянии, пациент сообщил ей, что не может работать и собирается уволиться. Мать настояла на консультации у специалиста. Врач-кардиолог объяснил, что симптомы не связаны с сердцем и рекомендовал обратиться к неврологу или психотерапевту.
При осмотре: несколько возбужден, беспокойно жестикулирует, ерзает на месте, во время разговора периодически вздыхает («лишние» вдохи). Фон настроения снижен, объясняет врачу, что тревога повлияла на многие сферы его жизни, но особенно на способность справляться с задачами, которые для многих людей являются повседневными, из-за чего он очень сильно сократил свою повседневную активность.
В статусе: усиление физиологического тремора в руках, тремор век, симптомы нервно-мышечной возбудимости (симптом Хвостека II степени, мышечные спазмы), другие вегетативные стигмы.
Врач диагностировал поствирусное паническое расстройство, РПА, синдром дисфункционального дыхания. Пациенту назначена комплексная терапия, включающая дыхательную гимнастику, антигипоксанты (Гипоксен), психотропную терапию (пароксетин в сочетании с Тералидженом). Через 3 недели у пациента наблюдалось облегчение симптомов.
В приведенном наблюдении хронический кашель послужил триггером развития панического расстройства. Определение способов борьбы с кашлем, связанным с COVID-19, может помочь предотвратить патогенный эффект, а также снять стигму этого симптома. Необходимо использовать научно обоснованные варианты лечения кашля, ассоциированного с COVID-19, поскольку пациенты с кашлем часто прибегают к лекарствам, отпускаемым без рецепта. Но не известно, эффективны ли они у лиц с кашлем после COVID-19.
Постоянный кашель при пост-COVID-синдроме приводит к состоянию гиперчувствительности гортани, что, в свою очередь, поддерживает хронический рефрактерный необъяснимый кашель.
В отдельных работах показано, что противоэпилептические препараты габапентин и прегабалин эффективны в борьбе с хроническим рефрактерным кашлем [11, 12]. Этот подход можно рассмотреть и при пост-COVID-синдроме, потому чтоуказанные препараты могут быть полезны при других симптомах, сопровождающих кашель, таких как боль. Антимускариновые лекарственные средства также можно использовать для борьбы с кашлем при COVID-19, потому что они способны снизить чувствительность к кашлю при острой вирусной инфекции верхних дыхательных путей[13].
Гипоксия, связанная с нарушением диффузионной способности легких после COVID-19, может поддерживать респираторные симптомы. В этом случае помощь могут оказать антиоксиданты, в частности Гипоксен — полидигидроксифенилентиосульфонат натрия (натриевая соль поли(n‑диокси-о‑фенилен)тиосерной кислоты, или поли-2,5-дигидроксифенилен-4-тиосульфокислоты, или поли- (2,5-дигидрокси-фенилен)-4-тиосульфокислоты. Известно, что полигидрофениленовая структура Гипоксена обеспечивает проявление выраженных антиоксидантных свойств — способности связывать большое число свободных радикалов, нейтрализовать окислители и продукты перекисного окисления липидов.
В присутствии Гипоксена снижается потребность клеток в кислороде, а также угнетается процесс генерации активных форм кислорода, лавинообразное накопление которых неизбежно при гипоксии. За счет улучшения усвоения кислорода Гипоксен способен снижать потребность тканей в кислороде в условиях гипоксии. Кроме того, в отдельных работах показана противовоспалительная активность Гипоксена[14].
Препарат широко применяется в клинической медицине, в частности для лечения ХОБЛ[15]. Он способствует уменьшению одышки, в том числе обусловленной физической активностью, и повышает переносимость физических нагрузок у пациентов с заболеваниями респираторной системы. Это снижает чувство усталости, увеличивает активность пациента, способствует большей приверженности к реабилитационным мероприятиям и возрастанию их эффективности, повышает качество жизни пациентов.
Мультифакторные фармакологические свойства Гипоксена расширяют наши возможности в лечении легочных последствий COVID-19.
Дыхательные практики как часть мультимодальной терапии могут быть эффективны в качестве легочной реабилитации при пост-COVID-синдроме, особенно у пациентов с сопутствующими тревожными расстройствами[16].
НЕЙРОПСИХИЧЕСКИЕ ПОСЛЕДСТВИЯ COVID-19
Подобно больным с хроническим пост-SARS-синдромом, лица, перенесшие COVID-19, сообщают о хроническом недомогании, диффузных миалгиях, депрессивных симптомах и сне, не приносящем ощущения бодрости, мигренеподобных головных болях, против которых часто не помогают традиционные анальгетики. Потеря чувства вкуса и запаха также может сохраняться после исчезновения других симптомов примерно у 10% пациентов при последующем наблюдении до 6 месяцев. Важной проблемой Long COVID-19 являются флуктуирующие когнитивные нарушения, включая «мозговой туман», под которым подразумевают ухудшение концентрации внимания, памяти, беглости речи и/или нарушения исполнительных функций. Психические расстройства, такие как тревога и депрессия, у больных, перенесших COVID-19, встречается значительно чаще, чем в сопоставимых контрольных когортах пациентов с диагнозом гриппа и других инфекций дыхательных путей[17].
Поствирусная усталость — довольно частое явление после любого типа вирусной инфекции. После гриппа или инфицирования вирусом Эпштейна — Барр многие люди испытывают стойкую усталость в течение нескольких недель или даже месяцев после предполагаемого выздоровления. Каким бы неприятным ни был этот продолжительный опыт, большинство людей полностью выздоравливают. Но у некоторых пациентов болезнь никогда не кончается.
Вирусные заболевания являются одной из основных причин миалгического энцефаломиелита, также известного как синдром хронической усталости (CХУ). Это длительное состояние характеризуется в первую очередь крайней усталостью, а также «мозговым туманом», болезненными ощущениями в суставах и симптомами, напоминающими грипп.
Long COVID-19 во многих отношениях отражает поствирусный СХУ. Пока невозможно сказать, отличается ли Long COVID-19 клинически от СХУ, или это одно и то же заболевание, возникающее массово из-за четко идентифицируемой причины, имеющей собственное значение.
В настоящее время СХУ определяется как системная непереносимость физических нагрузок, при которой у пациента должно быть значительное нарушение способности участвовать в образовательной, профессиональной, личной или социальной деятельности на уровне, предшествующем заболеванию. Последние критерии диагностики СХУ/интолерантности к нагрузке были сформулированы в 2015 г.
Для диагностики СХУ/интолерантности к нагрузке требуется наличие у пациента трех главных симптомов:
- значимое снижение уровня активности, включая профессиональную, образовательную, социальную, личностную, длящееся более 6 месяцев, сопровождающееся выраженной усталостью, которая не является результатом чрезмерной нагрузки и существенно не облегчается после отдыха; нарушение повседневной активности и чувство усталости непривычны для пациента, они имеют отчетливое начало (не являются чертой характера);
- недомогание (ухудшение симптомов) после какого-либо (физического, умственного или эмоционального) напряжения;
- сон, не приносящий чувства восстановления (свежести, бодрости).
Необходимо оценить выраженность двух последних симптомов. Диагноз устанавливается, если они беспокоят пациента как минимум в течение половины дня и их выраженность достигает средней или тяжелой степени. Нужно также оценивать выраженность одного из следующих двух состояний, наличие как минимум одного из которых свидетельствует о СХУ/интолерантности к нагрузке:
- когнитивные нарушения (обычная мыслительная деятельность требует дополнительных усилий);
- ортостатическая интолерантность.
Однако эксперты подчеркивают, что следует начинать лечение, даже если симптомы длятся менее 6 месяцев. Присутствие других неспецифических симптомов, включая более ранние диагностические критерии 1994 г. (боль в горле, болезненность шейных лимфоузлов и др.), не исключает диагноз, а рассматривается как дополнительный аргумент для диагностики СХУ.
Субъективно больные могут по-разному формулировать основную жалобу: «я чувствую себя совершенно измочаленным», «у меня постоянно не хватает энергии», «я полностью истощен», «я обессилил», «обычные нагрузки доводят меня до изнурения» и т. д.). Важно, что чувство усталости сохраняется даже после длительного отдыха или сна.
У отдельных больных при активном расспросе удается выявить связь между такими неопределенными симптомами, как головокружение, ощущение «пустоты в голове», затуманивание зрения, общая слабость, дискомфорт в груди, дрожь, короткое отрывистое дыхание, головная боль в период ортостатического стресса. В ответ на быстрый переход из положения лежа или сидя в положение стоя, при физическом усилии или приеме пищи у некоторых пациентов возникают отчетливые ортостатические гипотензивные симптомы (ощущение «пустоты в голове», головокружение, предобморочное состояние) в сочетании с привычными симптомами: общей слабостью, ощущение усталости, умственная заторможенность, затуманивание зрения, головной болью, болью в шее, в грудной клетке.
Симптомы ортостатической интолерантности могут усугубляться дегидратацией, физическими усилиями, повышением температуры окружающей среды, приемом алкоголя и пищи, некоторыми лекарственными препаратами. Для подтверждения ортостатической интолерантности требуется исследование гемодинамики во время стояния или нахождения в вертикальной позиции на поворотном столе.
Приблизительно 85% пациентов жалуются на нарушение концентрации внимания, ослабление кратковременной памяти, однако рутинное нейропсихологическое обследование нарушений мнестической функции обычно не выявляет. Впрочем, при углубленном исследовании часто обнаруживают незначительные, но несомненные нарушения памяти и усвоения информации. У некоторых пациентов наблюдается вербальная дислексия, которая периодически проявляется невозможностью подобрать нужное слово во время обычного разговора. В целом больные с СХУ обладают нормальными когнитивными и интеллектуальными возможностями. Однако эти типичные нарушения могут затруднять профессиональную деятельность. Даже привычные профессиональные действия занимают больше времени, чем до болезни.
Хотя существует множество теорий о причинах СХУ, тремя наиболее распространенными провоцирующими факторами являются инфекционное заболевание, стресс или серьезное жизненное событие, а также воздействие токсинов окружающей среды[18]. Несколько исследований показали, что пациенты с СХУ избыточно реагируют на стрессоры, в частности у них происходит аномальное повышение уровня кортизола в сыворотке и ЧСС в ответ на стресс[19].
Патогенез СХУ/Long COVID-19 связан со множеством процессов, включая нарушение регуляции иммунной системы, гипервоспалительное состояние, окислительный стресс. Дополнительные механизмы включают метаболические и эндокринные нарушения, когда организму не хватает энергии и драйва, потому что у клеток есть проблемы с выработкой и использованием энергии из кислорода, сахаров, липидов и аминокислот.
ТЕРАПИЯ LONG COVID-19
Поскольку при Long COVID-19 и СХУ могут происходить определенные общие патологические процессы, можно предположить, что методы лечения СХУ, такие как антиоксидантная терапия, вероятно, полезны и при симптомах Long COVID-19[20]. Этилметилгидроксипиридина малат (Этоксидол) — широко применяемый на протяжении многих лет антиоксидант. Препарат также улучшает микроциркуляцию и реологические свойства крови, уменьшает агрегацию тромбоцитов, стабилизирует мембранные структуры клеток крови. Малотоксичный антиоксидант второго поколения Этоксидол рекомендован экспертами для использования в острый период COVID-19. Этоксидол ускоряет диссоциацию оксигемоглобина на гемоглобин и кислород в эритроцитах, усиливает насыщение крови кислородом, тем самым улучшая оксигенацию. При этом Этоксидол дополнительно увеличивает концентрацию фоллистатина, способствуя ограничению воспалительного процесса в легких, снижая содержание провоспалительных цитокинов, концентрацию и активность активина А путем его связывания с фоллистатином, а также нейтрализуя активные формы кислорода[21].
Он ингибирует перекисное окисление липидов, повышает активность супероксиддисмутазы, уменьшает содержание общих органических перекисей, что способствует ускорению метаболизма альдостерона (путем нормализации активности изофермента CYP3A4), увеличивает соотношение липид/белок, снижает вязкость мембраны и усиливает ее текучесть.
Ноотропы могут применяться при Long COVID-19. Нанотропил Ново (фонтурацетам) — препарат с ноотропным и антиастеническим действием. Фонтурацетам уменьшает физическую и психическую астению.
В клинической практике широко применяют антидепрессанты, позволяющие успешно купировать некоторые симптомы СХУ (улучшают сон и уменьшают боли, выраженность тревоги, депрессии). В некоторых открытых исследованиях установлен положительный эффект обратимых ингибиторов моноаминоксидазы, особенно у больных с клинически значимыми вегетативными симптомами.
Впрочем, следует учитывать, что большинство пациентов с СХУ плохо переносят лекарственные препараты, действующие на ЦНС, поэтому терапию следует начинать с низких доз. Предпочтение должно отдаваться селективным ингибиторам обратного захвата серотонина (СИОЗС), антидепрессантам с благоприятным спектром переносимости. Атипичные нейролептики эффективны в отношении как всех видов тревожных расстройств, так и отдельных симптомов Long COVID-19. Они могут использоваться в качестве дополнения к СИОЗС или как альтернатива СИОЗС.
Одним из наиболее востребованных препаратов этой группы в практике врачей интернистов и неврологов является алимемазин (Тералиджен)2. Алимемазин отличается слабым антагонистическим влиянием на дофаминовую систему. Оно ограничивается преимущественно мезолимбическим и мезокортикальным трактами без существенного воздействия на нигростриарный путь в мозге[22]. Слабое влияние на дофаминовую систему и, как следствие, слабый антипсихотический эффект оборачиваются преимуществом алимемазина при использовании его в общесоматической практике[23].
Еще одним полезным свойством алимемазина, показанным в ранних исследованиях, является потенцирование его анксиолитического эффекта в комбинированных схемах в сочетании с антидепрессантами[24]. Это открывает широкие возможности комбинации алимемазина с СИОЗС при лечении расстройств тревожного спектра. Во-первых, одновременное назначение алимемазина с препаратом из группы СИОЗС облегчает для пациента инициальный период лечения, когда возможно усиление тревоги за счет антидепрессивной терапии. Во-вторых, клинически значимый терапевтический эффект развивается в более ранние сроки.
Кроме того, алимемазин воздействует на некоторые трудно курабельные симптомы, связанные с вегетативной дисфункцией, в частности диспептические и вестибулярные.
При назначении алимемазина большинство специалистов используют восходящее титрование дозы. Это позволяет индивидуально подобрать адекватную дозу препарата и минимизировать побочные явления начала терапии (преходящую сонливость)[23]3.
Лечение, направленное на улучшение ортостатических ресурсов пациентов, может облегчить основные симптомы заболевания. В первую очередь желательно избегать провоцирующих факторов, в частности дегидратации, длительной иммобилизации.
Широко применяют когнитивную поведенческую терапию, предназначенную для устранения патологической перцепции и извращенной интерпретации телесных ощущений (факторов, играющих значительную роль в поддержании симптомов СХУ). Персонализированная когнитивная поведенческая терапия также может быть полезна для обучения больного более эффективным копинг-стратегиям, что повышает адаптивные возможности. В контролируемых исследованиях установлено, что положительный эффект отмечают 70% пациентов.
Полезным может быть сочетание программы ступенчатых физических упражнений с когнитивной поведенческой терапией. Ступенчатую физическую нагрузку увеличивают каждые 4 недели на протяжении 6–12 месяцев до достижения целевого уровня нагрузки: 30 минут аэробных упражнений средней тяжести 5 раз в неделю.
Наиболее приемлемой физической активностью для описываемых больных являются такие аэробные занятия, как ходьба, плавание, езда на велосипеде. На первых занятиях физическая активность продолжается несколько минут и не должна вызывать чувство усталости. Если физическая активность приводит к усталости, ее следует уменьшить. Аэробные занятия не только редуцируют чувство усталости, но и позитивно влияют на качество сна, дневное функционирование, общее качество жизни, снимают боль. Улучшения состояния на фоне аэробной физической нагрузки стоит ожидать у каждого второго пациента.
Техники глубокого дыхания, мышечной релаксации, массаж, кинезиотерапия, йога рассматриваются как дополнительные методы воздействия (главным образом для устранения коморбидной тревожности).
ЗАКЛЮЧЕНИЕ
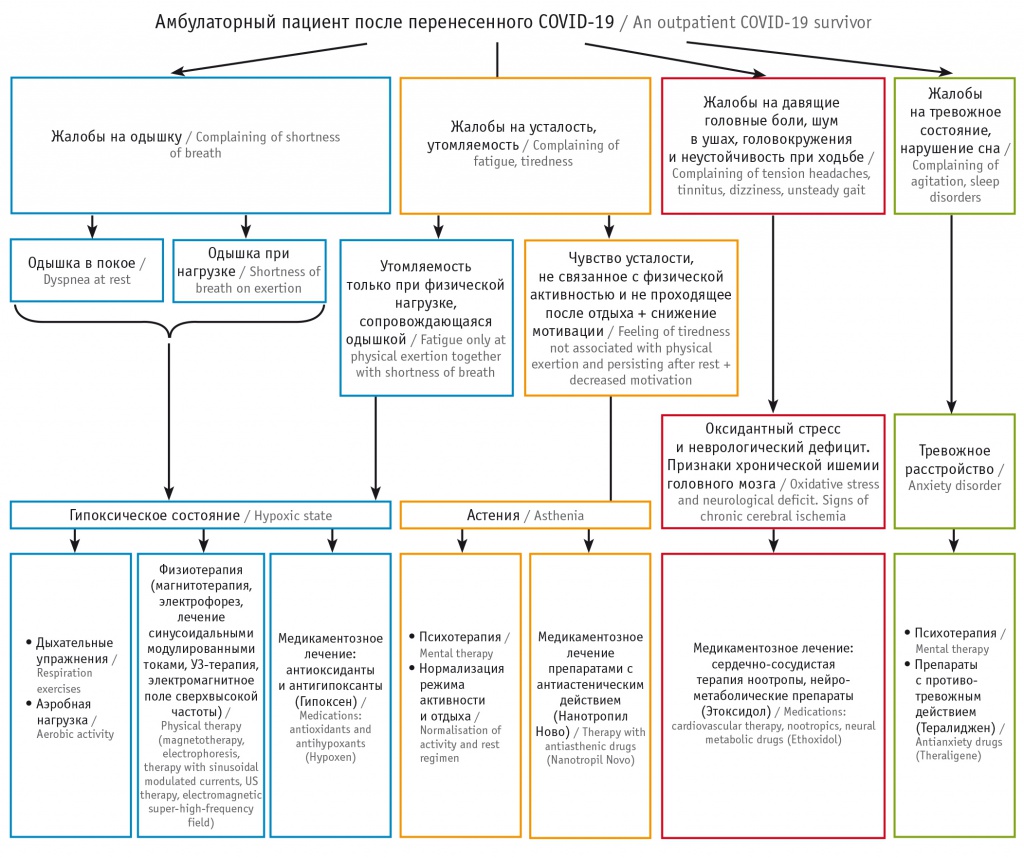
Сложная симптоматика Long COVID-19 требует комплексного лечения, выбор основных препаратов должен основываться на их влиянии на ведущие/целевые симптомы (респираторные, интолерантность к нагрузке, когнитивные нарушения и т. д). Примерный алгоритм выбора комплексного лечения представлен на рисунке.
Рис. Алгоритм выбора комплексного лечения Long COVID-19[25, 26]4
Поступила: 10.06.2021
Принята к публикации: 24.06.2021
__________
1 Centers for Disease Control and Prevention. Interim Guidance on Ending Isolation and Precautions for Adults with COVID-19. Updates as of February 13, 2021. URL: https://www.cdc.gov/coronavirus/2019-ncov/hcp/duration-isolation.html (дата обращения — 15.05.2021).
2 Отчет по результатам Неинтервенционной программы скрининга пациентов, страдающих расстройством вегетативной нервной системы, в условиях повседневной клинической практики (СТАРТ-1). ОАО «Валента Фармацевтика». 2014.
3 Там же.
4 Временные методические рекомендации. Медицинская реабилитация при новой коронавирусной инфекции (COVID-19). Версия 2 от 31.07.2020. URL: https://xn--80aesfpebagmfblc0a.xn--p1ai/ai/doc/461/attach/28052020_Preg_COVID-19_v1.pdf (дата обращения — 15.05.2021).








