Лечение при этом заболевании заключается в проведении регулярной заместительной терапии внутривенными иммуноглобулинами. Одним из вариантов лечения может быть также трансплантация гемопоэтических стволовых клеток. Прогноз обычно плохой из-за чрезвычайно высокого риска возникновения злокачественных образований [2].
Первичные иммунодефицитные состояния могут быть обнаружены с помощью измерения уровней эксцизионных колец Т-клеточного рецептора (англ. T-cell receptor excision circles, TREC) и рекомбинационных колец каппа-делеционного элемента (англ. kappa-deleting recombination excision circles, KREC) в сухом пятне крови на карте неонатального скрининга или в периферической крови методом ПЦР в режиме реального времени [3, 4]. TREC являются побочным продуктом рекомбинации гена Т-клеточного рецептора, а KREC — В-клеточного. Низкие уровни несущих эти молекулы лимфоцитов в периферической крови указывают на Т- и/или В-клеточную лимфопению [4, 5].
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
Девочка родилась 7 сентября 2011 г. от первой физиологически протекавшей беременности, первых преждевременных родов на 33-й неделе. Сразу после рождения у ребенка была выявлена свищевая форма атрезии ануса, прооперирована в ноябре 2011 г. Наблюдалась кардиохирургами в ДГКБ № 13 им. Н. Ф. Филатова (г. Москва) с дефектом межжелудочковой перегородки. С первого года жизни ребенка ежемесячно беспокоили острые тонзиллофарингиты и обструктивные бронхиты, был один эпизод пневмонии. Вакцинирована БЦЖ и против гепатита В. Наследственный анамнез не отягощен. Аллергологом-иммунологом не консультировалась.
Второго июля 2015 г. в возрасте 3 лет 9 месяцев ребенок поступил в десятое инфекционное отделение (ОРВИ) ДГКБ № 9 им. Г. Н. Сперанского (г. Москва) в связи с затяжным течением ОРВИ и стоматитом. На пятый день госпитализации лечащий врач вызвал аллерголога-иммунолога с целью консультации по поводу рецидивирующих обструктивных бронхитов и для решения вопроса о возможном дальнейшем обследовании ребенка на предмет аллергических заболеваний. Консультант обратил внимание на внешний вид, анамнез жизни ребенка и назначил иммунологическое обследование: общий анализ крови; проточную цитометрию с целью фенотипирования субпопуляций Т-, В- и NK-лимфоцитов; ПЦР в режиме реального времени для оценки количества TREC и KREC в цельной крови. Результаты обследования представлены в таблице 1.
Таблица 1
Результаты иммунологического обследования в инфекционном отделении на фоне течения острой респираторной вирусной инфекции и стоматита
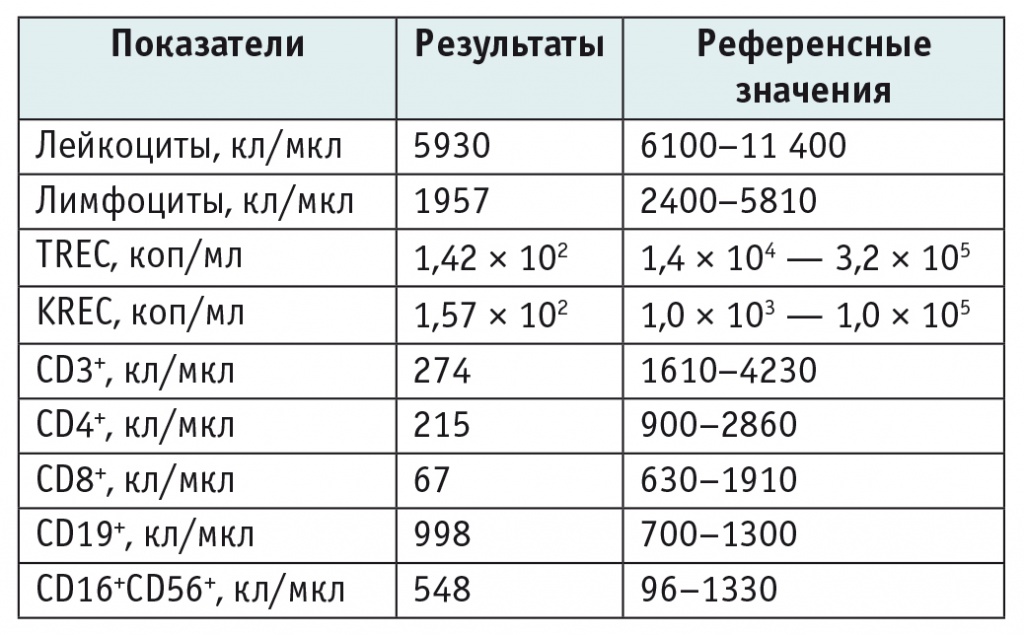
На основании анамнеза жизни, данных физикального осмотра и результатов лабораторного исследования был поставлен предварительный диагноз: «первичное иммунодефицитное состояние: синдром Ниймеген». 12 июля в лаборатории ДНК-диагностики он подтвердился результатами молекулярно-генетического исследования: была выявлена мутация 657del 115 в гене NBS1. Проведена заместительная терапия внутривенным препаратом иммуноглобулина человека в дозе насыщения — 1 г/кг.
В сентябре 2015 г. состоялась повторная госпитализация ребенка в профильное отделение больницы с целью обследования в динамике, а также проведения заместительной терапии внутривенными иммуноглобулинами. Показатели гуморального и клеточного иммунитета во время плановой госпитализации в отделение иммунопатологии приведены в таблице 2.
Таблица 2
Результаты иммунологического обследования в отделении иммунопатологии
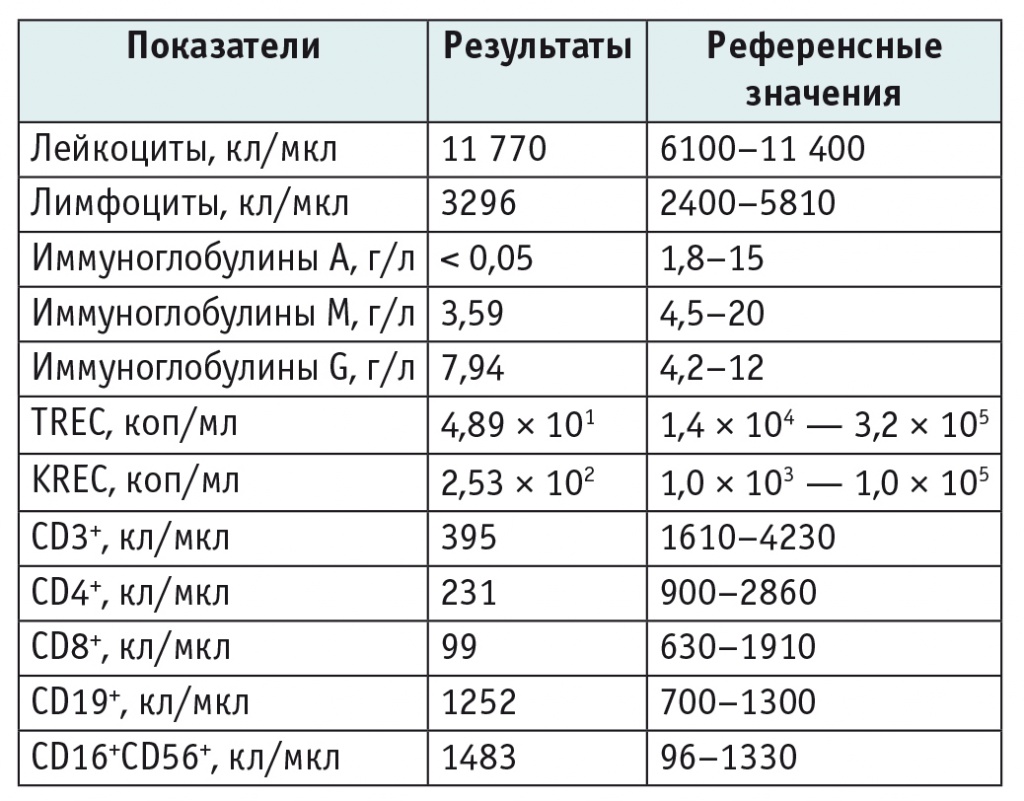
В дальнейшем ребенок еще несколько раз госпитализировался в отделение иммунопатологии ДГКБ № 9 им. Г. Н. Сперанского как для лечения острых ринитов и бронхитов, так и планово — для проведения заместительной терапии внутривенными иммуноглобулинами. Осенью 2016 г. в Национальном медицинском исследовательском центре детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева была проведена трансплантация гемопоэтических стволовых клеток.
ОБСУЖДЕНИЕ
Синдром Ниймеген характеризуется такими достаточно специфическими внешними признаками, как микроцефалия, отставание в физическом и умственном развитии. Даже если не принимать во внимание частую заболеваемость, врач общей практики должен был заподозрить врожденное заболевание и направить ребенка на консультацию к аллергологу-иммунологу или генетику. В представленном случае этого не произошло, ребенок был проконсультирован специалистом случайно. Судя по всему, причиной такой ситуации явилась недостаточность клинических симптомов иммунодефицита у данного ребенка, а возможность провести лабораторную диагностику методом проточной цитометрии в консультативных центрах первого уровня не предусмотрена в силу дороговизны анализа и сложности его интерпретации.
Как известно из данных литературы [6], а также видно из результатов обследования ребенка в представленном клиническом случае, уровни TREC и KREC у пациентов с синдромом Ниймеген значительно снижены, что позволяет заподозрить проблемы клеточного иммунитета до проведения фенотипирования лимфоцитов методом проточной цитометрии. Таким образом, возможность проведения малозатратного и простого в выполнении и интерпретации лабораторного исследования уровней TREC и KREC является крайне важной для работы медицинских учреждений первого и второго уровней, т. е. районных поликлиник и окружных амбулаторных центров.
ЗАКЛЮЧЕНИЕ
Внедрение исследования количества эксцизионных колец Т-клеточного рецептора и рекомбинационных колец каппа-делеционного элемента в лабораториях медицинских учреждений первого и второго уровней позволит значительно расширить диагностические возможности врачей общей практики в плане выявления пациентов с дефектами клеточного иммунитета, нуждающихся в углубленном обследовании аллергологом-иммунологом.
Выявление детей с врожденными иммунодефицитными состояниями до развития у них инфекционных, аутоиммунных и прочих осложнений значимо снизит детскую смертность, инвалидизацию и финансовую нагрузку на систему здравоохранения.








