К основным микрокристаллическим артритам относятся подагра и болезнь депонирования кристаллов пирофосфата кальция (БДПК). Подагра — системное тофусное заболевание, характеризующееся отложением кристаллов моноурата натрия (МУН) в различных тканях и развивающимся в связи с этим воспалением у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами[1]. БДПК является результатом накопления кристаллов пирофосфата кальция (ПФК) в суставном хряще и возникающего из-за этого воспаления иммунного характера[2]. Осаждение кристаллов МУН и ПФК может способствовать развитию острого и хронического воспаления суставов. О наличии в синовиальной жидкости одновременно кристаллов МУН и ПФК было сообщено несколькими авторами[9, 22, 23].
«Золотой стандарт» диагностики обоих заболеваний — обнаружение кристаллов в синовиальной жидкости. Тем не менее использование различных методов визуализации имеет большое значение для диагностики и лечения смешанных микрокристаллических артритов. Это особенно важно для диагностики БДПК, которой уделяется мало внимания.
Обычная рентгенография (Рг) благодаря ее низкой стоимости и доступности является основным методом визуализации. Она широко используется для обнаружения специфических признаков обоих заболеваний: кальцификации хряща (хондрокальциноза — ХК) при БДПК или внутрикостных тофусов при подагре. При кристалл-верифицированном диагнозе БДПК рентгенологически ХК выявляется в 29–98% случаев[17–19]. Ранее сообщалось, что Рг показывает наличие ХК только у 50% больных с кристалл-верифицированным диагнозом БДПК[6].
В соответствии с рекомендациями Европейской лиги борьбы с ревматизмом (European League Against Rheumatism) по диагностике подагры, Рг суставов недостаточно, чтобы подтвердить диагноз на ранней стадии, хотя рентгенологические изменения могут существовать на всех стадиях заболевания[26].
Недавно опубликованные данные подтверждают, что КТ суставов является важным методом визуализации при подагре и БДПК. КТ более информативна, чем Рг, в обнаружении ХК коленных суставов у пациентов с БДПК[6]. Показано, что применение КТ, а не МРТ и УЗИ, у больных хронической тофусной подагрой способствует выявлению мягкотканных и внутрикостных тофусов[15]. Кроме того, КТ суставов дает возможность отличить МУН от кальция, содержащего депозиты, благодаря различным значениям их плотности[20].
УЗИ суставов стало широко используемым методом визуализации в течение последних нескольких лет. При подагре УЗИ может показать отложения МУН в мягких тканях (тофусы) и на поверхности хряща — двойной контур[4]. Название «двойной контур» связано со способностью кристаллов МУН депонироваться на поверхности хряща, что при УЗИ выглядит как дополнительная светлая линия, параллельная линии перехода субхондральной кости в хрящ. УЗИ оказалось также чувствительным и специфичным методом для обнаружения ХК у пациентов с БДПК[6, 9, 10]. Тем не менее работ по сравнению информативности различных методов визуализации при смешанных микрокристаллических артритах мало.
Цель исследования: оценить информативность Рг, КТ и УЗИ при дифференциальной диагностике подагры и БДПК.
МАТЕРИАЛЫ И МЕТОДЫ
В одномоментное исследование, проведенное в 2014 г. в Научно-исследовательском институте ревматологии им. В. А. Насоновой, были включены 73 пациента (54 мужчины и 19 женщин), которые поступили с подозрением на микрокристаллический артрит. На основании результатов анализа синовиальной жидкости участников разделили на три группы: 22 человека с кристаллами МУН и ПФК в синовиальной жидкости составили I группу; 26 пациентов с кристалл-верифицированным диагнозом БДПК — II группу; 25 больных с кристалл-верифицированным диагнозом подагры — III группу.
У всех пациентов на момент осмотра был артрит, им произвели диагностическую пункцию с исследованием синовиальной жидкости методом поляризационной микроскопии (микроскоп Olympus СХ31-Р, Япония). Пациентам делали УЗИ, Рг и КТ коленных суставов. Основные данные больных представлены в таблице.
Таблица
Клиническая характеристика больных (n = 73)
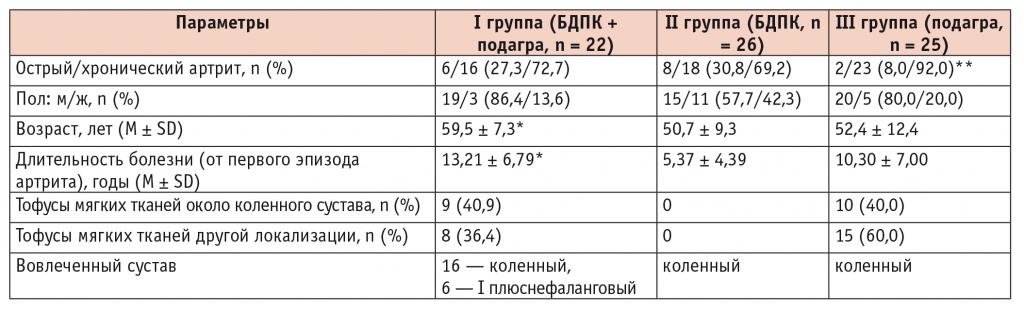
* Отличие от II группы статистически значимо (р < 0,05).
** Отличие от I и II групп статистически значимо (р < 0,05).
Примечание. БДПК — болезнь депонирования пирофосфата кальция.
Все пациенты подписали информированное согласие на участие в исследовании.
Критерием включения был возраст старше 18 лет. Критерии исключения: возраст младше 18 лет, подозрение на септический артрит и другое ревматическое заболевание.
Статистическая обработка полученных данных проводилась с использованием программ Statistica 8.0, Биостатистика. Результаты представлены в виде средних значений и средних квадратических отклонений (M ± SD), использовали непараметрический критерий Манна — Уитни, критерий χ2. Статистически значимыми считали различия при p < 0,05.
РЕЗУЛЬТАТЫ
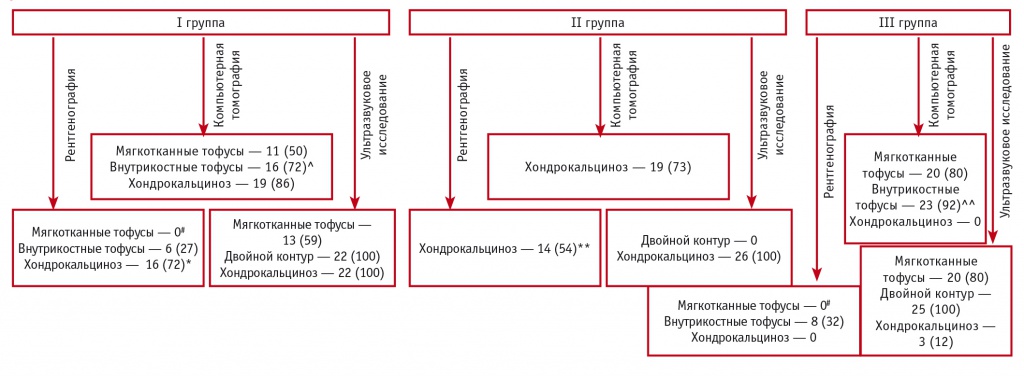
С помощью Рг не удалось выявить ХК и мягкотканные тофусы у больных подагрой (рис.). ХК при БДПК и при сочетании ее с подагрой статистически значимо чаще выявляли при помощи УЗИ, чем Рг (p = 0,0001 и р = 0,008 соответственно), различий между КТ и Рг, а также между КТ и УЗИ не было. КТ и УЗИ чаще Рг показывали наличие мягкотканных тофусов как у больных подагрой, так и при сочетании ее с БДПК (р = 0,0001 в обоих случаях). Внутрикостные тофусы у пациентов обеих этих групп чаще были видны при КТ, чем при Рг (в I группе p = 0,0001, в III группе p = 0,0026).
Рис. Информативность различных методов визуализации, n (%).
Примечание.
- Знаком (*) отмечены статистически значимые различия в частоте выявления хондрокальциноза при рентгенографии и УЗИ: (*) — в I группе (р = 0,008), (**) — во II группе (р = 0,0001).
- Знаком (#) отмечены статистически значимые различия в частоте выявления мягкотканных тофусов при КТ и УЗИ по сравнению с рентгенографией в I и III группах (р = 0,0001).
- Знаком (^) отмечены статистически значимые различия в частоте выявления внутрикостных тофусов при КТ и рентгенографии: (^) — в I группе (р = 0,0001), (^^) — в III группе (р = 0,0026)
ОБСУЖДЕНИЕ
Сочетание БДПК и подагры встречается достаточно редко. Существует несколько описывающих его публикаций[5, 8, 12, 24, 25], причина такого сочетания не до конца ясна[16]. Диагноз БДПК в исследованиях[5, 8] ставили на основе наличия ХК по данным Рг пораженных суставов. Возможно, что аномальный хрящ и воспаление, обусловленное кристаллами ПФК, могут способствовать осаждению кристаллов МУН и, наоборот, кристаллы ПФК откладываются в случае воспаления при подагре. Тем не менее и БДПК, и подагра — довольно распространенные заболевания, и неудивительно, что в некоторых случаях они сосуществуют, особенно у пожилых пациентов[26]. Нам не встретилось в литературе сравнение различных методов визуализации у больных со смешанными микрокристаллическими артритами.
Достаточно хорошо известен рентгенологический феномен, типичный для поздней подагры, — симптом «пробойника». Рентгенографически диагностируемые изменения развиваются в 10–40% случаев после повторных атак артрита и являются одним из поздних проявлений болезни[3, 22]. У большинства больных с рецидивирующим артритом и длительностью болезни 3–5 лет не удается идентифицировать какие-либо костные дефекты. Таким образом, рентгенологические изменения нельзя считать ранними для подагры[27].
При разработке классификационных критериев подагры было показано, что субкортикальные кисты без эрозий обнаруживаются у 11,9% больных подагрой и у 1,0–3,4% пациентов с пирофосфатной артропатией, ревматоидным и септическим артритом. Несмотря на низкую чувствительность и специфичность, этот рентгенологический признак был включен в клинико-лабораторный перечень критериев подагры.
W. C. Peh установлено, что типичные, четко дифференцированные «перфорированные» околосуставные эрозии с нависающими краями определяются рентгенологически не ранее чем через 6–12 лет после первого острого приступа подагры[21]. По нашим данным, внутрикостные тофусы при Рг выявляются у 32% больных подагрой и у 27% пациентов с сочетанием ее с БДПК.
В настоящее время Рг является «золотым стандартом» диагностики ХК в ежедневной практике и в клинических исследованиях. Однако ее чувствительность и специфичность либо не изучены (для коленных суставов), либо низкие. Так, для выявления ХК в лучезапястных суставах Рг обладает низкой чувствительностью (ОШ = 0,29; 95%-й ДИ: 0,05–0,62) и специфичностью (ОШ = 0,20; 95%-й ДИ: –0,15–0,55)[28]. Выявление ХК при Рг может быть затруднено малым размером кристаллов ПФК, недоступной локализацией либо значительной потерей хряща вследствие его разрушения[11]. Было показано, что ХК по данным Рг диагностируется у 50% больных[6], что согласуется с результатами нашего исследования: Рг позволила выявить ХК у 54% пациентов с БДПК и у 72% с сочетанием ее с подагрой.
УЗИ суставов при подагре и БДПК считается перспективным методом, и не исключено, что при создании новых критериев диагностики подагры такой признак, как двойной контур, будет предложен в качестве инструментального критерия.
Другим патологическим признаком, который можно идентифицировать с помощью УЗИ при подагре, является тофус. Выявление тофусных структур способствует проведению ранних терапевтических мероприятий.
По нашим данным, двойной контур был у всех пациентов с подагрой и с сочетанием подагры и БДПК. Мягкотканные тофусы выявлены у 80% больных подагрой и у 59% с сочетанием ее с БДПК.
УЗИ показало наличие ХК у всех пациентов с БДПК и с подагрой и БДПК, а также у 12% больных подагрой. Такой результат согласуется с данными G. Filippou и соавт., которые зафиксировали высокую чувствительность (ОР = 0,87; 95%-й ДИ: 0,69–1,04) и специфичность (ОР = 0,96; 95%-й ДИ: 0,90–1,03) УЗИ суставов в диагностике ХК[9].
Необходимо подчеркнуть, что из трех критериев наличия ХК, предложенных B. Frediani, мы учитывали при УЗИ только типичный признак — линейную кальцификацию в толще хряща, аналогичную рентгенологическому признаку[10]. Несколько работ («случай — контроль») доказали значимость УЗИ для выявления ХК в коленных суставах[9, 10]. Результаты, полученные в нашей работе, согласуются с данными зарубежных авторов, согласно которым УЗИ суставов дает возможность обнаружить кальцификацию хряща, невидимую при использовании рентгеновских методов.
Основным недостатком при трактовке данных УЗИ является недостаточное количество исследований суставов на сегодняшний день, а также отсутствие динамических наблюдений, которые прояснили бы взаимосвязь результатов УЗИ и Рг. Это помогло бы понять, когда и на какой стадии болезни изменения хряща, обнаруживаемые при УЗИ, становятся видимыми и при Рг.
Другой метод, потенциально значимый для визуализации тофусов, — КТ. Она позволяет выявить тофусы, локализующиеся как внутрикостно, так и в области сухожилий и мягких тканей[13, 14, 17]. КТ (в сравнении с УЗИ и МРТ) дает возможность более точно дифференцировать тофусные массы, так как средний показатель по шкале ослабления рентгеновского излучения (шкале Хаунсфилда) для депозитов кристаллов МУН достаточно стабилен и существенно отличается от такового для депозитов основных кристаллов кальция, причем независимо от кальцификации тофуса[15]. Особенно отчетливо видны тофусы на трехмерной КТ. По нашим данным, частота выявления мягкотканных тофусов у больных подагрой составила 80%, при сочетании ее с БДПК — 50%. Внутрикостные тофусы были у 92% больных подагрой и у 72% с сочетанием подагры и БДПК.
Значимость КТ в диагностике ХК неизвестна. В литературе нам встретилось только одно исследование, где сравнивается информативность КТ и Рг при выявлении ХК[6]. По данным исследования, КТ позволила определить ХК у 71% больных, что согласуется с нашими данными (ХК выявлен у 73% больных БДПК и у 86% с сочетанием подагры и БДПК). Стандартная Рг дает лишь двухмерное изображение сустава, что делает вероятной потерю изображения имеющихся депозитов ПФК в недоступных местах. Преимуществом КТ является трехмерная визуализация сустава, что помогает исключить эту проблему[7].
ЗАКЛЮЧЕНИЕ
Можно констатировать, что наиболее информативным методом дифференциальной диагностики микрокристаллических артритов, по нашим данным, является ультразвуковое исследование суставов. Компьютерная томография превосходит рентгенографию в выявлении внутрикостных тофусов и эрозий у больных подагрой и хондрокальциноза у пациентов с болезнью депонирования пирофосфата кальция. Но для подтверждения диагностической значимости различных методов необходимы дальнейшие исследования.








