ВВЕДЕНИЕ
Преэклампсия занимает одно из ведущих мест в структуре причин материнской и перинатальной заболеваемости и смертности. Клинически данное заболевание характеризуется появлением артериальной гипертензии и протеинурии после 20-й недели беременности. Одними из патогенетически доказанных звеньев развития преэклампсии являются патологическая плацентация и, как следствие, эндотелиальная дисфункця. Принято различать умеренную и тяжелую преэклампсию. Тяжелая преэклампсия сопровождается развитием полиорганной недостаточности.
Впервые HELLP-синдром в виде триады симптомов — гемолиза, тромоцитопении и цитолиза — был описан L. Weinstein в 1982 г. Частота развития HELLP-синдрома у женщин с преэклампсией достигает 10–20%[1–3]. Однако в 20% случаев HELLP-синдром не сопровождается предшествующими типичными симптомами преэклампсии (артериальной гипертензией и протеинурией), но характеризуется поражением таких органов, как печень, сердце, легкие, головной мозг и почки[4–6].
В настоящее время HELLP-синдром рассматривают как один из частных случаев тромботической микроангиопатии (ТМА), связанных с беременностью, который может возникнуть спонтанно, без предшествующей гипертензии. ТМА представляет собой клинико-морфологический синдром группы гетерогенных заболеваний с повреждением эндотелия сосудов микроциркуляторного русла, артериолярными и капиллярными тромбозами, развитием гемолитической анемии, тромбоцитопении и ишемическими повреждениями органов вплоть до полиорганной недостаточности[7–9]1.
Поиск этиологических механизмов развития ТМА и HELLP-синдрома — актуальная проблема современного акушерства, так как материнская смертность от HELLP-синдрома составляет 24%, а перинатальная смертность достигает 60%, при этом классическая триада симптомов может отсутствовать или быть стертой, что вызывает трудности в постановке диагноза, а тактика ведения таких пациенток остается предметом дискуссии.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Представляем клинический случай HELLP-синдрома, развившегося в послеродовом периоде.
Пациентка Г. 19 лет в 2019 году была переведена из родильного дома со стремительным течением тяжелой преэклампсии на 1-е сутки послеродового периода в федеральный специализированный перинатальный центр ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России с диагнозом: 1-е сутки после первых своевременных самопроизвольных родов в головном предлежании гипотрофичным плодом на 38–39-й неделе гестации. Тяжелая преэклампсия. Угрожающий разрыв промежности. Перинеотомия-перинеорафия.
В родильное отделение пациентка поступила с началом родовой деятельности на сроке гестации 38 1/7 недели. При поступлении у нее диагностирована преэклампсия умеренной степени на основании протеинурии в разовой порции мочи 3,0 г/л, синдрома задержки роста плода, повышения артериального давления (АД) до 130/80 мм рт. ст. Остальные лабораторные параметры были в пределах референсных значений.
Роды протекали в умеренном темпе на фоне длительной эпидуральной аналгезии, в связи с угрожающим разрывом промежности выполнена перинеотомия. В 09:15 родилась живая доношенная девочка массой 2250 г, длина тела — 45 см, оценка по шкале Апгар — 8/9 баллов. Общая кровопотеря после родов составила 300 мл. Общая продолжительность родов — 8 часов 30 минут, безводный период — 5 часов.
В раннем послеродовом периоде отмечались подъем АД (максимально до 160/100 мм рт. ст.), макрогематурия. Начата магнезиальная комбинированная антигипертензивная терапия (метилдопа, блокаторы кальциевых каналов). Через 10 часов после родов появился геморрагический синдром: носовое кровотечение, кровотечения из десен и языка, петехии на коже, щипковый симптом положительный. Состояние тяжелое. По данным лабораторного исследования, установлены анемия, тромбоцитопения, гипербилирубинемия, нарастание активности аланинаминотрасферазы (АЛТ), аспартатаминотрансферазы (АСТ) и лактатдегидрогеназы (ЛДГ), появление шизоцитов 9 промилле, протеинурия 3 г/л (табл. 1). В связи с тяжестью состояния пациентка переведена в стационар III уровня.
Таблица 1. Динамика лабораторных показателей пациентки Г. в городском родильном доме
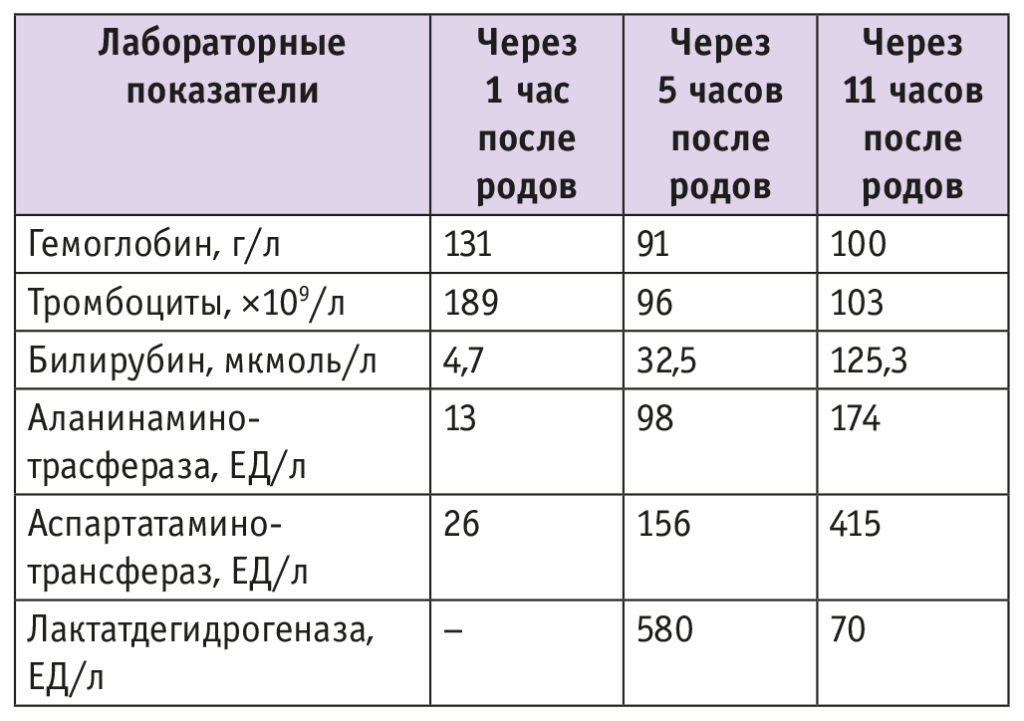
Из анамнеза известно, что в женской консультации беременная регулярно наблюдалась с 8–9 недель. Данная беременность первая, наступила самостоятельно. Масса тела на момент поступления — 66 кг, рост — 170 см, прибавка массы за беременность физиологическая. Аллергический анамнез не отягощен. В детстве болела ветряной оспой, простудными заболеваниями; страдает миопией слабой степени, другие хронические заболевания и травмы отрицала. Наследственность: у бабушки острое нарушение мозгового кровообращения в 76 лет. Во время беременности не болела, стационарно не лечилась.
В федеральный перинатальный центр ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России пациентка переведена реанимационно-хирургической бригадой скорой медицинской помощи. На момент осмотра активно жалоб не предъявляла. Состояние тяжелое. Тяжесть состояния обусловлена заторможенностью, сонливостью. Кожа бледная, теплая, петехиальные кровоизлияния на коже в местах прикрепления электродов электрокардиографа, манжеты тонометра. Склеры иктеричные. Видимые слизистые чистые, розовые, кровоточивость десен. Периферические отеки: пастозность голеней.
Дыхание самостоятельное, эффективное. Частота дыхательных движений — 16 в мин. Гемодинамика с тенденцией к гипертензии. Пульс ритмичный. Частота сердечных сокращений — 102 в мин. Синусовая тахикардия. АД — 170/100 мм рт. ст.
Живот мягкий, безболезненный при пальпации, подвздут. Перистальтика вялая. Матка плотная, дно матки на II поперечных пальца ниже пупка. Выделения из половых путей скудные, кровянистые. Диурез по мочевому катетеру почасовой, 50 мл/час, макрогематурия. Пациентка была госпитализирована в отделение анестезиологии и реаниматологии взрослых (ОАиРВ).
В лабораторных анализах на фоне анемии выявлены шизоциты, тромбоцитопения третьей степени, по классификации Mississippi, гипопротеинемия, повышение активности трансаминаз и ЛДГ, реакция Кумбса отрицательная.
Наблюдалось также повышение содержания провоспалительных маркеров, а именно С-реактивного белка и прокальцитонина (табл. 2, 3).
Таблица 2. Динамика показателей клинического анализа крови пациентки Г.
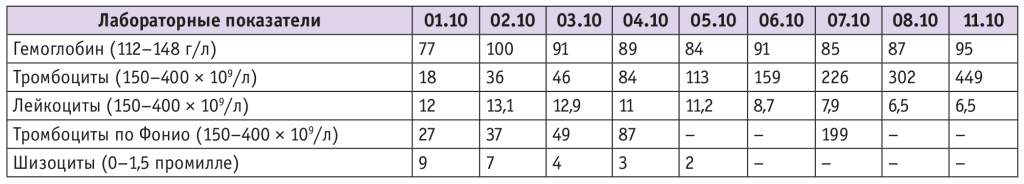
Примечание. Здесь и в таблице 3 в скобках указаны нормативные значения.
Таблица 3. Динамика лабораторных показателей пациентки Г.
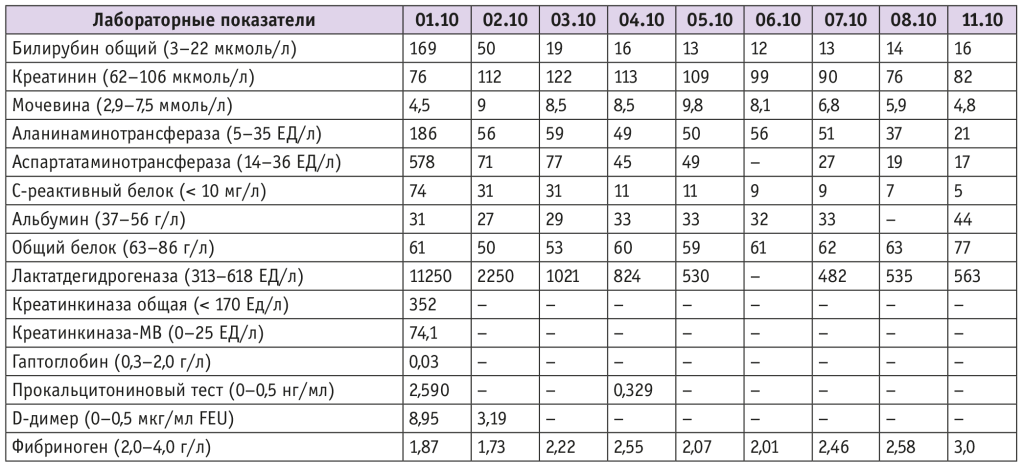
На основании полученных данных сложилось представление о текущей ТМА (Кумбс-негативная гемолитическая анемия, шизоциты в мазке периферической крови, повышение активности ЛДГ, снижение уровня гаптоглобина), генез которой требовал уточнения и дифференциальной диагностики тромботической тромбоцитопенической пурпуры (ТТП), атипичного гемолитико-уремического синдрома (аГУС), катастрофического антифосфолипидного синдрома, вторичной ТМА на фоне воспалительного процесса, HELLP-синдрома.
В ходе дифференциальной диагностики с высокой долей вероятности подтвержден HELLP-синдром I степени тяжести, по классификации Mississipi trial (активность АСТ — 578 ЕД/л, АЛТ — 186 ЕД/л, ЛДГ — 11250 ЕД/л, гемолитическая анемия, тромбоцитопения 18 × 109/л).
Терапией первой линии при HELLP-синдроме и ТМА, согласно письму «Тромботическая микроангиопатия в акушерстве» от 2017 г., в послеродовом периоде является терапевтический плазмообмен в дозе 30–40 мл/кг2, его и начали проводить. Продолжены также терапия сернокислой магнезией, антигипертензивная (метилдопа 500 мг 3 раза в сутки, нифедипин 20 мг 2 раза в сутки), утеротоническая, антифибринолитическая, эмпипирическая антибактериальная терапия с целью профилактики восходящей инфекции (антибиотики широкого спектра действия), профилактика тромбоэмболических осложнений с применением низкомолекулярных гепаринов, гастропротекция. С учетом гематологических показателей произведена гемотрансфузия эритроцитарной массы по индивидуальному подбору в объеме 1000 мл[8].
После первого сеанса плазмообмена на фоне интенсивной терапии отмечена положительная динамика лабораторных показателей: гемолиз не нарастал, активность АЛТ, АСТ, ЛДГ снизилась. Зафиксировано нарушение выделительной функции почек (нарастание уровней креатинина с 76 до 122 мкмоль/л и мочевины с 4,5 до 9,8 ммоль/л), однако диурез сохранен (см. табл. 3). На фоне многокомпонентной антигипертензивной терапии наблюдалась тенденция к понижению АД. Продолжены сеансы плазмообмена и комплексное интенсивное лечение.
В ходе дообследования исключены:
-
катастрофический антифосфолипидный синдром (антитела к кардиолипинам IgG — 1,6 Е/мл, IgM — 1 Е/мл, к β2-гликопретеину — 4 Е/мл, к гликопротеину I не выявлены);
-
ТТП (активность ADAMTS-13 в плазме крови составила 73%);
-
ГУС (бактериологическое исследование фекалий на Escherichia coli O151:Н7 и других шига-продуцирующих бактерий — полимеразная цепная реакция отрицательная);
-
пароксизмальная ночная гемоглобинурия (ПНГ-клон не обнаружен).
В течение последующих трех суток от начала терапии отмечалась положительная динамика в состоянии пациентки, которую наблюдала и вела мультидисциплинарная команда специалистов: анестезиолог-реаниматолог, акушер-гинеколог, гематолог, нефролог. В отделении ОАиРВ пациентка находилась 7 суток. Проводилось многокомпонентное лечение: плазмообмен (4 сеанса), гемотрансфузия (переливание 1000 мл эритроцитарной взвеси по индивидуальному подбору), утеротоническая, инфузионная, магнезиальная (2 суток), многокомпонентная антигипертензивная, антибактериальная терапия (антибиотики широкого спектра действия); применялись низкомолекулярные гепарины.
На 7-е сутки послеродового периода пациентка переведена в послеродовое отделение в удовлетворительном состоянии с нормализацией клинико-лабораторных параметров (см. табл. 2, 3). На 11-е сутки в удовлетворительном состоянии ее выписали на амбулаторный этап ведения с рекомендациями наблюдения у нефролога с диагнозом: Послеродовый период 11-е сутки. Тяжелая преэклампсия. Тромботическая микроангиопатия. HELLP-синдром. Анемия легкой степени. Осложненный гинекологический анамнез.
ОБСУЖДЕНИЕ
Данный клинический случай продемонстрировал стремительное развитие заболевания у первобеременной 19 лет в раннем послеродовом периоде. Вероятнее всего, в данном случае родоразрешение послужило триггером столь стремительного нарастания симптоматики HELLP-синдрома. По данным литературы, в 30% случаев HELLP-синдром возникает в послеродовом периоде, и если это осложняется острой почечной недостаточностью вследствие выраженного гемолиза, отличить его от ГУС, в 74% случаев развивающегося в III триместре беременности и раннем послеродовом периоде, очень сложно[8]. В описанном клиническом наблюдении выделительная функция почек была нарушена, но ее удалось восстановить на фоне интенсивной терапии, диурез был сохранен, что обеспечило благоприятный прогноз.
Пациентка Г., в соответствии с письмом «Тромботическая микроангиопатия в акушерстве» 2017 г.3, маршрутизирована на III уровень оказания помощи, где ее дообследовали, согласно алгоритму.
Интерес акушеров-гинекологов вызывает дифференциальная диагностика HELLP-синдрома, ТМА и аГУС. Постановка диагноза сложна, так как происходит методом исключения в ходе динамического наблюдения за больной.
Дообследование пациентки Г. выполнено в полном объеме, по международным рекомендациям. Таким образом, эффективная терапия и профилактика HELLP-синдрома возможны при одновременном влиянии на все патогенетические звенья.
HELLP-синдром является частой причиной острого повреждения почек (ОПП) во время беременности, он становится причиной 36–50% всех случаев ОПП, связанных с беременностью[9]. По результатам проведенного систематического обзора и метаанализа, у пациенток с HELLP-синдромом в 4,87 раза (95% ДИ: 3,31–7,17, p = 0,000) выше риск острой почечной недостаточности[10]. Примечательно, что HELLP-синдром симптоматически схож с ГУС, особенно с аГУС, и ТТП в послеродовом периоде[11].
ТМА после родов включает в себя состояния, которые напоминают HELLP-синдром по лабораторным показателям и клинической картине, но ее течение характеризуется постепенным нарастанием признаков тромбоза в микроциркуляторном русле и развитием полиорганной недостаточности.
ТМА не поддается классическим методам лечения, эффективным в отношении HELLP-синдрома. В этих случаях обычно улучшение состояния пациенток следует за началом терапевтического плазменного обмена[12]. Исследование M.A. Erkurt и соавт. 2021 г. доказало, что у всех пациенток с HELLP-синдромом после терапевтического плазменного обмена произошло очень существенное клиническое и лабораторное улучшение в течение 24 часов[13].
Вызывает споры использование плазмообмена при лечении HELLP-синдрома. Во время беременности у женщин с диагностированным HELLP-синдромом плазмообмен не показан, так как откладывает сроки родоразрешения с сохранением главного триггера активации комплемента — плаценты. Однако в послеродовом периоде при сохраняющихся клинико-лабораторных проявлениях ТМА рекомендовано проводить плазмообмен для предотвращения лавинообразного характера развития ТМА4. В представленном случае постепенное улучшение состояния пациентки и нормализация гематологических параметров доказали его эффективность.
По результатам многих исследований, использование терапевтического плазмообмена — эффективный метод лечения HELLP-синдрома у пациенток с отсутствием эффекта от общепринятой терапии, что значительно снижает риски материнской смерти[14]. Данные современной литературы доказывают, что терапевтический плазмообмен также эффективен у пациенток с полиорганной недостаточностью[15].
Женщин с HELLP-синдромом, текущей ТМА должны вести совместно акушер-гинеколог и анестезиолог-реаниматолог с соответствующим клиническим опытом и современными знаниями, а также смежные специалисты (кардиолог, гематолог, нефролог) в стационаре III уровня[16–19].
ЗАКЛЮЧЕНИЕ
Всем практикующим врачам, которые предположили диагноз ТМА, необходимо немедленно проинформировать об этом главных внештатных специалистов и организовать перевод беременных и родильниц в перинатальный центр при многопрофильном стационаре. Подход к лечению пациенток с тяжелой преэклампсией, HELLP-синдромом и текущей ТМА должен быть мультидисциплинарным в стационарах III группы. Такой подход позволит своевременно провести дополнительную диагностику и оказать квалифицированную специализированную помощь.
Поступила: 30.11.2023
Принята к публикации: 09.01.2024
________
1 О направлении информационно-методического письма «Тромботическая микроангиопатия в акушерстве». Письмо Министерства здравоохранения РФ № 15-4/1560-07 от 5 мая 2017 года. URL: https://docs.cntd.ru/document/456072686 (дата обращения — 07.02.2024).
2 О направлении информационно-методического письма «Тромботическая микроангиопатия в акушерстве»...
3 О направлении информационно-методического письма «Тромботическая микроангиопатия в акушерстве»...
4 Преэклампсия. Эклампсия. Отеки, протеинурия и гипертензивные расстройства во время беременности, в родах и послеродовом периоде. Клинические рекомендации. 2021. URL: https://mz.mosreg.ru/dokumenty/informaciya/klinicheskie-rekomendacii/06-07-2021-10-31-15-preeklampsi... (дата обращения — 07.02.2024).







