ВВЕДЕНИЕ
Врожденная диафрагмальная грыжа (ВДГ) — не только медицинская, но и социальная проблема, так как интенсивная терапия и реабилитация детей при ВДГ одни из наиболее длительных и дорогостоящих среди таковых при пороках развития плода. В США стоимость одного случая ведения новорожденного с ВДГ составляет от 180 до 810 тысяч долларов в год. При этом значительная финансовая нагрузка ложится на семью ребенка с ВДГ, расходы которой не удается подсчитать[1].
ВДГ представляет собой аномалию внутриутробного развития, которая встречается с частотой 1 : 3000 — 1 : 5000 живорожденных детей и связана с дефектом диафрагмы, через который в течение антенатального развития органы брюшной полости перемещаются в грудную клетку плода. Это создает повышенное внутригрудное давление, что препятствует нормальному развитию альвеолоцитов и легочных сосудов[2].
Как правило, формирование ВДГ происходит до 10 недели беременности, и ее фенотипические проявления варьируют от эвентрации диафрагмы или локальных ее дефектов до полной агенезии купола диафрагмы.
Благодаря моделям животных с ВДГ стало понятно, что снижение пролиферации, усиление апоптоза, а также дефекты миграции и дифференцировки клеток-предшественников являются основными механизмами, лежащими в основе ВДГ[3]. Этиология и патогенез заболевания остаются недостаточно ясными, делались попытки объяснить формирование ВДГ генетическими нарушениями[4–7]. Как правило, хромосомные аномалии сочетаются с множественными аномалиями развития, в состав которых входит ВДГ, а при изолированной ВДГ хромосомная патология обнаруживается редко. Главной нерешенной проблемой ВДГ остаются не выявленные генетические аномалии, возникающие de novo. Они ассоциируются с более высокой смертностью, стойкой легочной гипертензией и худшим исходом для развития нервной системы в постнатальном периоде[3, 8]. Смертность новорожденных, связанная с ВДГ, в Европе и США составляет 30–50%[1, 4, 9].
Развитие перинатальной медицины, совершенствование реанимационной помощи, использования ИВЛ и экстракорпоральной мембранной оксигенации, оксида азота повысили выживаемость новорожденных с ВДГ. Но, несмотря на эти значительные успехи, прогнозирование степени тяжести ВДГ, риска развития тяжелой легочной гипертензии и полиорганной недостаточности, а следовательно, выживаемости и заболеваемости новорожденных продолжает оставаться несовершенным[1, 10].
В настоящее время существует ряд прогностических маркеров тяжести гипоплазии легких при ВДГ, которые основаны на показателях, полученных при диагностике порока развития плода во время беременности с помощью УЗИ и МРТ. К ним относятся отношение размеров контралатерального легкого и окружности головки плода (o/e LHR), индекс компрессии сердца (ИКС), отношение наблюдаемого к ожидаемому объему легкого (TFLV o/e), отношение объема печени в грудной клетке к объему грудной клетки (LiTR), определение положения печени и желудка в грудной клетке плода[11–14].
В связи с этим целью нашего исследования стал анализ частоты выявления ВДГ у плода на антенатальном этапе и перинатальных исходов у новорожденных с ВДГ в Российской Федерации на примере выборки женщин, обратившихся на перинатальный консилиум ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
МАТЕРИАЛЫ И МЕТОДЫ
Проведен ретроспективный анализ 235 случаев ВДГ у плодов и новорожденных трех вариантов локализации (левосторонняя, правосторонняя, билатеральная), отобранных при проведении федерального перинатального консилиума с последующим родоразрешением и оказанием специализированной помощи новорожденным на базе ФГБУ «НМИЦ акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России.
Проанализированы возраст, социальное положение, регион проживания женщины, срок беременности при установлении диагноза ВДГ, срок и метод родоразрешения, сопутствующие пороки развития плода, массо-ростовые показатели новорожденных, оценка состояния по шкале Апгар на 1-й и 5-й минутах, экстренность кесарева сечения, перинатальная смертность.
Для сравнения двух не связанных между собой выборок использовали непараметрический критерий Манна — Уитни, сходные характеристики сравнивали с помощью критерия χ2.
Статистический анализ и управление данными выполняли с применением программ Statistica 10.0 (Statsoft Inc., США) и Excel (Microsoft Corporation, США). Статистически значимыми результаты считали при p < 0,05.
РЕЗУЛЬТАТЫ
На базе ФГБУ «НМИЦ АГП им. Кулакова» Минздрава России организована работа федерального перинатального консилиума, благодаря которому в Центре концентрируются женщины со всеми вариантами аномалий развития плода, включая различные варианты ВДГ. За 4 года работы консилиума (2018–2021) наблюдалась четкая тенденция к увеличению частоты обращений женщин с ВДГ плода, общее количество которых составило 235 (рис. 1).
Рис. 1. Динамика числа обращений женщин на перинатальный консилиум ФГБУ «НМИЦ АГП им. Кулакова» Минздрава России в связи с выявлением врожденной диафрагмальной грыжи у плода
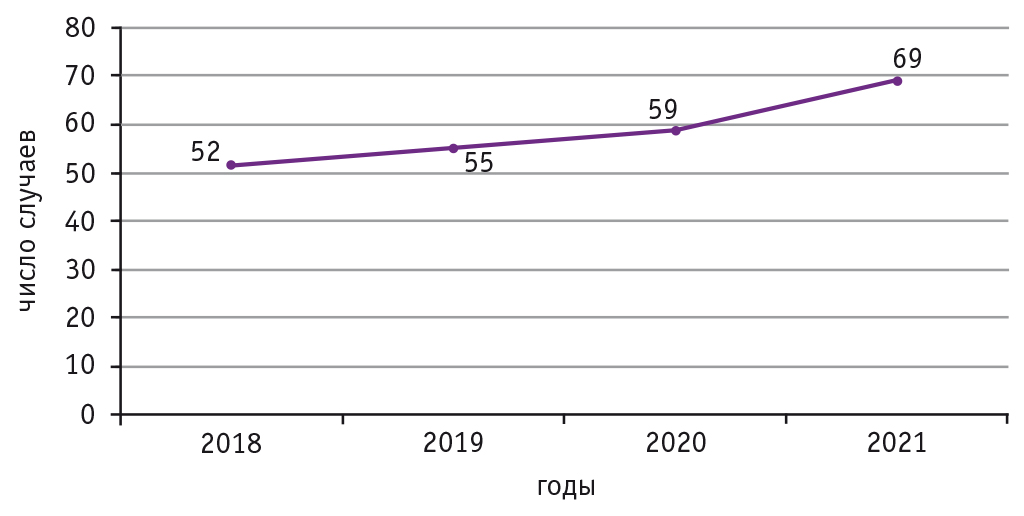
Диагностика ВДГ возможна с 13 недели беременности, но, согласно мировому опыту, 2/3 случаев выявления порока развития приходятся на второй триместр беременности[6, 15]. В нашей стране наблюдается подобная же закономерность, что свидетельствует о высоких диагностических возможностях на региональном уровне. Так, в третьем триместре ВДГ обнаружена в 56 (23,8%) случаях, во втором триместре — в 177 (75,3%), а в первом триместре — только у 2 (0,9%) женщин.
Согласно современному представлению о формировании ВДГ, причины ее развития можно разделить на три группы: геномная, эпигеномная и протеомная. Вторая и третья группы причин определяют развитие ВДГ в большинстве случаев (70%), но остаются малоизученными, а первая встречается реже (30%) и всегда сочетается с хромосомными аномалиями или генетическими синдромами, которые достаточно хорошо известны[1, 16, 17].
К сожалению, в РФ мало внимания уделяется данному аспекту формирования ВДГ, так как среди обратившихся на перинатальный консилиум пациенток с ВДГ плода только у 38 (16,2%) проведено пренатальное генетическое исследование. В связи с этим в некоторых случаях можно было предусмотреть возникновение во время беременности аномалии развития плода, то есть определить курабельность случая на неонатальном этапе. Тем не менее у 8 (21,1%) из 38 пациенток выявлена генетическая аномалия, которая в 5 случаях оказалась показанием для прерывания беременности. Остальные 3 пациентки продолжили ее до доношенного срока в связи с поздним выявлением аномалии и категорическим отказом от прерывания беременности.
По локализации в подавляющем большинстве случаев выявлены левосторонние ВДГ (n = 211, 89,7%), значительно реже — правосторонние (n = 22, 9,4%), и только у 2 (0,9%) пациенток диагностировано двустороннее поражение. Данное распределение случаев ВДГ по локализации полностью соответствует аналогичным показателям в мире [6].
У 103 (43,8%) женщин возраст на момент рождения ребенка с ВДГ составил от 18 до 29 лет, у 117 (49,8%) — 30–39 лет, у минимального числа пациенток (n = 15, 6,4%) — 40 лет и более.
Социальный статус беременных не различался в зависимости от возраста (табл. 1). Более 50% женщин не имели постоянной работы или о ней не информировали, в остальных случаях были служащими в государственных или коммерческих учреждениях.
Таблица 1
Возраст и социальный статус пациенток с врожденной диафрагмальной грыжей плода, n (%)
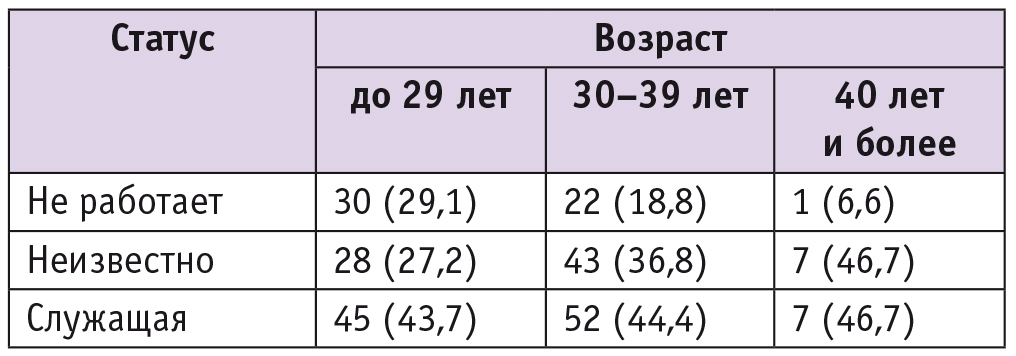
Большое значение для перинатального исхода при ВДГ имеет срок беременности, в котором установлен диагноз порока развития. При обнаружении до 22 недель беременности есть возможность оценить тяжесть гипоплазии легких при ВДГ и перспективу выживаемости новорожденного и в зависимости от результата принять решение о целесообразности пролонгирования или прерывания беременности. Нами установлено, что в регионах выявляют ВДГ до 22 недель беременности почти в каждом третьем случае (32,4%), но в Центр для проведения перинатального консилиума женщины с данной патологией плода направлялись в 2,1 раза реже (15,4%). Эту разницу можно объяснить решением пациенток прервать беременность и низкой осведомленностью медицинского персонала в регионах о диагностических и лечебных возможностях ФГБУ «НМИЦ АГП им. Кулакова» Минздрава России.
На основании проведенного федерального перинатального консилиума специалисты Центра для каждого случая ВДГ приняли одно из возможных решений, которое обусловлено степенью тяжести гипоплазии легких. В 31 (13,2%) случае в связи с выраженной гипоплазией легких, компрессией сердца, сочетанием с генетической аномалией или множественными пороками развития рекомендовано прерывание беременности. На поздних сроках беременности в связи с некурабельностью новорожденного и настойчивым желанием женщины сохранить беременность в 21 (9%) случае предложено родоразрешение по месту жительства.
В связи с трудностью визуализации порока развития или необходимостью пренатальной инвазивной диагностики 33 (14%) женщинам рекомендовано повторное обследование, от которого они отказались и продолжили наблюдение по месту жительства.
Тем не менее наиболее значительной группе пациенток (n = 150, 63,8%) с ВДГ плода предложено родоразрешение с последующим постнатальным лечением патологии новорожденного в условиях Центра.
Согласно критериям оценки тяжести гипоплазии легких при ВДГ мировой литературы[9] и на основании методик, разработанных в Центре[12, 18, 19], выявленные ВДГ распределялись на три степени тяжести в зависимости от выраженности гипоплазии легких и компрессии сердца: легкую, умеренную и тяжелую (табл. 2).
Таблица 2
Оценка степени тяжести врожденной диафрагмальной грыжи (ВДГ) на антенатальном этапе, n (%)
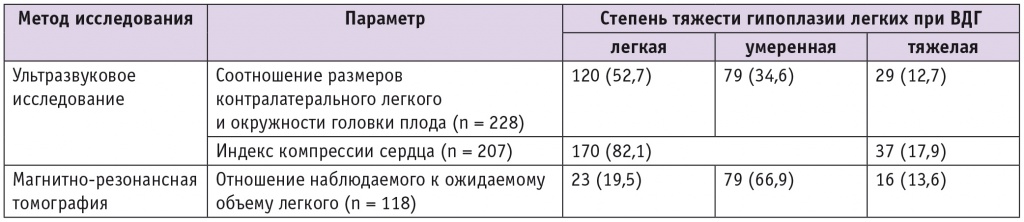
Из полученных результатов следует, что определение степени тяжести ВДГ по трем параметрам двух методов исследования не является рутинным. Так, расчет o/e LHR проводится практически в каждом случае (n = 228, 97%), реже определяют ИКС (n = 207, 88,1%), и, к сожалению, практически у каждой второй беременной не проводят МРТ плода (n = 118, 50,2%). При этом достоверность и чувствительность методов диагностики тяжелой ВДГ сопоставима. В то же время случаи ВДГ умеренной степени, по данным УЗИ, трактуются МРТ как тяжелые.
Проникновение печени в грудную клетку вызывает более выраженную компрессию легких и сердца, поэтому для диагностики ее визуализация имеет определяющее значение. В связи с этим для прогнозирования выживаемости новорожденных с ВДГ введены понятия liver up и liver down. При первом состоянии смертность новорожденных со средней и тяжелой ВДГ составляет 40 и 60% соответственно, а при втором — 15%[15].
У пациенток перинатального консилиума Центра также проведена оценка этого показателя, и установлено, что проникновение печени в грудную клетку плода наблюдается, по данным УЗИ, в 45,6% и на МРТ в 60,8% случаях в группе с умеренной степенью ВДГ.
Это является неблагоприятным фактором для выживаемости новорожденного. Таким образом, группа с низкой прогнозируемой выживаемостью, по данным УЗИ, увеличивается в 2,2 раза (12,7 против 28,5%), а по данным МРТ — в 4 раза (13,6 против 54,2%), что требует поиска новых методов предотвращения инвазии печени в грудную клетку в антенатальном периоде и лечения тяжелой полиорганной недостаточности на неонатальном этапе (табл. 3).
Таблица 3
Прогнозирование перинатальных исходов после выявления liver up с помощью ультразвукового исследования и магнитно-резонансной томографии, n (%)

Дополнительным осложняющим фактором течения неонатального периода у новорожденного с ВДГ может стать ее сочетание с другим вариантом аномалии развития. Нами выявлено, что у плода почти каждой второй беременной (n = 115, 48,9%) ВДГ была изолированным пороком развития. Более чем в трети случаев (n = 93, 39,6%) наблюдалось ее сочетание с врожденным пороком развития сердца (ВПС), и почти с равной частотой ВДГ входила в состав множественных пороков развития или сочеталась с другими вариантами врожденных пороков развития: 14 (6%) и 13 (5,5%) соответственно.
Наиболее распространенными типами ВПС оказались различные варианты дефекта межжелудочковой перегородки (59,1%) и гипоплазия отделов аорты (23,7%).
Почти все отобранные на перинатальном консилиуме для родоразрешения женщины (n = 136, 90,7%) завершили беременность в условиях Центра. Критериями исключения для отбора на родоразрешение в Центре являлись наличие анеуплоидии плода, известные структурные геномные варианты, другие серьезные аномалии плода или синдромальная мутация. Из отобранных пациенток родоразрешены через естественные родовые пути (ЕРП) 87 (64%). В остальных 49 (36%) случаях произведена операция кесарева сечения.
Родоразрешение проведено в сроках беременности от 32 до 41 недели. Преждевременно родились 20 (14,7%) детей и своевременно 116 (85,3%). Смертность новорожденных после преждевременного родоразрешения составила 9 (45%), причем гибель наступила в возрасте от 1 до 29 суток и в большинстве случаев (n = 8, 88,9%) до проведения реконструктивной операции диафрагмы. На доношенном сроке беременности уровень смертности был 50 (43,1%). Среди погибших детей в 6 случаях удалось выполнить операцию по восстановлению целостности диафрагмы.
Общий уровень перинатальной смертности составил 59 (43,4%).
Изучение перинатальной смертности в зависимости от метода родоразрешения показало, что после родов через ЕРП погибли 33 (37,9%) новорожденных, из которых только трем (9,1%) удалось провести оперативное вмешательство на диафрагме. Путем кесарева сечения родоразрешены 49 женщин, у которых в неонатальном периоде погибли 26 (53,1%) новорожденных, включая трех (11,5%) детей с выполненной оперативной коррекцией диафрагмы (р > 0,05).
На первый взгляд, на основании полученных данных можно предположить, что рутинное проведение кесарева сечения не улучшает перинатальный исход для новорожденных с ВДГ.
Однако более детальное рассмотрение экстренности выполнения оперативного родоразрешения и показаний к нему свидетельствует, что повышение перинатальной смертности происходит, если кесарево сечение выполняется по экстренным показаниям в родах.
Так, смертность новорожденных после экстренных оперативных родоразрешений составила 58,6%, что на 16,5% выше аналогичного показателя при плановом кесаревом сечении (42,1%) (р > 0,05). Несмотря на то что это различие не является статистически значимым, на наш взгляд, оно отражает тенденцию, которая может стать закономерностью по мере увеличения выборки.
Кроме того, наиболее распространенным показанием к экстренному оперативному родоразрешению послужила гипоксия плода в родах, которая развивалась почти в каждом втором случае (44,4%). Среди новорожденных, перенесших в родах гипоксию, смертность составила 50%. Особенно неблагоприятными были показатели смертности у новорожденных от матерей, перенесших преиндукцию, индукцию родов и в связи с неэффективностью и гипоксией плода в последующем родоразрешенных путем кесарева сечения.
Однако наиболее часто (83,3%) новорожденные погибали после кесарева сечения, выполненного в связи с отсутствием эффекта от проведения преиндукции или индукции родов.
В мировой литературе продолжается спор о выборе оптимального срока родоразрешения при ВДГ у плода[20–22]. Одни ученые считают оптимальным сроком родов 38–39 недель беременности, другие, напротив, такой закономерности не наблюдают. Мы также провели подобный анализ и пришли к выводу, что вне зависимости от вида родоразрешения уровень перинатальной смертности повышается с ростом срока гестации от 38 до 40 недели и более (рис. 2).
Рис. 2. Уровень смертности новорожденных в зависимости от срока беременности и метода родоразрешения, n (% от общего числа родоразрешенных в данный срок)
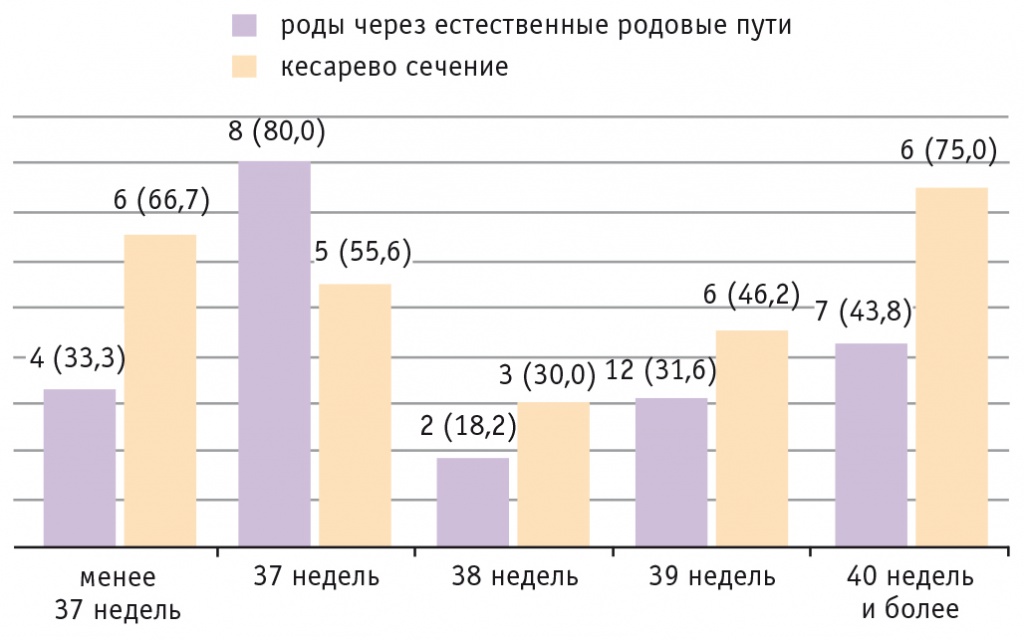
При этом новорожденные гибнут в 2 раза чаще на сроке беременности 40 недель и более после выполнения операции кесарева сечения, чем после родов через ЕРП. Однако показаниями для проведения оперативного родоразрешения служили отсутствие эффекта от преиндукции или индукции родов и гипоксия плода в родах.
Установлено также, что у младенцев, родившихся на сроке беременности 37 недель через ЕРП и на сроке менее 37 недель после кесарева сечения, повышен риск гибели в неонатальном периоде. Перинатальная смертность составила 80 и 66,7% соответственно. Таким образом, оптимальным сроком родоразрешения и прогнозирования минимального уровня перинатальных потерь для плодов с ВДГ следует считать 38–39 недель.
Первыми постнатальными предикторами выживаемости считаются масса тела при рождении и оценка состояния плода по шкале Апгар[3].
Масса новорожденных и их оценка по шкале Апгар статистически значимо не различались в зависимости от вида родоразрешения. Так, средняя масса новорожденного после родов через ЕРП и кесарева сечения составила 3180 ± 399,5 и 3099 ± 698,2 г соответственно (р > 0,05).
Оценка по шкале Апгар на 1-й минуте — 5,9 ± 0,72 балла после родов через ЕРП и 5,6 ± 0,95 балла после кесарева сечения (p > 0,05). Подобное соотношение наблюдалось и на 5-й минуте после родов: 7,1 ± 0,61 и 6,8 ± 0,67 балла соответственно (p > 0,05). Следовательно, статистически значимой разницы в оценке по шкале Апгар у новорожденных с ВДГ в общей когорте после родов через ЕРП или кесарева сечения нет.
Более детальный анализ состояния новорожденных на 1-й и 5-й минуте в зависимости от постнатального исхода, вида родоразрешения и экстренности проведенной операции кесарева сечения также не выявил статистически значимые различия.
ОБСУЖДЕНИЕ
Проведенный ретроспективный анализ позволил сделать ряд выводов. Частота обращения женщин с ВДГ плода на перинатальный консилиум Центра ежегодно продолжает расти, что свидетельствует о повышении осведомленности врачей и пациенток о возможностях национального федерального лечебного учреждения как на антенатальном, так и на постнатальном этапе.
У 3 из 4 пациенток с ВДГ плода, обратившихся на перинатальный консилиум, диафрагмальная грыжа обнаружена во втором триместре беременности, что превосходит европейский уровень своевременной диагностики данного порока развития (2 из 3 случаев ВДГ). Этот факт, несомненно, свидетельствует об удовлетворительном техническом обеспечении и высокой квалификации врачей ультразвуковой диагностики в регионах. Однако выявить связь формирования ВДГ с генетической аномалией практически невозможно в связи с крайне низким уровнем инвазивной пренатальной диагностики. Это приводит к запоздалому решению о нецелесообразности пролонгирования беременности при сочетании ВДГ и хромосомной или генетической аномалии.
Кроме того, инструментальная диагностика степени тяжести ВДГ требует усовершенствования: необходимы комплексное УЗИ с расчетом параметров ИКС и o/e LHR и проведение МРТ плода с определением o/e TFLV.
Такой подход на антенатальном этапе продиктован вариабельной интерпретацией прогноза выживаемости новорожденного с помощью каждого отдельно взятого метода исследования, что требует их интегрального использования для понимания перспектив каждого клинического случая. Это позволит также более четко формировать группу пациентов, которым показано проведение фетальной эндоскопической баллонной окклюзии.
В настоящее время полная инструментальная диагностика (УЗИ и МРТ) в регионах проводится лишь в половине случаев, что является недостаточным и требует дополнительного обследования на базе Центра. В результате обнаруживаются случаи проникновения печени в грудную клетку, что увеличивает группу с прогнозом низкой неонатальной выживаемости в 2,2–4 раза относительно предварительных результатов.
Благодаря развитию технологии реанимации и интенсивной терапии новорожденных общий уровень перинатальной смертности с ВДГ в Центре составляет 43,4%. Наиболее распространенный метод родоразрешения — роды через ЕРП. Оптимальным сроком родоразрешения с наименьшим уровнем постнатальной смертности следует считать 38–39 недель беременности.
Преиндукция и индукция родов, а также осложнения родов любого характера становятся дополнительными факторами, ухудшающими прогноз выживаемости новорожденного. При этом оценка по шкале Апгар статистически значимо не различается у выживших и умерших новорожденных вне зависимости от метода родоразрешения, что свидетельствует о более глубоких нарушениях адаптации ребенка.
ЗАКЛЮЧЕНИЕ
Частота выявления врожденной диафрагмальной грыжи (ВДГ) и перинатальная смертность новорожденных в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России аналогичны данным зарубежных перинатальных центров. Повышения выживаемости новорожденных с ВДГ можно достичь при проведении комплексной диагностики ВДГ и совершенствовании методов ее лечения. Оптимальным подходом к прогнозированию выживаемости новорожденных следует признать разработку интегральной системы диагностики, которая будет включать как традиционные методы УЗИ, так и МРТ и кариотипирование, а также генетические исследования с использованием микроматричного анализа.
Для эффективного применения терапевтических методик (как антенатальных, так и оперативных после рождения) необходима разработка персонифицированного подхода к терапии в зависимости от степени выраженности компрессии легких и сердца плода и прогноза выживаемости новорожденного.
Поступила: 29.08.2022
Принята к публикации: 23.09.2022








