Проблема ведения беременности у больных эпилепсией женщин очевидна. Благодаря демократизации общества, снижению социальной стигматизации, разработке и внедрению новых противоэпилептических препаратов (ПЭП), существенно повышающих качество жизни больных, обеспеченности современными методами исследования и наблюдения за течением беременности, все больше женщин с эпилепсией стремятся завести детей. Однако спектр вопросов, которые приходится решать врачам, наблюдающим беременную с эпилепсией, чрезвычайно широк: взаимовлияние эпилепсии и беременности, особенности ведения родов, прогноз рождения соматически здорового ребенка, вероятность развития у него эпилепсии, тактика ведения беременности с учетом многофакторности влияний [1, 2].
Эпилепсия занимает третье место по распространенности среди болезней нервной системы (Петрухин А.С., 2012) [3]. В 2017 году Международная лига борьбы против эпилепсии впервые с 1989 года обновила классификацию данного заболевания [4]. В предыдущей классификации в основе ее построения находился анатомический принцип, основанный на выделении различных приступов, характерных для активации той или иной области головного мозга. На данный момент после проведения многочисленных исследований в основу положен патофизиологический принцип, который характеризует эпилепсию как болезнь нейрональных сетей, а не симптом локального поражения мозга [5]. Эпилептический приступ — это развитие транзиторных знаков и/или симптомов, вызванных аномальной чрезмерной или синхронной нейрональной активностью головного мозга [6].
Происхождение заболевания обусловлено рядом экзогенных и эндогенных факторов. Реализация приобретенной, врожденной и наследственной предрасположенности становится причиной возникновения двух принципиально различных этиологических форм эпилепсии — симптоматической и идиопатической [7].
При идиопатической эпилепсии отсутствуют признаки первичного поражения головного мозга, появление ее чаще всего объясняется наследственной предрасположенностью.
Симптоматическая эпилепсия является следствием приобретенных и врожденных поражений головного мозга. Основной удельный вес имеет эпилепсия, обусловленная перинатальными причинами, в частности перенесенной гипоксией (44%), травмой головного мозга (6,4%), врожденными TORCH-инфекциями (4,8%).
Иммунологическим аспектам эпилепсии посвящены работы многих авторов [2, 8]. В патогенетический механизм судорожного синдрома, помимо сенсомоторной коры, вовлечены отделы головного мозга, входящие в аппарат нервной регуляции функций иммунной системы, — гиппокамп и амигдалярный комплекс, что обусловливает наличие иммунологических расстройств у больных эпилепсией [9]. В крови и ликворе пациенток с эпилепсией обнаружены аутоантитела различной нейроспецифичности, в связи с чем в эпилептическом очаге создаются предпосылки для индукции нейроиммунных реакций.
Определяющим в степени выраженности нейроаутоиммунного процесса в пределах ЦНС является баланс между про- и противовоспалительными цитокинами, способствующий поддержанию хронического воспалительного процесса [10].
Нарушение иммунного статуса у больных эпилепсией характеризуется как вторичное иммунодефицитное состояние. Иммунодефицитное состояние при эпилепсии осложняется нарушением механизмов неспецифической противоинфекционной защиты. Так, массовое микробиологическое обследование больных эпилепсией выявило множественные очаги стрептококковой и стафилококковой инфекции у 92% из них [11].
В патологический процесс при эпилепсии вовлекаются структуры ключевого отдела нейроиммунорегуляторного аппарата — гипоталамуса [12], поэтому есть основания полагать, что расстройства функций иммунологической защиты при эпилепсии связаны с нарушением состояния центрального аппарата нервной регуляции иммунной системы. Это свидетельствует о целесообразности исследования иммунного статуса пациентов с эпилепсией для своевременной коррекции расстройств функции иммунной системы.
Вопросы терапии больных эпилепсией сложны, до сих пор нет единого мнения о проведении лечебных мероприятий. Из-за особенностей патогенетических механизмов инфекции у больных с эпилепсией выбор препаратов должен проводиться с учетом имеющихся нарушений иммунного и цитокинового статуса и клинических проявлений патологического процесса [13].
Необходимо понимать, что беременность при эпилепсии — другой аспект проблемы, когда в течение относительно короткого периода перед нами стоит задача не столько достижения ремиссии заболевания, сколько избежания его декомпенсации на фоне применения минимальной дозы ПЭП и, конечно же, рождения здорового ребенка. Принципиальным является положение: больная эпилепсией может иметь детей. Исключение составляют женщины с тяжелым течением эпилепсии и психическими расстройствами [14].
С учетом вышесказанного нами проведен анализ особенностей функционирования системы нейроспецифичных белков как маркеров деструктивных изменений, происходящих в условиях гестационной перестройки у беременных с эпилепсией, и системы ИФН, отражающей уровень неспецифической резистентности организма.
Цель исследования: изучить течение беременности и родов при эпилепсии, уточнить влияние иммуномодулирующей терапии ИФН α-2b на иммунологическую реактивность у беременных с эпилепсией и на состояние новорожденных.
МАТЕРИАЛЫ И МЕТОДЫ
Работа выполнялась на базе акушерских отделений ГБУЗ МО «Московский областной НИИ акушерства и гинекологии» (директор — д. м. н., профессор Петрухин В.А.). Выборку составили 129 беременных женщин с диагнозом эпилепсии. Испытуемые были разделены на три группы в зависимости от уровней нейроспецифических белков: I группа (n = 59) — пациентки с гипосенсибилизацией к белку S-100, глиальному фибриллярному кислому протеину, основному белку миелина (с низким содержанием аутоантител); II группа (n = 42) — пациентки с признаками полинейросенсибилизации; группа сравнения (n = 28) — женщины с нейросенсибилизацией в пределах референсных значений, которые на момент наступления беременности не получали противоэпилептическую терапию и не имели приступов более 3 лет, — реконвалесценты по эпилепсии.
Были проведены общепринятые лабораторные исследования всех участниц: клинический анализ крови, общий анализ мочи, коагулограмма, биохимический анализ крови с оценкой активности печеночных ферментов, бактериологические посевы из различных локусов, а также определение гормонального спектра фетоплацентарного комплекса. Применялись и вирусологические и молекулярные методы (твердофазный иммуноферментный анализ на IgM и IgG к Herpes simplex 1-го и 2-го типа, Human cytomegalovirus, ПЦР).
Из инструментальных методов использовали УЗИ, доплерографию.
Нами проведен анализ анамнестических данных для выявления особенностей течения родов и раннего послеродового периода. Производились гистологические и морфологические (морфологическое исследование последа), нейроиммунологические исследования (оценка уровней иммуноглобулинов, ИЛ-2, ИЛ-6, сывороточных ИФН α и γ).
Изучены также массово-ростовые показатели новорожденных, перинатальные осложнения, пороки развития плода и состояние гемостаза, цитокиновый статус, уровни антител к нейроспецифическим белкам.
В основу математической обработки материала положены непараметрические методы математической статистики. Группы сравнивали с помощью непараметрических критериев (Вилкоксона — Манна — Уитни, Смирнова, Фишера, χ2). Различия считали статистически значимыми при p < 0,05. Вычисления проводили с использованием пакета стандартных и оригинальных статистических программ.
РЕЗУЛЬТАТЫ
Анализ исходной противоэпилептической терапии. В целом в режиме монотерапии, регламентируемой как «золотой стандарт» лечения эпилепсии, препараты получало большинство пациенток исследуемых групп. Наиболее часто в режиме монотерапии использовались традиционные антиконвульсанты: карбамазепин и вальпроевая кислота.
Течение беременности. Одним из показателей, влияющих на исход беременности у пациенток с эпилепсией, является контроль над судорожными приступами. Динамика судорожных приступов в исследуемых группах представлена на рисунке 1.
Рис. 1. Динамика судорожных приступов в I и II группах
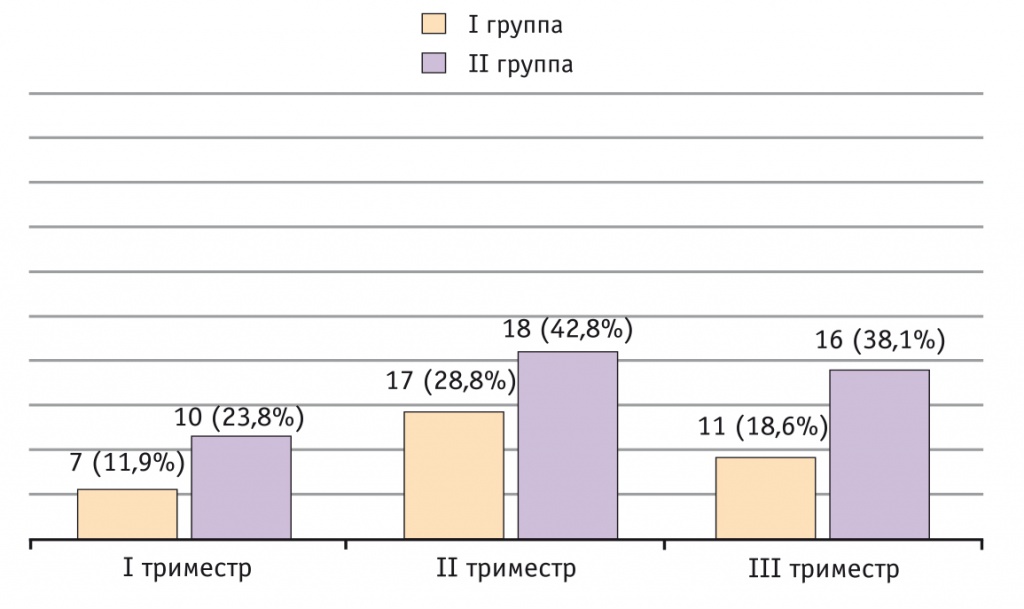
Наиболее часто развитие судорожных приступов у пациенток было связано с самостоятельной отменой или снижением дозы исходного ПЭП.
Течение настоящей беременности было осложненным у всех участниц I и II групп. Самыми частыми осложнениями I и II триместра беременности являлись ранний токсикоз и угроза прерывания. В III триместре преобладающим осложнением в I группе стала угроза преждевременных родов. Во II группе она отмечена у 11 женщин, однако с диагнозом «угроза прерывания беременности» 4 беременные были госпитализированы после развития судорожного приступа. Вторым осложнением по частоте встречаемости стала фетоплацентарная недостаточность, которая тоже более выражена во II группе — 14 случаев против 9 в I группе, что обусловлено более частыми генерализованными судорожными приступами, которые сопровождаются гипоксически-ишемическими нарушениями.
У всех 129 пациенток результаты общепринятых лабораторных исследований не показали значимого отличия от нормы.
По УЗИ, задержка внутриутробного роста плода (ЗВУР) в I группе выявлена у 11 (18,7%) беременных, во II группе — у 6 (14,3%) пациенток, в группе сравнения — у 2 (7,2%). Обращает на себя внимание высокий процент нарушений маточно-плацентарного кровотока, найденных при доплерометрии: 17 (28,8%) в I группе, 15 (35,7%) во II группе и 8 (28,6) в группе сравнения.
Течение родов и раннего послеродового периода. В условиях акушерских клиник ГБУЗ МОНИИАГ родоразрешены все беременные исследуемых групп. Гестационный срок родов у подавляющего числа женщин составил 39–40 недель. До 37 недель произошли роды у двух беременных.
Показанием для досрочного родоразрешения (36 недель гестации) в I группе явились признаки гемолитической болезни плода, выявленные при УЗИ, в связи с чем в интересах плода проведено плановое абдоминальное родоразрешение. Во II группе произошло преждевременное излитие околоплодных вод и спонтанное развитие регулярной родовой деятельности при сроке гестации 36–37 недель.
Среди всех обследованных 107 (82,9%) родоразрешены через естественные родовые пути. Количество самопроизвольных родов в I группе — 49 (83,1%), во II группе — 33 (78,6%), в группе сравнения — 25 (89,3%). У одной обследованной из I группы произошли срочные самопроизвольные роды при рубце на матке после кесарева сечения, которое ей было произведено ранее в связи с эпилепсией.
Основным показанием к родовозбуждению в исследуемых группах стало наличие экстрагенитальной патологии, так как, по современным представлениям, беременным с эпилепсией показано программированное родоразрешение.
Осложненное течение родов отмечалось у 13 родильниц: аномалии родовой деятельности (первичная и вторичная слабость, дистоция шейки матки) — у 3 (5,1%) в I группе, у 4 (9,5%) во II группе. У трех родильниц роды осложнились начавшейся острой гипоксией плода, в связи с чем они были закончены оперативным путем.
Кровопотеря в родах в среднем составила 200 ± 50 мл. Превышение допустимого объема кровопотери в раннем послеродовом периоде в обеих группах не отмечено. Судорожных приступов во время родов не было. Обезболивание у женщин с эпилепсией не отличалось отобщепринятого.
В 73 (68,2%) наблюдениях при самопроизвольных родах применялось медикаментозное обезболивание наркотическими анальгетиками в сочетании со спазмолитическими и седативными препаратами. Роды под длительной перидуральной (эпидуральной) анестезией проведены у 7 (6,5%) родоразрешенных пациенток. Количество случаев абдоминального родоразрешения в I группе — 10 (16,9%), во II группе — 9 (21,4%), в группе сравнения — 3 (10,7%).
Течение послеродового периода. Послеродовой период протекал нормально у 97,7% пациенток, что говорит о правильной тактике ведения родов с учетом основного заболевания. У 3 (2,3%) родильниц была диагностирована гематометра.
Во втором, критическом периоде могут происходить рецидивы эпилептических припадков, связанные с депривацией сна, которая возникает в период кормления, особенно в ночное время. Появление приступов в этот период может быть связано с частыми ночными подъемами, недосыпанием, пропуском приема ПЭП, переутомлением, низкой комплаентностью организма матери к дозировке лекарственных средств. Тем не менее во время кормления ни у одной роженицы эпилептических припадков не было. Грудное вскармливание осуществляли 127 (98,5%) женщин. Лактация была противопоказана 2 (1,5%) роженицам в связи с сохранением эпилептических приступов и проведением политерапии.
Морфологическое исследование последа. У всех пациенток проводилось морфологическое исследование последа. Морфологические признаки восходящей инфекции отмечены в I группе у 8 (13,6%) женщин, а во II группе — у 17 (40,5%), Признаки гематогенной инфекции найдены в 4 (6,8%) последах из I группы и в 7 (16,7%) из II группы, признаки хронической плацентарной недостаточности — в 9 (15,3%) и 6 (14,3%) соответственно. В группе сравнения патологические изменения при морфологическом исследовании последа не найдены. Воспалительные процессы в околоплодной среде и плодных оболочках ассоциировались с наличием внутриутробной инфекции у детей.
Нейроиммунологические аспекты эпилепсии. Результаты исследования продемонстрировали гипосенсибилизацию к белку S-100, глиальному фибриллярному кислому протеину, основному белку миелина у пациенток I группы. Нами также проанализированы показатели антител к фактору роста нервов: они находились в пределах референсных значений. Уровни аутоантител существенно снижены, что можно рассматривать в качестве благоприятного прогностического фактора как в отношении течения основного заболевания, так и в отношении течения беременности.
Во II группе нами выявлен высокий уровень сенсибилизации к широкому спектру нейроспецифических белков, в частности к белку S-100, глиальному фибриллярному кислому протеину, основному белку миелина, фактору роста нервов. Приведенные показатели указывают на выраженную полинейросенсибилизацию к глиальному фибриллярному кислому протеину. Соответственно, у пациенток существенно нарушена проницаемость гематоэнцефалического барьера. Все это приводит к снижению тормозных процессов в ЦНС и к выраженной эпилептизации нейронов, что проявляется неэффективностью медикаментозной терапии, эпилептическими приступами, а также развитием резистентных форм эпилепсии.
В группе сравнения исследуемые показатели находились в пределах нормы.
Далее мы изучили иммунный статус пациенток. О состоянии иммунного статуса судили по уровням интерферонов, интерлейкинов и иммуноглобулинов. В основу исследования было положено предположение о том, что нейросенсибилизация влечет за собой ряд изменений как в гуморальном, так и в клеточном звене иммунитета [2].
Показатели гуморального иммунитета были в пределах референсных значений во всех трех группах. Но отмечалось статистически значимое снижение содержания ИФН α и γ во II группе, тогда как в I группе и группе сравнения оно находилось в пределах нормальных значений (табл. 1).
Таблица 1
Содержание интерферонов в сыворотке, пкг/мл
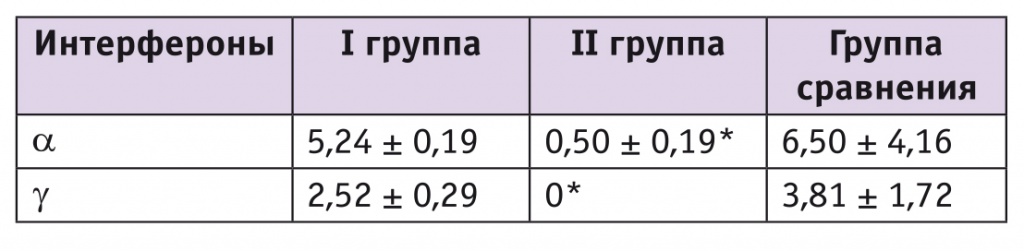
* Здесь и в таблице 2: отличия от группы сравнения статистически значимы (р < 0,05).
С целью достижения устойчивого снижения показателей нейросенсибилизации и коррекции диагностированных нейроиммунных изменений проведена иммуномодулирующая терапия пациенток II группы (со II триместра беременности). Они получали препараты ИФН α-2b по 1 свече (500 000 МЕ) в прямую кишку 2 раза в день (каждые 12 часов) в течение 10 дней, далее по 1 свече дважды в сутки 2 раза в неделю (всего 5 лечебных дней) [1].
Для оценки эффективности проводимой терапии за несколько дней до родоразрешения повторно исследовали нейроиммуннологический статус участниц II группы, а также пациенток I группы.
Показатели сенсибилизации к нейроспецифическим белкам у пациенток II группы, которые получали иммуномодулирующую терапию, значимо улучшились. В частности, существенно снизились показатели полинейросенсибилизации. Обращает на себя внимание и тот факт, что уровни антител к нейроспецифическим белкам уменьшились примерно в 2–2,5 раза, но не достигли референсных значений. Таким образом, достигнут более благоприятный прогноз для новорожденных и детей раннего возраста. Концентрации антител к нейроспецифическим белкам представлены на рисунке 2.
Рис. 2. Уровни антител к нейроспецифическим белкам в динамике у пациенток II группы, у.е.
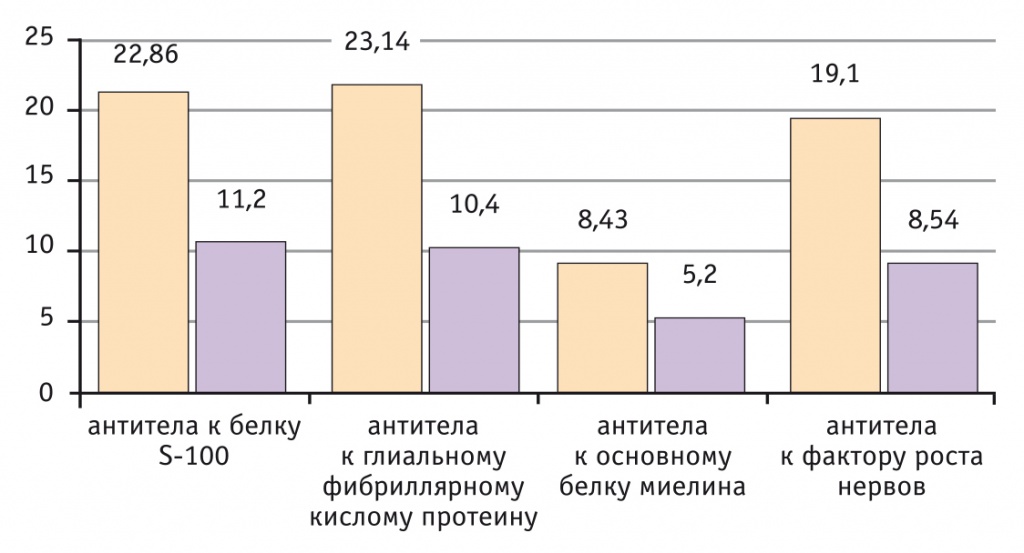
Кроме того, наблюдалась тенденция к уменьшению уровней ИФН α и γ сыворотки в I группе, тогда как во II группе — к их повышению.
Полученные результаты позволяют нам сформулировать выводы о том, что под влиянием интерферон-корригирующей терапии ИФН α-2b у пациенток происходит изменение иммунного статуса, что приводит к выраженному снижению нейросенсибилизации, а также способствует росту содержания интерферонов в крови.
Состояние новорожденных. Для определения эффективности иммуномодулирующей терапии и ее влияния на состояние новорожденных нами оценены клиническое состояние, уровень нейросенсибилизации, цитокиновый статус детей, родившихся от матерей с эпилепсией (табл. 2). Масса тела детей участниц I группы составила 3200 (2740–4250) г, II группы — 3300 (2100–4070) г, группы сравнения — 3400 (2840–4040) г.
Таблица 2
Состояние новорожденных, n (%)
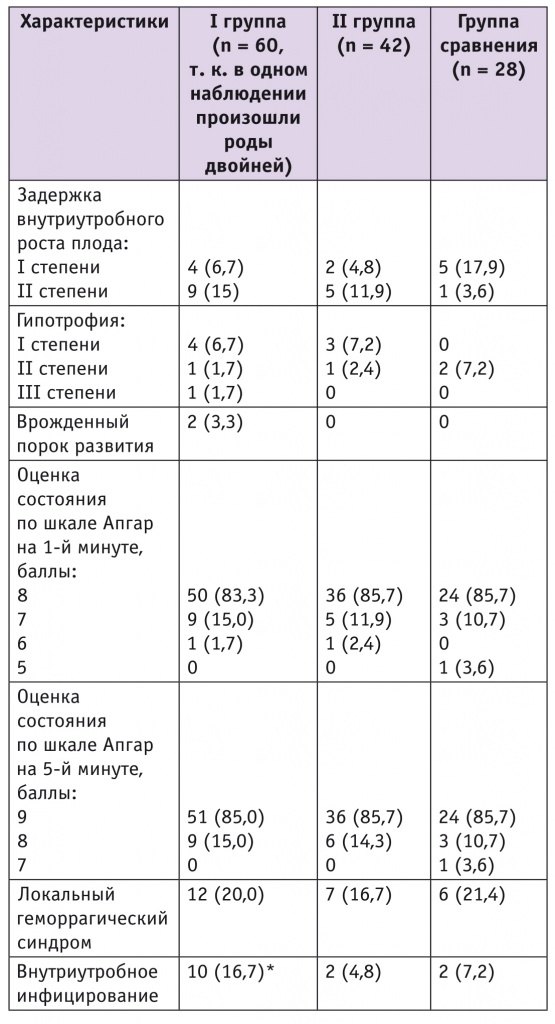
У младенцев всех групп были признаки локального геморрагического синдрома (кожные петехиальные кровоизлияния). У 2 новорожденных I группы диагностирован врожденный порок развития (Spina bifida поясничного отдела позвоночника), а у одного из них имели место и аномалии развития наружных половых органов. Анализ анамнестических данных позволяет заключить, что причиной указанных аномалий может быть неправильная тактика лечения во время беременности.
Иммунный статус оценивали по содержанию иммуноглобулинов и цитокинов. Значимых различий в их концентрациях между группами не было. Установили отсутствие выраженной сенсибилизации к нейроспецифическим белкам. У детей I группы отмечена гипосенсибилизация к основным группам нейроспецифических белков, что может указывать на развитие гипофункции иммунной системы, а также рассматривается в качестве предпосылки к формированию вторичного иммунодефицита.
У детей II группы уровни нейроспецифических белков находились в пределах референсных значений. Данные показатели противопоставляются исходному повышенному содержанию нейроспецифических белков у матерей.
У младенцев группы сравнения исследуемые показатели также были в пределах нормы, как и у их матерей.
ЗАКЛЮЧЕНИЕ
При анализе показателей здоровья новорожденных мы установили, что в большинстве случаев прогноз зависит от проведения антенатальной иммунокоррекции ИФН α-2b начиная со II триместра беременности. Так, у матерей II группы отмечалось тяжелое течение беременности, с осложнениями. Однако состояние здоровья новорожденных было значимо лучше, чем в I группе, у них реже встречались хроническая внутриутробная гипоксия, внутриутробные инфекции, задержка внутриутробного роста по сравнению с детьми, родившимися от матерей, которые не получали интерферонотерапию.
Таким образом, результаты исследования позволяют сформулировать вывод об эффективности антенатальной иммунокоррекции, проводимой с начала II триместра беременности, которая позволяет предотвратить нейросенсибилизацию и клинические проявления внутриутробной инфекции у новорожденных.








