По современным представлениям, гипергликемия, выявленная во время беременности, подразделяется на гестационный СД (ГCД) и прегестационный, к которому относятся СД 1 типа, 2 типа, MODY и манифестный CД, впервые выявленный во время беременности [1]. B Ceнт-Винceнтcкой декларации в качестве одной из целeй обозначено, что исходы беременности у женщин с СД должны быть близки к исходам у здоровых женщин [2].
До эры инсулинотерапии беременность наступала не более чем у 5% женщин с СД [3], при этом у них наблюдалась высокая материнская (до 50%) и перинатальная (до 90%) смертность. Достижения современной акушерской диабетологии дали возможность кардинально снизить у таких пациенток перинатальную заболеваемость, смертность, количество материнских осложнений при беременности, осложнений в родах и пуэрперии [4].
Частота нарушений развития плода при отсутствии лечения ГCД приближается к 100%, это приводит к высокой перинатальной смертности, достигающей в некоторых регионах России 30–40%. Отмечено, что мертворождаемость при прегестационном диабете (19,7‰) и при ГCД (33,7‰) выше, чем в здоровой популяции (5,5‰) [5].
В зависимости от срока проявления внутриутробной патологии при CД выделяют диабетическую гаметопатию, бластопатию, эмбриопатию и фетопатию (ДФ). Считается, что плод от матерей с СД, даже при удовлетворительном его контроле, всегда имеет риск развития ДФ [6], частота которой колеблется от 49% до 60%.
Обследование детей от матерей c CД выявило неблагоприятный кардиометаболический профиль и высокий риск развития у них CД 2 типа, ожирения, артериальной гипертензии и аритмий в более взрослом возрасте, что обусловлено внутриутробным метаболическим программированием [7]. Материнская гипергликемия и гиперинсулинизм плода проявляются в начале внеутробной жизни как инсулинорезистентность, и это играет главенствующую роль в возникновении будущих проблем со здоровьем. [8, 9]. Данное явление лежит в основе концепции фетального происхождения взрослых болезней.
Ранняя диагностика ДФ должна способствовать своевременному выбору адекватной акушерской тактики. ДФ — одно из показаний для инсулинотерапии. Своевременная и адекватная коррекция материнской гипергликемии обеспечивает успешность постнатальной адаптации новорожденного и профилактику у него гипогликемии.
Цель исследования: улучшение перинатальных исходов путем совершенствования антенатальной диагностики ДФ у беременных c различными типами СД.
МАТЕРИАЛЫ И МЕТОДЫ
В 2011–2017 гг. проведено экспериментальное одноцентровое проспективное когортное контролируемое исследование на базе ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии» (директор — д. м. н., профессор Петрухин В.A.). В исследовании принимали участие 668 беременных женщин. Все они были разделены на две группы. В основную группу вошла 241 беременная с подтвержденным диагнозом СД: ГСД, СД 1 типа или 2 типа; в контрольную — 427 беременных, у которых диагноз СД был исключен.
Состояние плода оценивали с помощью УЗИ и доплерометрического исследования, которое проводилось с использованием аппарата Accuvix V20 компании Samsung.
Мы выделили подгруппы плодов с макросомией (масса плода — более 90П) и группу плодов c массой плода менее 25П. В основной группе c макросомией плода было 87 беременных, в контрольной группе — 54. Беременных c плодом массой менее 25П в основной группе было 55, в контрольной — 123.
Для выявления наиболее значимых фенотипических, висцеральных признаков ДФ, оценки состояния плацентарного комплекса и определения особенностей гемодинамики плода при ДФ в основной группе мы выделили две подгруппы: 100 беременных, у детей которых после рождения не было ДФ, и 141 пациентка, новорожденным которых выставлен диагноз ДФ.
Статистическая обработка полученного материала осуществлялась при помощи программы Microsoft Excel. Для каждого показателя была рассчитана медиана, вычислены перцентили от 1 до 99. Определены линейная корреляция и ковариация показателей. Достоверность различий оценивали с помощью критерия Манна — Уитни. Проведен дискриминантный анализ данных. Различия считали статистически значимыми при p ≤ 0,05.
РЕЗУЛЬТАТЫ
Традиционная ультразвуковая диагностика ДФ включает в себя оценку макросомии и пропорциональности телосложения плода, фенотипических и висцеральных признаков; функционального состояния плода по гемодинамическим параметрам и состояния парафетальных структур.
В ходе исследования не найдены специфические признаки и сроки формирования ДФ в зависимости от типа СД.
Последовательность появления признаков ДФ во II триместре беременности следующая:
-
16–18 недель: изменение телосложения плода (снижение коэффициентов окружность головы/окружность живота (ОГ/ОЖ), длина бедренной кости (ДБ)/ОЖ, утолщение подкожной клетчатки шеи, живота, головы);
-
19–20 недель: появление макросомии, гепатомегалии, кардиомегалии, увеличение лопатки, буккального индекса, упругости стенки артерии пуповины (АП) и минутного объема в ней;
-
21–22 недели: утолщение поджелудочной железы, появление многоводия;
-
более 22 недель: кардиомиопатия (нарушение сократимости миокарда), диффузное утолщение плаценты.
Для оценки значимости каждого эхографического критерия в выявлении ДФ и последовательности их появления каждый признак был повторно ретроспективно оценен в когорте новорожденных после 30 недель с подтвержденными неонатальными признаками ДФ.
Одним из значимых критериев явилась макросомия. Чувствительность макросомии в III триместре составляет до 90%, специфичность — 79,5%, диагностическая точность — до 82,3%. Прогностическая ценность положительного результата — 72,3%, прогностическая ценность отрицательного результата для исключения ДФ на всех сроках беременности — до 94,6%. При массе плода менее 80П вероятность выявления ДФ — 5–19,5%. Макросомия плода не является специфичным признаком ДФ, требуется определение особенностей телосложения плода и типа макросомии.
В полной мере асимметрию телосложения плода характеризует снижение коэффициентов пропорциональности OГ/OЖ и ДБ/OЖ менее 20П. Коэффициенты OГ/OЖ и ДБ/OЖ c 34 недель у плодов с ДФ статистически значимо ниже, чем у плодов без ДФ и контрольной группы. Чувствительность коэффициента OГ/OЖ составляет до 75%, специфичность — 90,3%, точность — 80,3%. Чувствительность значения коэффициента ДБ/OЖ менее 20П составляет до 85,7%, специфичность — 80,6%, точность — 80,4%. Прогностическая ценность отрицательного результата высока на всех сроках гестации — от 80,6% до 97%.
При CД у матери и формировании ДФ плоды с предполагаемой массой менее 25П имеют такую же форму асимметрии телосложения, как и плоды с макросомией, несмотря на маленькую массу тела.
У плодов с ДФ ОЖ на всех сроках превышала 89П и была статистически значимо больше, чем ОЖ плодов контрольной группы, с 32 недель гестации. При этом эффективность выявления ОЖ более 80П для диагностики ДФ высока: чувствительность — 90%, специфичность — до 80%, прогностическая ценность положительного результата — 75%, прогностическая ценность отрицательного результата — 75–94,4%. При измерении среднего диаметра живота получены такие же закономерности, что при оценке ОЖ, но оно оказалось более эффективным: в 38–39 недель чувствительность — 85,7%, специфичность — 79,0%, точность — 80,0%. Эффективность других фетометрических данных для диагностики ДФ ниже, и по ним различия между группами не выявлены.
Анализ фенотипических признаков ДФ показал наибольшую диагностическую значимость повышения ширины лопатки, толщины подкожной клетчатки шеи и живота.
На большую ширину плечевого пояса плода при ДФ указывает статистически значимое увеличение ширины лопатки по сравнению с показателем контрольной группы после 32 недель (табл. 1).
Таблица 1
Медиана ширины лопатки (в скобках указана перцентиль относительно контрольной группы), мм
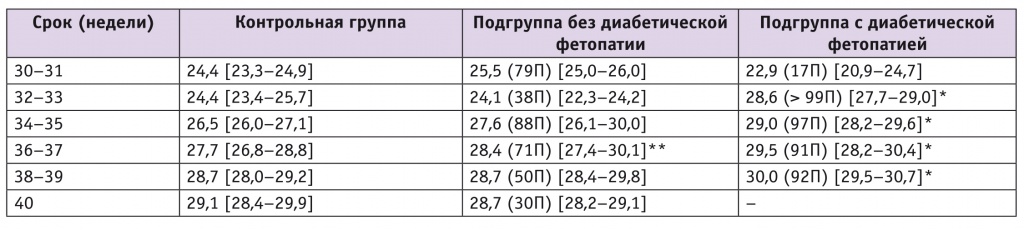
Примечание. Здесь и далее в таблицах отличия от контрольной группы статистически значимы: (*) — p ≤ 0,01; (**) — p ≤ 0,05.
Чувствительность признака — 88,9%, специфичность — 83,3%, прогностическая ценность положительного результата — 76,5%, прогностическая ценность отрицательного результата — 92,6%.
К наиболее показательным фенотипическим признакам относятся увеличение толщины подкожной клетчатки по задней поверхности шеи плода и передней полуокружности брюшной стенки на стандартном срезе живота.
Утолщение подкожной клетчатки шеи обнаружено у всех плодов с ДФ на всех сроках гестации после 30 недель, а также после 34 недель при СД у матери и отсутствии других признаков ДФ, что позволяет считать его наиболее ранним маркером хронической материнской гипергликемии (табл. 2).
Таблица 2
Медиана толщины подкожной клетчатки области шеи плода (в скобках указана перцентиль относительно контрольной группы), см
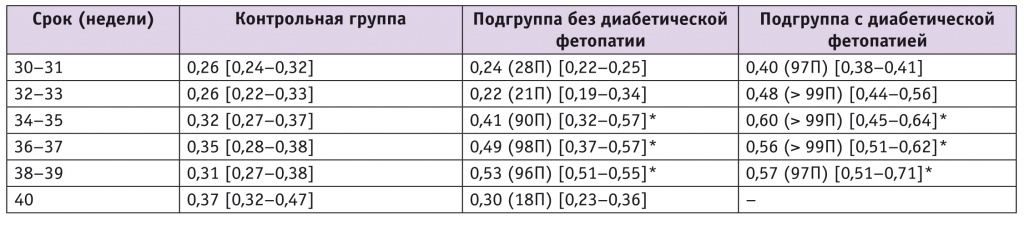
Эффективность его была высокой за счет чувствительности (до 97,0%), точности (до 87,5%) и прогностической ценности отрицательного результата (до 97,1%).
Толщина подкожной клетчатки живота у плодов как с ДФ, так и без ДФ тоже статистически значимо превышала нормативные показатели с 32 недель гестации (табл. 3).
Таблица 3
Медиана толщины подкожной клетчатки в области передней полуокружности живота плода (в скобках указана перцентиль относительно контрольной группы), см
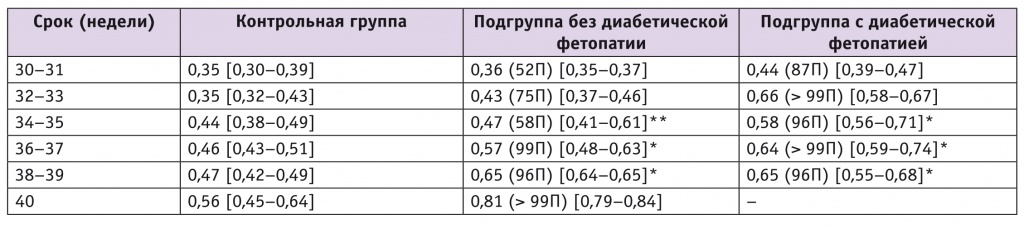
Среди висцеральных признаков ДФ гепатомегалия, кардиомегалия и кардиомиопатия, увеличение поджелудочной железы плода наиболее значимы.
Статистически значимое повышение размеров печени выявлено только у плодов с ДФ.
Чувствительность увеличения косого продольного размера печени плода снижалась с ростом срока гестации, однако специфичность, точность и ценность отрицательного результата оставались на высоком уровне.
Кардиомегалия характеризуется увеличением сердца и его перегородок. Об этом свидетельствуют масса левого желудочка (ЛЖ), толщина межжелудочковой перегородки (МЖП) и кардиоторакальный индекс (КТИ). В 38–39 недель толщина МЖП сердца в диастолу у плодов с ДФ была до 20,9% больше, чем у плодов контрольной группы. У плодов без ДФ отличий по толщине МЖП от контрольной группы не было (табл. 4).
Таблица 4
Медиана толщины межжелудочковой перегородки сердца плода в диастолу (в скобках указана перцентиль относительно контрольной группы), мм
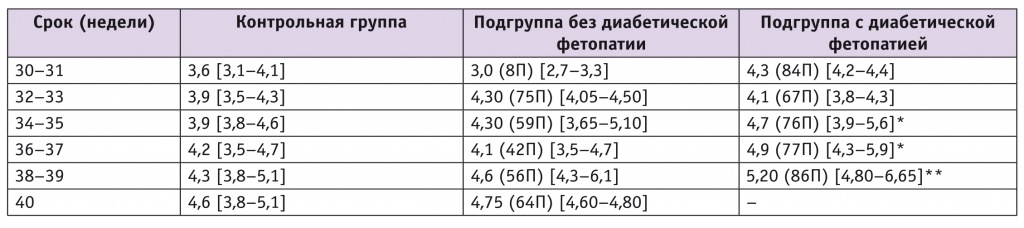
Чувствительность (до 66,7%), специфичность (до 73,3%) и точность (до 70,0%) утолщения МЖП и повышения массы ЛЖ были умеренными на всех сроках.
Применение КТИ для диагностики кардиомегалии у плодов с ДФ значимо при отсутствии макросомии плода. При макросомии происходит увеличение грудной клетки, и КТИ имеет нормальное значение, что снижает диагностическую ценность показателя.
В качестве висцерального признака ДФ нами впервые использовано увеличение поджелудочной железы плода. В литературе описано определение состояния поджелудочной железы для диагностики фетоплацентарной недостаточности. По толщине поджелудочной железы статистически значимые отличия от контрольной группы были у плодов как с ДФ (32–37 недель), так и без ДФ (34–37 недель) (табл. 5).
Таблица 5
Медиана толщины поджелудочной железы плода (в скобках указана перцентиль относительно контрольной группы), мм
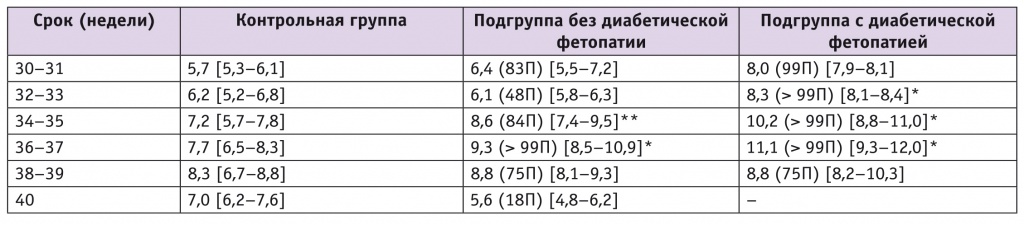
Измерение толщины поджелудочной железы плода высокоэффективно для диагностики ДФ: чувствительность — до 100%, точность — до 85%, специфичность сопоставима с измерением eе длины — 76,5%.
Состояние плацентарного комплекса. Умеренные специфичность (до 80,0%) и точность (до 78,0%) многоводия как показателя в совокупности с высокой прогностической ценностью отрицательного результата (до 89,5%) позволяют использовать этот показатель для уточнения степени тяжести ДФ. Утолщение плаценты в подгруппе ДФ встречалось чаще, чем в контрольной группе и подгруппе без ДФ, однако из-за низкой эффективности данный параметр можно применять лишь для уточнения тяжести ДФ.
Оценка гемодинамики плода. При нормально протекающей беременности коэффициенты сократимости миокарда МЖП и задней стенки ЛЖ характеризуются постоянной величиной на протяжении срока от 14 до 40 недель. Медиана коэффициента сократимости МЖП колеблется от 20,4% до 29,4%.
У плодов с ДФ толщина МЖП выше, чем в контрольной группе, после 30 недель беременности. У плодов без ДФ сократимость МЖП не отличалась от нормы и умеренно снижалась после 39 недель. У плодов с ДФ с 35 недель сократительная способность МЖП уменьшалась и в 38–39 недель стала статистически значимо ниже таковой в контрольной группе. Масса ЛЖ плода, толщина МЖП и фракция выброса ЛЖ имели низкую положительную корреляцию c уровнем гликированного гемоглобина матери (r = 0,38).
Параметры кардиотокограммы коррелировали c показателями центральной гемодинамики плода. У плодов контрольной группы более высокая вариабельность базального сердечного ритма отражает более высокую сократимость миокарда. Количество высоких эпизодов имеет отрицательную линейную корреляцию со степенью гипертрофии миокарда (r = –0,38). У плодов от матерей с СД как при наличии, так и при отсутствии ДФ на всех исследованных сроках количество aкцeлepaций выше, чем у плодов контрольной группы. Рост числа высоких эпизодов базального ритма сердца плодов в подгруппах СД на фоне увеличения толщины МЖП может свидетельствовать об apитмoгeннoй готовности миокарда плода и формировании кардиомиопатии на фоне кардиомегалии.
Нами исследована гемодинамика в АП, средней мозговой артерии, аорте плода, a также в обеих маточных артериях.
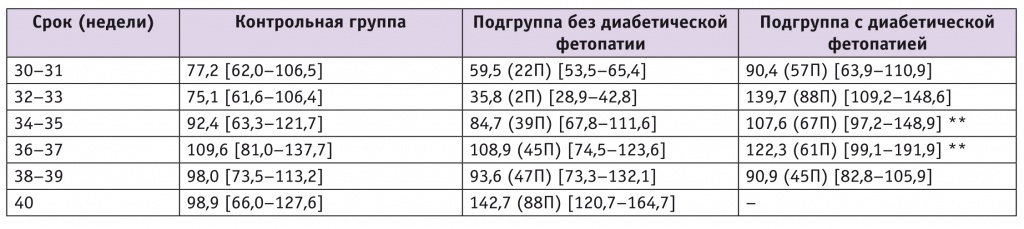
Различия в индексах периферической сосудистой резистентности (систоло-диастолическом соотношеним, пульсационном индексе и индексе резистентности) в указанных сосудах в зависимости от тяжести ДФ не выявлены. Статистически значимые различия между подгруппами ДФ и контрольной группой наблюдались по показателю объемного кровотока в АП (табл. 6). Высокая специфичность (до 75,0%) и прогностическая ценность отрицательного результата (до 88,8%) позволяют использовать его для уточнения степени тяжести ДФ.
Таблица 6
Медиана объемного кровотока в артериях пуповины (в скобках указана перцентиль относительно контрольной группы), мл/м
ЗАКЛЮЧЕНИЕ
Наименьший срок гестации, на котором можно заподозрить формирование диабетической фетопатии (ДФ) у плодов от матерей как с СД, так и без установленного диагноза СД, — 16 недель. Наличие ДФ можно предположить на основании снижения коэффициента окружность головы/окружность живота, утолщения подкожной клетчатки шеи, живота, a также кардиомегалии. Эти признаки можно считать скрининговыми для eе выявления. Макросомия ввиду eе высокой чувствительности может использоваться в качестве скринингового признака, несмотря на низкую пенетрантность. Специфичности относительно типа СД описанные признаки ДФ не имеют и при разных нарушениях углеводного обмена у матери формируются одинаково.








