Анестезия — важный компонент сопровождения процедуры ЭКО, так как она обеспечивает седацию и обезболивание на самом травматичном этапе — при трансвагинальной пункции яичников (ТПЯ). При этом возможны различные методы достижения результата: посредством только седации или седации в сочетании с анальгезией при сохранении сознания, общей анестезии, регионарной анестезии (спинальной, эпидуральной или парацервикального блока), местной анестезии, альтернативных методов (например, акупунктуры) и т. д. [2].
В течение последних двух десятилетий ингаляционные анестетики все шире распространяются в различных областях анестезиологии и интенсивной терапии [3]. Весьма привлекательными качествами этих средств являются быстрое начало действия, хорошая управляемость анестезией и возможность контролировать доставку анестетика тканям, используя такие параметры, как минимальная альвеолярная концентрация (МАК) и концентрация анестетика в конце выдоха [4]. Может применяться метод быстрой ингаляционной индукции (БИИ) с максимальной концентрацией анестетика (англ. vital capacity rapid inhalation induction), который был внедрен еще в 90х годах прошлого века [5, 6].
Ингаляционные анестетики получили применение и при обеспечении хирургических манипуляций в сфере репродуктивных технологий [7]. Однако необходимо отметить, что все известные работы по сравнению ингаляционной и внутривенной анестезии в клинике ВРТ были выполнены за рубежом [8–11]. Представляемое проспективное исследование — первая российская работа такого рода.
Цель исследования: изучить особенности ингаляционного и внутривенного методов анестезии, применяемых для трансвагинальной пункции яичников.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проведено на базе клиники «Москворечье» (г. Москва) и включало 80 пациенток репродуктивного возраста, которым выполнялась ТПЯ под контролем ультразвука. Пациентки были рандомизированы на две группы.
Первую группу составили 40 женщин, получавших ингаляционную анестезию севофлураном методом БИИ. Индукция проводилась с использованием лицевой маски и реверсивного дыхательного контура наркозного аппарата с поглотителем углекислого газа (абсорбент СО2). Пациентка по команде делала глубокий вдох и выдох при потоке кислорода, который подавался со скоростью 6 л/мин в условиях заполненного контура, содержавшего максимальную концентрацию севофлурана (7–8%). Оперативное вмешательство начинали по истечении 2й минуты индукции анестезии. В зависимости от продолжительности ТПЯ и при отсутствии реакции на хирургическую стимуляцию снижали скорость потока кислорода до 2 л/мин и регулировали подававшуюся концентрацию анестетика.
Во вторую группу были включены 40 женщин, которым была проведена внутривенная анестезия пропофолом по методу последовательной внутривенной индукции (ПВВИ). Метод ПВВИ заключался во введении болюса пропофола из расчета 2–3 мг/кг до достижения глубокого уровня седации и отсутствия двигательной реакции на прокол первого фолликула. В случае наличия двигательной реакции на хирургическую манипуляцию при применении этого вида анестезии вводились дополнительные болюсы.
Пациентки, включенные в исследование, соответствовали возрастному диапазону от 20 до 43 лет. Средний возраст женщин в первой группе составил 33,8 ± 0,64 года, во второй — 32,1 ± 0,76 года. По данному показателю группы статистически значимо не различались (р = 0,1). ИМТ в группе ингаляционной анестезии был равен 22,7 ± 0,54 кг/м2, в группе внутривенной анестезии — 22,3 ± 0,49 кг/м2 (р = 0,6).
По среднему количеству пунктируемых фолликулов группы также были сходны: 10,8 ± 0,95 шт. в первой группе и 13,8 ± 1,49 шт. во второй (p = 0,08). По классификации операционноанестезиологического риска Московского научного общества анестезиологов и реаниматологов у всех пациенток была констатирована умеренная степень риска (2 балла).
В исследовании учитывали продолжительность каждого этапа анестезии. Время этапов индукции и пробуждения зависело от выбранного метода анестезиологического обеспечения. Длительность этапа поддержания анестезии была обусловлена продолжительностью манипуляции — ТПЯ.
Интраоперационный мониторинг включал регистрацию ЧСС, сатурации (SpO2), частоты дыхания (ЧД), показателей систолического (САД) и диастолического (ДАД) артериального давления (измерявшихся неинвазивным методом), а также среднего артериального давления (СрАД). На протяжении всего времени подачи газонаркотической смеси проводили непрерывный контроль показателей газоанализа на вдохе и выдохе: концентрации O2, CO2 (методом капнометрии), — а также концентрации севофлурана и значения его МАК. В числе показателей восстановления после анестезии определяли интервал времени от прекращения подачи анестетика до начала пробуждения (речевого ответа на словесные команды, открывания глаз).
Для объективного контроля пробуждения после анестезии и безопасного перевода пациентки в палату применяли модифицированную балльную шкалу Альдрета (табл. 1) [12]. В шкалу включены пять критериев: сознание, дыхание, SpO2, кровообращение и двигательная активность. Каждый признак оценивается в диапазоне от 0 до 2 баллов, таким образом, максимальная оценка по шкале составляет 10 баллов. При достижении суммы баллов, равной 10, пациентку переводили в палату. Если сумма баллов составляла 9 и менее, продолжали наблюдение в операционной до достижения 10 баллов с регистрацией соответствующего времени.
Таблица 1
Шкала Альдрета [12]
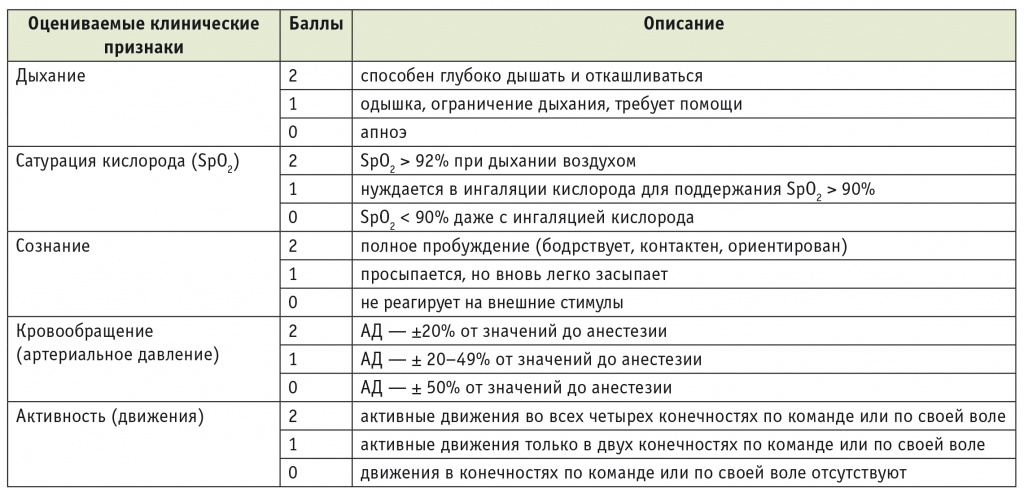
Примечание. АД — артериальное давление.
Эффективность программы ЭКО оценивали через 3 недели после переноса эмбрионов по данным УЗИ (наличию плодного яйца в полости матки).
Группы сравнивали между собой методом случайконтроль. Статистическую обработку проводили с помощью программного пакета Statistica. Общие данные представляли в виде X ± m (среднее значение ± стандартное отклонение) и анализировали с использованием непарного теста Стьюдента (tкритерий) и критерия Пирсона (χ2). Различия считали статистически значимыми при p ˂ 0,05.
РЕЗУЛЬТАТЫ
Проанализированы данные, полученные на трех этапах анестезии (индукции, поддержания, пробуждения) и в восстановительном периоде в двух группах.
Временной интервал индукции анестезии в группе ингаляционной анестезии севофлураном статистически значимо превышал таковой в группе внутривенной анестезии пропофолом: 2,1 ± 0,06 и 1,2 ± 0,07 минуты соответственно (р < 0,001).
В группе ПВВИ время внутривенной индукции составило 1,2 ± 0,07 минуты при средней индукционной дозе пропофола 138,2 ± 3,80 мг. В 39 из 40 случаев для достижения нужного клинического эффекта потребовались дополнительные болюсы пропофола, дополнительная доза пропофола равнялась в среднем 87,9 ± 7,98 мг. Общая доза пропофола у 40 пациенток составила 224,0 ± 8,62 мг.
В группе ингаляционной анестезии индукция проводилась с концентрацией севофлурана на вдохе 7,5 ± 0,06% в течение 2,1 ± 0,06 минуты до достижения целевой концентрации на выдохе 4,9 ± 0,13% и МАК 2,3 ± 0,06%.
Увеличение ЧД было отмечено в обеих группах. При ингаляционной анестезии на этапе индукции ЧД составила 23,2 ± 1,05/мин, при внутривенной анестезии — 19,5 ± 0,66/мин (р = 0,003). SpO2 на момент окончания индукции при разных методах анестезии не различалась: в первой группе — 98,3 ± 0,14%, во второй — 98,3 ± 0,15% (р = 0,9). Парциальное давление CO2 на выдохе после индукции севофлураном составило 22,1 ± 0,75 мм рт. ст., после внутривенного введения пропофола — 25,1 ± 0,76 мм рт. ст. (р = 0,007).
На этапе поддержания анестезии проведение процедуры ТПЯ в первой группе заняло 4,3 ± 0,30 минуты, во второй группе для этого потребовались 5,2 ± 0,50 минуты (p = 0,1). Показатели гемодинамики, регистрировавшиеся на момент окончания пункции яичников, характеризовали ответную реакцию организма на хирургическое вмешательство. ЧСС в первой группе (БИИ) составила 76,4 ± 2,29 уд/мин, во второй группе (ПВВИ) — 74,3 ± 1,44 уд/мин (р = 0,4). САД в анализируемых группах статистически значимых различий не имело: при анестезии севофлураном — 105,0 ± 2,25 мм рт. ст., пропофолом — 106,6 ± 2,46 мм рт. ст. (р = 0,6). ДАД в группе ингаляционной анестезии было достоверно ниже, чем в группе внутривенной анестезии: 62,3 ± 1,56 и 68,3 ± 1,75 мм рт. ст. соответственно (р = 0,01). Важно, что не было обнаружено статистически значимых различий между значениями СрАД: в первой группе этот показатель составил 77,0 ± 1,79 мм рт. ст., во второй — 80,3 ± 1,89 мм рт. ст. (р = 0,2).
Выявлены особенности на этапе пробуждения после применения севофлурана и пропофола. Средние показатели ЧСС, САД и СрАД на этом этапе в группе севофлурана были статистически значимо выше, чем в группе, в которой использовался пропофол (табл. 2).
Таблица 2
Показатели гемодинамики на этапе пробуждения (X ± m)
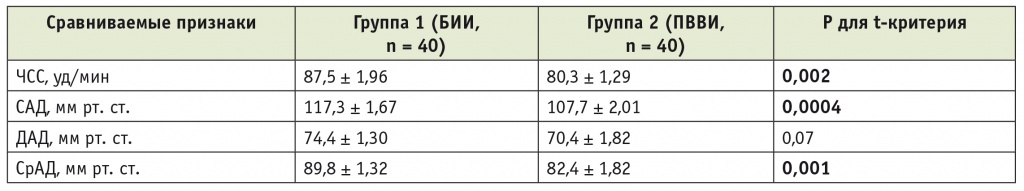
Примечание. БИИ — быстрая ингаляционная индукция; ПВВИ — последовательная внутривенная индукция; САД, ДАД и СрАД — систолическое, диастолическое и среднее артериальное давление соответственно; ЧСС — частота сердечных сокращений.
Время начала восстановления сознания в виде ответа на словесные команды после анестезии в группах не различалось: 6,2 ± 0,2 и 6,1 ± 0,4 минуты при использовании севофлурана и пропофола соответственно (р = 0,8). Однако среднее время достижения 10 баллов по шкале Альдрета в первой группе было достоверно меньше: 6,1 ± 0,1 минуты против 7,4 ± 0,1 минуты во второй группе (р = 0,04).
Оценка по балльной системе через 6 минут после анестезии в исследуемых группах была различной. В группе севофлурана всем 40 пациенткам (100%) был присвоен максимальный балл по каждому из пяти критериев шкалы Альдрета (рис.). В группе пропофола период пробуждения длился дольше. При анализе в группе ПВВИ только у 24 (60,0%) пациенток на момент пробуждения было установлено соответствие критериям безопасного перевода в палату (p ˂ 0,001 при сравнении с первой группой); у 14 (35,0%) пациенток суммарный показатель шкалы Альдрета составил 9 баллов и у 2 (5,0%) — 8 баллов (см. рис.).
Рис. Распределение баллов по шкале Альдрета на этапе пробуждения и начала восстановления после анестезии в исследуемых группах.
* P ˂ 0,001 при сравнении с первой группой
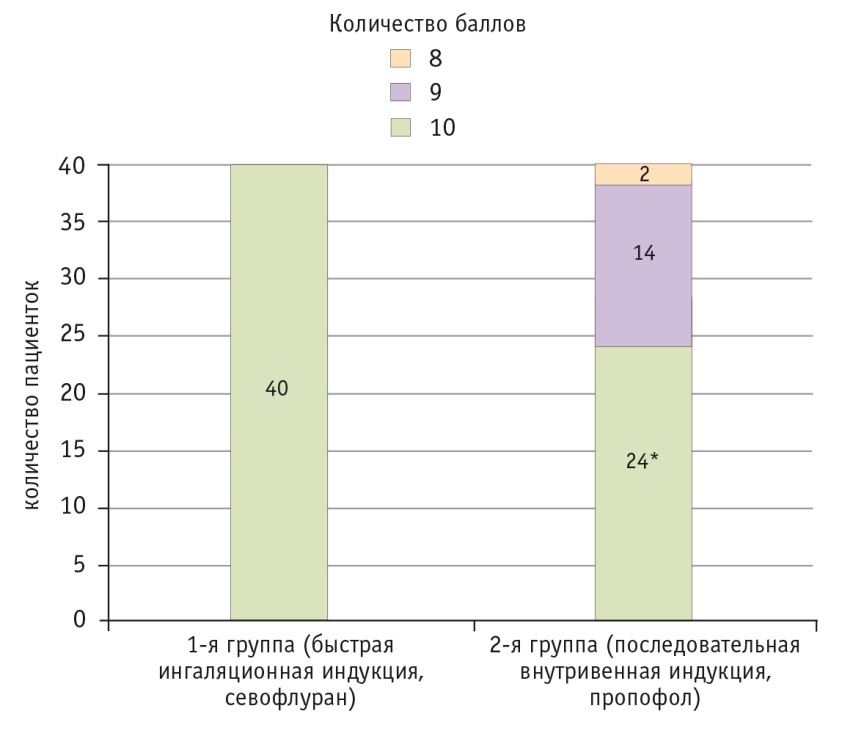
Таким образом, введение в практику балльной оценки параметров по шкале Альдрета позволяет объективно сравнить время полного восстановления при применении двух методов анестезии.
Частота наступления клинической беременности у пациенток двух групп не различалась: в группе ингаляционной анестезии севофлураном беременность наступила у 16 из 39 (41,0%) женщин, в группе пропофола — у 14 из 37 (37,8%) (p = 0,7). Не удалось включить данные о результатах ЭКО у 1 женщины (2,5%) группы севофлурана и у 3 (7,5%) женщин группы пропофола.
ЗАКЛЮЧЕНИЕ
На основании изучения клинических особенностей двух видов анестезии получены достоверные различия по ряду мониторируемых показателей.
Показано, что индукция анестезии до утраты сознания и отсутствия реакции на внешние раздражители при использовании пропофола достигается быстрее. При этом, несмотря на короткое время проведения трансвагинальной пункции яичников (ТПЯ), у 39 из 40 пациенток второй группы потребовалось дополнительное введение пропофола.
Во время пункции яичников статистически значимых различий по уровням среднего артериального давления и частоты сердечных сокращений (ЧСС) между группами ингаляционной и внутривенной анестезии не выявлено, у пациенток обеих групп мониторируемые гемодинамические показатели оставались в пределах нормативных значений.
На этапе пробуждения ЧСС после быстрой ингаляционной индукции была статистически значимо выше, чем после последовательной внутривенной индукции. Восстановление после анестезии быстрее происходило в группе ингаляционной анестезии, что выразилось в уменьшении времени, необходимого для достижения 10 баллов по шкале Альдрета (6,1 ± 0,1 минуты в первой группе и 7,4 ± 0,1 минуты во второй, p = 0,04).
Различий в результатах циклов экстракорпорального оплодотворения (ЭКО) не установлено. Наступление клинической беременности в исследуемых группах достоверно не различалось.
Таким образом, внутривенная анестезия пропофолом и ингаляционная анестезия севофлураном при проведении ТПЯ в клинике вспомогательных репродуктивных технологий имеют определенные особенности, связанные со скоростью индукции и восстановления после наркоза, а также с влиянием на артериальное давление и ЧСС. Оба варианта анестезии безопасны и могут применяться для анестезиологического обеспечения инвазивных процедур при ЭКО.








