Случайное открытие гепарина студентом Медицинского факультета Университета Джона Хопкинса Джеем Маклином в 1916 г. осталось в то время практически незамеченным, но впоследствии стало революционным. Сейчас, на рубеже столетнего юбилея этого замечательного открытия, проблема управления свертывающей/противосвертывающей системой крови становится все более актуальной. Это связано со многими факторами: наличием специфических заболеваний, сопряженных с возникновением тромбозов и коагулопатий; внедрением в практику обширных операций у больных с тяжелыми сопутствующими расстройствами; активным применением экстракорпоральных контуров в практике реаниматологии, нефрологии и т. д.; увеличением популяции больных со стентированными артериями и/или протезированными сердечными клапанами. Рассматриваемая проблема прямо касается врачей практически всех специальностей, но особенно — кардиологов, хирургов, анестезиологов-реаниматологов. Низкомолекулярные гепарины (НМГ) прочно заняли нишу профилактики тромбозов в практике интенсивной терапии благодаря их общепризнанным преимуществам, к числу которых относятся: 1) удобство назначения; 2) отсутствие необходимости в лабораторном мониторинге в большинстве случаев; 3) относительная безопасность[13]. Применение НМГ превратилось в повседневную рутину и часто остается за рамками размышлений клиницистов. Вместе с тем эта группа препаратов не совсем однородна, эффективность НМГ не всегда очевидна, кроме того, появляются их «фармакологические конкуренты», которые могут рутинно и длительно применяться для профилактики тромбозов без лабораторного контроля — так называемые новые оральные антикоагулянты (НОАК) (Novel Oral Anticoagulants — NOAC)[11]. Все это заставляет пересматривать сложившееся представление о роли НМГ в современной антитромботической стратегии.
Антитромботические препараты в коагуляционном каскаде. Классические представления о коагуляционном каскаде как о последовательности взаимозависимых биохимических реакций, имеющих внешний и внутренний пути инициации, актуальны и в настоящее время[5, 12]. Если терапевтические методы борьбы с кровотечениями относительно просты и, как правило, заключаются в использовании экзогенных факторов свертывания в том или ином виде, то механизмы антитромботической терапии представляются весьма сложными. Антитромботические препараты прямо или с вовлечением естественных антитромботических факторов блокируют различные звенья коагуляционного каскада. В зависимости от спектра ингибируемых факторов свертывания, особенностей воздействия на них фармакодинамические свойства антитромботических препаратов и возможности их клинического применения существенно различаются. Основными фармакологическими группами антитромботических препаратов являются гепарины (НМГ и нефракционированный гепарин — НФГ), пероральные антагонисты витамина К, представленные в настоящее время практически исключительно варфарином, а также антитромбоцитарные препараты (дезагреганты), рассмотрение которых выходит за рамки данной статьи. Основные особенности распространенных в современной клинической практике антикоагулянтов представлены в таблице 1.
Таблица 1
Фармакодинамические и клинические особенности антикоагулянтов, распространенных в современной клинической практике
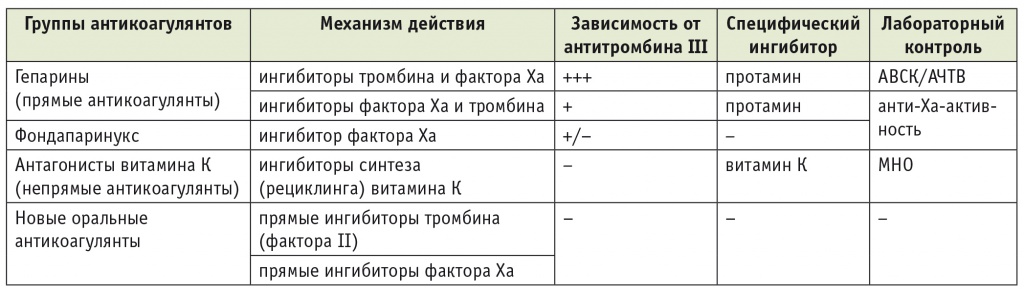
Примечание. АВСК — активированное время свертывания крови; АЧТВ — активированное частичное тромбопластиновое время; МНО — международное нормализованное отношение.
Гепарины. Эту группу антикоагулянтов принято называть прямыми, в отличие от непрямых антикоагулянтов — ингибиторов витамина К. С появлением действительно прямых (непосредственных) ингибиторов факторов свертывания из группы НОАК такая терминология может показаться несколько устаревшей, однако остается общепринятой. НФГ, как известно, — это серосодержащий гликозаминогликан, представленный несколькими полимерными цепями. Молекулярная масса коммерческих препаратов гепарина может быть различной, но, как правило, колеблется в пределах 12–16 килодальтон (кДа). Фармакодинамический профиль гепарина обусловлен его способностью активировать антитромбин III (АТ-III). Важнейшую роль в этом процессе играет специфический пентасахаридный участок молекулы гепарина, обеспечивающий связь с АТ-III. Этот участок имеется в молекулах НМГ и фактически в самостоятельном виде представляет собой препарат фондапаринукс[7]. Комплекс «НФГ + АТ-III» ингибирует тромбин (фактор II) и активированный фактор Xа, а также факторы IX, XI, XII. Но именно АТ-III-зависимое воздействие на второй и десятый факторы наиболее важно при клиническом применении гепарина. Причем, если ингибирование фактора Xа осуществляется при его контакте с активированным (любым из гепаринов или фондапаринуксом) АТ-III, то тромбин может быть ингибирован только при одновременном соприкосновении с АТ-III и с полимерной цепочкой гепарина. В этой связи именно размер молекулы гепарина определяет его способность эффективно блокировать тромбин. Соответственно, данная способность является основной для НФГ, менее выражена у НМГ и отсутствует у фондапаринукса, тогда как ингибирование фактора Xа в равной степени присуще всем перечисленным препаратам. Поэтому такие «временные» показатели, как АВСК и АЧТВ, информативны только для контроля терапии НФГ[5].
Создание фракционированных, или низкомолекулярных, гепаринов сделало возможным более удобное и безопасное применение прямых антикоагулянтов. Эти препараты гарантированно всасываются при подкожном введении. В связи с их ослабленным или практически отсутствующим влиянием на тромбин кровотечения при назначении НМГ достаточно редки. Во многих клинических ситуациях НМГ не требуют лабораторного контроля. Вполне закономерно, что эти препараты прочно заняли нишу рутинной профилактики тромбозов у самых разных категорий больных, прежде всего хирургических, ортопедических пациентов и больных, находящихся в отделениях реанимации. Подчеркнем также сравнительную безопасность длительного использования НМГ у беременных. Все это привело к достаточно формальному, упрощенному отношению клиницистов к НМГ как к однородной группе фармакологических средств, которые хороши для рутинной профилактики тромбозов, но недостаточно эффективны для лечения серьезных тромботических осложнений. Однако реальная ситуация не совсем такова. Разброс молекулярной массы НМГ достаточно велик — от 3 до 7 кДа. В свою очередь, молекулярная масса (или длина гепариновой цепочки) определяет выраженность ингибирующего влияния препарата на тромбин. Поскольку анти-Xа-активность является стабильным свойством всех НМГ, различную выраженность ингибирования тромбина выражают в виде отношения анти-Xа/анти-IIа. Чем оно меньше, тем антитромбиновая активность выше (табл. 2).
Таблица 2
Молекулярная масса и относительная антитромбиновая активность низкомолекулярных гепаринов
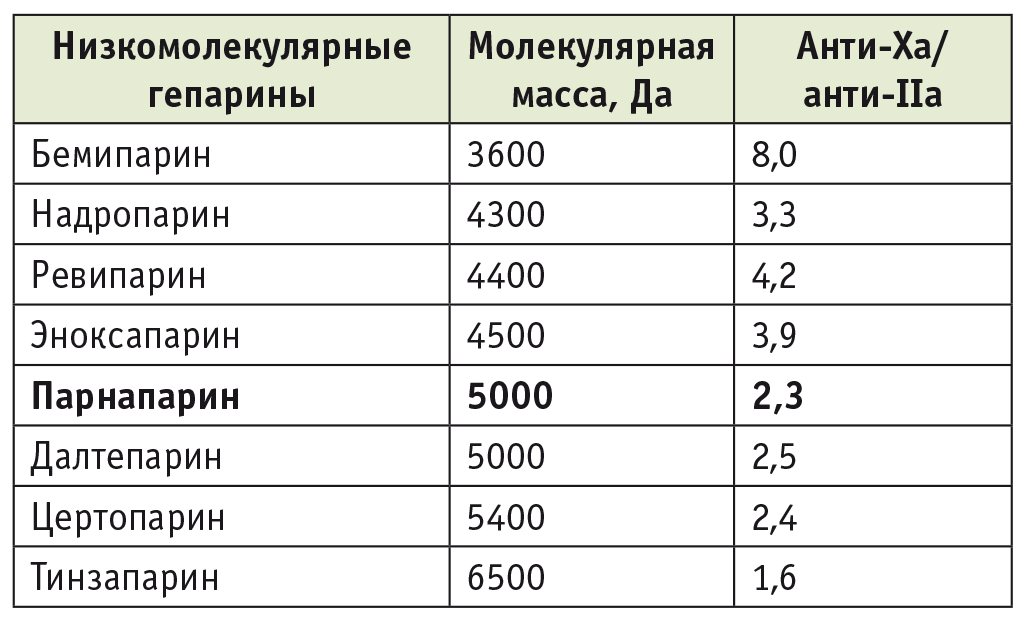
Как видно из таблицы 2, в целом подтверждается прямая зависимость антитромбиновой активности НМГ от его молекулярной массы. Наибольшее отношение анти-Xа/анти-IIа (наименьшую антитромбиновую активность) имеет препарат с наименьшей молекулярной массой (бемипарин). Самый «тяжеловесный» НМГ, тинзапарин, закономерно характеризуется наименьшим отношением анти-Xа/анти-IIа. Из препаратов, доступных на отечественном рынке лекарственных средств, наибольшей антитромбиновой активностью обладает парнапарин (Флюксум, «Альфа Вассерманн», Италия), многие годы применяемый в странах Западной Европы[6, 8, 9]. Некоторые исследователи предлагают выделять три группы гепаринов по их антитромбиновой активности: наиболее активный ингибитор фактора IIа — НФГ; активные ингибиторы тромбина из группы НМГ с высокой молекулярной массой (далте-, тинза- и парнапарин — Флюксум) и, наконец, слабые ингибиторы фактора IIа, такие как эноксапарин и надропарин[6]. Прямым антагонистом всех гепаринов является протамин, вступающий с ними в реакцию преципитации. Эффективность нейтрализации напрямую зависит от длины молекулярной гепариновой цепочки, поэтому НФГ нейтрализуется протамином в полной мере, тогда как НМГ — лишь частично.
Принципиально другим механизмом антикоагуляции характеризуются антагонисты витамина К. Эти препараты (сейчас используется практически только варфарин) подавляют синтез указанного витамина (точнее, его рециклинг), блокируя, таким образом, образование в печени целого ряда факторов свертывания[4, 11]. Несмотря на непрямой механизм, отсроченные начало и окончание действия, варфарин остается незаменимым антикоагулянтом в ряде ситуаций, прежде всего у больных с механическими протезами клапанов сердца. Эта ниша остается недоступной для препаратов из группы НОАК, являющихся прямыми, независимыми от АТ-III, ингибиторами десятого фактора или тромбина.
Таким образом, особенности механизма действия того или иного антикоагулянта определяют целесообразность его применения в различных клинических ситуациях. Рассмотрим возможности эффективного и дифференцированного применения традиционной группы препаратов — НМГ.
Особенности лабораторного мониторинга при терапии низкомолекулярными гепаринами. Такие традиционные «временные» лабораторные показатели, как АВСК или АЧТВ, используемые для контроля дозировки НФГ, неприменимы в случае назначения НМГ. Как правило, это обстоятельство не имеет отрицательного значения, так как терапия НМГ не требует никакого лабораторного контроля. Однако в ряде случаев бесконтрольное (или «стандартное») назначение НМГ является опасным. К ним относятся почечная недостаточность, масса тела менее 50 или более 100 кг, заболевания системы гемостаза, возникновение кровотечений или тромбозов на фоне антикоагулянтной терапии, в некоторых случаях — беременность. Практически единственным информативным лабораторным параметром, характеризующим эффективность НМГ, является анти-Xа-активность, выражаемая в международных единицах на мл (МЕ/мл). Имеющиеся способы оценки этого показателя достаточно дороги и сложны. Их принцип — определение активности остаточного фактора Xа после добавления в контрольный реагент, содержащий десятый фактор и избыточное количество АТ-III, плазмы больного, получающего НМГ. Чем выше остаточная активность фактора X, тем менее выражено действие НМГ. В общем виде терапия НМГ под контролем анти-Xа-активности описана в таблице 3.
Таблица 3
Контроль анти-Xа-активности при терапии низкомолекулярными гепаринами[3]
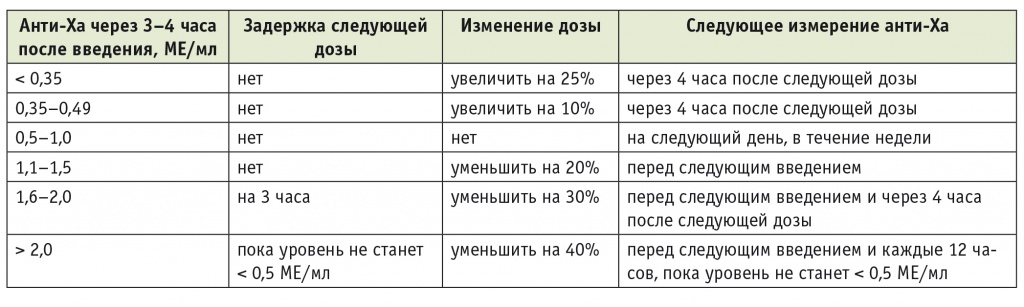
При этом нельзя уравнивать антитромботическую активность при терапии различными НМГ и одинаковом уровне анти-Xа-активности. Необходимо учитывать, что гепарины с низкой молекулярной массой в значительной степени (а фондапаринукс — полностью) лишены ингибирующего влияния на тромбин, тогда как препараты с массой от 5 кДа проявляют отчетливый эффект в отношении второго фактора. Эта фармакодинамическая особенность никак не отражается на рекомендованном при терапии НМГ показателе — анти-Xа-активности[4].
Профилактика венозных тромбозов в хирургии и ортопедии. Рутинная профилактика тромбозов глубоких вен в полостной хирургии и при ортопедических вмешательствах традиционно включает использование компрессионных средств (белья) и таких антикоагулянтов, как НФГ (сейчас крайне редко), НМГ, фондапаринукс, а в последнее время предусматривает и применение средств из группы НОАК. Антитромбоцитарные препараты в данной клинической ситуации неэффективны и достаточно опасны в связи с риском периоперационных кровотечений. Сравнение НОАК и НМГ в общем указывает на возможность эффективного профилактического применения лекарственных средств обеих групп. Однако при этом НМГ обычно рассматривают как однородную группу антикоагулянтов. Вместе с тем ранее было показано преимущество НМГ с большой (≥ 5 кДа) молекулярной массой, в частности парнапарина. Еще в 2007 г. группа итальянских авторов опубликовала впечатляющие результаты профилактического использования препарата Флюксум при артроскопии коленного сустава: дуплексное исследование не выявило ни одного (!) тромботического осложнения в группе более чем из пятисот больных (табл. 4)[9]. При этом и риск кровотечений при профилактическом назначении парнапарина остается весьма низким[9].
Таблица 4
Результаты применения низкомолекулярных гепаринов
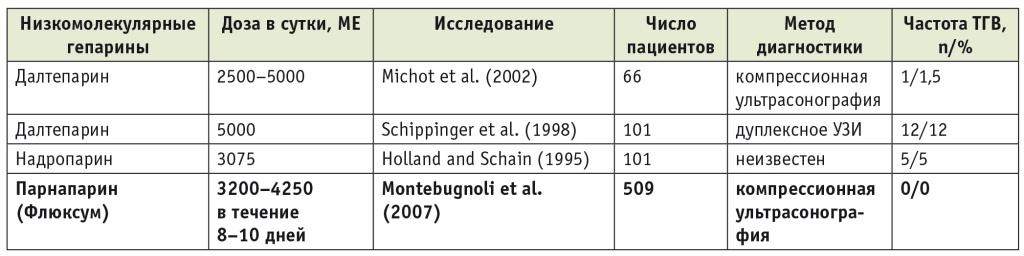
Примечание. ТГВ — тромбоз глубоких вен.
Профилактика тромботических осложнений у беременных. Различные формы тромбофлебитов и других вариантов венозных тромбозов, к сожалению, остаются весьма распространенными при беременности. Этому способствуют особенности системы гемостаза у беременных[1, 2, 10] и компрессия нижней полой вены в поздние сроки. Современная тенденция профилактики и лечения тромбозов у беременных состоит в определении факторов риска тромбозов и довольно агрессивном и раннем применении НМГ[8]. Авторы прямо предписывают назначать НМГ даже при недоказанном подозрении на поверхностный тромбофлебит и прекращать данную терапию, только если диагноз будет отвергнут после дополнительного обследования. Причем на амбулаторном этапе лечения допускают самостоятельное использование НМГ. Для длительного лечения тромбофлебита во время беременности более предпочтительны НМГ, чем препараты из группы НОАК (варфарин и его аналоги запрещены). Безусловно, неэффективность НМГ или наличие тромбоэмболических осложнений (тромбоэмболия легочной артерии) заставляют применять постоянную внутривенную инфузию НФГ с целевым двукратным увеличением АЧТВ.
Еще более сложной и ответственной задачей является ведение беременных с механическими протезами клапанов сердца. Данную проблему можно сформулировать двумя положениями: 1) эффективные для профилактики тромбозов протезов антикоагулянты противопоказаны в длительные периоды беременности; 2) рекомендуемые (безопасные) при беременности антикоагулянты малоэффективны для профилактики тромбозов механических протезов клапанов сердца. Авторы одной из самых новых публикаций с горечью отмечают: «Дилемма по поводу выбора антикоагулянтной терапии у беременных с [механическими] протезами клапанов сердца до сих пор не разрешена»[1]. Действительно, антагонисты витамина К (варфарин и др.) являются наиболее эффективными средствами профилактики тромбозов протезов и одновременно — мощнейшими тератогенными агентами. Их применение крайне опасно в первый триместр. Может быть использован НФГ, второй по профилактической эффективности препарат, однако он должен вводиться только в виде постоянной внутривенной инфузии с целевым двукратным приростом АЧТВ. Возможно ли это непрерывное лечение в течение многих месяцев? Кроме того, оно может вести к истощению запасов собственного АТ-III и к необходимости соответствующей заместительной терапии. Различные НМГ (предпочтительно оригинальные препараты, а не их биоаналоги) в совокупности — третья по эффективности в данной клинической ситуации группа антикоагулянтов, их назначение все-таки приемлемо. Подчеркнем, что применение НМГ для профилактики тромбозов механических протезов клапанов сердца вне беременности совершенно неоправданно, а во время беременности требует строжайшего лабораторного контроля. При этом следует четко понимать, что НМГ — вынужденная, но не полноценная альтернатива варфарину. В настоящее время нет сравнительных исследований, посвященных применению различных НМГ в данной ситуации. Однако приведенные выше принципы их фармакодинамики позволяют предположить, что выбор препаратов с большей молекулярной массой может быть более обоснованным. Такие НМГ, как парнапарин (Флюксум), сочетают в себе возможность длительного подкожного применения и относительно высокую антитромбиновую активность[6, 8].
Рассмотрим описываемую клиническую ситуацию подробнее (табл. 5). Первый триместр беременности является наиболее сложным для подбора антикоагулянтной терапии, так как в этот период происходит закладка органов и систем плода, тератогенное действие варфарина наиболее выражено. Тем не менее установлено, что этот неблагоприятный эффект характеризуется отчетливой дозозависимостью: дозировка антикоагулянта до 5 мг/сут может быть относительно безопасной[10]. Американские рекомендации предписывают подробно обсудить все риски и преимущества назначения варфарина (не более 5 мг/сут) в первом триместре с беременной, которая может отказаться от такой терапии. В том случае, если прием варфарина недостаточен (МНО меньше целевого значения) или невозможен (из-за отказа женщины), должен назначаться какой-либо из гепаринов, как указано в таблице 5. Период с начала второго триместра до 36-й недели обычно не представляет каких-либо трудностей, так как прием варфарина в необходимой дозировке является вполне допустимым. Рекомендуют также дополнительное назначение аспирина в дозе 75–100 мг/сут. Далее назначают только внутривенную инфузию НФГ с целевым двукратным подъемом АЧТВ, которую прекращают за 4–6 часов до, а возобновляют через 4–6 часов после родов[10].
Таблица 5
Профилактика тромбоза механических протезов клапанов сердца во время беременности
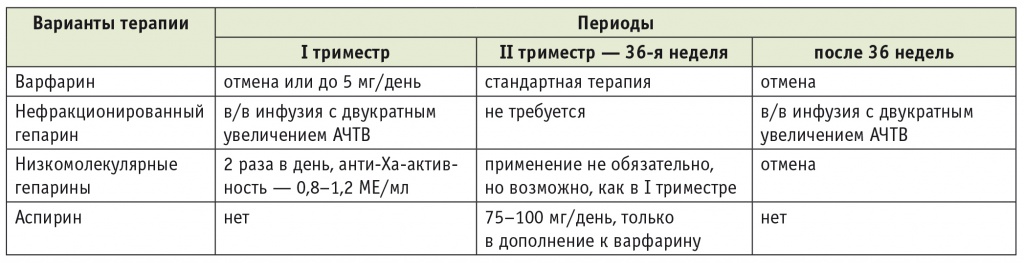
Примечание. АЧТВ — активированное частичное тромбопластиновое время.
Таким образом, НМГ прочно занимают свою нишу в общем спектре антикоагулянтных средств, прежде всего при профилактике тромботических осложнений, лечении различных форм тромбофлебитов и, конечно, у беременных. Фармакологическая группа НМГ не является однородной. Важнейшим отличительным свойством препаратов является их антитромбиновая активность, прямо зависящая от молекулярной массы и обратно выражаемая величиной анти-Xа/анти-IIа.
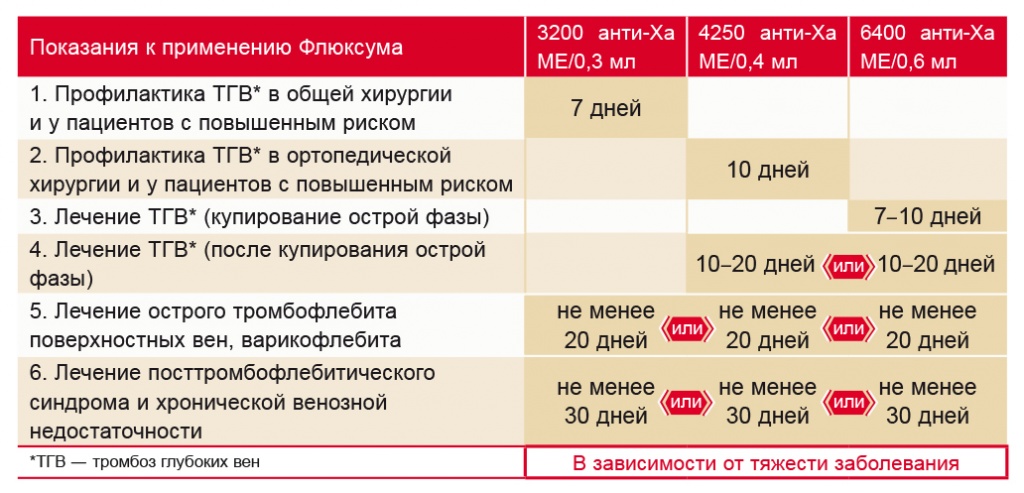
Парнапарин (Флюксум) — новый низкомолекулярный гепарин в российской практике. Считаем целесообразным обратить внимание читателей на то, что в России появился оригинальный НМГ из Италии — парнапарин (Флюксум). Этот препарат отличается от традиционно используемых в рутинной практике надропарина, эноксапарина и т. д. относительно большой молекулярной массой (5 кДа), а значит сравнительно высокой антитромбиновой активностью. В этой связи Флюксум не только более эффективен при назначении по традиционным для НМГ показаниям, но и имеет некоторые собственные, отсутствующие у других НМГ, показания, например посттромбофлебитический синдром. Парнапарин приближается по своим характеристикам к более известному российским коллегам средству — далтепарину, однако отношение анти-Xа/анти-IIа у парнапарина несколько ниже (см. табл. 2). При этом парнапарин характеризуется высокой безопасностью и возможностью длительного амбулаторного применения. Важно, что препарат выпускают в разных дозировках: 3200 анти-Xа МЕ (0,3 мл), 4250 анти-Xа МЕ (0,4 мл) и 6400 анти-Xа МЕ (0,6 мл). Дозы парнапарина и кратность его введения (1 или 2 раза в день) различаются в зависимости от целей терапии (профилактика или лечение) и клинической ситуации (рис.)[6, 8, 9].
Рис. Тактика применения препарата парнапарин (Флюксум)
ЗАКЛЮЧЕНИЕ
Несмотря на создание все новых средств для антикоагулянтной терапии, низкомолекулярные гепарины (НМГ) остаются препаратами выбора для рутинной профилактики и долгосрочного лечения тромбозов. Именно эта группа антикоагулянтов предпочтительна у такой сложной категории пациентов, как беременные. Традиционно НМГ рассматривают как множество однотипных взаимозаменяемых препаратов. Однако их относительная антитромбиновая активность серьезно различается в зависимости от средней молекулярной массы (прямая зависимость). Наиболее активным ингибитором тромбина из числа НМГ, доступных в отечественной клинической практике, является парнапарин (Флюксум). Высокий уровень безопасности и эффективность этого препарата делают целесообразным его широкое клиническое применение.








