Проведенные в конце прошлого века D. Cheng и соавт. исследования убедительно показали возможность снижения риска развития послеоперационных осложнений и улучшения результатов кардиохирургических вмешательств при ранней активизации больных[3]. Несколько позже была сформулирована концепция анестезии, ориентированной на быстрое пробуждение пациентов (так называемая fast-track cardiac anesthesia), как основы тактики послеоперационного ведения кардиохирургических больных, нацеленной на быструю экстубацию, активизацию и перевод из отделения интенсивной терапии[2]. В начале настоящего столетия целесообразность этих подходов была подтверждена в клинических исследованиях, что способствовало широкому применению принципов быстрой активизации во многих кардиохирургических клиниках[5, 6, 8].
Реализация принципов быстрой активизации затрудняется при ряде клинических ситуаций, требующих продленного мониторного наблюдения и интенсивной терапии. В кардиохирургической практике к таковым относятся послеоперационные кровотечения, развитие системной воспалительной реакции, повреждения ЦНС и, конечно, сердечная недостаточность. Вместе с тем эффективные технологии диагностики и терапии позволяют сокращать сроки лечения в ОРИТ и способствуют более быстрой активизации пациентов кардиохирургического профиля даже в случаях развития указанных осложнений.
Коронарное шунтирование остается наиболее эффективным методом реваскуляризации миокарда и самым распространенным из кардиохирургических вмешательств. Совершенствование техники операций, методов анестезии и искусственного кровообращения сделало коронарное шунтирование относительно безопасной процедурой с летальностью, не превышающей одного процента в ведущих кардиохирургических центрах. Однако до сих пор остается актуальной проблема острой сердечной недостаточности (ОСН), риск развития которой в раннем послеоперационном периоде достигает 15–25%[4].
Сегодня все большее внимание кардиологов и кардиохирургов привлекает роль правого желудочка (ПЖ) и его систолической дисфункции в генезе ОСН после операций на сердце. Снижение систолической функции ПЖ после коронарного шунтирования является доказанным фактором неблагоприятного прогноза[4].
Есть веские основания предполагать, что в клинической практике значительная часть случаев систолической дисфункции ПЖ остается нераспознанной, в первую очередь вследствие недостаточности инструментальной диагностики. Современные широко распространенные диагностические подходы, базирующиеся на сочетании манометрических и эхокардиографических данных, позволяют выявить только выраженную систолическую дисфункцию ПЖ[1]. Основываясь на указанных недостаточно чувствительных методах, клиницисты обнаруживают ее после 5–7,5% операций коронарного шунтирования[4]. Вместе с тем есть предположение, что при применении высокочувствительных методов диагностики систолической дисфункции ПЖ можно будет выявлять частые случаи менее выраженных нарушений этого отдела сердца, несомненно, влияющих на течение послеоперационного периода и продлевающих сроки лечения в ОРИТ. Возможно, использование в данных клинических ситуациях современных методов интенсивной терапии дисфункции ПЖ будет способствовать ранней активизации больных.
Цель исследования: повышение эффективности лечения послеоперационной ОСН путем своевременной диагностики и дифференцированной комплексной терапии правожелудочковой систолической дисфункции с ожидаемым сокращением сроков пребывания пациентов в ОРИТ.
В настоящем исследовании нами были выдвинуты две гипотезы. Первая предполагала неоднородность структуры причин сердечной недостаточности после коронарного шунтирования с длительными периодами применения инотропных препаратов и сроками пребывания в ОРИТ в случаях изолированной правожелудочковой дисфункции. После подтверждения этого положения была выдвинута вторая гипотеза, согласно которой модификация интенсивной терапии правожелудочковой дисфункции путем включения вазодилататора малого круга способна уменьшить сроки использования инотропных препаратов, а следовательно, и время лечения пациентов в ОРИТ.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование было выполнено в ФГБУ «Северо-Западный федеральный медицинский исследовательский центр им. В. А. Алмазова» (СЗФМИЦ) Минздрава России (генеральный директор — академик РАН, профессор Е. В. Шляхто) в период с января 2014 г. по май 2015 г. Протокол исследования был предварительно одобрен этическим комитетом указанного учреждения.
На первом этапе (с января по сентябрь 2014 г.) было проведено проспективное неконтролируемое описательное исследование особенностей клинического течения случаев изолированной систолический дисфункции правого или левого желудочка в послеоперационном периоде коронарного шунтирования. Были определены следующие критерии включения: выполненное изолированное коронарное шунтирование, осложнившееся развитием ОСН с необходимостью применения инотропной поддержки. В соответствии с внутренним протоколом СЗФМИЦ критерием назначения инотропных препаратов в послеоперационном периоде являлось снижение индекса ударного объема левого желудочка (ЛЖ) менее 35 мл/м2 при условии нормальных значений этого показателя в доперфузионном периоде. К критериям исключения относили наличие септальных дефектов, фибрилляции предсердий, а также снижение фракции изгнания ЛЖ менее 40%. Учитывая указанные критерии, в первый этап включили 25 пациентов.
На втором этапе (сентябрь 2014 г. — май 2015 г.) было проведено проспективное контролируемое нерандомизированное исследование, в которое включили 10 пациентов с подтвержденной изолированной дисфункцией ПЖ, требовавшей применения инотропных препаратов. Критерии исключения соответствовали установленным на первом этапе. В комплексную интенсивную терапию ОСН у пациентов, вошедших во второй этап исследования, была включена ингаляция оксида азота.
Для обеспечения оперативного вмешательства пациентам проводили общую внутривенную анестезию с интубацией трахеи и ИВЛ. Анальгезию обеспечивали фентанилом в дозе 6 мкг/кг/ч, гипнотический компонент поддерживали постоянной инфузией пропофола в дозе 6–8 мг/кг/ч. Искусственное кровообращение и защиту миокарда проводили по стандартному протоколу, принятому в СЗФМИЦ, использовали аппараты Stockert S/3 (Германия). Инвазивный мониторинг показателей центральной гемодинамики у всех пациентов осуществляли с помощью системы PiCCO plus и VoLEF (PULSION, Германия) в сочетании с системой Datex-Ohmeda S/5 (General Electric, США). Всем пациентам каждый час в течение первых послеоперационных суток вводили термоиндикатор с определением показателей центральной гемодинамики. Использование указанных мониторных систем позволяло избирательно оценивать систолическую функцию ПЖ (показатель — фракция изгнания ПЖ) и сократимость ЛЖ (показатель — индекс сократимости ЛЖ).
На втором этапе исследования при лечении изолированной недостаточности ПЖ дополнительно к стандартной терапии использовали оксид азота. Препарат подавался в дыхательный контур аппарата ИВЛ или в лицевую маску при спонтанном дыхании. Использовали дозу 20 ppm, ингаляция начиналась в момент прибытия пациента в ОРИТ и заканчивалась после полного прекращения инфузии инотропных препаратов.
Статистический анализ проведен с помощью пакета программ Statistica 7.0 (StatSoft Inc., США). Полученные результаты обрабатывали с использованием классических методов вариационной статистики и корреляционного анализа, а также с помощью непараметрических методов (критерий Манна — Уитни, точный критерий Фишера). Различия показателей считали статистически значимыми при р < 0,05. Данные в выборках с нормальным распределением представлены в виде М ± δ, в выборках с ненормальным распределением — как медиана (25-й процентиль; 75-й процентиль).
РЕЗУЛЬТАТЫ
В период выполнения первого этапа исследования коронарное шунтирование в условиях искусственного кровообращения было проведено 234 пациентам, у 32 (13,7%) из них в раннем послеоперационном периоде развилась ОСН с необходимостью применения инотропной терапии. В случаях ОСН закономерно требовалось статистически значимо более продолжительное лечение в ОРИТ: 19,5 часа (16,0; 23,0) по сравнению с 15,3 часа (13,7; 17,2) при отсутствии необходимости в инотропной терапии (p < 0,05). В соответствии с указанными выше критериями для дальнейшего анализа были выбраны 25 пациентов, данные о которых приведены в таблице 1. С целью избирательной оценки систолической функции правого и левого желудочков в этих случаях применялась мониторная система PiCCO plus с приставкой VoLEF. На основании полученных данных вся выборка была разделена на три группы. В первую группу вошли 8 (32%) пациентов с изолированным снижением систолической функции ЛЖ. Фракция изгнания ПЖ в этих случаях превышала 40%, а индекс сократимости ЛЖ был менее 1200 мм рт. ст./с. Во вторую группу вошли 10 (40%) больных с изолированным снижением систолической функции ПЖ. В данных наблюдениях фракция изгнания ПЖ составляла менее 40%, а индекс сократимости ЛЖ превышал 1200 мм рт. ст./с. В третьей группе снижение систолической функции носило бивентрикулярный характер, фракция изгнания ПЖ была менее 40% и индекс сократимости ЛЖ ниже 1200 мм рт. ст./с. Подобные показатели были отмечены у 7 пациентов, что составило 28% от всей выборки.
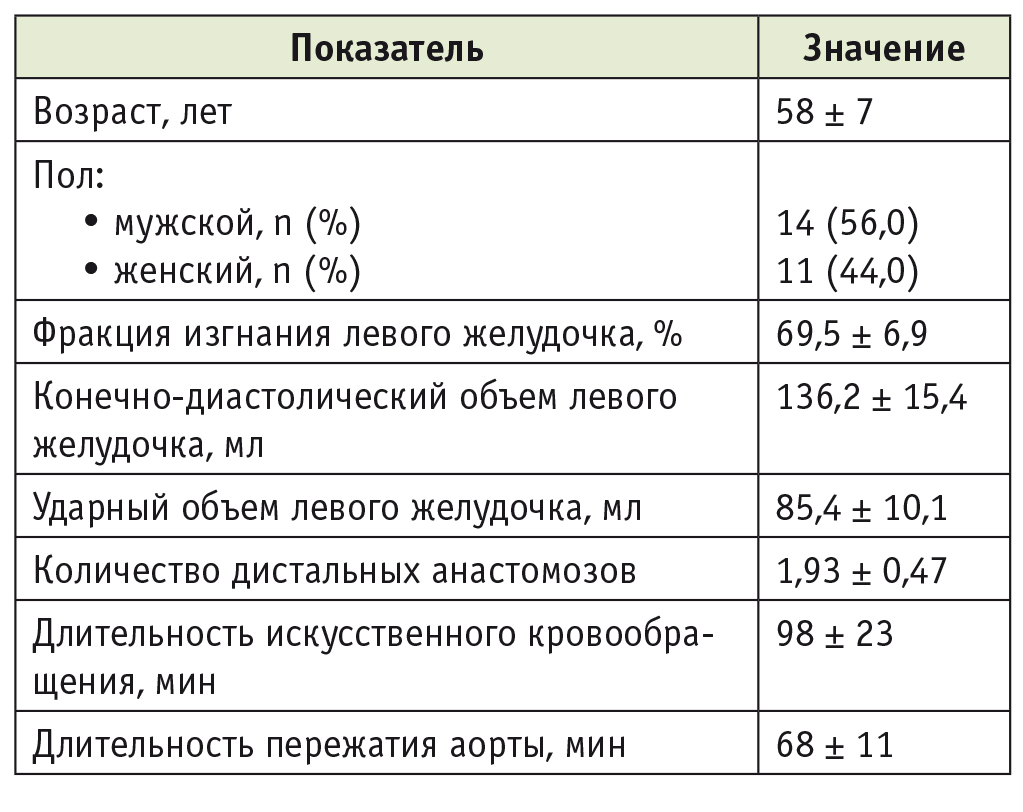
Таблица 1
Исходные данные и сведения о течении интраоперационного периода у пациентов, включенных в исследование (М ± δ), n = 25
Сравнительный анализ показателей клинического течения ближайшего послеоперационного периода был проведен в группах с изолированной систолической дисфункцией ЛЖ и изолированной систолической дисфункцией ПЖ. Как следует из данных, представленных в таблице 2, пациенты с изолированной недостаточностью ПЖ требовали статистически значимо более продолжительного периода инотропной терапии и, как следствие, более длительного лечения в условиях ОРИТ.
Таблица 2
Показатели клинического течения послеоперационного периода у пациентов с различными вариантами снижения систолической функции, медиана (25-й и 75-й процентили)
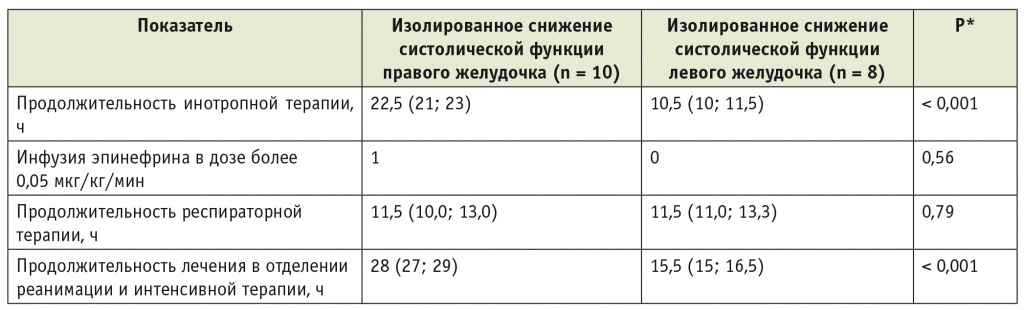
* U-тест Манна — Уитни.
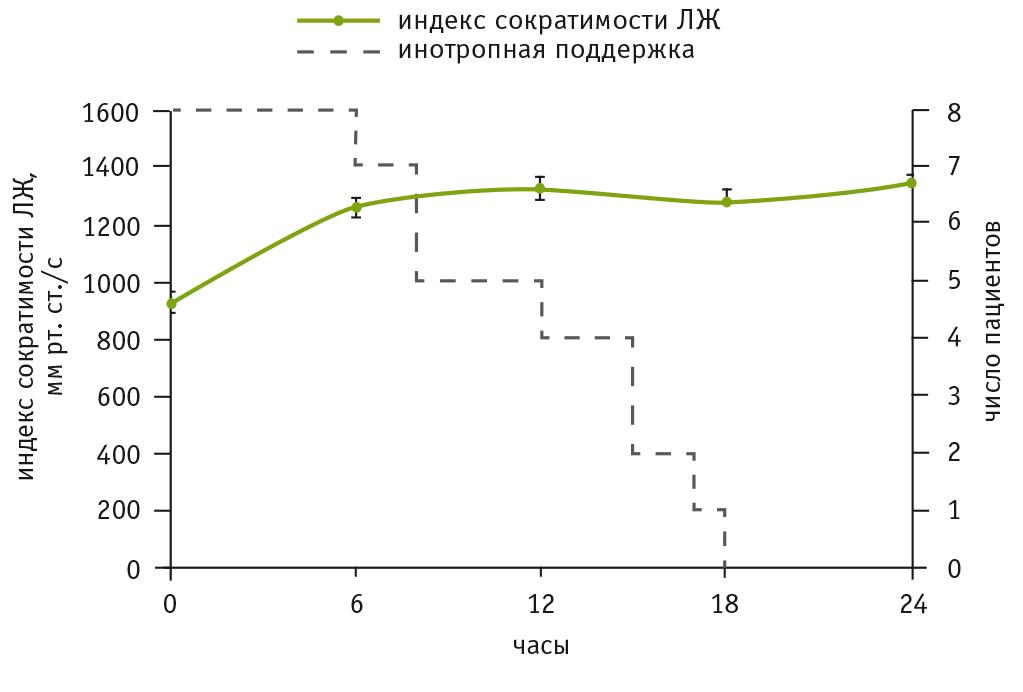
На рисунке 1 показана динамика восстановления систолической функции ЛЖ у пациентов первой группы. Через 12 часов после поступления в ОРИТ индекс сократимости ЛЖ у всех больных превышал 1200 мм рт. ст./с, что позволило в короткие сроки прекратить инотропную терапию и перевести пациентов в профильное отделение в течение первых послеоперационных суток.
Рис. 1. Динамика восстановления индекса сократимости при изолированной систолической дисфункции левого желудочка.
Примечание. На правой вертикальной оси отмечено число пациентов, нуждавшихся в проведении инотропной поддержки. ЛЖ ― левый желудочек
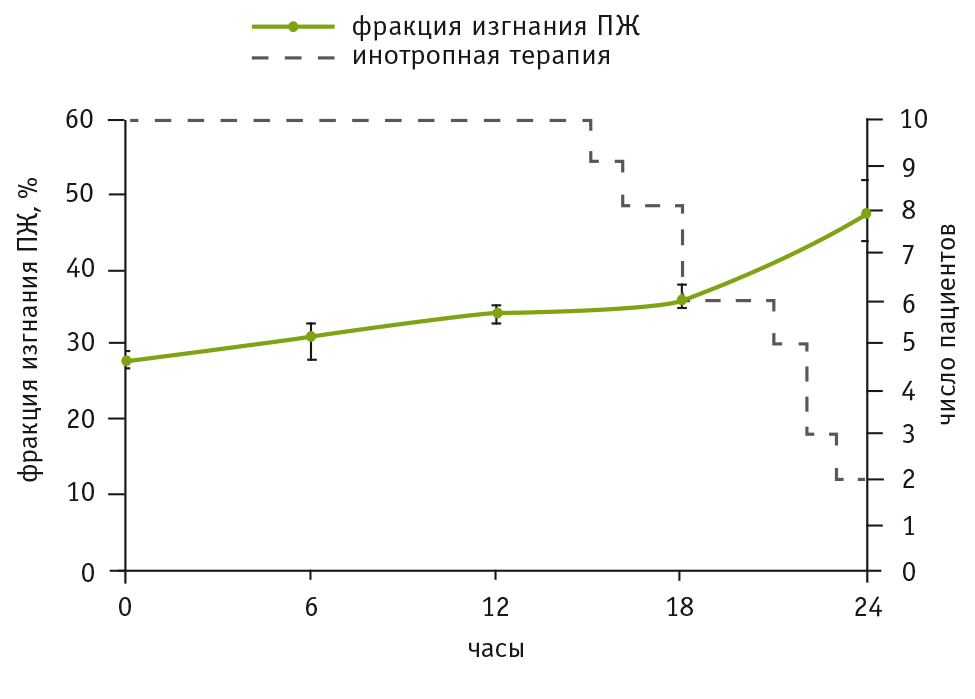
Как следует из данных, представленных на рисунке 2, в группе с изолированным снижением систолической функции ПЖ отмечалось длительное восстановление сократительной способности ПЖ, что увеличило время проведения инотропной терапии и продолжительность пребывания пациентов в ОРИТ. Только в трех случаях мы смогли перевести пациентов в профильные отделения в течение первых послеоперационных суток.
Рис. 2. Динамика восстановления фракции изгнания при изолированной систолической дисфункции правого желудочка.
Примечание. На правой вертикальной оси отмечено число пациентов, нуждавшихся в проведении инотропной поддержки. ПЖ ― правый желудочек
Применение мониторной системы PiCCO plus и дополнительной приставки VoLEF позволило провести углубленный анализ показателей гемодинамики, открывший ряд важных для клинической практики закономерностей. Мы обнаружили, что статистически значимая положительная зависимость (r = 0,71) между центральным венозным давлением и ударным объемом ПЖ имелась только в случаях сохраненной сократительной способности ПЖ (фракция изгнания ПЖ более 40%), в этих ситуациях увеличение объемной нагрузки приводило к повышению производительности ПЖ. Напротив, при сниженной сократительной способности ПЖ (фракция изгнания ПЖ менее 30%) корреляции между центральным венозным давлением и ударным объемом ПЖ не наблюдалось (r = 0,04), увеличение преднагрузки не приводило к росту выброса ПЖ.
Корреляционный анализ показателей сократительной способности ПЖ и постнагрузки выявил следующие зависимости: установлена статистически значимая отрицательная связь (r = – 0,95) между фракцией изгнания ПЖ и легочным сосудистым сопротивлением, а также между фракцией изгнания ПЖ и средним давлением в легочной артерии (r = – 0,73). Кроме того, в группе пациентов с изолированной дисфункцией ПЖ на момент поступления в ОРИТ показатели постнагрузки ПЖ были статистически значимо выше, чем в случаях изолированной левожелудочковой дисфункции. Так, легочное сосудистое сопротивление составляло 3 (2,9; 3) ед. Вуда при дисфункции ПЖ и 1,25 (1,2; 1,3) ед. Вуда при изолированной недостаточности ЛЖ, p < 0,001. Среднее давление в легочной артерии у пациентов с недостаточностью ПЖ составляло 23 (22; 23) мм рт. ст., а у больных с изолированным нарушением функции ЛЖ находилось на уровне 15 (15; 16) мм рт. ст., p < 0,001.
Обнаруженные гемодинамические закономерности позволили нам предположить, что включение в комплексную терапию недостаточности ПЖ вазодилататора малого круга приведет к более быстрому восстановлению систолической функции ПЖ и сокращению сроков лечения в ОРИТ. Для проверки этой гипотезы на втором этапе исследования была сформирована группа из 10 пациентов со сниженной систолической способностью ПЖ, основные данные об этих больных представлены в таблице 3.
Таблица 3
Исходные данные и сведения о течении интраоперационного периода у пациентов с изолированной дисфункцией правого желудочка, включенных в исследование на втором этапе (М ± δ), n = 10
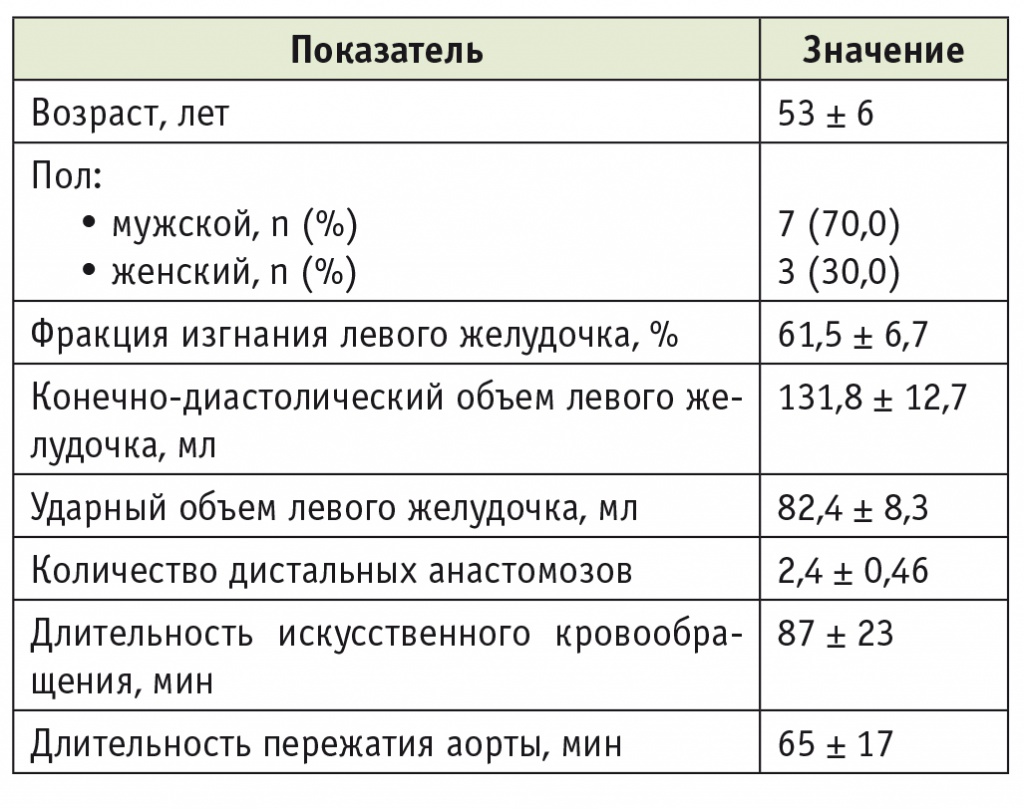
Всем пациентам, включенным во второй этап исследования, с момента поступления в ОРИТ проводили ингаляцию оксида азота в дозе 20 ppm. На фоне использования этого вазодилататора малого круга уже через час терапии отмечено статистически значимое снижение легочного сосудистого сопротивления с 2,9 (2,8; 3,0) до 1,35 (1,3; 1,4) ед. Вуда, p < 0,001; среднее давление в легочной артерии уменьшилось с 23,5 (23,0; 24,0) до 15,5 (14,0; 16,0) мм рт. ст., p < 0,001.
Для анализа изменений показателей гемодинамики и клинического течения на втором этапе исследования в качестве контрольной использовалась описанная выше группа из 10 пациентов с изолированной правожелудочковой дисфункцией, которые получали терапию инотропными препаратами без дополнительного применения вазодилататора малого круга. Назначение оксида азота сопровождалось статистически значимым снижением длительности применения инотропных препаратов и продолжительности лечения пациентов в ОРИТ (табл. 4).
Таблица 4
Показатели клинического течения послеоперационного периода у пациентов со снижением систолической функции правого желудочка, медиана (25-й и 75-й процентили)
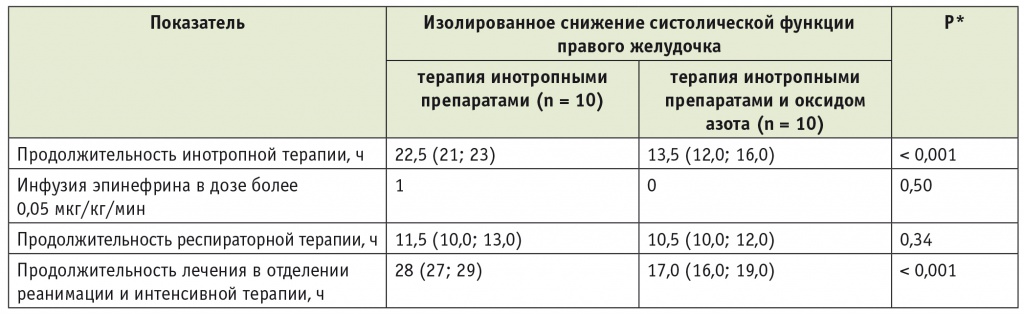
* U-тест Манна — Уитни.
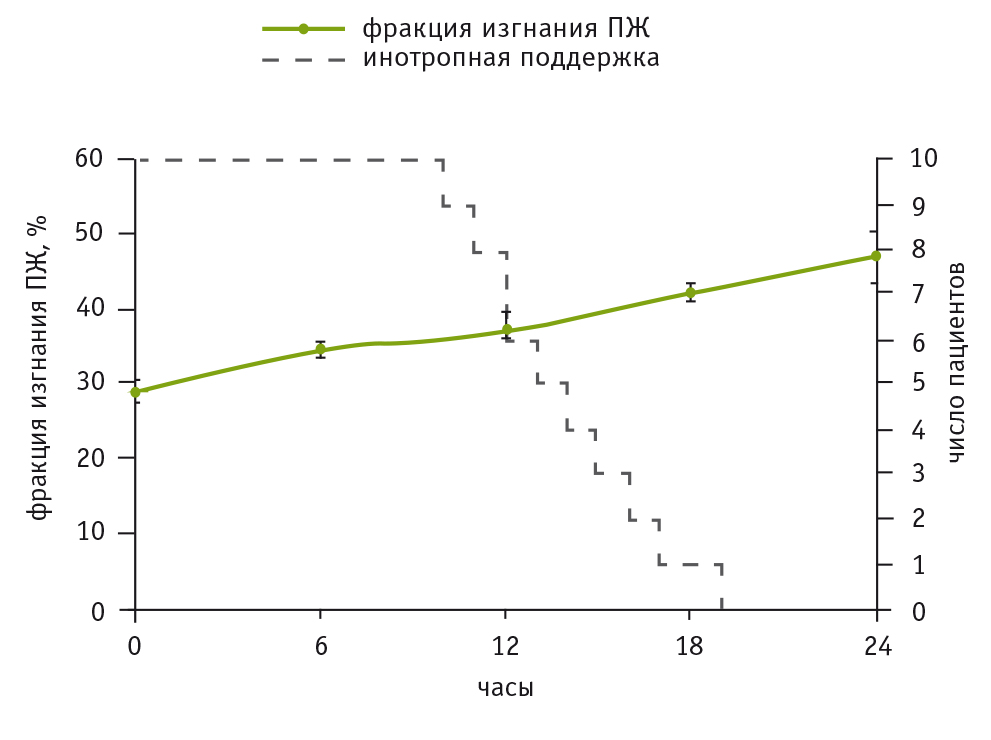
Достигнутое путем применения оксида азота снижение постнагрузки поврежденного ПЖ приводило к более быстрому восстановлению его сократительной способности. Как следует из данных, представленных на рисунке 3, уже через 20 часов после начала сочетанной терапии фракция изгнания ПЖ у всех пациентов превышала 40% и инотропные препараты не требовались.
Рис. 3. Динамика восстановления фракции изгнания при изолированной систолической дисфункции правого желудочка в случаях дополнительного применения оксида азота.
Примечание. На правой вертикальной оси отмечено число пациентов, нуждавшихся в проведении инотропной поддержки. ПЖ ― правый желудочек
ОБСУЖДЕНИЕ
Наше исследование подтвердило достаточно известное положение о том, что послеоперационная ОСН является фактором, затрудняющим раннюю активизацию пациентов и увеличивающим продолжительность лечения в ОРИТ. Применение комплексного мониторинга гемодинамики позволило избирательно оценить клиническое течение случаев изолированной систолической дисфункции правого или левого желудочка. При этом оказалось, что правожелудочковая сердечная недостаточность характеризуется более тяжелым течением с длительным восстановлением систолической функции ПЖ и необходимостью продолжительного лечения в ОРИТ (см. табл. 2, рис. 2).
Результаты дальнейшего исследования показали, что снижение производительности ПЖ происходит на фоне повышения давления в легочной артерии и увеличения легочного сосудистого сопротивления. Причины последних обстоятельств могли сложиться на интраоперационном этапе коронарного шунтирования, для которого характерны хорошо известные факторы повышения сопротивления сосудистого русла малого круга. Полученные нами данные позволяют определить увеличение легочного сосудистого сопротивления как значимый фактор снижения сократимости ПЖ и указывают на необходимость включения вазодилататоров малого круга в комплексную терапию правожелудочковой недостаточности.
На втором этапе исследования мы подтвердили, что дополнительное применение оксида азота в терапии изолированной правожелудочковой недостаточности приводит к быстрой нормализации показателей постнагрузки ПЖ и восстановлению его систолической способности. Это позволяет в более ранние сроки прекратить инотропную поддержку и сократить продолжительность пребывания пациентов в ОРИТ.
ЗАКЛЮЧЕНИЕ
- Послеоперационная острая сердечная недостаточность затрудняет раннюю активизацию и увеличивает сроки пребывания в ОРИТ пациентов кардиохирургического профиля.
- Изолированное снижение систолической функции правого желудочка характеризуется длительными гемодинамическими нарушениями, связанными с медленным восстановлением фракции изгнания. Сроки проведения инотропной поддержки и пребывания в ОРИТ в этих клинических случаях статистически значимо превышают таковые при изолированной левожелудочковой недостаточности.
- Своевременная диагностика снижения систолической функции правого желудочка и ее целенаправленная комплексная терапия способствуют сокращению времени применения инотропных препаратов и пребывания в ОРИТ.








