Заключительным этапом прогрессирования сердечно-сосудистых заболеваний, а также частой причиной госпитализации пациентов является ХСН[2, 16]. Данными многочисленных исследований подтверждено, что ХСН часто сочетается с сахарным диабетом 2 типа (СД2)[11–13]. Между СД2 и ХСН существует двусторонняя причинно-следственная связь[17]. При СД2 создаются условия, способствующие развитию миокардиодистрофии, ИБС, ХСН[3]. Длительное течение СД2 приводит также к возникновению диабетической автономной кардиальной нейропатии (ДАКН), что ухудшает прогноз сердечно-сосудистых заболеваний[9]. Существует ряд ассоциированных с СД2 механизмов прогрессирования ХСН. Среди них — инсулинорезистентность и эндотелиальная дисфункция[14], нарушения системы гемостаза[6] и гиперпродукция провоспалительных цитокинов[5], диабетическая нефропатия[8] и кардиоваскулярная автономная нейропатия[7].
Цель исследования: на основании данных ретроспективного анализа историй болезни пациентов, страдающих ИБС, с СД2 и c нормальным углеводным обменом и проспективного исследования с участием больных ИБС и ХСН с СД2 и c нормальным углеводным обменом изучить выраженность ХСН в зависимости от наличия нарушений углеводного обмена.
МАТЕРИАЛЫ И МЕТОДЫ
Проведен ретроспективный анализ 1986 историй болезни пациентов, находившихся на лечении в отделениях неотложной кардиологии ГКБ № 63 и ГКБ № 4 г. Москвы в период с 2011 по 2013 г. Анализу были подвергнуты истории болезни мужчин и женщин в возрасте от 55 до 75 лет, выписанных из стационара с диагнозами: нестабильная стенокардия, острый инфаркт миокарда (ОИМ) Q–, ОИМ Q+. В 1417 историях болезни пациенты имели нормальный углеводный обмен (первая группа, 642 мужчины и 775 женщин) и в 569 — СД2 (вторая группа, 214 мужчин и 355 женщин). Группы были сопоставимы по возрасту, ИМТ. Изучали распространенность ХСН II–IV ФК по NYHA, постинфарктного кардиосклероза (ПИКС), ОИМ Q–, ОИМ Q+, хронической аневризмы ЛЖ, постоянной и пароксизмальной форм фибрилляции предсердий.
В проспективном исследовании приняли участие 142 пациента 60–80 лет, которые находились на лечении в отделениях кардиологии ГКБ № 63 и ГКБ № 4 г. Москвы в 2012–2014 гг. Основную группу составили 105 больных c СД длительностью 5 и более лет, осложненным ДАКН (диагноз ДАКН выставляли на основе результатов проб Эвинга) в сочетании с ХСН II–III ФК по NYHA и ИБС. Установлено, что при длительности СД2 более 5 лет частота ДАКН статистически значимо возрастает[8], поэтому такие больные являются группой с высокой вероятностью наличия ДАКН.
В контрольную группу вошли 37 пациентов, страдавших ХСН II–III ФК по NYHA и ИБС, не имевших нарушений углеводного обмена. Всем больным проводили общее клиническое обследование, тест с 6-минутной ходьбой (ТШХ), ЭхоКГ, оценку выраженности боли в области сердца и одышки после нагрузки с помощью ВАШ, холтеровское мониторирование ЭКГ.
Статистическую обработку полученных данных выполняли с использованием пакета прикладных программ Statistica StatSoft Inc. (США), версия 6.0. Различия считали достоверными при р < 0,05.
РЕЗУЛЬТАТЫ
Данные, полученные при ретроспективном анализе, представлены в таблице 1.
Таблица 1
Клиническая характеристика больных, участвовавших в ретроспективном исследовании
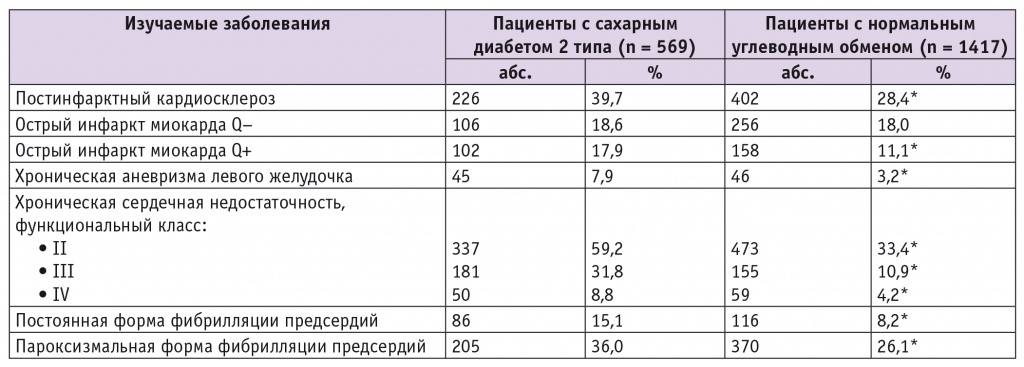
* P < 0,01.
Отмечено статистически значимое увеличение частоты выявления ПИКС, ОИМ Q+, хронической аневризмы ЛЖ, ХСН II–IV ФК по NYHA, пароксизмальной и постоянной форм фибрилляции предсердий при СД2 по сравнению с пациентами с нормальным углеводным обменом (р < 0,01 для всех показателей).
Установлено, что на развитие и течение ХСН в значительной мере влияют наличие в анамнезе ранее перенесенного инфаркта миокарда, нарушений сердечного ритма, хронической аневризмы ЛЖ. Это необходимо учитывать при изучении особенностей течения ХСН у той или иной когорты пациентов.
Результаты проспективного исследования представлены в таблице 2.
Таблица 2
Клинические проявления хронической сердечной недостаточности при сахарном диабете 2 типа и при нормальном углеводном обмене
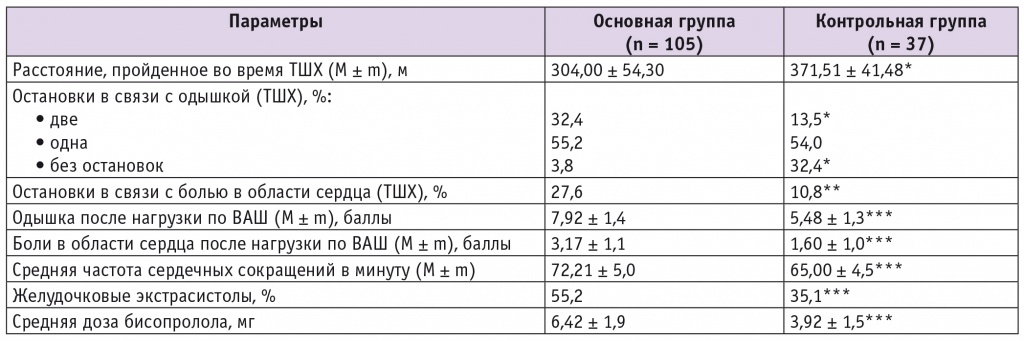
Примечания.
- ВАШ — визуальная аналоговая шкала, ТШХ — тест с 6-минутной ходьбой.
- (*) — p < 0,01; (**) — p < 0,02; (***) — p < 0,05.
По основным параметрам ЭхоКГ достоверных различий между группами не получено.
По данным нашего исследования, у пациентов с ХСН и СД2 отмечены более выраженные клинические проявления ХСН при проведении ТШХ, меньшая толерантность к физическим нагрузкам по сравнению с больными ХСН, не страдающими нарушениями углеводного обмена.
При проведении холтеровского мониторирования ЭКГ нами выявлены статистически значимо более высокая средняя ЧСС и бо’льшая частота встречаемости желудочковых экстрасистол в основной группе (р < 0,05). Согласно результатам нашего исследования, пациенты основной группы для контроля ЧСС нуждались в более высоких дозах β-адреноблокаторов. Средняя доза бисопролола в основной группе составила 6,42 ± 1,9 мг, в контрольной группе — 3,92 ± 1,5 мг (р < 0,05).
ОБСУЖДЕНИЕ
Результаты многочисленных исследований доказывают, что СД2 значительно увеличивает риск развития сердечно-сосудистых заболеваний[1, 4]. Известно, что поражение сердечно-сосудистой системы у больных СД2 обусловлено развитием микро- и макроангиопатии, которые являются патогенетическим субстратом для развития миокардиодистрофии, ИБС, диастолической дисфункции, ХСН[3]. Имеются также данные о том, что вклад в развитие ХСН при СД2 вносит поражение автономной нервной системы[10, 15]. Целью нашего исследования было на основании данных ретроспективного анализа историй болезни пациентов с ИБС изучить выраженность ХСН в зависимости от наличия нарушений углеводного обмена.
Ретроспективный анализ показал статистически значимое (р < 0,01) увеличение частоты выявления ПИКС, ОИМ Q+, хронической аневризмы ЛЖ, ХСН II–IV ФК по NYHA, пароксизмальной и постоянной форм фибрилляции предсердий при СД2 по сравнению с пациентами без нарушений углеводного обмена. Таким образом, нами подтверждено существующее мнение о влиянии хронической гипергликемии на развитие макроангиопатии с проявлениями в виде ОИМ, осложненного аневризмой ЛЖ, и формированием ХСН.
По данным нашего исследования, у пациентов с ХСН и ДАКН наблюдаются более выраженные клинические проявления ХСН при проведении ТШХ, меньшая толерантность к физическим нагрузкам по сравнению с пациентами с ХСН, не страдающими нарушениями углеводного обмена. Расстояние, пройденное во время ТШХ, в основной группе оказалось статистически значимо меньше (р < 0,01), чем в контрольной группе: 304,0 ± 54,3 м против 371,51 ± 41,48 м. При проведении ТШХ пациенты основной группы вынуждены были делать статистически значимо больше остановок в связи с появлением выраженной одышки и боли за грудиной, чем участники контрольной группы.
С помощью простого и наглядного метода характеристики клинических проявлений ХСН — ВАШ — были оценены субъективные проявления ХСН после нагрузки. Выраженность одышки и боли за грудиной была значимо выше в основной группе (р < 0,05 для обоих показателей). Таким образом, по полученным нами данным, субъективные проявления ХСН у больных ИБС, страдающих СД2, после нагрузки были сильнее, чем у пациентов с нормальным углеводным обменом.
Показатели, полученные при проведении ЭхоКГ, не имели достоверных различий между группами (р > 0,05). И в основной, и в контрольной группе наблюдались отклонения от нормы.
Необходимо отметить, что тахикардия покоя является ранним симптомом ДАКН, ее развитие связывают с поражением в первую очередь блуждающего нерва с относительным преобладанием тонуса симпатического отдела вегетативной нервной системы. Такого же мнения придерживается ряд исследователей, изучавших причины тахикардии покоя у пациентов с СД2, осложненным ДАКН[9]. Без сомнения, повышенная активность симпатической и сниженная активность парасимпатической нервной системы снижают порог фибрилляции желудочков, а использование β-адреноблокаторов в адекватной дозе, подобранной с учетом индивидуальных особенностей, позволяет достичь урежения ЧСС и тем самым улучшить состояние пациентов, что и было достигнуто в нашем исследовании.
ЗАКЛЮЧЕНИЕ
На основании данных ретроспективного анализа историй болезни пациентов с ИБС, страдающих сахарным диабетом 2 типа (СД2), установлено достоверное увеличение у них частоты постинфарктного кардиосклероза, острого инфаркта миокарда Q+, хронической аневризмы ЛЖ, пароксизмальной и постоянной форм фибрилляции предсердий по сравнению с больными ИБС с нормальным углеводным обменом, что определяет более выраженные клинические проявления ХСН. У пациентов с ИБС и СД2 ХСН III ФК встречается примерно в 3 раза, а IV ФК — в 2 раза чаще, чем у больных ИБС, имеющих нормальный углеводный обмен. У пациентов с ИБС, страдающих СД2, согласно данным холтеровского мониторирования ЭКГ, средняя ЧСС выше, чаще выявляют желудочковые экстрасистолы, что требует назначения более высоких доз β-адреноблокаторов для достижения целевых показателей ЧСС.







