ВВЕДЕНИЕ
Во всех развитых странах мира в структуре гинекологической патологии у девочек-подростков ведущее место занимают нарушения менструального цикла[1, 2]. В основе этих нарушений лежат незрелость центральных механизмов регуляции менструального цикла, высокая чувствительность их к действию различных неблагоприятных факторов. Характер менструального цикла в период полового созревания является критерием половой зрелости девочек-подростков[3, 4].
Роль ГнРГ в становлении пубертата хорошо известна, но в меньшей степени изучены механизмы регуляции секреции ГнРГ. В настоящее время считается, что большое значение в функционировании репродуктивной системы имеет нейропептид кисспептин[5–7]. Взаимодействие кисспептина и его клеточного рецептора GPR54 в мозге — определяющий фактор в активации нейронов, высвобождающих ГнРГ, который управляет секрецией ЛГ и ФСГ[7, 8]. Изучена роль кисспептина в возникновении некоторых заболеваний репродуктивной системы[8–12].
Терапия нарушений менструального цикла у девочек-подростков — непростая задача для специалистов. При возрастных функциональных расстройствах менструальной функции рационально использование немедикаментозных методов лечения. С учетом заинтересованности центральных механизмов в становлении и регуляции цикла предпочтительно применение трансцеребральных методов лечения. В настоящее время в различных областях медицины широко используются транскраниальные методы — лазерное воздействие, бегущее магнитное поле, электростимуляция центральных механизмов регуляции[13–15].
Цель исследования: оценить уровень кисспептина у девочек с нарушением менструальной функции с учетом массы тела и эффективность аппаратных методов коррекции клинико-гормональных изменений.
МАТЕРИАЛЫ И МЕТОДЫ
Обследованы 70 девочек-подростков 15–17 лет с различными нарушениями менструальной функции. Они были разделены на три группы в зависимости от массы тела: 1-ю группу составили 15 девочек с низкой массой тела в результате нервной анорексии, 2-ю группу — 35 девочек с ожирением, 3-ю группу — 20 девочек с нормальной или избыточной массой тела, у которых установлен диагноз формирующегося синдрома поликистозных яичников. В группу контроля вошли 20 здоровых девочек того же возраста.
Критерий включения: нарушения менструального цикла на фоне низкой, избыточной или нормальной массы тела. Критерии исключения: наличие соматической патологии, нарушений менструального цикла органической природы.
Все обследованные подписывали письменное информированное согласие на участие в исследовании.
Исследование одобрено этическим комитетом Саратовского государственного медицинского университета им. В.И. Разумовского по контролю над исследовательскими работами с участием человека (протокол № 6 от 06.02.2016 года).
Обследование включало изучение анамнезов жизни и заболевания, клинический осмотр с определением роста, массы тела, ИМТ, стадии полового развития по Таннеру, оценку выраженности симптомов эстрогенизации и гиперандрогении. Оценивали возраст менархе, наличие/отсутствие регулярного менструального цикла на момент осмотра.
Содержание кисспептина, ЛГ, ФСГ, пролактина, эстрадиола, 17-ОН-прогестерона, глобулина, связывающего половые стероиды; тестостерона, ТТГ определяли иммуноферментным методом на 4–5-й день менструального цикла, прогестерона — на 21–23-й день. Уровень кисспептина в сыворотке крови измеряли методом твердофазного ИФА набором реактивов Сloud-Clone Corp. (Китай). Учет показателей производился на микропланшетном фотометре StatFax (CША).
Эхографическая оценка состояния шейки и тела матки, яичников выполнялась стандартным методом на 4–5-й день менструального цикла и во вторую фазу цикла (21–23-й день) на ультразвуковом сканере Medison Accuvix V10 (производство Samsung Medison, Южная Корея).
Для коррекции нарушений менструального цикла пациентки 2-й и 3-й групп проходили курс транскраниальной магнитотерапии (ТкМт), выполненной с помощью аппарата «АМО-АТОС-Э», включающего приставку «Оголовье» и блок ТЭС-терапии (транскраниальной электростимуляции) с лобно-сосцевидными электродами на фиксаторах терминалов «Оголовья». Воздействие осуществлялось в режиме бегущего магнитного поля и ТЭС с помощью электродов, закрепленных на ремнях шлема. Частоту сканирования (модуляции) магнитного поля выбирали в диапазоне 1–12 Гц.
Сеансы магнитотерапии производились приставкой «Оголовье» в течение 7–12 минут. Использовалась битемпоральная методика, включающая одновременное воздействие на оба полушария при сканирующем характере магнитного поля с индукцией на поверхности излучателя 45 мТл при движении поля от височной доли к затылочной области. При этом в каждом из двух излучателей индукторы включались синхронно с противоположных сторон. ТЭС проводилась с выходным напряжением 20 ± 10%, средний ток — 15 мА, частота заполнения пачек импульсов выходного напряжения — 2,5 ± 10% кГц. Курс лечения включал 10 процедур.
Статистическая обработка полученных данных выполнялась с использованием пакета статистических программ Statistica 8. Все данные в работе представлены для параметрических критериев как среднее значение ± стандартное отклонение. Для сравнения двух групп по количественным признакам рассчитывался критерий Стьюдента. Различия считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
Анализируя анамнестические данные, мы установили, что 58 (82,9%) девочек в анамнезе имели гипоксическое поражение ЦНС, гипертензионно-гидроцефальный синдром отмечался у 38 (54,3%) участниц.
Средний рост пациенток 1-й группы составил 168 ± 4 см. ИМТ варьировал от 14,0 до 15,0 кг/м2 (в среднем 14,5 ± 0,5 кг/м2). Нарушения менструального цикла характеризовались вторичной аменореей (86,7%) и олигоменореей (13,3%). Возраст менархе находился в диапазоне от 13 до 16 лет.
При клиническом осмотре обращали на себя внимание слабое развитие подкожно-жировой клетчатки, сухость кожи, усиленное выпадение волос. Вторичные половые признаки развиты слабо. Имелись симптомы недостаточной эстрогенизации в виде бледного окрашивания ареолы сосков, недостаточного развития молочных желез, вторичного оволосения. При УЗИ матки и яичников определялись признаки гипоплазии матки, уменьшение толщины эндометрия.
Содержание кисспептина у больных 1-й группы — 96,0 ± 2,7 пг/мл, что значимо ниже, чем в группе контроля (167 ± 1,5 пг/мл). У них также были низкими уровни ЛГ (1,23 ± 0,44 МЕ/л) и ФСГ (2,53 ± 0,62 МЕ/л), эстрадиола (20,5 ± 4,695 пг/мл), что, по сути, является гипогонадотропным состоянием (табл. 1).
Таблица 1
Показатели гормонального статуса у девочек исследуемых групп
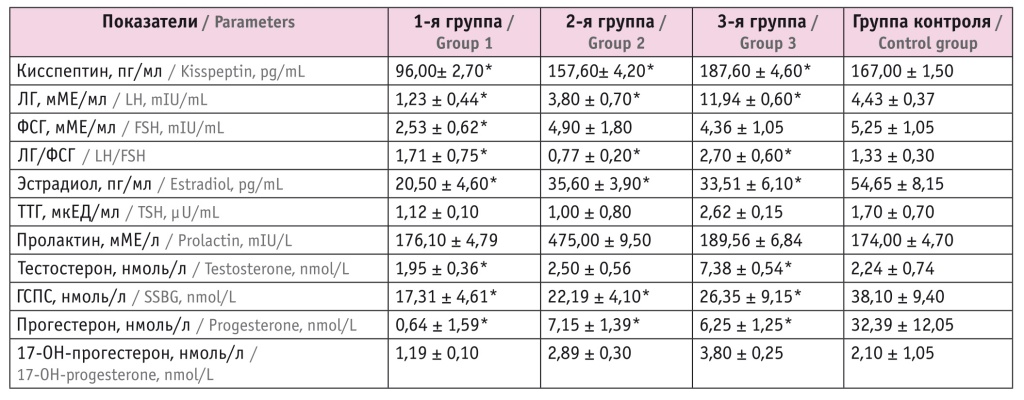
* Отличия от контрольной группы статистически значимы (р < 0,05).
Примечание. Здесь и в таблице 3: ГСПС — глобулин, связывающий половые стероиды, ЛГ — лютеинизирующий гормон, ТТГ — тиреотропный гормон, ФСГ — фолликулостимулирующий гормон.
У девочек с ожирением (2-я группа) средний рост составил 171 ± 3 см, ИМТ колебался от 31,2 до 43 кг/м2 (в среднем 37,1 ± 5,9 кг/м2). Возраст менархе — от 9,9 до 13,5 года.
Олигоменорея была самым частым нарушением менструального цикла и встречалась у 20 (57,1%) девочек, вторичная аменорея отмечалась у 12 (34,3%), аномальные маточные кровотечения — у 3 (8,6%). У 13 (37,1%) девочек олигоменорея сопровождала дисменорею. При УЗИ матка и яичники имели нормальные размеры, наблюдалась мультифолликулярная картина яичников, реже — обеднение овариального резерва.
Уровни кисспептина, ЛГ и ФСГ у них были существенно ниже, чем в группе контроля. Отмечалось также уменьшение содержания эстрадиола, пролактина, глобулина, связывающего половые стероиды, причем эти показатели не коррелировали с характером нарушения менструального цикла (см. табл. 1).
Антропометрические показатели пациенток 3-й группы: средний рост составил 169 ± 6 см, ИМТ у 5 больных находился в пределах нормы (23,7 ± 1,8 кг/м2), у 15 имел место избыток массы тела (28,2 ± 1,4 кг/м2).
Возраст менархе у участниц 3-й группы — от 13 до 16 лет (в среднем 14,5 ± 1,5 года). Нарушения менструации включали олигоменорею (15%), аномальные маточные кровотечения (10%), вторичную аменорею (75%).
Клиническая картина независимо от массы тела характеризовалась наличием множественных стрий, acanthosis nigricans в местах естественных складок кожи, АГ. Наиболее типичными при УЗИ внутренних половых органов были увеличение объема яичников (более 10 см3), наличие множества (более 10–12 в одном поле сканирования) мелких (2–4 мм) фолликулов, расположенных по периферии яичника, гиперплазия стромы.
Уровень кисспептина в периферической крови у девочек 3-й группы был значимо выше по сравнению с показателем группы контроля.
Установлено, что содержание кисспептина в сыворотке крови у больных с синдромом поликистозных яичников положительно коррелировало с уровнем ЛГ. Уровень ЛГ у них был выше (11,94 ± 0,6 МЕ/л), чем у девочек группы контроля и первых двух групп. Содержание тестостерона (7,38 ± 0,54 нмоль/л) в периферической крови у пациенток этой группы также выше, чем в группе контроля (см. табл. 1).
В группе контроля у всех девочек ИМТ находился в пределах нормальных значений (22,9 ± 1,6 кг/м2). Возраст менархе — от 10 до 13 лет (в среднем 12,0 ± 1,2 года). Длительность менструального кровотечения в среднем составила 4,0 ± 0,8 дня.
У всех участниц группы контроля отмечался регулярный менструальный цикл. Характеристика менструального цикла у девочек исследуемых групп представлена в таблице 2.
Таблица 2
Менструальная функция у девочек исследуемых групп
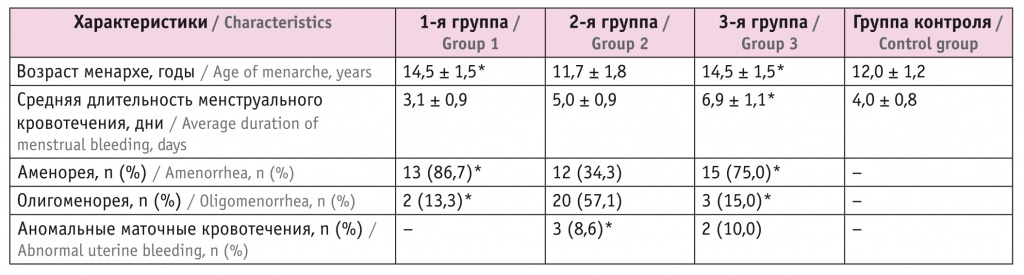
* Отличия от контрольной группы статистически значимы (р < 0,05).
Таким образом, полученные данные свидетельствуют об угнетении кисспептинергической системы у девочек-подростков с низкой массой тела, снижении ее активности при ожирении и активации при синдроме поликистозных яичников.
Для оценки эффективности и возможности использования транскраниальных методов коррекции нарушения менструальной функции девочкам 2-й и 3-й групп проведены 10–15 сеансов сочетанной битемпоральной магнитотерапии и ТЭС. У 30 (85,7%) участниц 2-й группы и у 18 (90%) 3-й группы после курса лечения отмечалось улучшение гормонального профиля (табл. 3) и менструальной функции. У 7 пациенток подобных изменений не произошло, что требует проведения повторных курсов, возможного назначения лекарственной терапии. Всем девочкам необходимо длительное динамическое наблюдение.
Таблица 3
Показатели гормонального статуса девочек 2-й и 3-й групп до и после лечения
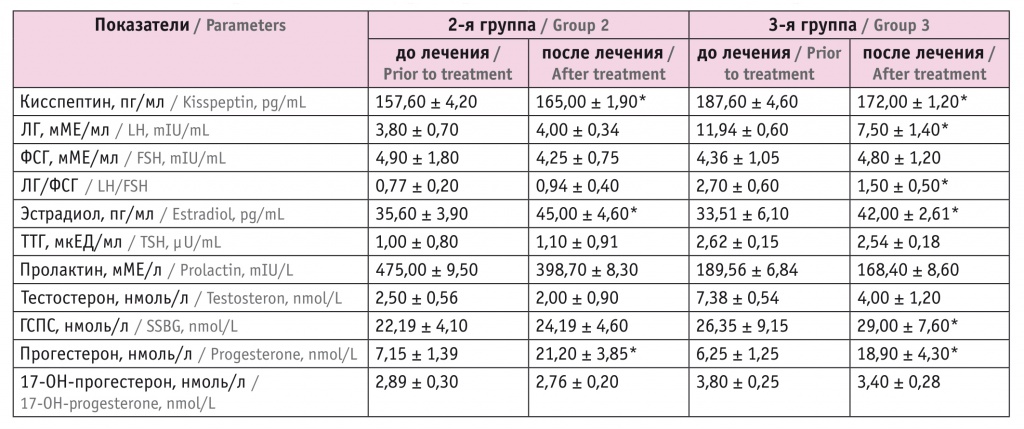
* Отличия от показателей до лечения статистически значимы (р < 0,05).
Под действием ТкМт и ТЭС наблюдалось улучшение клинической картины в виде нормализации менструального цикла у 48 (87,3%) из 55 девочек, что сопровождалось и улучшением гормональных показателей — повышением концентраций эстрадиола и прогестерона, снижением содержания пролактина, тестостерона. Отмечалось изменение уровня кисспептина: уменьшение его в случаях повышенного содержания при синдроме гиперандрогении в 3-й группе и увеличение в случаях его снижения у девочек 2-й группы, что свидетельствует в пользу регулирующего влияния транскраниальных методов на кисспептинергическую систему.
ОБСУЖДЕНИЕ
В последние годы в специальной литературе широко обсуждается вопрос о значении кисспептина в развитии и функционировании системы репродукции. Кисспептин относится к семейству пептидов, кодируемых геном Kiss1[5, 7, 16, 17]. Свои эффекты он реализует через G-протеиновый рецептор GPR54 и играет ключевую роль в межнейрональном взаимодействии, обеспечивающем синхронизацию полового развития. Кисспептин участвует в формировании циклической секреторной активности гонадотропинов и пика овуляторной стимуляции. Установлена взаимосвязь кисспептина с лептином[7, 17]. Отрицательный энергетический баланс сопровождается ингибированием экспрессии гена Kiss1.
В нашем исследовании изучены клинико-гормональные взаимоотношения у девочек-подростков 15–17 лет с различной массой тела и нарушением менструального цикла.
У девочек 1-й группы с белково-энергетической недостаточностью нарушения менструальной функции характеризовались вторичной аменореей у 86,7% или олигоменореей у 13,3%. В этой группе уровень кисспептина был значительно ниже, чем в группе контроля, равно как содержание ЛГ, ФСГ, прогестерона и эстрадиола. Это свидетельствует о подавлении кисспептинэргической системы в результате отрицательного энергетического баланса, что согласуется с литературными данными[8, 10]. В 1-й группе проводилось лечение, направленное на повышение массы тела и коррекцию метаболических нарушений.
В группе девочек с ожирением отмечались нарушения менструальной функции в виде олигоменореи, вторичной аменореи и аномальных маточных кровотечений. Уровень кисспептина у них также был снижен по сравнению с таковым в группе контроля, но в меньшей степени, чем у девочек с белково-энергетической недостаточностью. Во 2-й группе отмечалась активация гипоталамо-гипофизарно-надпочечниковой системы, что клинически проявлялось симптомами гиперкортицизма в виде наличия стрий, повышения АД, фолликулярного гиперкератоза, acanthosis nigricans.
Известно, что кортизол связывается с глюкокортикоидными рецепторами 2-го типа, локализованными на нейронах аркуатного ядра. Нарушение секреции динорфина и нейрокинина в нейронах приводит к угнетению синтеза кисспептина. Эти изменения могут подавлять активность ГнРГ-нейронов и ингибировать импульсную секрецию гонадотропинов, что и является причиной нарушений менструального цикла у девочек-подростков с нейроэндокринными нарушениями[5, 7, 18].
В 3-й группе были девочки как с нормальной (5 человек), так и повышенной массой тела (15 человек), у которых диагностирован синдром формирующихся поликистозных яичников. Наряду с нарушениями менструального цикла у девочек зафиксированы увеличение объема яичников, повышение концентрации тестостерона. Уровень кисспептина в периферической крови у них был выше, чем в группе контроля. Содержание кисспептина положительно коррелировало с концентрациями ЛГ и тестостерона, что согласуется с литературными данными[9, 19–23].
Прежде в наших работах мы указывали на улучшение гормональных показателей и нормализацию менструальной функции у девочек при воздействии ТкМт в сочетании с ТЭС[14, 15]. В данном исследовании также провели лечение 35 девочек с ожирением и 20 с диагнозом формирующегося синдрома поликистозных яичников с последующей оценкой клинических данных и определением уровня кисспептина.
Результаты научных разработок, направленных на техническую реализацию методов модуляции нейродинамических процессов при различных заболеваниях, весьма актуальны. Одним из перспективных методов, оказывающих нейрокорригирующее, адаптационное и антистрессовое воздействие на головной мозг, является ТкМт, которая стимулирует биосинтетические процессы, усиливает регионарный кровоток и микроциркуляцию, уменьшает спазм сосудов, улучшает реологические свойства крови, повышает тонус и резервные возможности организма[24].
Перспективно использование нескольких факторов электромагнитной природы, потенцирующих действие друг друга. Импульсные токи низкой частоты избирательно воздействуют на гипногенные и антиноцицептивные системы головного мозга. Проходя по структурам защитных механизмов мозга, селективно возбуждают эндогенную опиоидную систему ствола головного мозга и стимулируют выделение β-эндорфина и энкефалина[25]. Воздействие импульсным полем и наведенным током на мезодиэнцефальные структуры ствола головного мозга (ядра гипоталамуса и аденогипофиза) приводит к увеличению нейросекреции адренокортикотропного, соматотропного и меланоцитостимулирующего гормонов, ФСГ. Тропные гормоны гипофиза активируют работу эндокринных желез, а активация подкорковых центров регуляции восстанавливает вегетативную регуляцию функций внутренних органов и повышает уровень резерва адаптации. Обедняя поток восходящей импульсации в кору головного мозга, импульсные токи уравновешивают возбуждение и стабилизируют тормозные процессы в коре головного мозга, компенсируют процессы перевозбуждения и аффектации[26].
Поскольку так или иначе основой нарушения менструального цикла у подростков становится стресс, данные методики являются патогенетическим способом лечения. После проведения курса терапии у 87,3% девочек улучшилась менструальная функция и нормализовался уровень кисспептина. Подобные курсы проводились повторно с интервалом 3 месяца.
ЗАКЛЮЧЕНИЕ
Результаты данного исследования свидетельствуют, что показатели кисспептина зависят от физического развития девочек-подростков. Значительное снижение массы тела, а также ожирение приводят к угнетению кисспептиновых механизмов системы репродукции, что сопровождается различными нарушениями менструальной функции. Высокий уровень кисспептина, по всей вероятности, способствует формированию синдрома поликистозных яичников. Транскраниальная терапия улучшает клинический статус пациенток, способствует восстановлению менструального цикла за счет регулирующего влияния на кисспептинергическую систему.
Поступила: 29.05.2019
Принята к публикации: 15.07.2019








