ВВЕДЕНИЕ
К наиболее актуальным проблемам сахарного диабета 1 типа (СД1) справедливо относят вопросы эпидемиологии и особенностей манифестации в различных возрастных группах[1]. Изучение эпидемиологических показателей проводится с целью анализа динамики распространенности и заболеваемости, осложнений СД1 и прогнозирования их изменений.
Цель обзора: представить современную информацию по вопросам эпидемиологии и манифестации СД1 у детей и подростков.
ЗАБОЛЕВАЕМОСТЬ САХАРНЫМ ДИАБЕТОМ 1 ТИПА В МИРЕ
Более 90% форм диабета у детей и подростков приходится на СД1.
По данным Международной федерации диабета, сохраняется рост заболеваемости среди детей и подростков, количество новых случаев СД1 в возрасте 0–14 лет увеличилось с 98 200 до 108 300, а в возрасте 0–19 лет — со 128 900 до 149 500. Максимальный рост отмечен в регионах Африки, Ближнего Востока[2].
Заболеваемость отражает только вновь выявленные случаи заболевания за отчетный период и характеризуется значительными географическими особенностями. Средний прирост заболеваемости СД1 — 3–4% в год. По данным Международного общества детского и подросткового диабета, наименьшая стандартизированная по возрасту заболеваемость СД1 у детей и подростков в группе 0–14 лет была в Китае и Японии (1,9–2,2 на 100 тыс. человек; рис. 1), самые высокие показатели в течение нескольких десятилетий отмечены в Финляндии (до 52,2 на 100 тыс. человек) и Швеции (44,1 на 100 тыс. человек)[1]. Кувейт, Катар, Саудовская Аравия и Алжир, Норвегия, Соединенное королевство, Ирландия отнесены к странам с высокой заболеваемостью СД1[1].
Рис. 1. Стандартизированные по возрасту данные о заболеваемости СД1 у детей в возрасте от 0–14 лет[1]
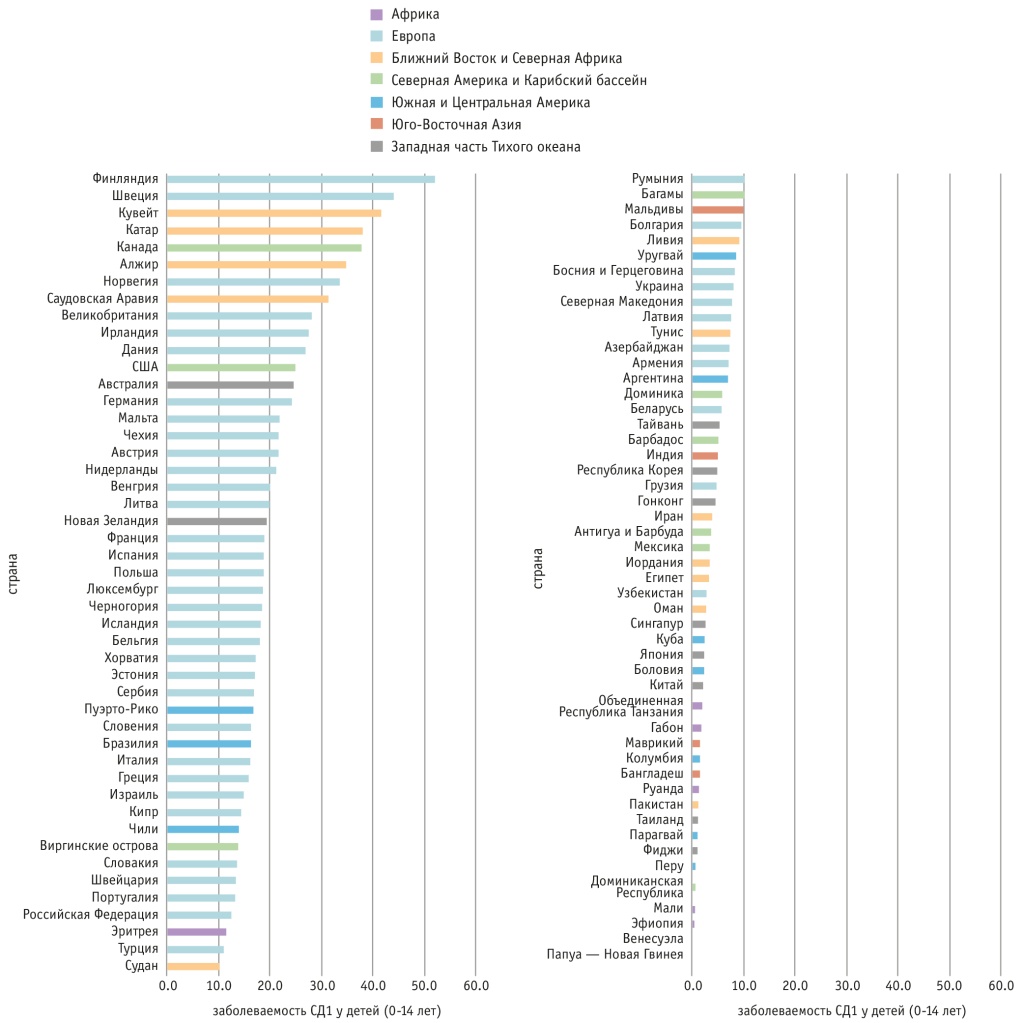
В возрастной группе пациентов 0–19 лет лидирующие позиции по заболеваемости — у Индии и Соединенных Штатов Америки (табл. 1)[2]. В России, как и в большинстве стран, на 2021 г. отмечается нарастание заболеваемости СД1 у детей и подростков, в возрастной группе 0–19 лет она составила 4,0 на 100 тыс. населения, что соответствовало 7-му месту среди стран, лидирующих по показателям заболеваемости[2].
Таблица 1. Заболеваемость СД1 детей и подростков (0–19 лет)[2]
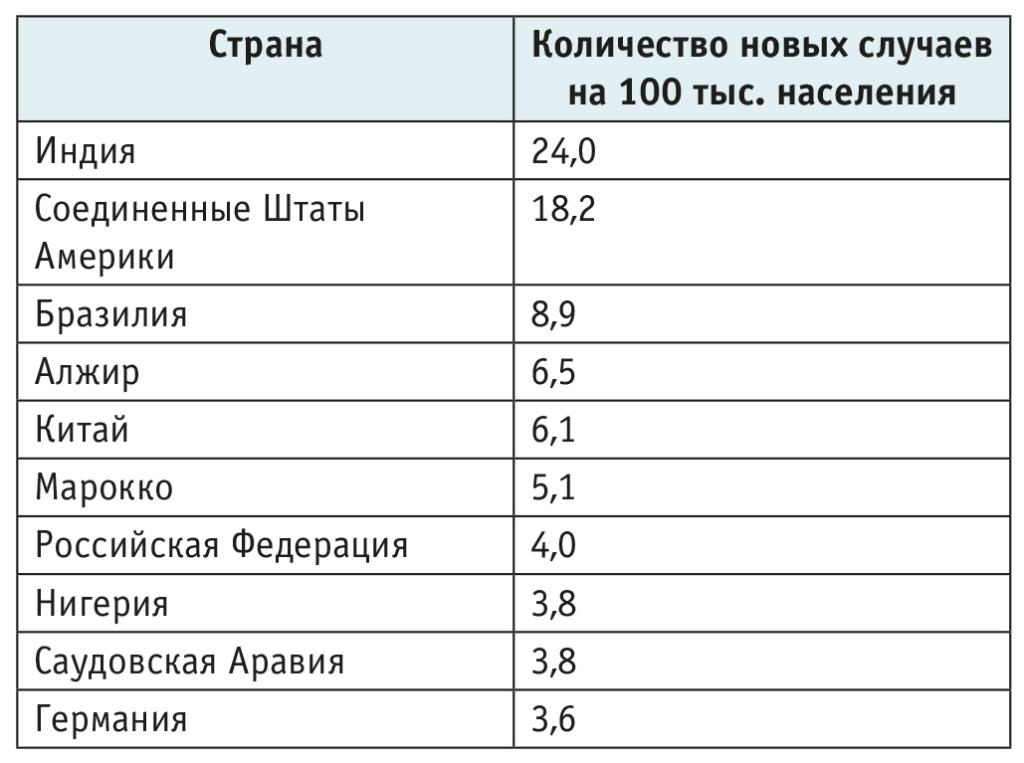
Наряду с географическими особенностями активно изучаются различия заболеваемости в зависимости от расы и этнической принадлежности. Так исследование SEARCH (США) продемонстрировало более высокую частоту СД1 у неиспаноязычных белых по сравнению с латиноамериканцами, чернокожими и американскими индейцами в возрасте до 20 лет. Вместе с тем анализ генетически сходных популяций, проживающих в странах с различной окружающей средой, также показал разные уровни заболеваемости СД1 у детей. Эпидемиологические различия, вероятно, объясняет сочетание географических, экологических, генетических и других внешних факторов[1].
Обсуждаются взаимосвязи заболеваемости с возрастом и гендерными особенностями. Во многих странах отмечена тенденция роста заболеваемости во всех возрастных группах без гендерных различий. Значительная часть публикаций указывает на пик заболеваемости в 10–14 лет, при этом исключением является Финляндия, где подъем заболеваемости регистрируется в более младшей возрастной группе — 5–9 лет[3–5]. Существенных гендерных различий в показателях заболеваемости СД1 у детей не отмечено, однако имеются отдельные сообщения о преобладании среди заболевших в возрастной группе старше 15 лет мальчиков (Азербайджан, Ирландия)[6, 7]. В Австралии и части европейских стран отмечается синусоидальная картина с 4–6-летними интервалами между годами пиковой заболеваемости[8]. Однако в последнее время ряд стран (Финляндия, Австрия, Германия, Ирландия, Австралия, Новая Зеландия, Швеция), где ранее наблюдались умеренная и/или высокая заболеваемость, сообщают о стабилизации и замедлении роста данного показателя. Влияние сезонности на заболеваемость СД1 у детей изучено недостаточно. В некоторых европейских странах и Австралии отмечается увеличение заболеваемости в прохладные осенние и зимние месяцы[1].
ЭПИДЕМИОЛОГИЧЕСКИЕ ПОКАЗАТЕЛИ САХАРНОГО ДИАБЕТА 1 ТИПА В РОССИИ
В России выполнено множество исследований, посвященных эпидемиологии СД1[9, 10]. В целом показатели распространенности и заболеваемости СД1 среди детей и подростков в нашей стране совпадают с общемировыми трендами и характеризуются постоянным ростом числа заболевших детей. Общая численность пациентов с СД1, по данным регионального регистра, в возрасте до 18 лет в России на 01.01.2023 составила 48 031 человек. Распространенность СД1 у детей — 136,1 на 100 тыс. детского населения, у подростков — 289,6 на 100 тыс. Заболеваемость СД1 у детей в 2021 г. составила 24 на 100 тыс. детского населения, у подростков — 32,1 на 100 тыс. подросткового населения[11]. По данным российских источников, в большинстве регионов страны в гендерной структуре заболевших СД1 преобладают мальчики. Подъемы заболеваемости отмечаются в возрастной группе 0–4 года, в также в пубертатном периоде[12].
На существование сезонных закономерностей указывают территории с выраженными временами года, где рост числа вновь выявленных случаев заболевания СД1 у детей преобладает в осенне-зимний и весенний периоды; взаимосвязь между сезонностью и заболеваемостью в географических зонах с относительно однородными (ровными) климатическими условиями менее значима. По результатам исследований отмечено увеличение заболеваемости СД1 среди детей и подростков в Брянской области в августе, осенью и весной с пиком в октябре и марте соответственно[13], в Ивановской и Тверской областях — весной и осенью[14, 15], в Пермском крае — в осенне-зимний период[16].
По данным государственного регистра, в Российской Федерации на фоне роста заболеваемости СД1 у детей отмечают существенные различия в показателях заболеваемости СД1 в различных регионах. Это может быть обусловлено разными причинами, среди которых не исключается вклад климатогеографических, этнических, социально-гигиенических и прочих факторов внешней среды, из числа которых многие остаются мало изученными и недооцененными[11].
На начало 2022 г. на территории Красноярского края наблюдалось 875 детей, страдающих СД1, общая распространенность составила 146,6 на 100 тыс. детского населения, общая заболеваемость — 25,3 на 100 тыс. населения. Распространенность заболевания у детей — 128,0 на 100 тыс. населения, у подростков — 248,9 на 100 тыс. населения. Заболеваемость на конец 2021 г. у пациентов до 15 лет — 26,1 на 100 тыс. населения, в группе 15–17 лет — 20,6 на 100 тыс. населения[11].
ЭТИОЛОГИЯ САХАРНОГО ДИАБЕТА 1 ТИПА
Данные о связи между более высокой заболеваемостью СД1 у детей и характеристиками окружающей среды, такими как степень урбанизации, плотность населения, социально-экономический статус района, более высокая широта или расстояние от экватора, требуют дальнейшего изучения и анализа. Актуален поиск экологических триггеров СД1[17]. Интерес представляют данные о возможном влиянии внешних факторов, в том числе природного радиационного фона, который создают присутствующие в земной коре естественные радиоактивные элементы (калий, торий и уран) и космические лучи. Природный фон существует повсеместно и является необходимым условием существования живых организмов. Уровни земной и космической радиации неодинаковы для разных мест земного шара, радиоактивных изотопов больше в горной местности, там, где присутствуют гранитные породы. Космическое излучение обычно возрастает с высотой над уровнем моря (чем выше, тем меньше воздуха, который выполняет роль защитного экрана), поэтому в высокогорных районах действие космического излучения в несколько раз больше, чем на уровне моря[18].
Обсуждаются данные о влиянии ионизирующего излучения на материнский организм с возможными отдаленными последствиями. Вероятность передачи цитогенетических эффектов, трансмиссии геномной нестабильности потомкам, развитие врожденных аномалий описаны во многих работах[19–21]. Иммунные нарушения, обусловленные действием радиации, могут являться триггерным механизмом развития опухолей и аутоиммунных заболеваний[22–24].
Эпидемиологические исследования проводятся в научной и практической эпидемиологии. Основной целью работ является описание заболеваемости населения и анализ эпидемиологических показателей для понимания причинно-следственных связей изменения заболеваемости на разных территориях с учетом специфики среды проживания, сезонности, возрастных и гендерных особенностей и выделение факторов и групп риска среди населения. На основании данных эпидемиологических исследований проводится оценка качества и эффективности программ и мероприятий. В разных странах проводят систематизацию и анализ данных о СД[25]. В России на основании приказа Минздрава России от 10.12.1996 № 404 с целью клинико-эпидемиологического мониторинга создан, а с 2014 г. переведен в онлайн-формат Федеральный регистр сахарного диабета[26]. Методологическим и организационным референс-центром регистра стало ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Министерства здравоохранения России, который и сегодня является ключевой аналитической платформой эпидемиологических характеристик СД. На 01.01.2022 в базу данных онлайн-регистра включены сведения из 85 регионов РФ. Регистр содержит данные о распространенности СД, рассчитываемой на 100 тыс. населения соответствующих возрастных групп: дети в возрасте младше 15 лет, подростки в возрасте 15–18 лет, взрослые старше 18 лет. Распространенность осложнений представлена у взрослых пациентов с СД на 10 тыс. пациентов с СД соответствующего типа. Информация о заболеваемости (первичная, по обращаемости) — показатель, оценивающий количество новых случаев заболевания, впервые зарегистрированных в текущем календарном году, рассчитывается на 100 тыс. населения соответствующей возрастной группы. Данные динамики осложнений представлены в процентном отношении в динамике в сравнении с предыдущими годами. Регистрация осложнений в регистре осуществляется согласно современной классификации, представленной в «Алгоритмах специализированной медицинской помощи»[26].
Мотивацией к рассмотрению особенностей манифестации заболевания является интерес к выявлению и исследованию факторов риска, предрасполагающих к развитию болезни. В течение СД1 манифестация является наиболее важной фазой, наступающей за доклинической. Заболевание характеризуется абсолютным дефицитом инсулина, который возникает при аутоиммунной деструкции 90% β-клеток островков поджелудочной железы[27].
Триггеры СД1 пока недостаточно ясны, предполагается многофакторный характер внешних влияний, требующий дальнейшего изучения. Согласно клиническим рекомендациям «Сахарный диабет 1 типа у детей» механизмы взаимодействия генетических факторов, экологических триггеров (инфекционных, алиментарных или химических) нуждаются в дальнейшем изучении. С ростом заболеваемости СД1 в ряде стран наблюдается уменьшение относительного вклада в развитие СД1 наиболее сильных генотипов HLA, что свидетельствует об увеличении роли факторов внешней среды. По-прежнему в числе значимых первопричин рассматриваются вирусы. В последние годы авторы ряда работ обращают внимание на энтеровирусную инфекцию, которая ассоциирована с активацией островкового аутоиммунитета и СД1, особенно если встреча с этим патогеном происходит в раннем детстве[28, 29]. Описаны случаи дебюта СД1 после инфицирования вирусами Коксаки B3 и B4, эпидемического паротита, краснухи и гриппа B (при этом вакцинация не повлияла на снижение заболеваемости СД1)[30, 31]. Причинная связь между СД1 и ротавирусом, цитомегаловирусом, вирусом герпеса и COVID-19 требует дополнительного изучения.
Относительно новыми являются дискуссии о взаимодействии между кишечной микробиотой и иммунной системой как важном факторе патогенеза СД1[27]. Известно, что микробиота кишечника при взаимодействии с иммунными клетками формирует иммунный ответ, влияет на системное воспаление вне кишечника и модулирует аутоиммунные реакции. При этом адекватное «обучение» иммунной системы происходит не всегда. Изучение состава микробиоты у пациентов с высоким риском развития СД1 показало обедненный состав комменсалов. На состав полезных микробных представителей кишечника могут влиять такие факторы, как способ родоразрешения, инфекции, особенности питания, лекарственные средства, в первую очередь антибиотики. В ряде работ в экспериментальных моделях на животных доказано положительное влияние пробиотиков на микрофлору и снижение патологического аутоиммунного ответа[28, 30]. При оценке влияния продолжительности грудного вскармливании получены неоднозначные результаты: часть работ указывает на возможный протективный эффект грудного молока в отношении СД1, однако увеличение длительности грудного вскармливания не дало защитного эффекта, но оказало более выраженное профилактическое влияние в отношении детей с наследственной предрасположенностью к СД1 в сравнении с коротким периодом грудного вскармливания. Изучение результатов раннего введения адаптированных молочных смесей на основе коровьего молока не привело к однозначным выводам: в проспективном исследовании DAISY отмечено влияние белка коровьего молока на частоту появления антител только у детей с генотипом HLA-DR низкого/среднего риска. Другие работы не подтвердили эту гипотезу. При использовании безмолочных смесей показан схожий риск развития СД1[30].
Обсуждается влияние ожирения на развитие заболевания у детей с генетической предрасположенностью. Предполагают, что ожирение приводит к инсулинорезистентности, увеличивает нагрузку на островковые клетки и, возможно, инициирует аутоиммунные процессы. Популяционные исследования показали, что дети, рожденные с высокой массой тела (более 4 кг), имеют более высокую частоту заболевания. Роль коровьего молока, глютена, антибиотиков не получила достаточного подтверждения в большинстве исследований. Прием витамина D, пробиотиков, омега-3 и полиненасыщенных жирных кислот в части работ повлияло на снижение риска развития СД1[31].
Изучение плановой профилактической вакцинации как фактора, способного внести изменения в иммунную систему ребенка, не представило достоверных доказательств пользы отказа от прививок[30, 31].
Несомненна роль острого и хронического стресса в увеличении риска развития СД1[30], однако механизм этого влияния на иммунную систему еще не описан. Изучение действия химических агентов или химических смесей на человека немногочисленны, и их результаты неоднозначны[32]. Действию радиоактивного излучения как триггера развития патологии эндокринной системы и СД1 посвящено небольшое количество работ. В основном изучали последствия аварии на Чернобыльской АЭС, и эти данные однозначно говорят о росте числа случаев заболевания[13, 33]. Описаны особенности заболеваемости населения на территории закрытых административно-территориальных образований[34]. Влияние антропогенных факторов на возникновение заболеваний, в том числе на СД1, изучено недостаточно.
ПРОФИЛАКТИКА САХАРНОГО ДИАБЕТА 1 ТИПА
Изучение этапа манифестации представляет научный и практический интерес, так как позволяет на основании клинических и лабораторных данных осуществлять мониторинг начальных проявлений СД1, что имеет исключительное значение в оценке эффективности проводимых профилактических мероприятий (особенно в группах риска) и прогнозировании течения заболевания.
Выделяют три уровня профилактики:
1. Первичная профилактика заключается в изучении влияния приема перорального инсулина детьми в возрасте от 4–7 до 36 мес с повышенным генетическим риском развития СД1 на частоту возникновения аутоантител к β-клеткам и диабета (исследование POInT вакцинации против вирусов, ассоциированных с СД1, и создание стратегий модуляции иммунной регуляции с участием микробиоты).
2. Вторичная профилактика направлена на людей, имеющих два вида аутоантител с признаками дисфункции β-клеток или без них. Сообщается о использовании непрерывного мониторинга уровня глюкозы и перорального теста на толерантность к глюкозе для прогнозирования заболевания. Кроме того, изучается влияние теплизумаба, моноклональных антител против CD3, не связывающихся с Fc-рецептором, на отсрочивание заболевания.
3. Третичная профилактика направлена на отдаление осложнений путем сохранения массы β-клеток и/или продления фазы ремиссии после начала СД1. Хорошие результаты получены в исследованиях с антитимоцитарным глобулином ATG. С разной степенью успешности изучается также влияние разных препаратов (циклоспорин плюс метотрексат, ритуксимаб, теплизумаб) на замедление прогрессирования заболевания и выздоровление. Большие надежды на остановку прогрессирования СД1 связывают с влиянием витамина Д[35].
Основной целью изучения периода манифестации является выявление детей из групп риска развития СД1, разработка и усовершенствование безопасных и действенных методов, направленных на профилактику заболевания.
ЗАКЛЮЧЕНИЕ
В России отмечается стабильный рост числа вновь заболевших СД1 детей и подростков. Анализ эпидемиологических характеристик по данным Федерального регистра сахарного диабета и отдельных исследований помогает в прогнозировании эпидемиологической ситуации и планировании профилактических и лечебных мероприятия у детей и подростков с СД1. Особенности дебюта диабета в определенной степени отражают гетерогенность рассматриваемой патологии. Механизм действия триггеров на манифестацию СД1 требует более глубокого изучения, что позволит в дальнейшем усовершенствовать профилактику заболевания, прежде всего по отношению к детям из группы риска, с целью максимального отсрочивания начала заболевания.
Поступила: 11.07.2023
Принята к публикации: 11.02.2024








