ВВЕДЕНИЕ
Контраст-усиленное ультразвуковое исследование (КУУЗИ) является одним из методов ультразвуковой диагностики, широко используемым в различных областях медицины, прежде всего в гепатологии[1–3]. КУУЗИ обладает хорошей переносимостью, в отличие от других диагностических методов (мультиспиральная компьютерная томография и магнитно-резонансная томография), поскольку метаболизм ультразвуковых контрастных препаратов не связан с мочевыделительной системой, не содержит йод, не вызывает аллергические реакции[1, 4, 5]. Микропузырьки контрастного препарата очень малы, их диаметр не больше эритроцитов, что способствует их проникновению в капилляры и расширению диагностических возможностей ультразвукового метода[6, 7]. Это позволяет использовать КУУЗИ при нарушениях структуры печени у пациентов с хроническими вирусными гепатитами с целью анализа состояния кровотока в различных участках паренхимы[6–10]. Таким образом, КУУЗИ может служить методом ранней неинвазивной диагностики при заболеваниях печени для комплексной оценки состояния паренхимы[11–14].
Цель исследования — определение диагностической эффективности КУУЗИ у пациентов с хроническими вирусными гепатитами В и С.
МАТЕРИАЛЫ И МЕТОДЫ
В 2019–2021 гг. на базе ОГБУЗ «Клиническая больница № 1» г. Смоленска были обследованы 240 человека. Всем пациентам, участвующим в исследовании, было проведено мульпараметрическое ультразвуковое исследование органов брюшной полости (В-режим, допплерография сосудов, эластография), включая КУУЗИ с оценкой качественных и количественных параметров (кроме пациентов 2-й группы).
Выделены 3 группы пациентов (табл. 1):
— 1-я группа (n = 125) — пациенты с хроническими вирусными гепатитами, которым были проведены КУУЗИ и ультразвуковая эластография 2D-SWE, 42 пациентам также осуществлена чрескожная биопсия печени:
-
1-я подгруппа (n = 58) — пациенты с хроническим вирусным гепатитом В;
-
2-я подгруппа (n = 67) — пациенты с хроническим вирусным гепатитом С;
— 2-я группа (n = 50) — пациенты с хроническими вирусными гепатитами В и С, которым не проводилось КУУЗИ печени;
— 3-я группа (n = 65) — пациенты без хронических вирусных гепатитов, которым было проведено КУУЗИ.
Таблица 1
Общая клиническая характеристика пациентов и референтных методов
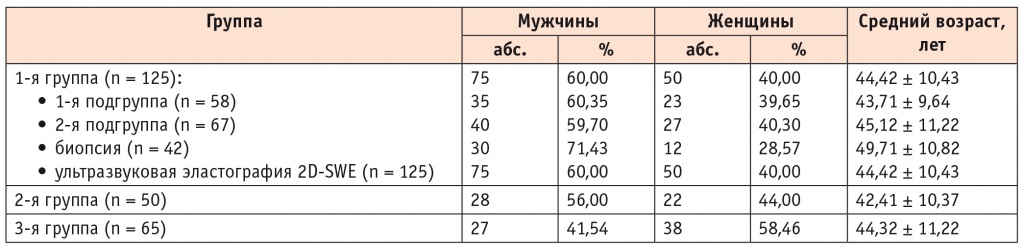
Критерии включения в исследование для пациентов 1-й и 2-й групп:
-
установленные диагнозы хронических вирусных гепатитов В и С на протяжении последних 6 мес, определение вирусной нагрузки и генотипа при HCV-инфекции;
-
отсутствие ранее проведенной терапии, включая противовирусную;
-
возраст старше 18 лет;
-
наличие информированного добровольного согласия на обследование.
Выделение 2-й группы было необходимо для определения диагностической эффективности метода в оценке развития осложненного течения (формирование цирроза, осложнений — асцита, портальной гипертензии, печеночно-клеточной недостаточности, кровотечения из расширенных вен пищевода).
Основными нозологическими формами у пациентов 3-й группы являлись хронический гастрит (41,54%), хронический дуоденит (30,77%), язвенная болезнь желудка и двенадцатиперстной кишки (15,38%), хронический некалькулезный холецистит (12,31%).
Критерии включения в качестве 3-й группы:
-
отсутствие HCV и HBV-инфекции;
-
отсутствие в анамнезе указаний на наличие признаков алкогольного, токсического, холестатического, аутоиммунного гепатита, а также алкогольной болезни и неалкогольной жировой болезни печени; отсутствие признаков острых и обострения хронических заболеваний на момент исследования, отсутствие указаний на наличие инфекционных, аллергических и иммунодефицитных состояний;
-
возраст старше 18 лет;
-
наличие информированного добровольного согласия на обследование.
Критерии исключения:
-
общее тяжелое состояние пациента;
-
наличие аутоиммунной и эндокринной патологии, заболеваний соединительной ткани, ВИЧ-инфекции;
-
органические нарушения центральной нервной системы;
-
беременность;
-
сочетанная HCV- и HBV-инфекция;
-
возраст младше 18 лет;
-
отсутствие добровольного информированного согласия пациента на обследование.
Для оценки соответствия параметров КУУЗИ данным, полученным по результатам референтных методов, использовался коэффициент согласия каппа Кохена.
Качественные параметры оценивали в баллах от 1 (норма) до 5 (цирроз) по предложенной стандартизированной программе[15]. В IV, V, VI, VII сегментах печени анализировали следующие параметры: в артериальную фазу оценивали наличие/отсутствие деформации сосудистого рисунка, симметричность накопления контрастного препарата; в портальную и позднюю венозную фазы — общую интенсивность контрастирования, краевое ослабление визуализации, наличие очагов неоднородного контрастирования и задержки выведения контрастного препарата.
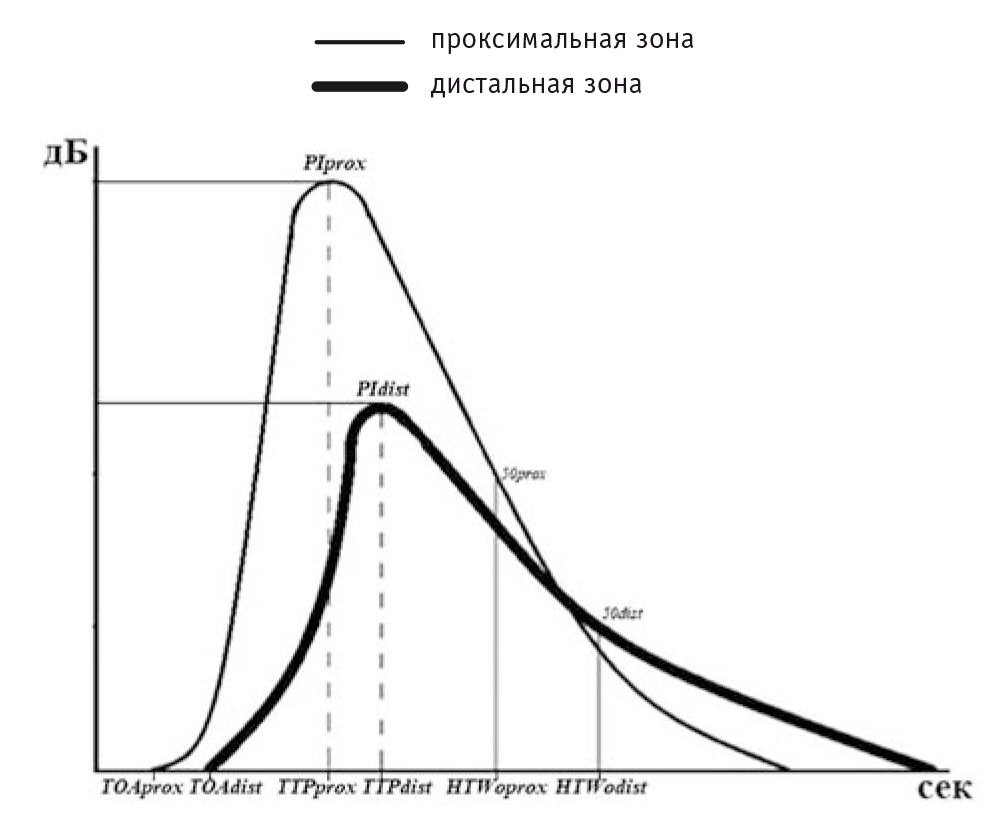
Оценка количественных параметров проводилась в проксимальных и дистальных зонах в зависимости от расположения относительно магистральных сосудов с дальнейшим автоматическим анализом полученных результатов и построением кривых накопления контрастного препарата (рис. 1). На полученных кривых определяли стандартные точки оценки количественных параметров контрастирования в проксимальных и дистальных зонах, а также их разницу: начало артериальной фазы (time of arrival — TOA), время достижения максимальной интенсивность накопления контрастного препарата (time to peak — TTP), максимальная интенсивность накопления контрастного препарата (peak intensity — PI) и время полувыведения контрастного препарата (half-time washout — HTWo)[16].
Рис. 1. Кривые накопления контрастного препарата в проксимальных и дистальных зонах с оценкой начала артериальной фазы (с), времени достижения максимальной интенсивности накопления контрастного препарата (с), максимальной интенсивности накопления контрастного препарата (дБ) и времени полувыведения контрастного препарата (с)[2]
РЕЗУЛЬТАТЫ
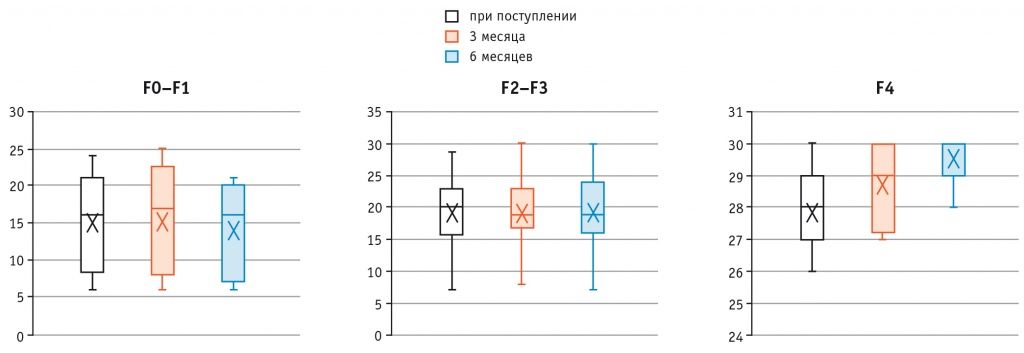
Всем пациентам 1-й и 2-й групп было проведено КУУЗИ с 1,0 мл контрастного препарата SonoVue (Bracco Suisse S.A.) с последующей оценкой качественных и количественных параметров контрастирования. Наибольшие изменения параметров КУУЗИ были выявлены у пациентов со стадией фиброза F4 по классификации METAVIR, установленной также референтными методами. У пациентов со стадией фиброза F2–F3 наблюдались более выраженные изменения данных параметров по сравнению с пациентами без патологии печени или с клинически незначимым фиброзом (F0–F1) (рис. 2).
Рис. 2. Анализ качественных параметров КУУЗИ у пациентов с различной стадией фиброза
В ходе исследования определены значения оценки качественных параметров КУУЗИ в сопоставлении со стадией фиброза по классификации METAVIR: 6–10 баллов — стадия F0, 11–15 баллов — F1, 16–20 баллов — F2, 21–25 и 26–30 баллов — F3–F4.
Для оценки диагностического потенциала качественных параметров применялся ROC-анализ и был выделен оптимальный порог отсечения перехода фиброза в цирроз, равный 26 баллам[17].
В случае количественных параметров наибольшей специфичностью обладали показатели разницы значений в проксимальных и дистальных зонах — ΔTOA, ΔTTP, ΔPI, ΔHTWo, т.к. при этом учитывалось состояние паренхимы комплексно, включая участки у крупных сосудов и на периферии. Например, оценка разницы показателей времени достижения максимальной интенсивности накопления контрастного препарата (ΔTTP) в проксимальных и дистальных зонах по данным ROC-анализа (табл. 2) и выделение оптимального порога отсечения перехода фиброза в цирроз — 15% (рис. 3). Кроме того, установлено, что чем выше стадия фиброза, тем более выраженные изменения качественных параметров (рис. 4, 5).
Таблица 2
Данные ROC-анализа для ΔTTP в динамике
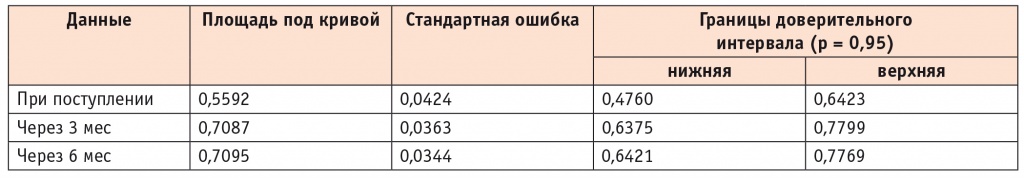
Рис. 3. Анализ ΔTTP в динамике
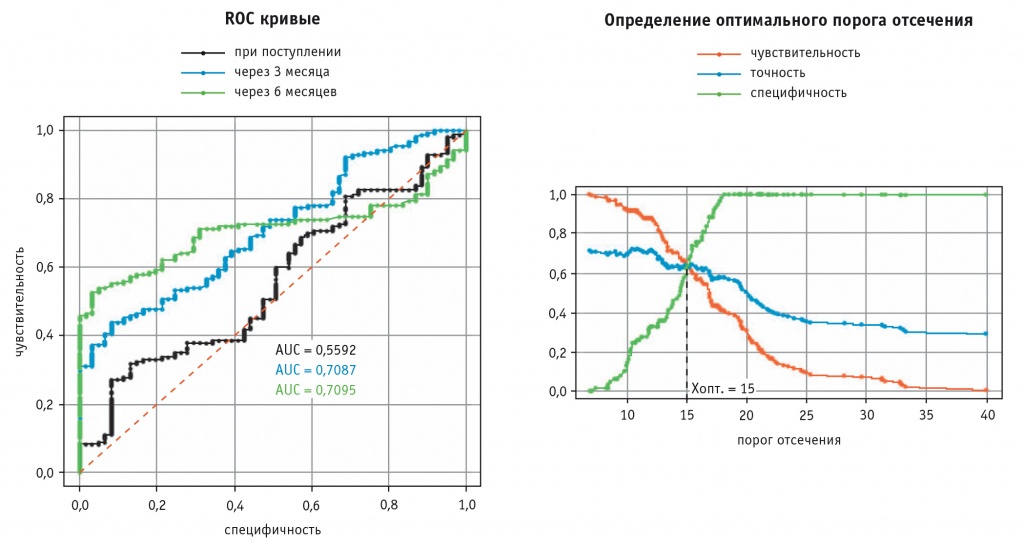
Рис. 4. Пациент Д., оценка качественных параметров: общая сумма баллов — 11, что соответствует стадии F1 фиброзных изменений (2D-SWE: 5,19 кПа/1,32 м/с). Иллюстрации здесь и далее предоставлены авторами.
Примечание. A — артериальная фаза (11–32 с): отсутствие деформации сосудистого рисунка, незначительное асимметричное накопление контрастного препарата; B — портальная фаза (33–121 с): незначительно выраженное асимметричное снижение общей интенсивности контрастирования, краевое ослабление визуализации контрастирования до 20 мм от края глиссоновой капсулы; C — поздняя венозная фаза (122–217 с): наличие очагов неоднородного выведения и задержки контрастного препарата в количестве до 10
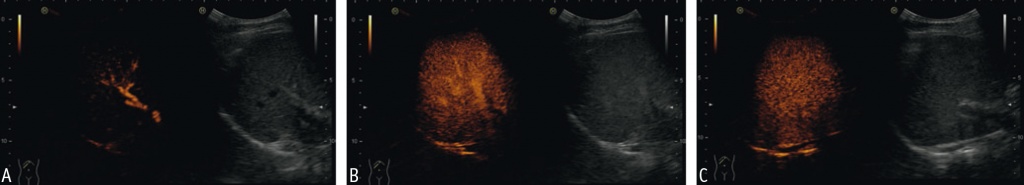
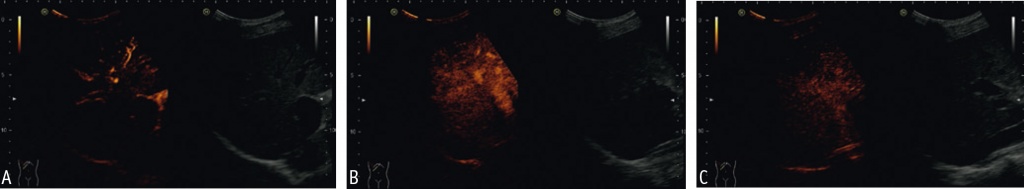
Рис. 5. Пациент И., оценка качественных параметров: общая сумма баллов — 27 баллов, что соответствует стадии F4 фиброзных изменений (2D-SWE: 11,21 кПа/1,93 м/с).
Примечание. A — артериальная фаза (8–29 с): деформация сосудистого рисунка (6 сосудов), значительное асимметричное накопление контрастного препарата; B — портальная фаза (30–95 с): выраженное асимметричное снижение интенсивности контрастирования, краевое ослабление визуализации контрастирования до 25 мм от края глиссоновой капсулы; C — поздняя венозная фаза (96–224 с): наличие очагов неоднородного выведения и задержки контрастного препарата в количестве до 15
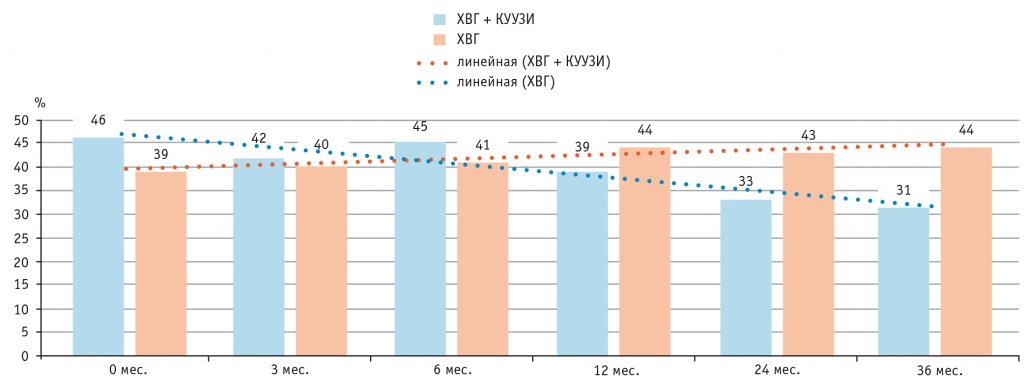
При включении КУУЗИ в стандартный алгоритм у пациентов 1-й группы за период динамического наблюдения (2 года) процент развития осложненного течения (асцит, портальная гипертензия, печеночно-клеточная недостаточность, кровотечение из расширенных вен пищевода) снизился с 46% до 31%; при этом у пациентов 2-й группы аналогичный показатель увеличился с 39% до 44% (рис. 6).
Рис. 6. Диагностическая эффективность применения КУУЗИ в стандартном алгоритме
ЗАКЛЮЧЕНИЕ
1. Использование контрастного препарата увеличивает ценность ультразвукового метода в диагностическом алгоритме при хронических вирусных гепатитах, особенно в остром периоде, когда эластография малоинформативна.
2. Наибольшим диагностическим потенциалом обладают такие параметры КУУЗИ, как разница количественных параметров в проксимальных и дистальных зонах, а также сумма баллов оценки качественных параметров более 26 баллов.
Поступила: 18.10.2022
Принята к публикации: 16.12.2022








