В 2015 г. состоялся Киотский консенсус, целями которого были систематизация и представление с позиций доказательной медицины накопленных за последние несколько лет данных о заболеваниях, ассоциированных с Helicobacter pylori (HP) [2, 35]. На текущий момент широкая распространенность инфекции HP в популяции в сочетании с ее ассоциацией с широким спектром заболеваний гастродуоденальной зоны (хроническим гастритом, хроническим дуоденитом, язвенной болезнью желудка и двенадцатиперстной кишки, MALT-лимфомой, а также аденокарциномой желудка) остро ставит вопрос о своевременной диагностике и эрадикации микроорганизма как о тактике, позволяющей не только профилактировать развитие заболеваний, склонных к формированию жизнеугрожающих осложнений, но и снизить экономические затраты практического здравоохранения [4, 5, 27].
В рамках Киотского консенсуса экспертным советом широко обсуждались вопросы, связанные с актуализацией существующих систем классификации хронического гастрита, анализировались роль данной нозологической единицы в формировании и прогрессировании предраковых изменений слизистой оболочки желудка (СОЖ), а также возможности ранней диагностики и эрадикационной терапии (ЭТ) HP-инфекции в качестве методов эффективной канцеропревенции [2, 35].
В настоящей статье нами представлены основные положения Киотского консенсуса, снабженные как оригинальными, так и собственными комментариями. Предложенные материалы знакомят российских гастроэнтерологов с мировыми трендами в отношении тактики ведения пациентов с HP-ассоциированными заболеваниями, и в первую очередь с HP-ассоциированным гастритом.
УТВЕРЖДЕНИЯ КИОТСКОГО КОНСЕНСУСА
В процессе обсуждения в рамках Киотского консенсуса экспертным советом были сформулированы 24 положения различных классов рекомендаций и уровней доказательности.
Положение 1. Классификация гастрита в системе МКБ-10 является устаревшей, так как она не отражает данных об этиологической роли инфекции HP (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Классификация гастрита по системе МКБ-10 (К29) была предложена в 1989 г. и к настоящему времени используется в большинстве стран, которые являются членами ВОЗ. Данная классификационная система не дает информации о широкой этиологической структуре гастрита, известной к настоящему времени. Открытие этиологической роли инфекции HP не было принято во внимание в силу недостаточной доказанности на момент составления классификации. Исследования последующих лет позволили определить ведущую этиологическую роль HP в формировании гастритических изменений, что открыло новую главу в изучении этой проблемы [20, 28]. Таким образом, в настоящее время ни одна система классификации гастрита не может рассматриваться как актуальная без выделения формы заболевания, ассоциированной с HP.
Положение 2. Новая редакция классификации гастрита и дуоденита по системе МКБ-11β представляет собой улучшенный вариант, так как она базируется на этиологических факторах (класс рекомендаций: сильный; уровень доказательности: умеренный).
Комментарии. Сформулированный на сегодняшний день вариант МКБ-11β (от января 2011 г.) является неокончательной версией и в настоящее время не утвержден ВОЗ. Классификация гастрита в системе МКБ-11β основана в первую очередь на каузативных факторах и включает три основные формы: HP-ассоциированный, лекарственно-индуцированный, аутоиммунный гастрит. Экспертным советом Киотского консенсуса была предложена обновленная версия классификации гастрита, представленной в системе МКБ-11β, которая также базируется на этиологических факторах, однако структурирована по несколько другому принципу (табл.). Данная система тоже представляется актуальной, но для ее внедрения в клиническую практику необходима широкая валидизация в различных странах мира.
Таблица
Классификация форм гастрита на основе этиологических факторов, предложенная в рамках Киотского консенсуса (2015)

Положение 3. Целесообразно классифицировать HP-ассоциированный гастрит по локализации, поскольку развитие рака желудка и язвенной болезни коррелирует с вовлеченным в патологический процесс отделом органа (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии.Знание локализации HP-ассоциированного гастрита позволяет прогнозировать, наряду с активностью воспалительного процесса, индивидуальный риск развития серьезных гастродуоденальных осложнений, в частности рака желудка [23, 39]. Так, пациенты с выраженным атрофическим гастритом (с кишечной метаплазией или без нее) в теле желудка имеют повышенный риск развития рака как кишечного, так и диффузного типа [9, 39]. В этой же когорте наблюдается увеличенный риск язвенной болезни желудка, тогда как у больных с антральным гастритом выше риск язвенной болезни двенадцатиперстной кишки [1, 4].
Положение 4. Целесообразно классифицировать гастрит по гистологическим признакам, поскольку риск развития рака желудка на фоне HP-ассоциированного гастрита варьирует в зависимости от распространенности и активности воспалительного процесса и выраженности явлений атрофии (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Патоморфологическая оценка гастрита является клинически релевантной, поскольку разные фенотипы HP-ассоциированного гастрита детерминируют различный риск развития гастродуоденальных осложнений. Выраженность и распространенность атрофического гастрита и кишечной метаплазии являются предикторами риска возникновения рака желудка [1, 29]. Новые системы стадирования атрофии и кишечной метаплазии в различных отделах желудка, такие как Operative Link for Gastritis Assessment (OLGA) и Operative Link on Gastric Intestinal Metaplasia Assessment (OLGIM), позволяют более подробно проанализировать индивидуальный риск рака желудка [7, 31].
Положение 5. Эрозии СОЖ должны описываться отдельно от гастрита, так как естественное течение и клинические проявления эрозивных повреждений слизистой оболочки зависят от этиологических факторов и требуют дальнейшего уточнения (класс рекомендаций: сильный; уровень доказательности: низкий).
Комментарии. Эрозии СОЖ могут быть ассоциированы с инфекцией HP, однако чаще эти дефекты бывают индуцированы приемом НПВП [15]. У таких пациентов при наличии множественных эрозий существенно возрастает риск язвенного дефекта и ассоциированных осложнений [16]. Поэтому в клиническом диагнозе эрозии СОЖ должны быть описаны вне рамок гастрита, что требует разработки классификации этих поражений с учетом их этиологических факторов и клинического течения.
Положение 6.HP-ассоциированный гастрит следует считать самостоятельным инфекционным заболеванием, даже если пациент не предъявляет жалоб и вне зависимости от наличия язвенной болезни или рака желудка (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии.Инфекция HP — наиболее распространенная бактериальная инфекция человека, приводящая к развитию хронического активного гастрита различной тяжести у всех инфицированных лиц [5]. На фоне гастрита повышается риск развития других HP-ассоциированных заболеваний, включая язвенную болезнь и злокачественные поражения желудка. Эрадикация инфекции HP приводит к регрессу воспалительного процесса в СОЖ, заживлению эрозивно-язвенных повреждений и уменьшению и/или полному нивелированию диспепсических симптомов [4, 5]. Помимо этого, ЭТ может способствовать профилактике других патологий, ассоциированных с инфекцией, включая язвенную болезнь и рак желудка. С учетом того что хронический поверхностный гастрит, ассоциированный с инфекцией HP, способен прогрессировать в более тяжелые формы гастрита, включая атрофическую (с кишечной метаплазией или без нее), увеличивающую риск рака желудка, ЭТ должна включаться в алгоритмы ведения этой группы пациентов в качестве способа канцеропревенции [1, 5, 12].
Положение 7.HP-ассоциированный гастрит является причиной явлений диспепсии у ряда пациентов (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Наиболее явный доказательный базис роли инфекции HP в генезе явлений диспепсии у ряда больных — данные клинических исследований, демонстрирующие небольшой, но статистически значимый эффект в купировании симптоматики после эрадикации микроорганизма с показателем number needed to treat, равным 8 и 14 [26, 43]. Как правило, после ЭТ нивелирование симптомов занимает по меньшей мере 6 месяцев, что, по-видимому, определено временем, необходимым для регресса воспалительных изменений в СОЖ [36]. Тем не менее на сегодняшний день нет критериев, позволяющих предсказать, будут ли купированы диспепсические симптомы у конкретного пациента после проведенной ЭТ.
Положение 8А. У HP-инфицированных пациентов с явлениями диспепсии симптомы могут быть обусловлены персистированием инфекции, в случае если ЭТ привела к длительному купированию имевшейся симптоматики (класс рекомендаций: сильный; уровень доказательности: высокий).
Положение 8В.HP-ассоциированная диспепсия является отдельной нозологической единицей (класс рекомендаций: сильный, уровень доказательности: умеренный).
Комментарии. Некоторые случаи гастрита, ассоциированного с HP, могут рассматриваться в рамках органической диспепсии, если ЭТ приводила к регрессу жалоб. Пациенты с HP-ассоциированным гастритом, у которых симптоматика продолжает персистировать, несмотря на успешную ЭТ, должны быть отнесены к группе функциональной диспепсии (ФД). Стабильный регресс симптоматики после ЭТ позволяет рассматривать инфекцию HP как органическую причину появления симптомов диспепсии и считать HP-ассоциированную диспепсию отдельной нозологической единицей (рис. 1).
Рис. 1. Алгоритм диагностики диспепсии, ассоциированной с Helicobacter pylori
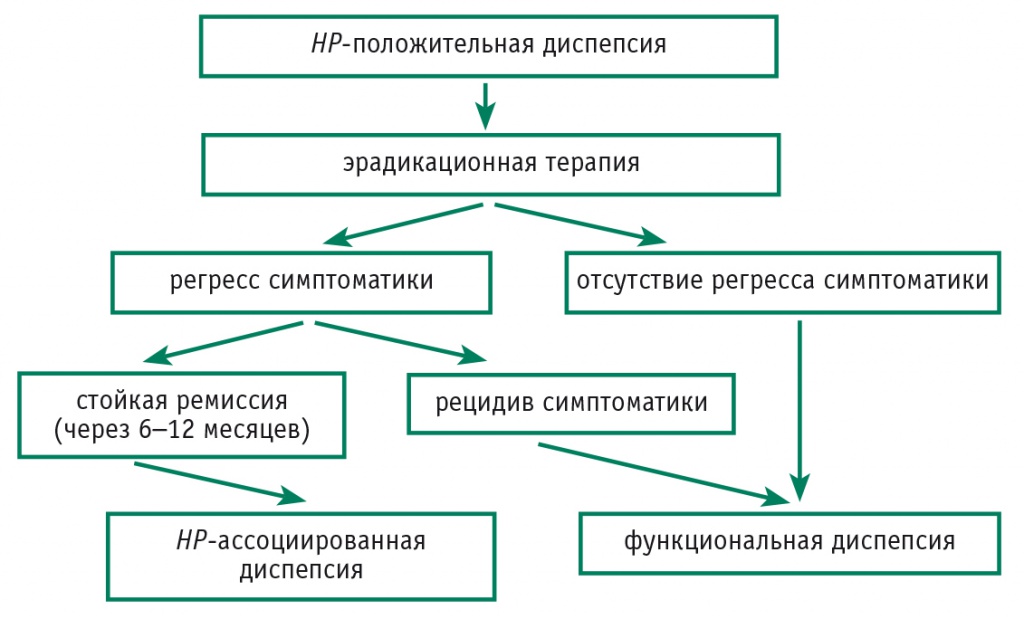
Положение 9. Эрадикация HP должна быть терапией первой линии у пациентов с HP-ассоциированной формой диспепсии (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Исходя из положения 8, существует целая когорта больных с HP-ассоциированной диспепсией, для которых инфекция HP — каузативный фактор клинических симптомов. ЭТ у таких пациентов должна купировать явления диспепсии (но не моментально). После успешной эрадикации данные больные могут быть полностью «излечены». На сегодняшний день это единственная тактика, приводящая к таким результатам, что позволяет определить ЭТ как терапию первой линии.
Положение 10. С целью купирования диспепсических симптомов ЭТ более эффективна, нежели плацебо, у пациентов с HP-ассоциированной формой диспепсии и является предпочтительным вариантом лечения (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Изучение эффективности ЭТ у HP-инфицированных пациентов с ФД продемонстрировало уменьшение диспепсических жалоб у ряда больных [21, 36]. Таким образом, даже несмотря на то что обычно после ЭТ регресс симптоматики занимает по меньшей мере 6 месяцев, данный метод должен быть предпочтительным.
Положение 11. Состояние, когда у пациента сохраняются диспепсические симптомы после успешной ЭТ, следует считать ФД (класс рекомендаций: слабый; уровень доказательности: умеренный).
Комментарии. Исходя из утверждения 8, HP-инфицированные больные с явлениями диспепсии, но без макроскопических изменений слизистой оболочки (по результатам эндоскопического исследования), у которых отмечен регресс симптоматики после ЭТ, страдают именно от HP-ассоциированной диспепсии. Напротив, если при успешной ЭТ симптоматика не уменьшается, это позволяет сделать вывод, что HP-ассоциированный гастрит не является причиной симптомов у таких пациентов. Соответственно, их следует отнести к страдающим ФД.
Положение 12. Атрофия СОЖ и кишечная метаплазия могут быть идентифицированы с помощью современных методов эндоскопического обследования после соответствующей подготовки персонала (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Конвенционные методы эндоскопии не являются адекватным инструментом для идентификации атрофии и кишечной метаплазии, и требуется обязательное проведение биопсии для детальной оценки гистоморфологических изменений СОЖ по Сиднейской системе [30]. Тем не менее современные эндоскопические методики (узкоспектральная эндоскопия, эндоскопия высокого разрешения, хромоэндоскопия, лазерная конфокальная эндомикроскопия) — точные и воспроизводимые методы диагностики предраковых изменений СОЖ в руках обученного персонала [6, 38].
Положение 13. Точная гистологическая оценка гастрита требует взятия биоптатов слизистой как из тела, так и из антрального отдела желудка (класс рекомендаций: сильный; уровень доказательности: высокий).
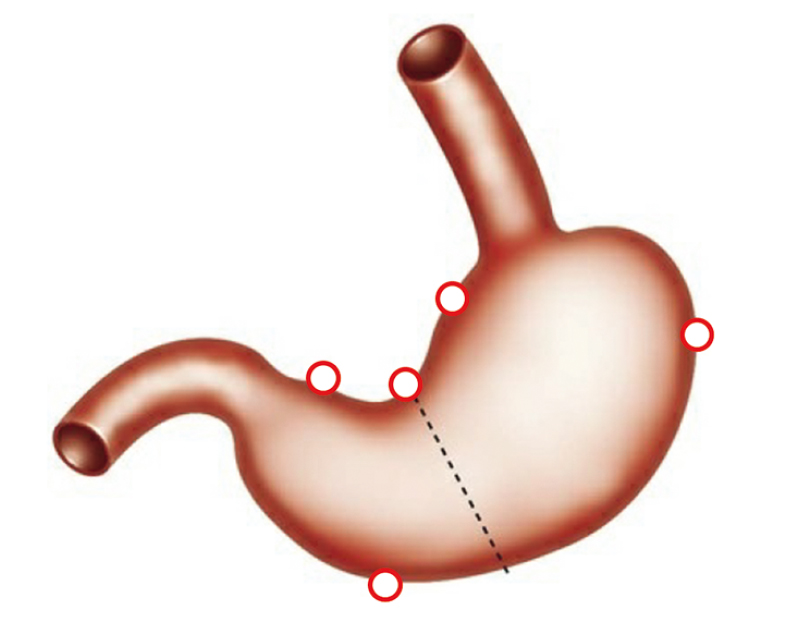
Комментарии. Для детальной гистологической оценки гистоморфологических изменений СОЖ необходима биопсия как из участка антрального отдела, так и из тела желудка. Данная тактика позволяет более точно оценить риск развития рака желудка. Сиднейская система рекомендует взятие биоптатов из пяти участков, к ним относятся большая и малая кривизна антрального отдела, угол, а также тело желудка по большой и малой кривизне (рис. 2) [30].
Рис. 2. Рекомендуемые участки взятия биоптатов для последующей патоморфологической оценки слизистой желудка [4]
Положение 14А. Риск рака желудка коррелирует с выраженностью и распространенностью атрофического гастрита (класс рекомендаций: сильный; уровень доказательности: высокий).
Положение 14В. Системы гистологического стадирования OLGA и OLGIM позволяют стратифицировать риск рака желудка (класс рекомендаций: сильный; уровень доказательности: низкий).
Комментарии. Рак желудка развивается в рамках многоэтапного пути канцерогенеза, известного как каскад P. Correa. Эта модель предполагает, что существует временна́я последовательность предраковых изменений, которые в конечном счете приводят к возникновению рака желудка [1, 9]. У пациентов, инфицированных HP, воспалительный процесс в СОЖ вызывает атрофический гастрит (потерю железистой ткани) с последующим прогрессированием в кишечную метаплазию, дисплазию, ранний рак желудка и впоследствии в распространенный рак. Согласно многочисленным исследованиям, формирование атрофического гастрита, кишечной метаплазии и дисплазии значительно увеличивает риск рака желудка. Так, в популяционном исследовании в Нидерландах, включавшем около 98 тысяч пациентов с предраковыми изменениями СОЖ, было показано, что риск развития рака желудка возрастает на 2–3% в течение 10 лет [11]. К группе максимального риска относятся пациенты с дисплазией. Патоморфологический анализ биоптатов СОЖ является высокоинформативным методом для стратификации риска рака желудка. В качестве основных методов гистологической оценки могут использоваться системы OLGA и OLGIM [32, 33]. Больные с III и IV стадиями процесса по этим стратификационным системам имеют высокий риск [31, 34].
Положение 15. Серологические тесты (пепсиноген I и II, антитела к HP) имеют значение для индивидуальной оценки риска рака желудка (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Уровень пепсиногена I ≤ 70 нг/л и соотношение пепсиноген I/пепсиноген II ≤ 3 — негативные прогностические факторы, отражающие повышенный риск рака желудка [24, 25]. У лиц с нормальными значениями пепсиногенов вне зависимости от инфицирования HP ежегодная частота прогрессирования в рак очень низка. У пациентов с нарушенными уровнями сывороточных пепсиногенов данный показатель намного выше и достигает 3,5–6 случаев на 1000 в год [40].
Положение 16. Целесообразно скрининговое обследование на HP среди молодых людей до развития атрофического гастрита и кишечной метаплазии с учетом локальных эпидемиологических данных (класс рекомендаций: сильный; уровень доказательности: умеренный).
Комментарии. ЭТ снижает риск рака желудка, однако этот эффект, как правило, достигается лишь у пациентов, у которых отсутствовали явления атрофии и метаплазии [8, 13]. У больных с данными предраковыми состояниями ЭТ приводит к регрессу воспалительных изменений СОЖ, но может не остановить дальнейшее прогрессирование в рак [10]. Исходя из этого, целесообразно проводить скрининговые мероприятия у пациентов младших и средних возрастных групп до формирования у них явлений атрофии и кишечной метаплазии. В основе такой тактики должны лежать локальные эпидемиологические данные о распространенности предраковых изменений желудка в конкретных возрастных группах [42].
Положение 17.HP-инфицированные лица должны быть подвергнуты ЭТ при отсутствии противопоказаний к ее проведению и других причин (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Потенциальные преимущества ЭТ для каждого больного включают остановку прогрессирующего повреждения СОЖ, профилактику и лечение HP-ассоциированной язвенной болезни, уменьшение риска гастроинтестинальных осложнений, связанных с терапией НПВП, снижение риска рака желудка [1, 4, 17]. Преимущества ЭТ для популяции в целом: уменьшение числа зараженных, способных передавать инфекцию, и снижение затрат здравоохранения, связанных с диагностикой и лечением HP-ассоциированных заболеваний и их осложнений [4, 5]. Таким образом, HP-инфицированные пациенты должны получать курс ЭТ, за исключением тех из них, для кого эрадикация микроорганизма на текущий момент не является приоритетной задачей (лица с конкурирующими коморбидными состояниями), а также случаев, когда локальная политика здравоохранения не предусматривает ЭТ в качестве необходимого инструмента для имплементации во всей популяции инфицированных.
Положение 18. Прогностический эффект ЭТ в рамках канцеропревенции максимален при ее проведении до развития атрофических процессов в СОЖ (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Максимальный канцеропревентивный эффект ЭТ проявляется в том случае, если она была успешно проведена до развития хронического атрофического гастрита и других предраковых состояний желудка [8, 13]. Частота рака желудка возрастает с возрастом, как и частота развития хронического атрофического гастрита. Как только процесс атрофии принимает выраженный и распространенный характер, риск развития рака желудка возрастает экспоненциально [4, 27]. Таким образом, целесообразно проводить скрининговые мероприятия и, при необходимости, назначать ЭТ с целью канцеропревенции до развития хронического атрофического гастрита.
Положение 19. Выбор протокола эрадикации инфекции HP должен основываться на локальных данных по эффективности конкретных схем ЭТ, антибиотикорезистентности и уровню потребления конкретных антибиотиков в рассматриваемой популяции. Оптимальным является подбор схемы ЭТ на основании индивидуальной чувствительности штамма (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Эффективность ЭТ зависит от распространенности антибиотикорезистентности штамма в популяции и от индивидуальных генетических особенностей пациента, связанных с метаболизмом препаратов (полиморфизмы генов CYP2C19, MDR1) и иммунным ответом (полиморфизм гена IL-1b) [3, 18]. Распространенность антибиотикорезистентности HP к основным препаратам, которые используются в схемах ЭТ, широко варьирует в мире и ассоциирована с уровнем потребления конкретных антибиотиков в регионе [5, 22]. Только схемы ЭТ с эффективностью ≥ 90% должны использоваться в качестве эмпирической терапии [14, 41].
Положение 20. Эрадикация HP уменьшает риск развития рака желудка. Степень снижения риска зависит от наличия, тяжести и распространенности атрофических процессов к моменту назначения эрадикации (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Инфекция HP является ведущей причиной развития рака желудка [1, 4, 5, 9]. Успешная эрадикация HP нивелирует основной каузативный фактор рака и тем самым снижает частоту этой неоплазии в популяции. Эффективность эрадикации HP в рамках превенции рака желудка зависит от выраженности и распространенности атрофических изменений слизистой оболочки на момент назначения ЭТ и варьирует от полного нивелирования риска у пациентов с неатрофическим гастритом до стабилизации или уменьшения риска у больных с уже сформировавшимися атрофическими изменениями [8, 13, 37]. Индивидуальный риск возникновения рака желудка может быть определен с использованием валидизированных стратификационных систем патоморфологической оценки биоптатов OLGA и OLGIM [32–34].
Положение 21. Необходим контроль эффективности назначенной схемы ЭТ, предпочтение должно отдаваться неинвазивным тестам (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. С учетом того что частота неудачи при назначении ЭТ достаточно высока, в каждом индивидуальном случае необходим контроль успешности эрадикации [3, 5]. Предпочтение следует отдавать неинвазивным тестам, таким как уреазный дыхательный тест или ИФА кала на антиген HP [5, 19]. У пациентов, которым требуется динамическое эндоскопическое наблюдение (например, после эндоскопического удаления аденомы желудка), контроль эффективности ЭТ может проводиться путем гистологической оценки биоптата.
Положение 22. Эрадикация HP не может полностью элиминировать риск развития рака желудка. Пациенты с выраженными и распространенными явлениями атрофии СОЖ остаются в группе риска. Для этой когорты целесообразно длительное динамическое наблюдение с регулярной эндоскопической и гистологической оценкой (класс рекомендаций: сильный; уровень доказательности: высокий).
Комментарии. Пациентам, у которых инфекция HP была диагностирована неинвазивным путем (уреазный дыхательный тест или ИФА кала), может потребоваться дополнительная гистологическая оценка биоптата для индивидуальной стратификации риска рака желудка. К ним относятся лица старших возрастных групп, у которых возрастает вероятность атрофических изменений СОЖ, а также пациенты с отягощенным анамнезом по язвенной болезни желудка и те, у кого уровень пепсиногена I ≤ 70 нг/л и соотношение пепсиноген I/пепсиноген II ≤ 3. У таких больных высок риск развития рака желудка, они нуждаются в длительном наблюдении и регулярных эндоскопических обследованиях [1, 4, 24, 25].
ЗАКЛЮЧЕНИЕ
В целом Киотский консенсус по проблеме хронического гастрита стал своеобразным рубежом, который, с одной стороны, подвел итоги многолетних исследований по данному распространенному страданию, а с другой — очертил круг важных задач, требующих решения сегодня, и наметил отчетливые перспективы дальнейшего движения. Самым главным, стратегическим, направлением в настоящее время является канцеропревенция, а среди способов ее обеспечения приоритет имеет преодоление резистентности пилорического хеликобактера как основной причины гастрита и его грозного осложнения — рака желудка. Немаловажно и то, что наконец четко определен алгоритм дифференциации органической (ассоциированной с Helicobacter pylori) и функциональной диспепсии, позволяющий в реальной практике применять конкретные методы лечения, адекватные характеру патологического процесса.








