Одной из наиболее актуальных проблем в гнойной хирургии является распространенный гнойный перитонит, осложненный тяжелым абдоминальным сепсисом. Трудности в лечении связаны с общими витальными нарушениями со стороны жизненно важных органов, приводящими к повышению летальности, и местными гнойно-некротическими процессами[2, 7, 4, 8].
По современным представлениям, тяжелый абдоминальный сепсис характеризуется совокупностью процессов эндотоксикоза и синдрома полиорганной недостаточности. Полиорганная недостаточность (ПОН) представляет собой тяжелый вид патологии, который развивается в силу различных этиологических факторов, но является самостоятельной нозологической формой с присущими ей общими чертами и не зависит в дальнейшем своем течении от этиологии. Это патологическое состояние может усугубляться до септического шока либо регрессировать до сепсиса и обратно[3, 6, 9].
Ведущее место в комплексном лечении этой тяжелой патологии занимает санация брюшной полости[1, 7, 13].
Отмечают рост релапаротомий, что связано с изменением структуры и тяжести ургентных хирургических заболеваний, в первую очередь за счет возрастания значимости распространенного перитонита. Изменились показания к релапаротомиям, увеличивается удельный вес программируемых вмешательств. Показания к повторным лапаротомиям по требованию возникают в связи с прогрессированием интраабдоминального воспалительного процесса или его осложнениями[10].
Основными причинами летальных исходов при перитоните являются эндогенная интоксикация и развитие ПОН. На рост летальности влияют поздняя госпитализация, увеличение числа пациентов с онкологическими заболеваниями, больных пожилого возраста, истощенных пациентов и другие факторы. Особый вклад вносит появление высоковирулентной микрофлоры, резистентной к антибактериальным препаратам[11, 12].
В микробных ассоциациях при гнойных перитонитах ведущее место занимает кишечная палочка. Важную роль играют возбудители нозокомиальных инфекций: Pseudomonas aeruginosa, Staphylococcus aureus, и особенно Methicillin-resistant St. aureus (MRSA). В патогенезе распространенного гнойного перитонита важнейшую роль играют продолжительность контаминации (скорость элиминации возбудителей из очага) и правильный выбор антибактериальных препаратов[5, 14].
Важнейшее значение в комплексном лечении этой грозной патологии принадлежит санации брюшной полости, выбору эффективных методов хирургической обработки раневой поверхности.
Цель исследования: изучить клиническую эффективность ультразвуковой кавитации и применения токов высокой частоты с аргоновым усилением при местном лечении больных распространенным гнойным перитонитом и провести сравнительную оценку результатов лечения без дополнительных методов хирургической обработки раневой поверхности.
Задачи исследования
- Оценить клиническую эффективность применения ультразвуковой кавитации и токов высокой частоты с аргоновым усилением для местного лечения раневой инфекции при распространенном гнойном перитоните.
- Провести сравнительный анализ эффективности лечения без применения дополнительных методов местного лечения у аналогичной группы больных.
МАТЕРИАЛЫ И МЕТОДЫ
Работа выполнена в клинике кафедры хирургических болезней факультета повышения квалификации и профессиональной подготовки специалистов Уральского государственного медицинского университета (заведующий кафедрой — д. м. н., профессор М. И. Прудков) на базе ГБУЗ Свердловской области «Свердловская областная клиническая больница № 1» (далее — ГБУЗ СО СОКБ № 1; главный врач — д. м. н., профессор Ф. И. Бадаев).
Пациенты по способу лечения были распределены на две группы. В первую вошли 15 больных распространенным фибринозно-гнойным перитонитом, осложненным тяжелым абдоминальным сепсисом, которым проводили комплексное лечение, санации брюшной полости без использования дополнительных методов хирургической обработки раневой поверхности передней брюшной стенки и брюшной полости (группа сравнения). Во вторую группу включили 15 пациентов с аналогичной патологией, которым проводили комплексное лечение, включая дополнительные методы хирургической обработки. При хирургической обработке для санации гнойной раны передней брюшной стенки применяли струю аргоновой плазмы, создавали тонкий слой струпа монополярным, бесконтактным методом воздействия с использованием аппарата «Фотек ЕА142» в режиме «Фульгур» (ООО «Фотек», г. Екатеринбург) и затем осуществляли некрэктомию электродом-ножом с попутной коагуляцией тканей высокочастотным электрическим током (режим «Смесь»). Производили также ультразвуковую кавитацию брюшной полости с целью повышения эффективности очищения раны от гнойно-некротических масс кавитационным аппаратом «Фотек АК100» (ООО «Фотек», г. Екатеринбург).
В исследовании приняли участие 16 (53,3%) мужчин и 14 (46,7%) женщин. Средний возраст больных в первой группе составил 45,8 ± 13,7 года, во второй — 43,9 ± 15,1 года. Различий по возрасту не выявлено (p > 0,1). Бо́льшая часть больных была работоспособного возраста. Сроки поступления пациентов (сутки от начала заболевания): в первой группе — на 13,4 (95%-й ДИ: 12,5–14,3), во второй — на 12,1 (95%-й ДИ: 11,2–13,0). Сроки от первой операции (количество суток): в первой группе — 7,6 (95%-й ДИ: 7,5–7,7), во второй — 7,5 (95%-й ДИ: 7,4–7,6].
Группы были сопоставимы по половым, возрастным показателям, тяжести и давности начала заболевания.
До поступления в отделение гнойной хирургии все пациенты были ранее оперированы в стационаре по месту жительства или в других отделениях многопрофильной больницы ГБУЗ СО СОКБ № 1.
У пациентов в исследуемых группах отмечали, как правило, по два сопутствующих заболевания. В целом структура таковых была сходной в обеих группах.
Критерием включения в исследование служило наличие у пациента распространенного гнойного перитонита, осложненного тяжелым абдоминальным сепсисом, развившимся вследствие острых хирургических заболеваний органов брюшной полости.
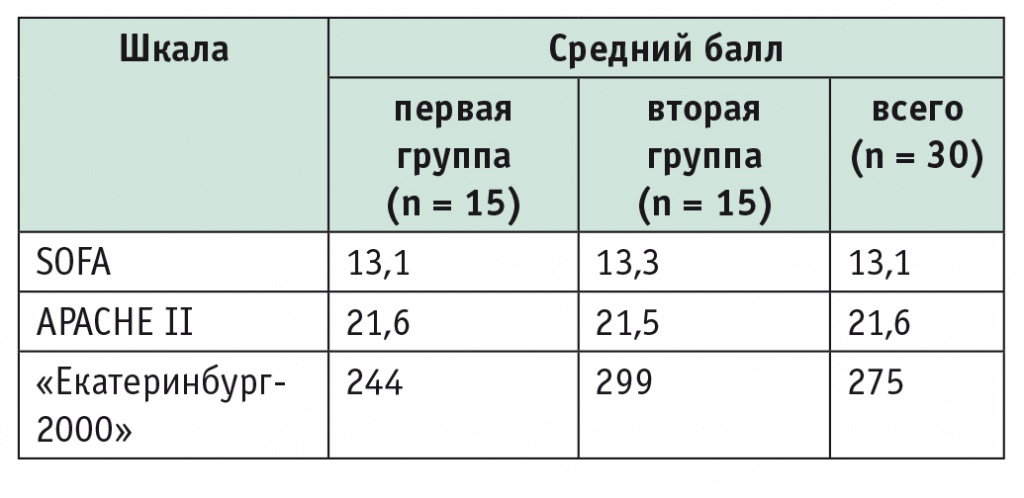
Больным проводили УЗИ в динамике, фиброгастродуоденоскопию, КТ. При поступлении больным выполняли комплексную клинико-лабораторную диагностику. Тяжесть состояния больных в день поступления оценивали по шкалам «Екатеринбург-2000», SOFA (Sepsis-related Organ Failure), APACHE II (Acute Physiology And Chronic Health Evaluation II). Состояние всех больных было оценено как тяжелое с ПОН. Риск летального исхода в сравниваемых группах не различался, что подтверждает сопоставимость групп по данному прогностическому признаку (p > 0,1).
Оценка исходного состояния больных в баллах представлена в таблице 1.
Таблица 1
Оценка исходного состояния больных в баллах
Оценку тяжести перитонита проводили по величине Мангеймского индекса перитонита (МИП). Он предусматривает выделение трех степеней тяжести перитонита на основании балльной оценки присутствующих у пациентов факторов риска (ФР). Для первой степени тяжести величина МИП составляет менее 20 баллов, для второй — от 20 до 30, а для третьей — более 30 баллов. Сопоставление ФР и балльной шкалы отражено в таблице 2.
Таблица 2
Мангеймский индекс перитонита
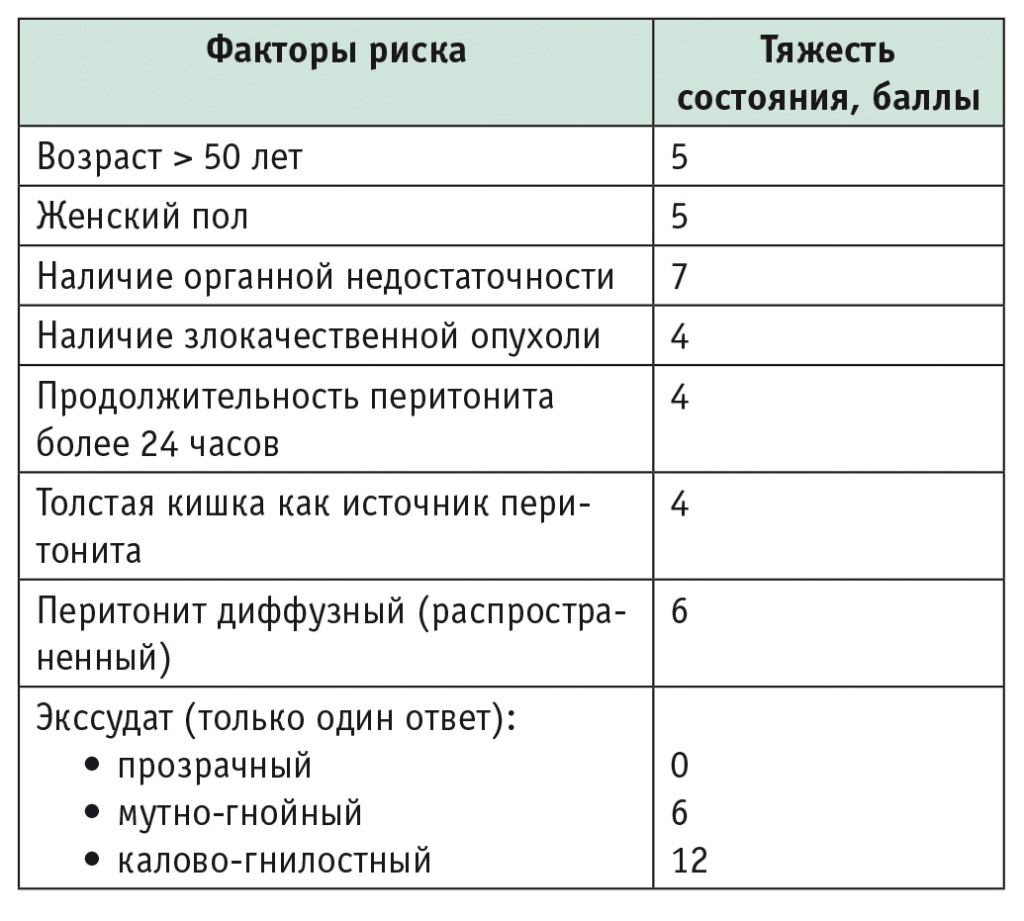
По критериям МИП степень тяжести состояния пациентов и вероятность летального исхода были высокими. В первой группе МИП составил 31 ± 7 баллов, во второй — 31 ± 6 баллов. Степень тяжести перитонита в сравниваемых группах не различалась.
Микробиологические методы исследования отделяемого раневой поверхности проведены у всех пациентов. В разработку включены результаты посевов отделяемого брюшной полости до начала лечения и на 3–5-е сутки от начала лечения. При поступлении высеяны ассоциации микроорганизмов. Ведущими из них при первом посеве у пациентов обеих групп являлись St. аureus (в первой группе в 13,3%, во второй — в 26,7% случаев), St. аureus в сочетании с MRSA высевался в обеих группах в 6,7% случаев.
Enterococcus faecalis в первой группе обнаруживали в 20%, во второй — в 26,7% случаев; Acinetobacter baumannii в первой группе не высевали, во второй высевали в 6,7% случаев; Pseudomonas aeruginosa выявляли у 13,3 и 6,7% пациентов соответственно; Escherichia coli высевали в 40,0 и 53,3% случаев и Klebsiella spp. — у 13,3 и 6,7% пациентов соответственно.
Комплексная консервативная терапия включала следующие основные направления: интенсивную терапию, проведение мониторинга органных дисфункций с последующей коррекцией выявленных нарушений, лечение ПОН, антибактериальную терапию. В комплекс лечения были также включены антибиотики широкого спектра действия (цефалоспорины III и IV поколений, карбапенемы, глицилциклины, фторхинолоны в комбинации с метронидазолом, оксазолидиноны) и парентеральное питание.
Всем больным выполнено оперативное вмешательство. Проведена срединная лапаротомия, обеспечивающая возможность полноценной ревизии и санации всей брюшной полости. Патологическое содержимое удаляли и осушали брюшную полость. Затем ее промывали 0,02%-ным водным раствором хлоргексидина и физиологическим раствором до «чистых вод». В среднем на санацию уходило 5–7 литров жидкости.
После первичной санации брюшной полости на переднебоковой части брюшной стенки справа и слева на середине расстояния между свободным концом 12-го ребра и гребнем подвздошной кости выполняли по одному поперечному мини-разрезу длиной 3–4 см через все слои брюшной стенки.
На передней брюшной стенке (в местах традиционной установки дренажей) выполняли 2–4 (в зависимости от наличия или отсутствия у больного сформированных стом) косопоперечных мини-разреза брюшной стенки длиной 3–4 см (в правом и левом подреберьях, правой и левой подвздошных областях). В каждый мини-разрез устанавливали плоский дренаж шириной 3–4 см. Через эти разрезы дренировались правое и левое поддиафрагмальные пространства, подпеченочное пространство, боковые каналы, полость малого таза, межпетлевые пространства и область, прилегающая к срединной ране. После установки дренажей укладывали петли кишечника, на них помещали большой сальник (при его наличии) и закрывали перфорированной пленкой или атравматической сеткой (сетчатая структура предотвращает прилипание пленки (сетки) к кишечнику, раневым поверхностям и салфеткам, способствует абсорбции жидкости из брюшной полости). Пленку (сетку) многослойно обкладывали салфетками, брюшную полость оставляли открытой (проводили открытое дренирование брюшной полости через срединный доступ брюшной стенки), гнойные края раны изолировали от брюшной полости дополнительными салфетками. Последующие санации проводили через срединную лапаротомную рану с интервалом в 24 часа, с промыванием всей брюшной полости и заменой салфеток, пленки (сетки) и дренажей.
При полном очищении краев срединной раны и снижении внутрибрюшного давления (обычно после 2–3 плановых санаций) срединную лапаротомную рану послойно ушивали (рис.).
Рис. Послойно ушитая рана передней брюшной стенки после нескольких санаций брюшной полости по поводу разлитого фибринозно-гнойного перитонита, осложненного тяжелым абдоминальным сепсисом. (фото из личной практики Ф. В. Галимзянова)
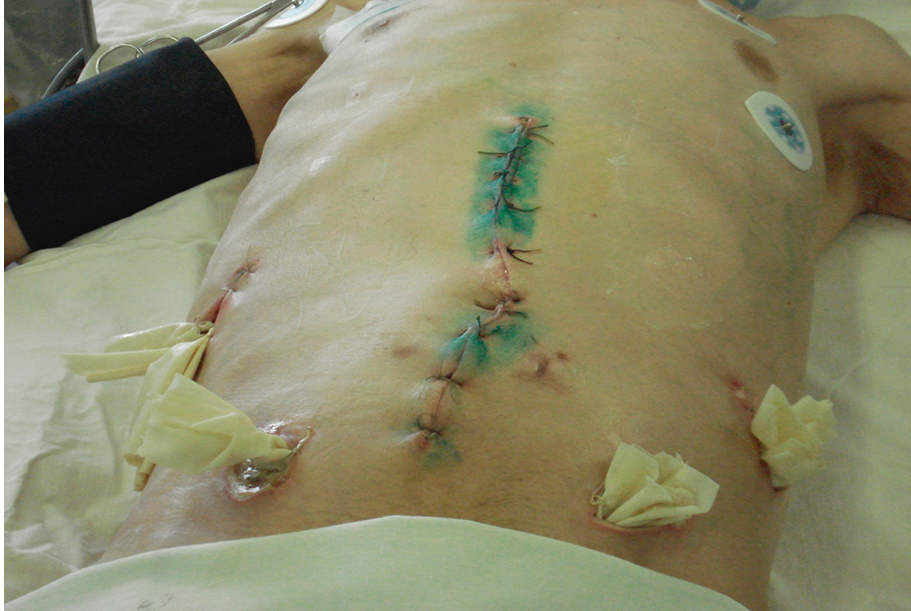
Это позволяло активизировать больного, что улучшало дренирование брюшной полости. Дальнейшие санации проводили через мини-лапаротомные разрезы раздельно по областям брюшной полости.
Санации проводили через каждые 24–48 часов. При ликвидации явлений перитонита и гнойного отделяемого в какой-либо области брюшной полости ее санацию прекращали и переходили к санированию остальных областей. После полной ликвидации перитонита и гнойного отделяемого санации прекращали. Дренажи оставляли в мини-разрезах до прекращения выделения из брюшной полости серозного содержимого (обычно на 2–3 дня), затем их удаляли. Заживление мини-лапаротомных ран, остававшихся после извлечения дренажей, происходило путем вторичного натяжения.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В обеих группах происходило купирование гнойно-воспалительных явлений в ране, причем во 2-й группе — в более ранние сроки.
Органную недостаточность во второй группе пациентов купировали в более ранние сроки. Так, в группе, где санации брюшной полости осуществляли без дополнительных методов хирургической обработки раневой поверхности, после начала лечения отмечены нарастание органной недостаточности и ее продолжительная (до 7 суток) высокая выраженность. Снижение органной недостаточности документировалось лишь к 8-м суткам.
В группе больных, где использовали ультразвуковую кавитацию и применяли токи высокой частоты с аргоновым усилением при санациях, тяжесть недостаточности эффективно снижалась уже к 5-м суткам. Данный феномен, по-нашему мнению, связан с заселением брюшной полости у пациентов первой группы госпитальными возбудителями. У пациентов, лечившихся с применением дополнительных методов хирургической обработки раневой поверхности, госпитальная микрофлора высевалась в 2,9 раза реже.
Результаты исследования посевов показали, что на 4–5-е сутки от начала лечения в первой группе произошло увеличение доли госпитальных возбудителей, обладающих высокой резистентностью. Так, Ps. аeruginosa, St. aureus выделены у 19 и 20% больных соответственно, Kl. pneumoniae и Ent. faecium — у 20% пациентов. У 21% больных микрофлоры не обнаружено.
Во второй группе у 6% больных выделены Candida spp., в 11% случаев обнаруживали St. aureus и St. epidermidis, у 6% пациентов выявлены Ps. aeruginosa и Citrobacter youngae. У 61% больных, которым санации брюшной полости проводили с применением ультразвуковой кавитации и токов высокой частоты с аргоновым усилением, микрофлоры не обнаружено.
Температурную реакцию во второй группе купировали быстрее и в более ранние сроки, чем в первой группе больных. В последней очищение срединной послеоперационной раны наступило на 5–11-й день. Во второй группе — на 3–7-й день. Средние сроки пребывания в стационаре составили соответственно 25 и 24 дня.
Средние сроки стационарного лечения в обеих группах были одинаковы и связаны с исходной тяжестью состояния.
ЗАКЛЮЧЕНИЕ
- При применении ультразвуковой кавитации и токов высокой частоты с аргоновым усилением для местного лечения раневой инфекции при распространенном гнойном перитоните купирование воспалительных явлений происходит в более короткие сроки, чем при санациях брюшной полости без дополнительных методов хирургической обработки раневой поверхности.
- Использование ультразвуковой кавитации и токов высокой частоты с аргоновым усилением для местного лечения раневой инфекции при распространенном гнойном перитоните способствует более эффективному снижению микробной контаминации раневой поверхности, замедлению роста госпитальных и резистентных штаммов микроорганизмов.
- Включение ультразвуковой кавитации и токов высокой частоты с аргоновым усилением для местного лечения раневой инфекции при распространенном гнойном перитоните в комплексную программу санаций брюшной полости способствует ускорению ликвидации органной недостаточности.








