За последние два десятилетия все больше внимания уделяется редкой клинической нозологии — аутоиммунным заболеваниям печени [1].
Аутоиммунный гепатит (АИГ) — это необратимое хроническое заболевание печени, которое чаще встречается у женщин и характеризуется гипергаммаглобулинемией, даже при отсутствии цирроза печени, наличием циркулирующих аутоантител, ассоциации с человеческими антигенами лейкоцита (HLA) DR3 или DR4, интерфейса гепатита при гистологическом исследовании и положительным ответом на иммуносупрессивную терапию [2].
В 1950-х гг. шведский врач Jan Waldenström первым опубликовал данные о новом хроническом гепатите у молодых женщин, страдающих от тяжелой формы персистирующего гепатита, связанного с угревой сыпью и стриями на коже, сосудистыми звездочками, артралгиями, ановуляторной аменореей и повышением уровней иммуноглобулинов в сыворотке крови и скоплением плазматических клеток в печени [3].
В исследованиях пациентов с «HbsAg-негативным гепатитом», проведенных в начале 1960-х гг., сообщалось о хорошем ответе на лечение стероидами [4-6]. В последующие годы АИГ был признан отдельной клинической формой, которую назвали «хроническим активным аутоиммунным гепатитом». Этот термин использовался вплоть до конца 1980-х гг. После двух международных рабочих встреч групп по изучению АИГ (International Autoimmune Hepatitis Group), состоявшихся в 1992 г. (Брайтон, Великобритания) и в 1994 г. (Лос-Анджелес, США), он был заменен на термин «аутоиммунный гепатит». Данные изменения были сделаны на основании того, что заболевание часто характеризовалось волнообразным течением с периодами лекарственной или спонтанной ремиссии и, как следствие, не протекало активно [7].
Позднее было описано, что у пациентов с АИГ могут быть выявлены клинические, биохимические, серологические и/или гистологические особенности холестатических заболеваний печени: первичного билиарного холангита (ПБХ) или первичного склерозирующего холангита (ПСХ) [2].
ЭПИДЕМИОЛОГИЯ АУТОИММУННОГО ГЕПАТИТА
АИГ считается редким заболеванием, так, в Европе его частота составляет 11,6-18,3 на 100 000 населения [8, 9]. В недавних эпидемиологических исследованиях показано преобладание женщин среди пациентов с АИГ (80%) [10, 11]. Распределение возраста считается бимодальным, с пиками во время полового созревания и между четвертой и шестой декадами жизни [12].
Больные АИГ в 42,9 случаев на 100 000 и 24,5 случаев на 100 000 жителей были уроженцами Аляски и Новой Зеландии [2]. В Дании распространенность АИГ в период с 1994 по 2012 г. составляла 1721 на 100 000 населения [2].
КЛИНИЧЕСКАЯ КАРТИНА АУТОИММУННОГО ГЕПАТИТА
Для дебюта АИГ характерны клинические варианты поражения печени от бессимптомного течения заболевания до фульминантного. До 25% пациентов могут иметь бессимптомное течение болезни [13]. Неспецифические жалобы чаще встречаются у женщин молодого или среднего возраста [14]. У части пациентов выявлено бессимптомное повышение уровней АЛТ, АСТ. Иногда обнаруживаются признаки внутрипеченочного холестаза (увеличение содержания щелочной фосфатазы, гамма-глютамилтранспептидазы), неспецифические симптомы заболевания (усталость, тошнота, боли в животе и артралгии), которые диагностируются после случайной находки в изменениях функциональных проб печени [15-18].
У 30% больных дебют заболевания проявляется остро с желтухи, развернутой печеночно-клеточной недостаточности, без предвестников заболевания печени. У трети пациентов при первичном обращении АИГ устанавливается на стадии цирроза печени, с синдромом портальной гипертензии, желудочно-кишечного кровотечения, что указывает на то, что болезнь протекает длительное время бессимптомно (табл. 1).
Таблица 1
Клинические проявления аутоиммунного гепатита (АИГ) [2]

Вариантные формы различных заболеваний печени аутоиммунной этиологии (АИГ, ПБХ, ПСХ) называют синдромом перекреста. Обсуждаются их патофизиологические механизмы: случайное совпадение двух независимых аутоиммунных заболеваний или наличие у одного пациента одновременно двух аутоиммунных заболеваний [2, 19-21]. Сопутствующее заболевание печени усложняет диагностику и лечение АИГ [2].
СОПУТСТВУЮЩИЕ АУТОИММУННЫЕ ЗАБОЛЕВАНИЯ
Кроме поражения печени аутоиммунного генеза, у пациента могут наблюдаться сопутствующие аутоиммунные заболевания [22] — аутоиммунный тиреоидит, ревматоидный артрит, системная красная волчанка и др. (до 25% случаев) [9]. Развитие нескольких заболеваний аутоиммунной этиологии у одного пациента пытаются объяснить мозаичностью аутоиммунитета, хотя генетический потенциал или иммунологические механизмы этого явления до сих пор до конца не изучены [23].
Так, в исследовании C. Efe и соавт. [23] ассоциативных заболеваний у пациентов с синдромом перекреста на стадии цирроза печени выявлено, что 56,4% участников имели два, 32,3% — три, 11,3% — четыре аутоиммунных заболевания одновременно. В 18,3% случаев (наиболее часто) встречались аутоиммунные болезни щитовидной железы. Были также диагностированы синдром Шегрена, целиакия, псориаз, ревматоидный артрит, витилиго, системная красная волчанка [23].
ДИАГНОСТИКА АУТОИММУННОГО ГЕПАТИТА
Диагностика АИГ представляет значительные трудности. Необходимо исключить вирусные гепатиты В и С, алкоголь-ассоциированные и лекарственные поражения печени. Нередко АИГ является диагнозом исключения. Он выставляется в соответствии с диагностическими критериями American Association for the Study of Liver Diseases (AASLD) (2010) [24], клиническими рекомендациями European Association for the Study of the Liver (EASL) (2015) [2] и клиническими рекомендациям по диагностике и лечению АИГ (2013) [25].
Лабораторные исследования
Из лабораторных изменений для АИГ наиболее характерны гипергаммаглобулинемия и повышение содержания сывороточного IgG. Уровень IgG используют для мониторинга ответа на лечение и достижения ремиссии, он также хорошо коррелирует с гистологическим воспалением [2]. Другие биохимические отклонения неспецифичны, встречаются и при других поражениях печени [26-28]. Биохимические показатели крови способны спонтанно нормализоваться (биохимическая ремиссия), несмотря на гистологическую активность [2, 17, 18]. Такие спонтанные биохимические ремиссии могут привести к недооценке тяжести состояния печени [2].
Важная часть диагностического обследования — определение аутоантител. На основании наличия аутоантител АИГ классифицируется на тип 1 или тип 2. Около 70-80% больных АИГ имеют AНA в титре 1 : 40 или выше, или антитела к гладкой мускулатуре (SMA), или оба. Диагностический титр AНA у взрослых — 1 : 40 [2]. Антитела к микросомам печени и почек 1-го типа (анти-LKM1), иногда в титре < 1 : 40, имеют около 34%, а до 20% пациентов не имеют ни одного из них [16, 17]. Наличие антител играет важную роль в диагностике и классификации АИГ [13, 27].
Классификация аутоиммунного гепатита [2]
АИГ-1 (почти 90% всех случаев АИГ). Для него характерны выявление антинуклеарных антител (ANA), SMA или антител к растворимому антигену печени и печеночно-панкреатическому антигену (анти-SLA/LP); ассоциация с HLA DR3, DR4 и DR13; начало заболевания в любом возрасте. Лечение редко бывает неудачным, но требуется длительная поддерживающая терапия (высок риск рецидива после отмены препаратов).
АИГ-2 (около 10% всех случаев АИГ): обнаружение анти-LKM1, антител к цитозольному антигену печени 1-го типа (анти-LC1) и редко — антител к микросомам печени и почек 3-го типа (анти-LKM3); ассоциация с HLA DR3 и DR7; начало, как правило, в детском и юношеском возрасте; большой процент острых форм с высокой степенью тяжести. Часто отмечается неудача лечения с рецидивом после отмены поддерживающей терапии.
АИГ-3 характеризуется наличием анти-SLA/LP. Он очень схож с АИГ-1; часто определяется анти-Ro52. Характеризуется более тяжелым течением (табл. 2).
Таблица 2
Упрощенная система балльной оценки аутоиммунного гепатита (АИГ) (2008) [2]
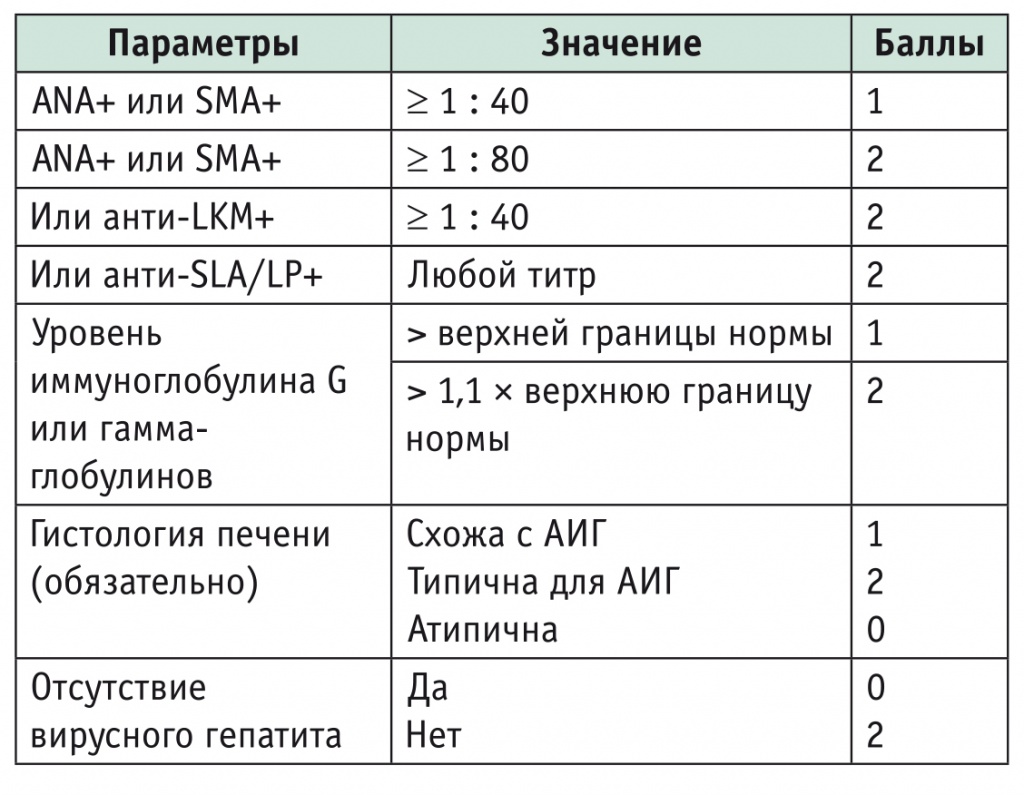
Примечание: определенный АИГ ≥ 7 баллов, вероятный АИГ ≥ 6 баллов.
Биопсия печени остается «золотым стандартом» диагностики АИГ, хотя патогномоничных поражений, специфичных для АИГ, нет, наиболее характерным является перицентральный некроз [2]. По данным рекомендаций AASLD [24], гистологическая картина может быть разнообразной: в виде интерфейса гепатита умеренной или тяжелой активности, без лобулярного гепатита, встречаются центролобулярные (в 3-й зоне ацинуса) повреждения, но без поражений билиарной системы [24]. К типичным признакам также относят лимфоплазмацитарную инфильтрацию, формирование гепатоциллюлярной розетки, эмпериполез, отек гепатоцитов и/или пикнотический некроз гепатоцитов [2, 29]. В инфильтрате могут присутствовать эозинофилы; наблюдаются ступенчатые, мостовидные, мультилобулярные некрозы.
В случае острого дебюта отсутствие гистологических данных не должно быть препятствием для начала терапии [30]. У трети пациентов при диагностике АИГ отмечается цирроз печени [29]. Помимо диагностики, результаты биопсии используются для определения тактики лечения [2] (табл. 3).
Таблица 3
Суммарные критерии аутоиммунного гепатита (АИГ), предложенные в 1999 г. Международной группой по изучению АИГ [2]
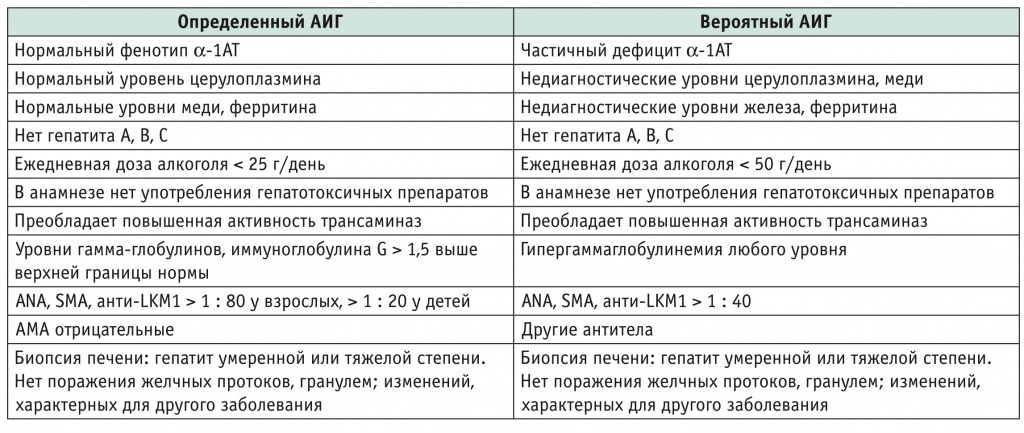
ЛЕЧЕНИЕ АУТОИММУННОГО ГЕПАТИТА
Целями лечения АИГ являются полная ремиссия и предотвращение дальнейшего прогрессирования заболевания печени. Показания к иммуносупрессивной терапии приведены в международных рекомендациях по АИГ AASLD (2010) [24] (табл. 4).
Таблица 4
Показания к иммуносупрессивной терапии аутоиммунного гепатита [24]
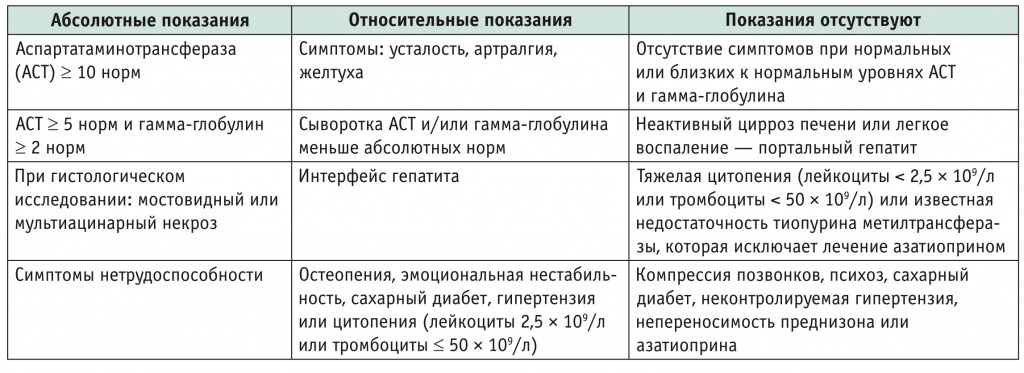
Препаратами выбора базисной терапии служат преднизолон или метилпреднизолон [25]. В качестве средства начальной терапии используют преднизолон. Его стартовая доза должна быть от 0,5 до 1 мг/кг/сутки. Более высокие начальные дозы могут вызывать более быструю ремиссию, но возможны побочные эффекты приема кортикостероидов [2]. Приблизительно 13% пациентов прерывают базисную терапии из-за побочных влияний преднизолона, из них почти 50% — из-за косметических проблем [1].
Азатиоприн, производное 6-меркаптопурина, добавляют к терапии кортикостероидами с целью повышения эффективности иммуносупрессии и уменьшения их доз. Азатиоприн обладает антипролиферативной активностью [25]. Он может быть инициирован всякий раз, когда уровень билирубина станет ниже 6 мг/дл (100 µмол/л), рекомендован после 2 недель от начала терапии стероидами. Начальная доза должна быть 50 мг/сутки, увеличение поддерживающей дозы возможно до 1-2 мг/кг/сутки [2]. Повышение дозы азатиоприна до 150 мг в сутки не сопровождается существенным увеличением частоты побочных эффектов [25]. Самый частый из них — панцитопения [1]. В связи с этим рекомендован контроль лейкоформулы через 2-3 недели.
Известно, что гистологическая ремиссия АИГ отстает от биохимической на 3-8 месяцев [1], поэтому отмена иммуносупрессоров обязательно должна сопровождаться морфологической оценкой ремиссии АИГ [25].
К средствам альтернативной терапии относится будесонид. Будесонид является синтетическим глюкокортикостероидом со скоростью печеночного метаболизма первого прохождения 80-90%. Препарат метаболизируется в печени с помощью продуктов, которые обладают незначительной глюкокортикоидной активностью, но выраженным сродством к глюкокортикоидным рецепторам [31]. При пероральном приеме препарат на 90% задерживается печенью, где в высоких концентрациях воздействует на патогенные лимфоциты [25].
Существуют схемы иммуносупрессивной терапии в соответствии с международными рекомендациями по АИГ AASLD (2010) [24] и EASL (2015) [2], которые содержат некоторые различия в дозах азатиоприна. В рекомендациях AASLD [24] представлены абсолютные показания для иммуносупрессивной терапии. При тяжелом течении АИГ одинаково эффективно использование двух схем. Монотерпия преднизолоном (60 мг ежедневно) или более низкая доза преднизона (30 мг) совместно с азатиоприном в дозе 50 мг ежедневно (табл. 5).
Таблица 5
Схемы иммуносупрессивной терапии взрослых при аутоиммунном гепатите [24]
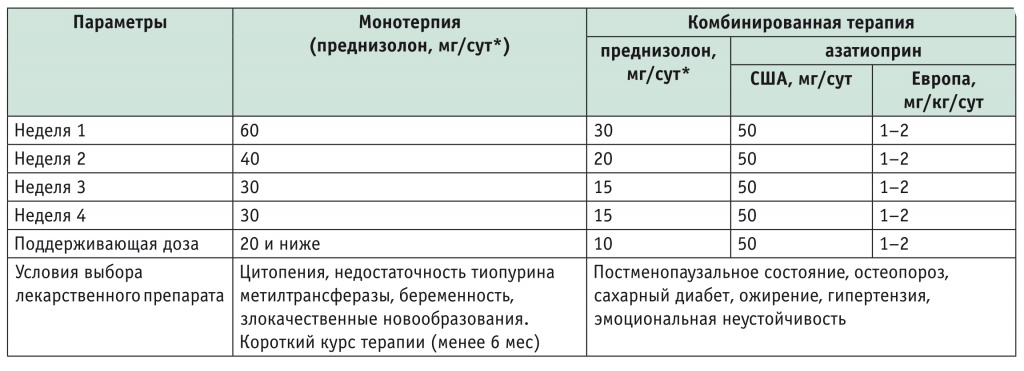
* Преднизолон можно использовать вместо преднизона в эквивалентных дозах.
Возможно уменьшение дозы преднизолона до 20 мг/сутки, ее достаточно для поддержания ремиссии. Дозу преднизолона следует снижать на 5 мг каждую неделю до достижения 10 мг/сутки, а затем по 2,5 мг еженедельно до 5 мг/сутки.
Комбинация преднизона и азатиоприна уменьшает риск развития побочных эффектов терапии большими дозами преднизолона (преднизона) (10% против 44%). Монотерапия преднизолоном рассматривается в качестве единственного варианта у пациентов с тяжелой цитопенией (продолжительность терапии < 6 месяцев), у беременных или планирующих беременность, у лиц с некоторыми активными злокачественными новообразованиями и с недостаточностью триопурина метилтрансферазы.
Во время лечения преднизолоном пациенты должны проходить осмотр окулиста для контроля развития/прогрессирования катаракты и глаукомы, а принимающим азатиоприн в любой дозе необходимо контролировать уровни лейкоцитов и тромбоцитов из-за вероятности развития лейкопении и тромбоцитопении [24].
Микофенолата мофетил — пролекарство микофеноловой кислоты, которая является мощным необратимым ингибитором инозинмонофосфата дегидрогеназы и оказывает цитостатическое влияние на лимфоциты [1]. Действие микофенолата распространяется только на активированные Т- и В-лимфоциты, что обусловливает ограничение нежелательной системной иммуносупрессии. Дозировка — 2 г/сут [25].
K. Zachou и соавт. проспективно исследовали эффективность и безопасность микофенолата при лечении АИГ: 59,3% пациентов достигли полного ответа на проводимую терапию, но у 28,8% потом были рецидивы [32].
Циклоспорин А является ингибитором кальциневрина, который действует, связываясь в единый комплекс с циклофилином [33]. Механизм его действия определяется влиянием на Са2+-зависимую передачу внутриклеточного сигнала и следующим за этим подавлением Т-клеточного звена иммунного ответа посредством репрессии гена, кодирующего ИЛ-2. Дозировка — 2,5-5 мг/кг/сут [25]. Применение циклоспорина ограничено его нефротоксичностью [1].
Такролимус представляет собой макролидное лактоновое соединение [25]. Данный препарат обладает тем же механизмом действия, что и циклоспорин, но с бóльшим иммуносупрессивным эффектом. Такролимус ингибирует Т- и В-клетки [1, 34].
Обзор литературы показал, что такролимус имеет смысл назначать пациентам, невосприимчивым к обычной терапии, его можно использовать как вторую линию лечения АИГ. Однако у этого препарата широкий спектр побочных эффектов: нефротоксичность, АГ, токсичность для костного мозга, СД, нейротоксичность и оппортунистические инфекции [1, 35, 36].
Существуют другие альтернативные варианты терапии АИГ. Они включают назначение урсодезоксихолевой кислоты, инфликсимаба, этанерцепта, метотрексата, рапамицина и ритуксимаба, но клинических данных на сегодняшний день недостаточно для оценки эффективности и безопасности их применения [1, 25].
ТРАНСПЛАНТАЦИЯ ПЕЧЕНИ
Приблизительно у 10% больных АИГ трансплантация печени является единственным способом ликвидации непосредственной угрозы жизни. Обычно основанием для включения в лист ожидания служит появление признаков декомпенсации цирроза или кровотечение из варикозно расширенных вен пищевода [25]. Пересадка печени у пациентов с АИГ составляет приблизительно 4-6% от всех пересадок органов у взрослых в США и Европе [37]. Прогноз трансплантации благоприятный: 5-летняя выживаемость превышает 90%. Вместе с тем следует учитывать возможность рецидива, частота которого составляет в среднем 10-35% [25].
ЗАКЛЮЧЕНИЕ
Несмотря на многолетнюю осведомленность о данной аутоиммунной нозологии, аутоиммунный гепатит (АИГ) остается клинически и диагностически сложным заболеванием. Пациенты с АИГ характеризуются хорошим ответом на иммуносупрессивную терапию, но существует потребность в поиске новых препаратов для лечения, достижения морфологической и лабораторной ремиссии.








