ВВЕДЕНИЕ
Хронический панкреатит (ХП) отличается длительным течением и тяжелыми осложнениями, что в итоге существенно снижает качество жизни пациентов. В последние годы происходит смена парадигмы в понимании патологических процессов при ХП, рассматриваемых не столько с позиций клинического течения заболевания, сколько со стороны природы патофизиологических процессов, лежащих в основе ХП и обусловливающих его осложнения. Эти изменения отразились в мировом признании «механистического» определения ХП, данного D.C. Whitcomb в 2016 г. и закрепленного в рекомендациях Американской коллегии гастроэнтерологов в 2020 г. Согласно данному определению, в основе ХП лежат фиброзно-воспалительные изменения в ткани поджелудочной железы (ПЖ) [1, 2].
Фиброз ПЖ представляет собой прогрессивное накопление внеклеточных матричных протеинов в межуточном пространстве ПЖ. Прогрессирующее накопление фиброзной ткани нарушает функции органов, ухудшает регенерацию и предрасполагает к развитию рака. В случае ХП фиброз ПЖ также ухудшает секрецию и проходимость протоков, способствуя возникновению хронической боли [3].
Фиброз при ХП является, как правило, результатом некроза клеток ПЖ, а также следствием дисбаланса между синтезом и деградацией белкового межклеточного матрикса [4]. Активация панкреатических матрикс-продуцирующих звездчатых клеток (ПЗК) приводит к развитию фиброза ПЖ. Процесс активации ПЗК — это закономерная патофизиологическая реакция на повреждающий агент и может рассматриваться как этап репарации. В результате активации ПЗК меняются морфологически, становясь миофибробластоподобными клетками, и приобретают способность к продукции гладкомышечного актина α, ламинина, фибронектина (ФН), а также коллагенов I и III типов — веществ, минимально представленных в нормальной строме ПЖ [5–7].
Активация ПЗК приводит к изменениям в межклеточном матриксе, который при длительном повреждающем воздействии приобретает большое количество коллагена I типа, имеющего множество поперечных сшивок, слабопроницаемого и плохо расщепляемого протеазами [8, 9]. Помимо влияния на межклеточный матрикс, некоторые авторы описывают ремоделирующее воздействие активированных ПЗК на паренхиму ПЖ, проявляющееся в формировании регенераторных центров и тубулярных комплексов, метаплазии секреторного эпителия ацинусов в протоковый эпителий [10].
Среди веществ межклеточного матрикса отдельного упоминания заслуживает гликопротеид ФН, который синтезируется гепатоцитами и клетками ретикулоэндотелиальной системы и встречается в организме в нерастворимой форме в межклеточном матриксе и в растворимой форме в крови.
Влияние ФН многообразно и в основном реализуется через регуляцию адгезии клеток, путем связывания интегринов и активации различных сигнальных белков, что приводит к секреции клетками металлопротеиназ и стимуляции их миграции. Это проявляется в ряде физиологических и патологических процессов, включая сепсис, синдром диссеминированного внутрисосудистого свертывания, острые воспалительные заболевания и развитие злокачественных опухолей [11–13].
Изменения уровня сывороточного ФН достаточно давно привлекают внимание исследователей. G. Adler и соавт. и C.F. Bellows и соавт. в своих работах показали, что при остром панкреатите и тяжелом обострении ХП уровень ФН в сыворотке крови понижается [14, 15]. J.E. Domínguez-Muñoz и соавт. выявили отсутствие изменений сывороточной концентрации ФН у пациентов с ХП вне зависимости от длительности его течения [16]. Участие ФН в процессах воспаления и онкогенеза в ПЖ реализуется на уровне межклеточных взаимодействий, преимущественно за счет матриксной фракции ФН [13, 17].
Фиброз ПЖ описывается не только при ХП, но и при раке ПЖ. Влияние активированных ПЗК на развитие рака ПЖ осуществляется через формирование фиброза с нарастающей тканевой гипоксией, секрецией факторов роста и через другие молекулярные взаимодействия [9, 17, 18].
Таким образом, между хроническим воспалением тканей ПЖ, развитием фиброза и рака ПЖ имеются связи, реализующиеся на клеточном и молекулярно-генетическом уровнях, в том числе в дисбалансе между стимуляцией и ингибированием продукции коллагенов. Нарастание фиброза ПЖ и деградация ее паренхиматозных элементов приводят к функциональной экзокринной и эндокринной недостаточности ПЖ при ХП [7, 8, 17, 19, 20].
Кроме того, фиброз ПЖ оказывает влияние на эффективность хирургического и лекарственного лечения рака ПЖ. Фиброз ПЖ меняет структуру органа, что приводит к изменению физических качеств ПЖ и делает ее более плотной. В ряде работ показана связь между высокой плотностью ПЖ, вызванной фиброзом, и более низким риском развития панкреатической фистулы после операций на ПЖ по сравнению с так называемой «мягкой» ПЖ, при которой панкреатические фистулы и ассоциированные с ними осложнения развиваются значимо чаще [21–23].
Основным способом выявления фиброза ПЖ является морфологический метод, включающий изучение микропрепаратов и измерение плотности тканей, как описано в работе R.J. Torphy и соавт. [24]. В связи с этим возникает необходимость неинвазивного распознавания фиброза ПЖ с использованием методов лабораторной и лучевой диагностики. В настоящее время высокоспецифичные биомаркеры фиброза ПЖ отсутствуют, однако в лабораторной диагностике фиброза ПЖ внимание уделяется определению уровня металлопротеиназ плазмы крови (ММП-9), а также ряду косвенных факторов.
A. Venkateshwari и соавт. обнаружили значимое повышения уровня ММП-9, которое приводило к активации панкреатических звездчатых клеток и избыточному разрушению коллагена IV типа [25]. В работе Л.В. Винокуровой и соавт. также показана значимость изменений уровня ММП-9 у пациентов с ХП [26].
К косвенным признакам фиброза ПЖ можно отнести повышение концентрации трансформирующего ростового фактора β в сочетании с нарастанием содержания ламинина и гиалуроновой кислоты в сыворотке крови [27].
В лучевой диагностике фиброза ПЖ, опирающейся на косвенные признаки, могут быть использованы практически все методы [24, 28–30].
Как правило, мультиспиральная КТ использовалась для оценки фиброза стромы опухоли [24] или прогнозирования развития послеоперационной панкреатической фистулы [30]. ХП в связи с фиброзом рассматривался только в работе E. Bieliuniene и соавт., где панкреатический фиброз изучали в контексте развития саркопении при ХП и раке ПЖ, опираясь на КТ-волюметрию ПЖ [31].
Таким образом, существует необходимость улучшения неинвазивной диагностики панкреатического фиброза. В связи с этим нами была поставлена следующая цель: поиск новых подходов к неинвазивной диагностике фиброза ПЖ у пациентов с ХП.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включены 43 пациента с ХП различной степени тяжести, проходившие в 2019 г. обследование и лечение в ГБУЗ «МКНЦ им. А.С. Логинова ДЗМ», в возрасте от 35 до 82 лет (средний возраст — 47,8 ± 11,9 года); 27 (62,8%) мужчин и 16 (37,2%) женщин. Критериями невключения в исследуемую когорту были новообразования ПЖ, наличие портального тромбоза без реканализации тромбов, а также стенозирование артерий целиако-мезентериального бассейна свыше 10%, вызванное атеросклерозом или экстраваскулярной компрессией.
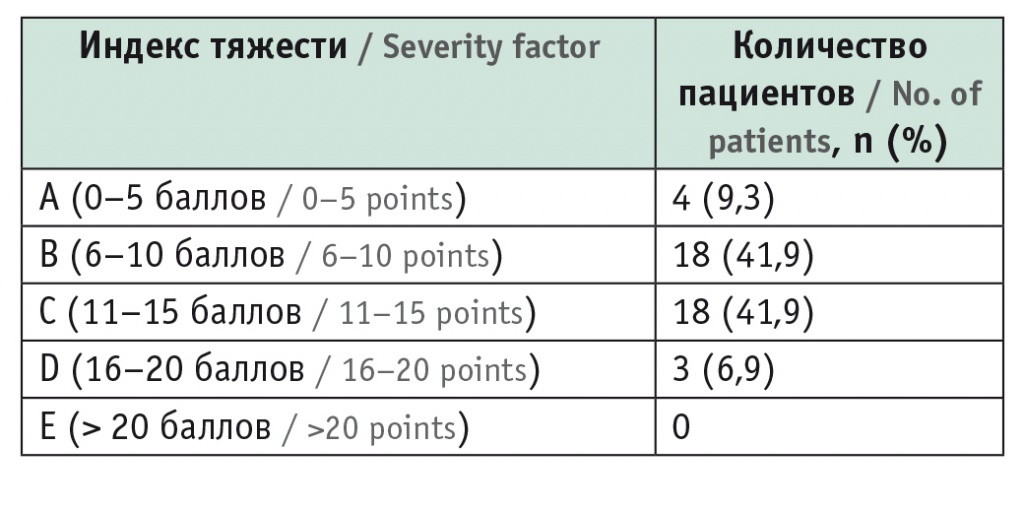
У 22 (51,2%) пациентов диагностирован кальцифицирующий ХП, у 21 (48,8%) — ХП, развившийся в исходе острого панкреатита с панкреонекрозом. Пациенты подразделялись по длительности ХП: до 5 лет — 17 (39,5%), от 6 до 10 лет включительно — 12 (27,9%) и более 11 лет — 14 (32,6%). Степень тяжести оценивали согласно классификации M-ANNHEIM, результаты распределения по тяжести представлены в таблице 1. Большинство пациентов имели индексы тяжести B и С.
Таблица 1
Распределение пациентов с хроническим панкреатитом по тяжести его течения, согласно классификации M-ANNHEIM (n = 43)
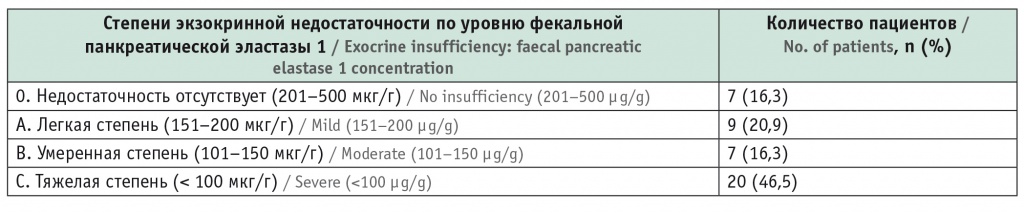
Для количественной оценки экзокринной функции ПЖ определяли уровень фекальной панкреатической эластазы 1 методом ИФА, согласно методике производителя (ScheBo, Германия). В соответствии с содержанием фекальной эластазы 1 пациенты подразделялись по тяжести экзокринной недостаточности (табл. 2). Около половины включенных в исследование имели тяжелую степень экзокринной недостаточности ПЖ — 20 (46,5%) человек.
Таблица 2
Распределение пациентов с хроническим панкреатитом по степени экзокринной недостаточности поджелудочной железы (n = 43)
Для выявления эндокринной недостаточности ПЖ проводили исследование С-пептида с помощью иммунохроматографического анализа, согласно методике производителя (Siemens, Германия).
Для изучения возможности применения уровня ФН как маркера для диагностики фиброза ПЖ определяли его концентрацию в плазме крови методом ИФА на анализаторе ChemWell с помощью реактивов фирмы Technoclone (Австрия), согласно методике производителя.
У всех пациентов выполнена мультисрезовая КТ с внутривенным болюсным контрастированием. Исследования проведены на 128-рядном компьютерном томографе Aquilion CXL 128 с алгоритмом реконструкции с толщиной среза 1 мм и шагом реконструкции 1 мм. Для внутривенного болюсного контрастирования применялись неионные рентгеноконтрастные препараты (КП) с содержанием йода 350 мг/мл. КП вводился со скоростью 3,5 мл/с в объеме до 100 мл в зависимости от массы тела пациента.
Исследования проводились по мультифазному протоколу, включающему бесконтрастное, или нативное, исследование, артериальную, позднюю артериальную, или панкреатическую, венозную и отсроченную фазы, распределение по времени было стандартным.
С целью изучения возможностей КТ для неинвазивной диагностики фиброза ПЖ при обработке полученных данных использованы подходы, основанные на методиках оценки стромы, описанных в работах R.J. Torphy и соавт., Y. Hashimoto и соавт. [24, 30]. Для этого проводилась последовательная денситометрия головки, тела и хвоста ПЖ и крови в аорте на уровне ПЖ в ограниченных участках площадью 0,2–0,8 см2. Рентгеновскую плотность измеряли в нативную, позднюю артериальную и венозную фазы. Рентгеновская плотность измерялась в единицах Хаунсфилда.
На основании полученных значений рентгеновской плотности тканей ПЖ и крови в аорте рассчитывали нормализованные коэффициенты контрастирования КП в панкреатическую и венозную фазы по отдельности в головке, теле и хвосте ПЖ. Последовательно для разных отделов ПЖ рассчитывали соотношение контрастирования по методикам R.J. Torphy и соавт. и Y. Hashimoto и соавт. [24, 30]. Результаты по отдельным зонам ПЖ у каждого пациента обобщались в виде средних значений и медиан.
Формулы, по которым проводились вычисления, приведены в таблице 3. Соответствие фаз контрастирования, использованных авторами, для применения в нашем исследовании определено по стандартным временны́м интервалам контрастирования. Затем рассчитывали значения среднего и медианы нормализованных коэффициентов накопления и соотношения контрастирования для ПЖ в целом. Анализ полученных диагностических изображений и денситометрия производились врачом-рентгенологом, специализирующимся в абдоминальной КТ, с опытом работы более 5 лет с помощью лицензионного программного обеспечения Vitrea и RadiAnt DICOM Viewer (рис. 1).
Таблица 3
Формулы, использованные для обработки результатов денситометрии
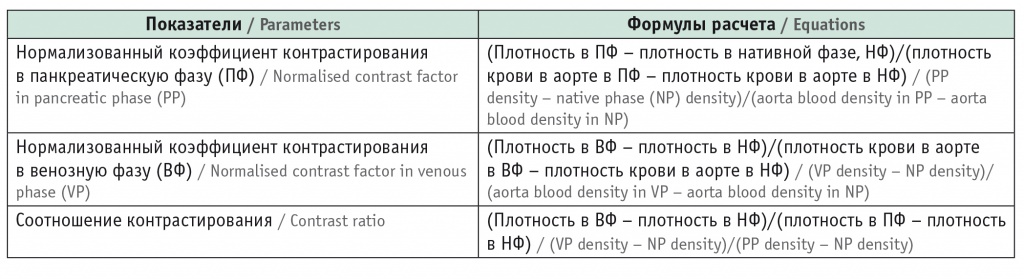
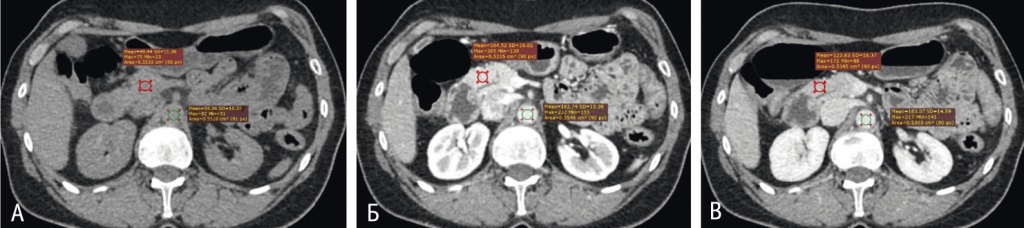
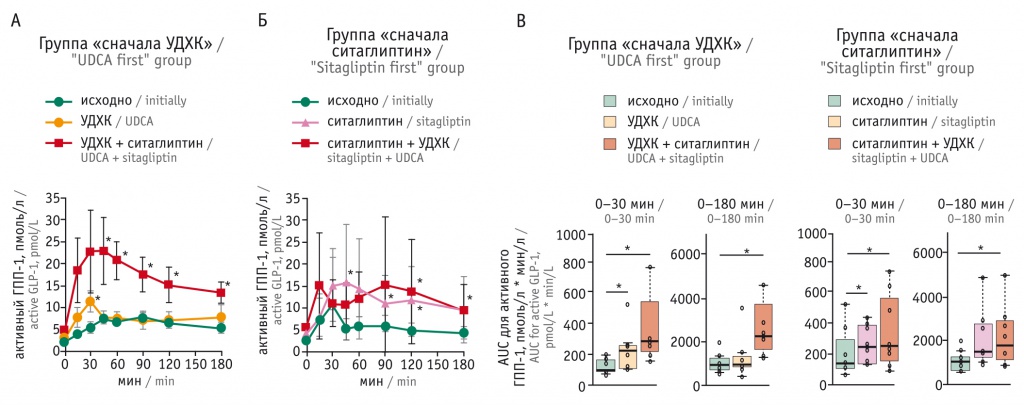
Рис. 1. Компьютерные томограммы в аксиальной плоскости в нативную (А), панкреатическую (Б) и венозную (В) фазы контрастирования с примерами измерений рентгеновской плотности. Здесь и далее в статье иллюстрации авторов
Расчет приведенных в таблице 3 показателей осуществлялся с помощью лицензионного программного обеспечения Microsoft Excel. В рамках статистической обработки полученных данных проведен парный корреляционный анализ с вычислением коэффициента корреляции Пирсона (r) и Спирмена, форму распределения значений в выборке получали с помощью теста Колмогорова — Смирнова. Последующее определение достоверности и оценка значимости межгрупповых различий производились с помощью Т-критерия, дисперсионного анализа (ANOVA), а также непараметрических тестов Краскела — Уоллиса и Манна — Уитни для попарного анализа групп с распределением значений, отличным от нормального.
Доверительный интервал составил 95%, различия считались статистически значимыми при р < 0,05. Весь комплекс статистической обработки проводился с помощью лицензионного программного обеспечения SPSS.
РЕЗУЛЬТАТЫ
Средняя продолжительность заболевания от манифестации у пациентов с кальцифицирующим ХП составила 11,3 ± 4,7 года, что статистически значимо дольше, чем у больных ХП после панкреонекроза — 5,3 ± 3,9 года, p = 0,0001. Таким образом, высокая длительность ХП увеличивает вероятность формирования кальцинатов в ПЖ.
Развернутая картина СД установлена у 16 (37,2%) человек. Снижение уровня С-пептида выявлено у 23 (53,5%) пациентов, из которых у 14 (32,6%) не было СД. Средняя концентрация С-пептида у пациентов с кальцифирующим ХП (0,95 ± 0,5 нг/мл) статистически значимо не отличалась (p = 0,18) от таковой при ХП после панкреонекроза (1,4 ± 1,1 нг/мл).
Наблюдается положительная корреляция между снижением концентраций С-пептида и фекальной эластазы 1 в исследованной популяции (r = 0,61, р = 0,0001). Количество баллов по системе M-ANNHEIM ожидаемо отрицательно коррелировало с уровнем фекальной эластазы 1 (r = –0,59, p < 0,0001).
Средняя концентрация фекальной эластазы 1 была ниже (108,36 ± 144 мкг/г) у пациентов с кальцифицирующим ХП, чем при ХП после панкреонекроза (185,67 ± 145,1 мкг/г). При использовании критерия Манна — Уитни подтверждена статистическая значимость данного различия (p = 0,03).
При распределении пациентов с ХП по группам, сформированным по уровню фекальной эластазы 1, статистически значимые межгрупповые различия сохранялись (p = 0,012). Высокая длительность течения ХП коррелировала с понижением содержвания С-пептида плазмы крови (r = 0,42, p = 0,005) и фекальной эластазы 1 (r = 0,43, p = 0,004).
Статистически значимые различия в концентрации ФН в сыворотке крови у пациентов с ХП после панкреонекроза и с кальцифицирующим ХП отсутствовали (р = 0,34). Продолжительность ХП также не влияла на уровень ФН. Однако выявлена отрицательная корреляционная зависимость количества баллов по системе M-ANNHEIM от содержания ФН в сыворотке крови (r = –0,36, p = 0,018).
Сывороточная концентрация ФН слабо-положительно коррелировала с уровнем фекальной панкреатической эластазы 1 (r = 0,365, p = 0,016), что отражает тенденцию к более высокому уровню ФН у пациентов с сохранной функцией ПЖ.
Для оценки возможностей методик изучения контрастирования при КТ в определении фиброза ПЖ у пациентов с ХП результаты денситометрического анализа сопоставлены с данными лабораторных исследований. При анализе данных c помощью дисперсионного анализа ANOVA не получены статистически значимые различия между значениями нормализованных коэффициентов контрастирования в панкреатическую и венозную фазы у больных ХП после панкреонекроза и кальцифицирующим ХП (р > 0,05).
При оценке межгрупповых различий медиан показателей соотношения контрастирования с помощью непараметрического теста Краскелла — Уоллиса обнаружена статистически значимая (p = 0,033) связь между указанными показателями пациентов с ХП после панкреонекроза и с кальцифицирующим ХП (рис. 2).
Рис. 2. Диаграмма размаха: результаты анализа межгрупповых различий медиан значения соотношения контрастирования поджелудочной железы
Этот результат подтвержден при парном анализе с помощью теста Манна — Уитни (p = 0,033). Среднее значение медианы соотношения контрастирования в ПФ у лиц с кальцифицирующим ХП было выше (1,01 ± 0,06), чем у участников с ХП после панкреонекроза (0,95 ± 0,14). Значит, показатель соотношения контрастирования неодинаков при разных степенях фиброза. Пример измерения соотношения контрастирования у пациента с кальцифицирующим ХП представлен на рисунке 3.
Рис. 3. Пациент М., 41 год, страдает кальфицирующим хроническим панкреатитом (ХП) в течение 20 лет. Компьютерные томограммы в аксиальной плоскости с измерением плотности в головке, теле и хвосте поджелудочной железы в нативную, панкреатическую и венозную фазы. Медиана значений соотношения контрастирования составила 1,52, что выше среднего соотношения контрастирования в группе пациентов с кальцифицирующим ХП (1,01 ± 0,06)
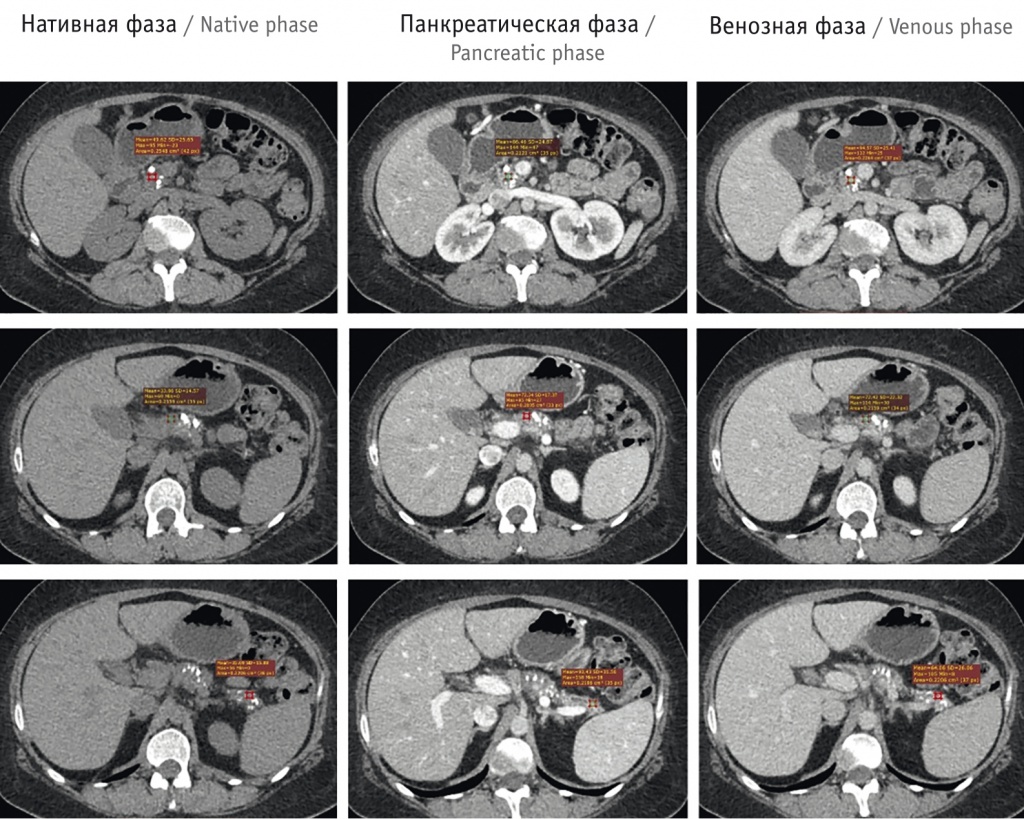
Выявлена слабая тенденция к росту значения медианы соотношения контрастирования ПЖ и отдельно головки ПЖ при увеличении продолжительности ХП — коэффициент Спирмена составил 0,31 (р = 0,04) и 0,36 (p = 0,02). Статистически значимые корреляции остальных показателей контрастирования с продолжительностью течения ХП и результатами лабораторных анализов не обнаружены.
ОБСУЖДЕНИЕ
ХП имеет важную патофизиологическую особенность, которая заключается в сочетании процессов воспаления и фиброза, усиливающих друг друга и приводящих к необратимым изменениям ПЖ. Полученные в нашем исследовании данные по продолжительности ХП соответствуют современным представлениям о течении ХП, согласно которым развитие кальцифицирующего ХП характерно для более поздних этапов заболевания по сравнению с ХП, сформировавшимся после панкреонекроза [2, 32].
Снижение концентрации фекальной эластазы 1 при кальцифицирующем ХП, полученное в нашем исследовании, укладывается в концепцию развития экзокринной недостаточности при ХП, описанную в обзорной статье T. Shimosegawa [32]. Несмотря на выявленное уменьшение уровней С-пептида и фекальной эластазы 1 при длительном течении ХП, нами не найдены статистически значимые различия в содержании С-пептида при кальцифицирующем ХП и при ХП после панкреонекроза, что позволяет предположить схожую динамику развития эндокринной недостаточности ПЖ при обоих вариантах ХП.
Кроме того, эндокринная функция страдает не только из-за прямого поражения островкового аппарата ПЖ, но и в результате внутриклеточных изменений в β-клетках, что приводит к неравномерному развитию экзо- и эндокринной недостаточности ПЖ и позволяет объяснить полученные нами результаты [3, 33].
Более выраженная экзокринная недостаточность ПЖ при кальцифицирующем ХП соответствует данным D. Thomas и P. Radhakrishnan, согласно которым фиброзная ткань как при ХП, так и при раке активно замещает интактную паренхиму, что обусловливает развитие осложнений ХП, в первую очередь экзокринных нарушений [17].
Снижение уровня С-пептида у 14 (32,6%) больных без СД отражает раннее поражение и изменение активности β-клеток при ХП до формирования СД, что позволяет включить таких пациентов в группу риска развития СД [3, 33]. Кроме того, данные изменения могут быть вызваны высокой вариабельностью инсулинемии и гликемии, описанной C.K. Kramer и соавт., при раннем СД, не имеющем развернутой клинической и лабораторной картины [34].
В нашем исследовании уровень сывороточного ФН не менялся в зависимости от продолжительности течения ХП и варианта его развития. Более высокие сывороточные концентрации ФН выявлены у пациентов с сохранной экзокринной функцией ПЖ, а понижение уровня ФН в сыворотке крови встречалось у лиц с более тяжелым течением ХП (по системе M-ANNHEIM). Мы полагаем, что более низкие значения ФН у пациентов с бо́льшим количеством баллов по системе M-ANNHEIM, отражающим тяжелое течение ХП, могут быть обусловлены эффектом длительного повышенного потребления ФН, в частности ПЖ в связи с продолжающимся ее фиброзированием, по типу истощения запаса ФН в сыворотке крови. Данное предположение согласуется с приведенными выше источниками и исследованием, опубликованным нами ранее [13–16, 35].
Среди различных методик лучевой диагностики заболеваний ПЖ интерес в отношении неинвазивного распознавания фиброза ПЖ представляет КТ с внутривенным контрастированием, благодаря распространенности отработанной методики и возможности четкого разделения фаз контрастирования для изучения микроциркуляторного русла с денситометрией на любом участке исследованной области. Изменения рентгеновской плотности тканей при внутривенном контрастировании вызваны наполнением сосудов микроциркуляторного русла [36].
При изучении возможностей КТ в неинвазивной диагностике фиброза ПЖ мы исходили из гипотезы, основывающейся на современном определении ХП, предполагающем более выраженное развитие фиброза при поздних формах заболевания, то есть при кальцифицирующем ХП. Следовательно, изменения в характере контрастирования ткани ПЖ у пациентов с кальцифицирующим ХП, вероятнее всего, отражают изменения микроциркуляции в тканях, развивающиеся при фиброзе ПЖ. В большинстве работ, касающихся неинвазивной оценки фиброза ПЖ, изучаются фиброзные изменений в ткани рака ПЖ или периопухолевой ткани, однако их результаты можно экстраполировать на фиброзные изменения при ХП в связи с принципиально типовым течением фиброза как патологического процесса [37].
Оценка рака ПЖ и фиброза стромы с помощью КТ отражена в ряде исследований, наибольший интерес из которых представляет работа H. Hata и соавт. [38]. Изучая результаты КТ с внутривенным контрастированием и микропрепараты, авторы обнаружили, что накопление контрастного препарата при КТ с внутривенным контрастированием выше в опухолях с большим количеством сосудов и выраженным фиброзом стромы. Сложность интерпретации результатов КТ в исследовании была обусловлена необходимостью оценки результатов денситометрии с построением графиков динамики контрастирования [38].
Избежать подобных сложностей и, следовательно, потенциальных ошибок можно с помощью расчета интегральных показателей контрастирования ПЖ. Одна из наиболее крупных работ представлена R.J. Torphy и соавт., в которой результаты измерения плотности опухоли ПЖ и контрастированной крови в аорте, полученные при КТ с внутривенным контрастированием, сравнивались с прямой денситометрией удаленных препаратов ПЖ. Авторами выявлена положительная корреляция полученных при КТ результатов со значениями плотности стромы, измеренной на препарате; определены взаимосвязи между плотностью стромы опухоли и значениями общей и безрецидивной выживаемости пациентов после хирургического лечения рака ПЖ. Кроме того, R.J. Torphy и соавт. описали бо́льшую эффективность адъювантной химиотерапии у пациентов с низкой плотностью опухоли [24].
Использование в нашем исследовании нормализованных коэффициентов контрастирования по методике, описанной в работе R.J. Torphy и соавт. [24], не позволило выявить изменения характера контрастирования у пациентов с ХП после панкреонекроза и с кальцифицирующим ХП. Вероятно, это связано с тем, что способ обработки результатов денситометрии отдельных зон интереса нивелировал тонкие изменения контрастирования при ХП.
Y. Hashimoto и соавт. успешно применили методику оценки соотношения контрастирования ПЖ в венозную фазу с целью неинвазивной оценки плотности тканей ПЖ для стратификации риска несостоятельности панкреатоэнтероанастомоза с формированием панкреатических фистул, что может улучшить ранние результаты панкреатодуоденальных резекций. В исследовании Y. Hashimoto значение соотношения контрастирования ≤ 1 соответствовало «мягкой» ПЖ с менее выраженным фиброзом и повышенным риском развития панкреатической фистулы [30].
Применяя методику оценки контрастирования ПЖ, представленную Y. Hashimoto и соавт., мы выявили статистически значимую связь более высокого значения медианы соотношения контрастирования (> 1,01) у пациентов с кальцифицирующим ХП, а следовательно, с более выраженным фиброзом ПЖ. Это позволяет утверждать, что показатель соотношения контрастирования ПЖ отражает качественные изменения в ПЖ, обусловленные фиброзом при ХП. Повышенное контрастирование стромы опухоли связано с миграцией молекул контрастного препарата в межклеточное пространство, которое в условиях фиброза дольше и в большем количестве, чем в норме, задерживает контрастный препарат [39–41].
С учетом типового характера течения фиброза как патофизиологического процесса [37] полученные нами результаты соответствуют данным H. Hata и соавт. Согласно последним, количество фиброзных изменений в строме рака ПЖ у пациентов с контрастированием опухоли средней выраженности статистически значимо выше, чем у больных со слабым контрастированием опухоли [38]. Таким образом, обнаруженное нами повышение соотношения контрастирования ПЖ у пациентов с кальцифицирующим ХП свидетельствует о более выраженном фиброзе у таких больных и укладывается в современную концепцию развития ХП [1, 2].
Несмотря на принципиальную схожесть патофизиологических процессов при фиброзе стромы ПЖ при раке и ХП, неодинаковая проницаемость сосудов в строме ПЖ и незрелых сосудов опухоли может затруднять прямое сравнение результатов оценки контрастирования в различных исследованиях [42]. Это может быть объяснением противоположности наших результатов и данных Y. Hattori и соавт., получивших отрицательную корреляционную связь между степенью развития фиброза и соотношением показателей плотности контрастированной паренхимы в артериальную фазу с плотностью контрастированной крови в аорте [40].
Кроме того, причиной отличий наших результатов от сведений Y. Hattori и соавт. является применение нами методики Y. Hashimoto, обобщающей показатели контрастирования в панкреатическую и венозную фазы, в то время как Y. Hattori и соавт. проводили пофазный анализ результатов КТ. Они обращают внимание на то, что контрастирование в венозную фазу показывает накопление контрастного препарата в межклеточном пространстве [40].
Наше исследование имело ограничения, в частности не уточнялись возможные микроструктурные особенности строения стенки сосудов микроциркуляторного русла, которые могут претерпевать изменения при ХП и являться одной из причин выявленных изменений соотношения контрастирования. Кроме того, потенциальным ограничением в трактовке результатов стал денситометрический анализ в отдельных зонах интереса, как и в ряде других исследований [24, 30, 40]. Это ограничение можно преодолеть при увеличении зон интереса вплоть до анализа всей железы, что планируется осуществить в будущем.
Требуются дальнейшие исследования, которые смогут определить степень выраженности фиброза, достаточную для ремоделирования микроциркуляции в ПЖ, что будет приводить к изменениям характера контрастирования и может отразиться на показателе соотношения контрастирования.
ЗАКЛЮЧЕНИЕ
У пациентов с кальцифицирующим хроническим панкреатитом (ХП), характеризующимся более длительным течением, чем ХП, развившийся после панкреонекроза, выявлено снижение уровня фекальной панкреатической эластазы 1, соответствующее тяжелой степени экзокринной недостаточности. Однако вне зависимости от длительности заболевания концентрации С-пептида (показателя эндокринной недостаточности) в этих двух группах статистически значимо не различались.
Снижение уровня фибронектина у пациентов с тяжелым течением ХП может быть обусловлено эффектом длительного повышенного потребления ФН в связи с продолжающимся фиброзированием поджелудочной железы (ПЖ).
Нарастание фиброза ПЖ влияет на характер контрастирования ПЖ, что проявляется в повышении значения соотношения контрастирования при КТ. Это позволяет использовать данный показатель для неинвазивной диагностики фиброза ПЖ у пациентов с ХП.
Поступила: 15.09.2020
Принята к публикации: 07.10.2020








