ВВЕДЕНИЕ
В настоящее время часто изучают ассоциации между факторами риска хронических неинфекционных заболеваний и такими патологиями, как сердечно-сосудистые заболевания, АГ, желчнокаменная болезнь [1], СД 2 типа, болезни органов дыхания, хроническая болезнь почек, неалкогольная жировая болезнь печени, онкологические болезни некоторых локализаций [2]. Традиционно повышенный уровень общего холестерина (ОХС) сыворотки крови связывают с риском сердечно-сосудистых заболеваний [3], вместе с тем авторы приводят противоречивые результаты исследования связи между ОХС и риском развития острого панкреатита (ОП), хронического панкреатита (ХП), рака поджелудочной железы (РПЖ).
Гипертриглицеридемия более 10 ммоль/л занимает важное место в патогенезе ОП [4, 5], столь высокая концентрация триглицеридов в сыворотке крови встречается редко, поэтому представляют интерес исследования роли умеренной гипертриглицеридемии при ОП и ХП.
В работе S.B. Pedersen и соавт. (2016) доказано, что ОП может возникать при уровне триглицеридов 177 мг/дл [6]. Гиперлипидемия и гипертриглицеридемия являются этиологическими факторами ХП, согласно классификациям TIGAR-O (1994) и M-ANNHEIM (2007) [4], однако роль нарушений липидного обмена в развитии отдельных этиологических форм ХП (алкогольной, билиарнозависимой) остается малоизученной. Данные о влиянии дислипидемии на риск РПЖ весьма разноречивы [7].
Цель исследования: определить уровни липидов сыворотки крови и частоту дислипидемий у больных ОП, ХП, РПЖ и сравнить эти показатели.
МАТЕРИАЛЫ И МЕТОДЫ
В ходе наблюдательного многоцентрового клинического кросс-секционного неконтролируемого исследования по типу «серия случаев» за период 2014–2019 гг. в ГБУЗ Новосибирской области «Городская клиническая инфекционная больница № 1» (ГБУЗ НСО ГИКБ № 1), ГБУЗ Новосибирской области «Государственная Новосибирская областная клиническая больница» (ГБУЗ НСО ГНОКБ), Научно-исследовательском институте терапии и профилактической медицины — филиале ФГБНУ «Федеральный исследовательский центр Институт цитологии и генетики Сибирского отделения Российской академии наук» (НИИТПМ — филиала ИЦиГ СО РАН) обследованы 44 больных ОП, 97 пациентов с ХП и 45 с РПЖ, группы были сравнимы по полу и возрасту.
Письменное информированное согласие на участие получено от каждого пациента. Исследование одобрено этическим комитетом НИИТПМ — филиала ИЦиГ СО РАН, ГБУЗ НСО ГИКБ № 1 и ГБУЗ НСО ГНОКБ.
Критерии включения в исследование: больные ОП, ХП или РПЖ мужского и женского пола в возрасте 25–70 лет без тяжелой сопутствующей патологии.
Для верификации диагноза использовали общеклинические, лабораторные, инструментальные и морфологические методы обследования поджелудочной железы [4]. Диагноз ХП установлен на основании комплексной оценки результатов проведенных инструментальных исследований поджелудочной железы (УЗИ, КТ или МРТ) и лабораторных тестов (определения уровней гликемии, эластазы 1 кала) с учетом критериев M-ANNHEIM.
«Определенный» ХП диагностировался при наличии одного или нескольких из следующих критериев: кальцификации поджелудочной железы, умеренных или тяжелых изменений ее протоков, выраженной постоянной экзокринной недостаточности поджелудочной железы. «Вероятный» ХП: легкие изменения протоков поджелудочной железы, псевдокиста, патологические результаты функциональных тестов (эластазы 1 кала), эндокринная недостаточность. При наличии типичной клинической картины в отсутствие критериев «вероятного» и «определенного» ХП выставлялся диагноз «пограничного» ХП [4].
У всех больных по стандартным методикам определены уровни липидов сыворотки крови: ОХС, ХС ЛПВП, триглицеридров. Концентрации ХС ЛПНП, ХС липопротеинов очень низкой плотности (ЛОНП) и ХС, не связанного с ЛПВП (ХС неЛПВП), рассчитывали по формулам.
Гиперхолестеринемией считали уровень ОХС > 5,0 и/или уровень ХС ЛПНП > 3,0 ммоль/л; гипертриглицеридемией — уровень триглицеридов натощак > 1,7 ммоль/л [3]. Коэффициент атерогенности (КА) рассчитывали по формуле: КА = (ОХС – ХС ЛПВП)/ЛПВП.
Выявленные нарушения липидного обмена были разделены по фенотипам гиперлипидемии согласно классификации ВОЗ. Для анализа полученных результатов выделили три группы: больные ОП (n = 44; 61,4% мужчин и 38,6% женщин; средний возраст — 51,1 ± 1,6 года, средний ИМТ — 24,2 ± 0,7 кг/м2), больные ХП (n = 97; 19,6% мужчин и 80,4% женщин; средний возраст — 54,5 ± 1,2 года, средний ИМТ — 26,3 ± 0,5 кг/м2), больные РПЖ (n = 45; 48,9% мужчин и 51,1% женщин, средний возраст — 58,3 ± 1,1 года, средний ИМТ — 26,2 ± 0,7 кг/м2).
В соответствии с классификацией ОП В.С. Савельева (2004), выявили 20 (45,5%) пациентов с отечным ОП и 24 (54,5%) с панкреонекрозом [4]. По классификации ХП M-ANNHEIM (Schneider A., 2007) в нашем исследовании больные ХП распределены по клиническим формам: «пограничный» ХП — 44 (45,4%), «вероятный» ХП — 41 (42,2%), «определенный» ХП — 12 (12,4%) [4]. У 41 (91,1%) больного РПЖ выявлена аденокарцинома поджелудочной железы и у 4 (8,9%) — нейроэндокринный рак. Распределение пациентов с РПЖ по стадии болезни: Т1-Т2 — 26 (57,8%), Т3 — 13 (28,9%) и Т4 — 6 (13,3%).
Статистическую обработку данных осуществляли при помощи пакета программ SPSS (13.0). Проверку нормальности распределения признака проводили с использованием критерия Колмогорова — Смирнова, сравнение частот качественных признаков — с помощью критерия χ2 и t-критерия Стьюдента, ОР с 95%-ным ДИ — по таблице сопряженности c поправкой Мантеля — Хенцеля.
При отсутствии нормального распределения исследуемых показателей вычислялись медиана (Me), 25-й и 75-й процентили (Q1 и Q3), для сравнительной оценки средних значений количественных признаков применялся метод Манна — Уитни. Для выявления и оценки силы связи между двумя рядами количественных показателей использовали коэффициент ранговой корреляции Спирмена.
Многомерный анализ связей главных признаков проводился с помощью логистического регрессионного анализа (метод Enter) и пошаговой обратной регрессией (метод Вальда). Exp (B) (экспонента В) показывает, во сколько раз изменяется риск возникновения исхода, если значение предиктора изменяется на единицу [8]. Различия считались статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
Анализ распределения признака (критерий Колмогорова — Смирнова) выявил ненормальное распределение показателей липидов сыворотки крови (ОХС, триглицеридов, ХС ЛПВП, ХС ЛОНП, ХС ЛПНП, ХС неЛПВП) у больных ОП, ХП и РПЖ, поэтому сравнительный анализ проведен методом Манна — Уитни. Концентрации липидов у участников исследования представлены в таблице 1. Среди обследованных наиболее высокие уровни ОХС, ХС ЛПНП выявлены у больных ХП, наиболее низкие — у больных РПЖ. Показатели триглицеридов в группах не различались. У пациентов с РПЖ отмечены наиболее низкое содержание ХС ЛПВП и наиболее высокий КА.
Таблица 1
Средние уровни липидов сыворотки крови (ммоль/л) и коэффициент атерогенности (КА) у обследованных больных, Mе (Q1; Q3)
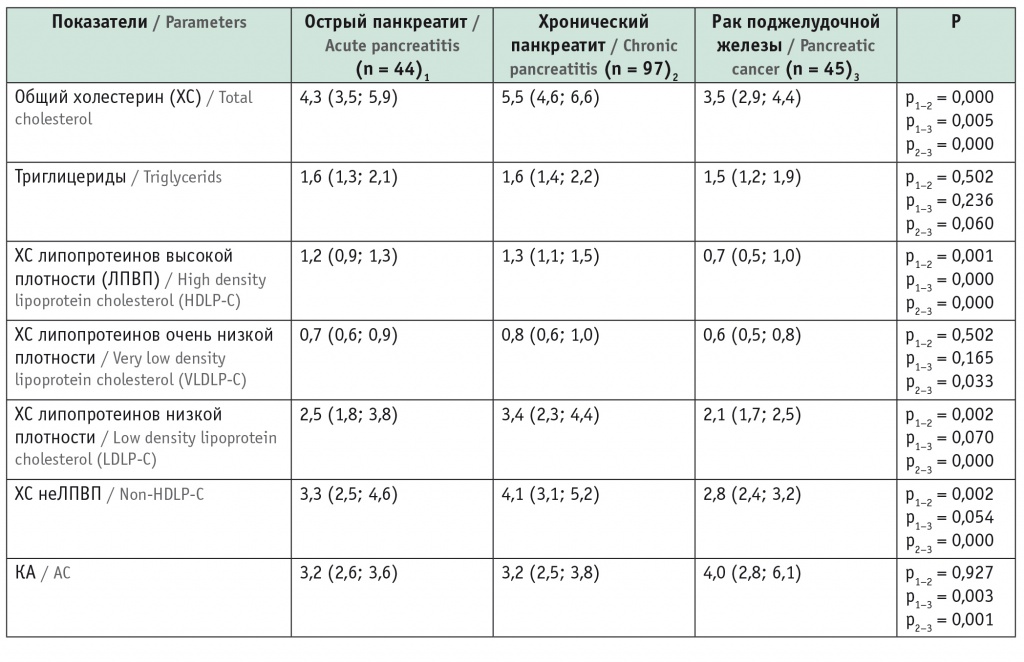
У больных ОП и ХП концентрации ОХС различались в зависимости от формы болезни: у лиц с панкреонекрозом средний уровень ОХС ниже, чем при отечном ОП: 4,1 (3,2; 5,4) ммоль/л против 5,5 (3,7; 6,3) ммоль/л, p = 0,037. У больных «определенным» ХП средний уровень ОХС (4,5 (3,8; 6,0) ммоль/л) был ниже, чем при «пограничном» (6,2 (4,6; 6,7) ммоль/л, p = 0,021), при «вероятном» ХП он значимо не отличался от такового ни при «определенном», ни при «пограничном» ХП (5,5 (4,7; 6,5) ммоль/л, p > 0,05 в обоих случаях).
При разных стадиях или формах РПЖ средние уровни ОХС практически не различались, p > 0,05 во всех случаях.
По результатам логистического регрессионного анализа с зависимыми (ОП, ХП и РПЖ), независимыми переменными (возраст, ИМТ, уровни ОХС, триглицеридов, ХС ЛПВП, ХС ЛПВП) выявлена прямая связь повышения содержания ХС ЛПВП на 1 ммоль/л с риском ХП (Exp (B) = 21,618; 95%-ный ДИ: 4,741–98,582, p = 0,000) и обратная — с риском РПЖ (Exp (B) = 0,015; 95%-ный ДИ: 0,002–0,092, p = 0,000).
Частота нарушений липидного обмена (гиперхолестеринемии, гипергриглицеридемии, гиперлипидемии, гипоальфахолестеринемии, дислипидемии) у участников представлена в таблице 2. Гиперхолестеринемию чаще выявляли у больных ХП (58,8%), чем ОП (40,9%, χ2 = 3,9, p = 0,049), РПЖ (15,6%, χ2 = 23,2, p = 0,000). У пациентов с ОП частота гиперхолестеринемии не различалась при отечном ОП и панкеонекрозе, у мужчин и женщин, при билиарной и алкогольной этиологии (p > 0,05 во всех случаях).
Таблица 2
Частота дислипидемий у обследованных больных, n (%)
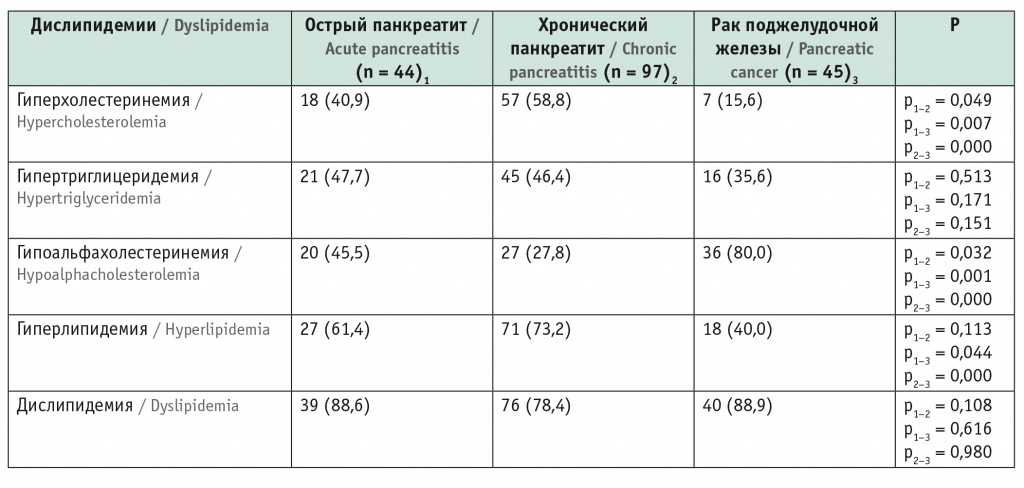
У лиц с ХП частота гиперхолестеринемии не зависела от этиологии, но отмечены гендерные различия: у женщин гиперхолестеринемия имела место в 3,2 раза чаще (n = 53, 67,9%), чем у мужчин (n = 4, 21,1%), χ2 = 13,9, p = 0,000). У больных «вероятным» ХП (n = 28, 68,3%) она наблюдалась чаще, чем при «определенном» ХП (n = 4 (33,3%), χ2 = 4,7, p = 0,029).
Распространенность гиперхолестеринемии у больных ХП (58,8%) не отличалась от таковой в целом по России по данным исследования ЭССЕ-РФ (57,6%, t = 0,2, p = 0,817) [9]; у больных ОП (43,2%, t = 2,2, p = 0,025) и у больных РПЖ (15,6%, t = 5,7, p = 0,000) гиперхолестеринемия встречается реже.
Частота гипертриглицеридемии у обследованных была сопоставимой (см. табл. 2). Гиперлипидемию значительно реже выявляли у больных РПЖ (40,0%) по сравнению с больными ОП (61,4%, χ2 = 4,1, p = 0,044), ХП (73,2%, χ2 = 14,5, p = 0,000).
У пациентов с ОП не найдены значимые различия в частоте гиперлипидемии в зависимости от пола, этиологии и формы болезни.
У пациентов с ХП отмечены гендерные различия: у женщин гиперлипидемию диагностировали чаще (у 62 из 78, 79,5%), чем у мужчин (у 9 из 19, 47,4%); χ2 = 8,0, p = 0,005. При этом частота гиперлипидемии не зависела от этиологии ХП, p > 0,05. У больных «определенным» ХП (n = 6, 50%) она имела место реже, чем при «вероятном» (n = 33 (80,5%), χ2 = 4,4, p = 0,035); у больных «пограничным» ХП распространенность гиперлипидемии значительно не отличалась от таковой в других группах (n = 32 (72,7%), p > 0,05 в обоих случаях).
У лиц с РПЖ не было гендерных различий в частоте гиперлипидемии. У больных с 1–2-й стадией РПЖ гиперлипидемия встречалась чаще, чем у больных 3-й стадией: 13 из 26 (50%) против 2 из 13 (15,4%); χ2 = 4,4, p = 0,036.
У больных с гиперлипидемией распределение по фенотипам было следующим: при ОП частота IIa типа составляла 6 (22,2%), IIb типа — 12 (44,5%) и IV типа — 9 (33,3%); при ХП — 26 (36,6%), 31 (43,7%) и 14 (19,7%); при РПЖ — 2 (11,1%), 5 (27,8%) и 11 (61,1%) соответственно. У пациентов с ХП IIa фенотип обнаруживали значимо чаще, чем при РПЖ (t = 2,1, p = 0,040), при ОП распространенность IIа фенотипа не отличалась от таковой при ХП и РПЖ. Частота IIb фенотипа гиперлипидемии у больных ОП, ХП или РПЖ была сопоставимой; IV фенотип у больных РПЖ наблюдался существенно чаще, чем у пациентов с ХП (t = 3,7, p = 0,000), в отличие от случаев ОП (p = 0,073).
Гипоальфахолестеринемия значительно чаще встречалась у участников с РПЖ, чем у больных ОП и ХП (см. табл. 2). Распространенность ее при ОП и ХП не зависела от пола, этиологии, формы болезни. У больных РПЖ частота гипоальфахолестеринемии также не различалась в зависимости от пола, стадии, формы рака.
Частота дислипидемии (гипоальфахолестеринемии или гиперлипидемии) у лиц с ОП (88,6%), ХП (78,4%), РПЖ (88,9%) была сопоставимой.
У больных ОП распространенность дислипидемии не зависела от пола, этиологии, формы болезни, у больных РПЖ — от пола, стадии, формы рака.
Среди пациентов с ХП отмечены гендерные различия: дислипидемия чаще выявлена у женщин (84,6%), чем у мужчин (52,6%, χ2 = 9,2, p = 0,002). При «определенном» ХП (50,0%) она встречалась реже, чем при «вероятном» (87,8%, χ2 = 8,1, p = 0,005), при «пограничном» ХП (77,3%) — с сопоставимой частотой (p > 0,05).
При пошаговой обратной регрессии с включением в зависимые переменные панкреонекроза, «определенного» ХП или 3–4-й стадии РПЖ и в независимые — возраста, пола, уровней ОХС и триглицеридов, КА выявлена связь уровня ОХС с панкреонекрозом и «определенным» ХП: на каждый 1 ммоль/л прироста содержания ОХС риск панкреонекроза снижался на 37,7% (Exp (B) = 0,623; 95%-ный ДИ: 0,389–0,996, p = 0,048), «определенного» ХП — на 47,4% (Exp (B) = 0,526; 95%-ный ДИ: 0,305–0,908, p = 0,021).
ОБСУЖДЕНИЕ
Нами определена относительно низкая частота гиперхолестеринемии у больных РПЖ, ОП по сравнению со средней ее распространенностью в России, у больных ХП частота гиперхолестеринемии практически не отличалась от среднероссийских показателей. По литературным данным, гипертриглицеридемия положительно связана с риском развития и худшим прогнозом ОП [10]. В нашем исследовании гипертриглицеридемия не превышала 4 ммоль/л, связь между уровнями триглицеридов и ОП, ХП или РПЖ не выявлена. Кроме того, гипертриглицеридемия обеспечивает только 29% риска ОП [11].
В клиническом исследовании определена отрицательная связь концентраций аполипопротеина А-I и ХС ЛПВП с неблагоприятными клиническими исходами ОП [12]. В экспериментальной работе отмечены более высокие уровни ОХС (1,97 ± 0,21 против 1,46 ± 0,32 ммоль/л, p < 0,01), триглицеридов (2,69 ± 0,86 против 1,35 ± 0,51 ммоль/л, p < 0,01) и более низкое содержание ХС ЛПВП (0,46 ± 0,07 против 0,68 ± 0,11 ммоль/л, p < 0,01) у мышей с индуцированным ОП и ожирением, чем в контрольной группе мышей с ОП без ожирения [13].
По данным исследования Q. Ni и соавт. (2014), уровни ОХС, триглицеридов, ХС ЛПНП не различались у больных ХП и контрольной группы (p > 0,05), в то время как уровни ХС ЛПВП в группе ХП были значимо ниже (p < 0,01) [14].
В другом исследовании при сравнении больных ХП с СД 3с типа и группы контроля с СД «непанкреатического генеза», т. е. СД 1 и 2 типа, показано снижение уровня ОХС (164 против 183 мг/дл, p = 0,0028). Авторы предположили, что концентрация ОХС у пациентов с ХП может более точно отражать экскреторную недостаточность поджелудочной железы, чем другие пищевые маркеры, такие как альбумин [15]. По нашим данным, на каждый 1 ммоль/л прироста содержания ОХС риск «определенного» ХП снижался на 47,4%.
По данным метаанализа (2015), ни в Европе, ни в Азии уровень ОХС не был ассоциирован с РПЖ, однако диетический холестерин может быть связан с повышенным риском РПЖ [16]. В корейском проспективном исследовании (n = 78 419) получены позитивные и негативные результаты ассоциации содержания ОХС и рака, в целом авторы считают, что уровень ОХС связан с риском нескольких различных видов рака, хотя эти отношения заметно различались в зависимости от локализации рака [17].
В работе G.C. Kabat и соавт. (2018) выявлена обратная связь между сывороточным уровнем ХС ЛПВП и РПЖ [18].
Влияние гипоальфахолестеринемии на риск РПЖ практически не изучено. Наши результаты не противоречат имеющимся данным о значительной обратной связи между исходными уровнями ХС ЛПВП и частотой возникновения онкологических заболеваний: на каждые 10 мг/дл прироста концентрации ХС ЛПВП приходится 36%-ное снижение риска рака (95%-ный ДИ: 24–47%) (р < 0,001), не зависящее от возраста, ИМТ, пола, курения и наличия СД [19].
В недавнем экспериментальном исследовании получены данные о протективном эффекте ХС в отношении онкогенеза: у мышей с повышенным уровнем ОХС после инъекции химического канцерогена развивались опухоли меньшего размера и в меньшем количестве [20].
Высокая частота гипоальфахолестеринемии у больных РПЖ косвенно подтверждает эпидемиологические данные об обратной зависимости между уровнем ХС ЛПВП и общей заболеваемостью раком [19]. В нашей работе выявлено, что на каждый 1,0 ммоль/л прироста уровня ХС ЛПВП приходится 98,5%-ное снижение риска развития РПЖ.
ЗАКЛЮЧЕНИЕ
Гиперхолестеринемию чаще всего выявляли при хроническом панкреатите (ХП), гипоальфахолестеринемию — при раке поджелудочной железы (РПЖ); частота гипертриглицеридемии при описанных заболеваниях не различалась. Найдена прямая связь содержания холестерина (ХС) ЛПВП с риском ХП, обратная — с риском РПЖ. Уровень общего ХС был обратно ассоциирован с риском панкреонекроза и «определенного» ХП. Полученные данные обусловливают необходимость дальнейшего изучения ассоциации заболеваний поджелудочной железы с уровнями липидов крови.
Поступила: 12.03.2020
Принята к публикации: 03.05.2020








