Острый деструктивный панкреатит (ОДП) является одной из важнейших проблем неотложной хирургии органов брюшной полости. Это обусловлено неуклонным ростом заболеваемости, увеличением частоты осложнений и высокой летальностью[1, 2, 7]. При ОДП летальность составляет 20–45% без учета клинической формы, достигая при инфицированном панкреонекрозе 85%, а при фульминантном течении заболевания — 100%[1].
Анализ данных литературы позволяет признать, что на данный момент мы не располагаем четкими критериями и методами дифференциального диагноза клинико-морфологических форм ОДП и его постнекротических осложнений. Ни один из существующих сегодня методов диагностики сам по себе не может быть признан абсолютно точным для раннего распознавания панкреонекроза и его осложнений. Следовательно, требуется комплексный подход с учетом клинических и лабораторных данных, ультразвуковой томографии (УЗТ), лапароскопии, рентгенологических методов исследования, КТ и МРТ[1, 2, 7]. По нашему мнению, общепринятые методики обследования могут быть эффективно дополнены минимально инвазивной многочастотной биоимпедансометрией, позволяющей в режиме реального времени определить состояние метаболизма зоны деструкции[3].
На основании имеющихся сведений в отечественной и зарубежной литературе, актуальным представляется вопрос о своевременном выявлении инфицированного панкреонекроза и об аргументированном определении показаний к использованию контролируемых минимально инвазивных хирургических методик на различных стадиях развития заболевания[4, 9, 10].
МАТЕРИАЛЫ И МЕТОДЫ
В исследование вошли 293 пациента Федерального научно-клинического центра специализированных видов медицинской помощи и медицинских технологий ФМБА России, поступившие с различными клинико-морфологическими формами ОДП, которым были выполнены минимально инвазивные вмешательства под контролем УЗТ и рентген-телевизионного оборудования (РТВ). Среди них мужчин было 224 (76,5%), женщин — 69 (23,5%). Возраст больных варьировал от 19 до 84 лет. При анализе причин развития заболевания алкогольный фактор выявлен у 225 (76,8%) больных, билиарный — у 25 (8,5%), другая этиология (травма, послеоперационный, идиопатический) — у 42 (14,3%) больных.
В соответствии с классификацией острого панкреатита, принятой на Международном согласительном симпозиуме в Атланте (1992 г.), больные были распределены на группы, соответствовавшие клинико-морфологической форме заболевания: 87 (29,7%) больных были с острыми жидкостными скоплениями, 28 (9,6%) — с панкреатическим некрозом, 79 (26,9%) — с панкреатогенным абсцессом, 99 (33,8%) — с панкреатической ложной кистой.
Всем больным осуществлялись комплексная клинико-лабораторная диагностика и инструментальные исследования, основными целями которых были верификация клинико-морфологических форм ОДП, определение наличия и формы осложнений, абдоминального сепсиса и полиорганной недостаточности. Выявленные различия в симптоматике и данных лабораторных методов исследования позволили дифференцировать основные формы ОДП.
Лучевые методы диагностики включали рентгенографию органов грудной клетки и органов брюшной полости, УЗИ органов брюшной полости в режиме серой шкалы, цветового доплеровского картирования и энергетического доплера, пошаговую КТ. Ведущим методом для постановки диагноза, динамического наблюдения за фазами течения патологического процесса и решения вопроса о применении диапевтических технологий, а также для динамического контроля эффективности лечения являлась УЗТ. Для описания диффузных и очаговых поражений поджелудочной железы были использованы стандартизированные ультразвуковые критерии[3]. Эта оценка предполагает стандартизацию в определении значимости качественных признаков описания изображения. КТ в основном выполнялась больным с распространенными гнойными осложнениями перед планируемыми лечебными минимально инвазивными манипуляциями для уточнения распространенности патологического процесса и получения информации о состоянии парапанкреатической и забрюшинной клетчатки.
Всем больным были выполнены различные по объему диагностические и лечебные минимально инвазивные вмешательства под контролем УЗТ и РТВ. В целях детализации этапа эволюции заболевания, а также морфологической и бактериологической верификации диагноза у всех пациентов применялись тонкоигольные диагностические пункции (ТДП) под контролем ультразвука. Показанием к ТДП считали наличие изменений, подозрительных в отношении деструкции, или очагового поражения поджелудочной железы, сальниковой сумки или забрюшинного пространства. ТДП проводили по мультифокальной программе: забор производили из 4 точек не менее 2 отделов поджелудочной железы и зоны сальниковой сумки иглой типа Chiba и Angiomed G 19–20–21 с тангенциальным расположением биопсийного адаптера на конвексном датчике 3,5–7,5 МГц. Сопоставляли результаты УЗТ, цитологической и бактериологической картины заболевания.
Во время выполнения ТДП у 124 (42,3%) больных была проведена минимально инвазивная многочастотная биоимпедансометрия образования с использованием диэлектрической иглы с многочастотным биоимпедансным томографом «ИМТ» (г. Ярославль). Все показатели импеданса рассматривались относительно полярности электродов (моно- и биполярно) и частоты переменного тока. Измерение электрического импеданса проводилось на трех частотах: 1, 10 и 100 кГц. Показатели импеданса, снимавшиеся в режимах in vivo и in vitro, имели свои особенности. Система измерения in vivo состоит из изолированных пункционных игл, электродов и регистрирующего биоимпедансные параметры устройства, последовательно подключенных между собой. Благодаря небольшим размерам игл (G22) с диэлектрическим наконечником, а также использованию ультразвукового мониторинга, были возможны точное позиционирование игл и фиксация в интересующей зоне исследования. У всех пациентов с очаговым поражением мы исследовали биоимпеданс капсулы очага, периферии и центральной зоны образования (рис. 1).
Рис. 1. Ультразвуковые томограммы монополярной мультизональной биоимпедансометрии жидкостного образования при остром деструктивном панкреатите. Фото авторов
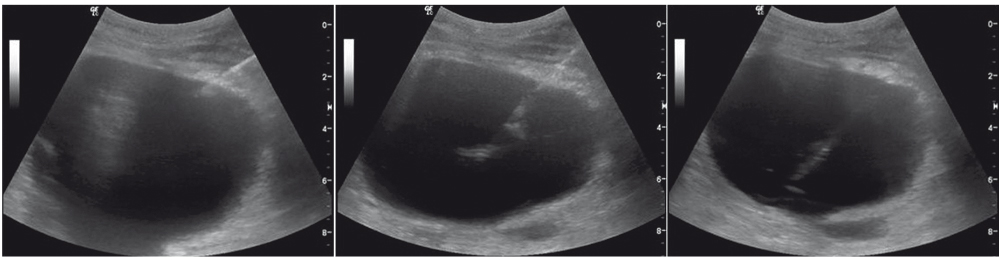
Во время биполярной биоимпедансометрии диэлектрические иглы фиксировались таким образом, чтобы максимально охватить исследуемый участок органа, при этом расстояние между ними составляло 10 мм. Исследование аспирата in vivo во время минимально инвазивного вмешательства позволяет оценить характер жидкости в реальном времени, однако это зачастую дает ложноположительные и ложноотрицательные результаты. Использование биполярной импедансометрии in vitro позволяет уменьшить количество таких ошибок.
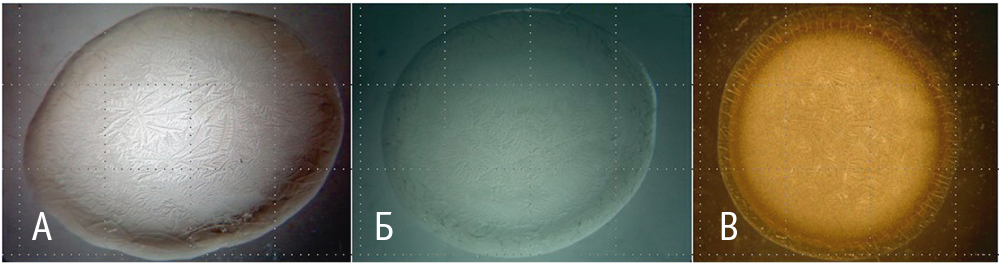
Наряду с другими исследованиями мы применяли метод клиновидной дегидратации аспирата, полученного при проведении минимально инвазивных вмешательств под контролем УЗТ и РТВ[3]. Сущность кристаллографического исследования заключается в исследовании параметров капли аспирата (фации), в процессе дегидратации которой формируются фиксированные структуры. Их вид и локализация определяются комплексом количественных и качественных параметров присутствующих веществ и характером их взаимосвязей[8]. Исследование структурообразующих элементов натурных образцов высушенных капель (фации) проводилось с помощью светового микроскопа и бинокулярной лупы при увеличениях ×32, ×56 и ×72. Параметры фации определяли путем обработки цифровых фотографий с помощью компьютерной программы для морфометрии (рис. 2). Определялись следующие параметры: радиус периферической зоны, общий радиус, длина трещины (минимальная, максимальная), число и форма трещин, порядок деления кристаллов, углы кристаллизации, длина осей кристаллизации, а также стабильность указанных параметров в динамике[8].
Рис. 2. Кристаллографическое исследование фации острого жидкостного скопления (А), ложной кисты (Б) и панкреатогенного абсцесса (В) поджелудочной железы. Фото авторов
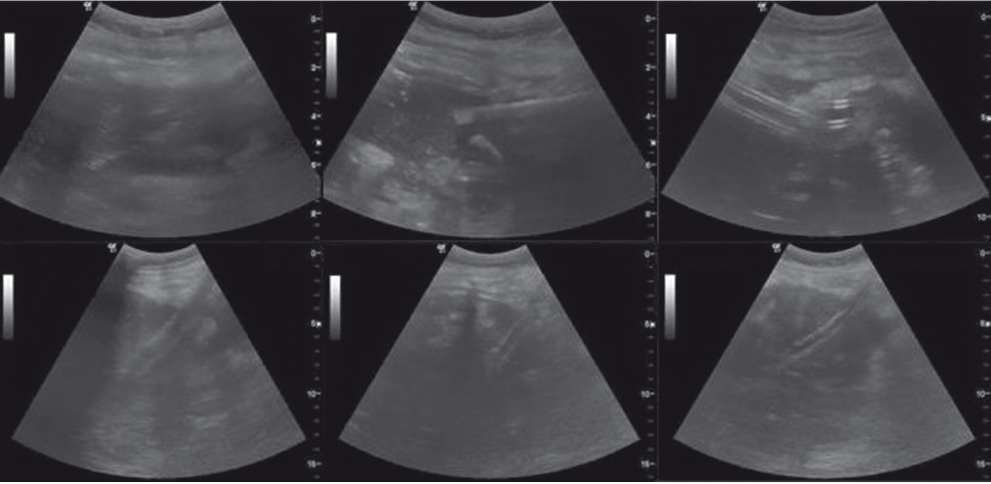
Показаниями к чрескожному дренированию считали экссудативные образования и зоны деструкции, осложнявшие течение ОДП, при рефрактерности их к комплексной консервативной терапии. Малокалиберное дренирование осуществляли одноразовыми пункционными нефростомическими дренажными наборами Rush (Teleflex Medical, США) по двухмоментной методике Сельдингера и одномоментной методике с помощью стилет-катетера с установкой дренажа с памятью формы типа pigtail. При крупнокалиберном дренировании операционный доступ осуществляли с помощью известной техники телескопической дилатации дренажного канала от 8 Fr до 36 Fr (рис. 3).
Рис. 3. Крупнокалиберное дренирование зоны деструкции в поджелудочной железе. Фото авторов
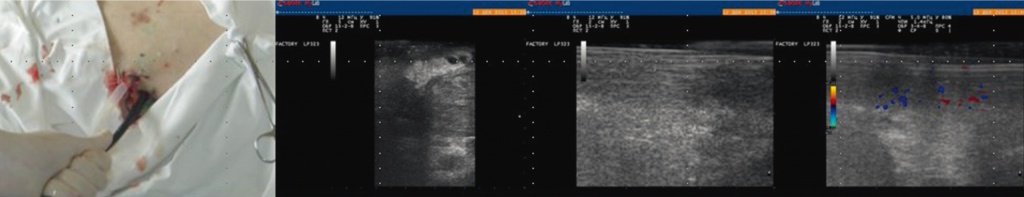
У 61 (20,8%) пациента с гнойно-некротическими осложнениями ОДП была использована эндосонография для интракавитальной ультразвуковой оценки состояния гнойных полостей. С целью повышения точности оценки динамики патологического процесса, а также прогнозирования дальнейшего течения заболевания производилась интракавитальная УЗТ патологического очага с определением структуры капсулы, эхоструктуры стенки очага и его ультразвуковой пальпацией. УЗТ выполнялась с использованием конвексного эндоскопического ультразвукового датчика (5,0 МГц) на аппарате Aloka SSD-630 и линейного лапароскопического датчика частотой 7,5 Мгц, сопряженного со сканером SonoScape S8 или MyLab 50 (рис. 4).
Рис. 4. Интракавитальная ультразвуковая томография гнойной полости в поджелудочной железе. Фото авторов
Статистическая обработка данных проводилась с указанием числа наблюдений для каждого признака, с вычислением уровня статистической значимости, доверительного интервала (для основных результатов исследования) и частоты выявления признака. Полученные данные представлялись с помощью следующих показателей: M ± SD, Me (LQ; UQ), % (n/N). Проверка статистических и корреляционных гипотез осуществлялась на уровне значимости α = 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
У больных, поступивших в клинику, наблюдались различные клинические формы течения ОДП. Обращала на себя внимание зависимость выраженности и характера клинической картины заболевания от фазы патологического процесса. Так, на ранних стадиях деструктивного процесса превалировали признаки ферментной токсемии (83,7%). Клиническая картина более позднего периода заболевания характеризовалась развитием гнойно-септических осложнений (95,2%).
Изменения при лабораторном исследовании крови (красная кровь, развернутая лейкоцитарная формула, лейкоцитоз, повышение СОЭ) не были специфичными и являлись вспомогательными признаками заболевания. При биохимическом исследовании крови выявлялись нарушения функции поджелудочной железы и печени разной степени выраженности в зависимости от стадии патологического процесса.
Минимально инвазивные вмешательства под контролем УЗТ и РТВ осуществляли в определенной последовательности: в виде сочетания разных по кратности пункционных и дренажных вмешательств с постановкой дренажей различного диаметра и типа. Выбор вмешательства определялся этапом развития патологического процесса в соответствии с современной классификацией острого панкреатита на основании преимущественно эхографической картины[5, 6].
Острое жидкостное скопление характеризовалось наличием одного или нескольких анэхогенных или гипоэхогенных образований неправильной формы с четкими или нечеткими, чаще неровными контурами, однородной структуры, расположенных внутри железы, в парапанкреатическом и забрюшинном пространствах или в брюшной полости. При инфицированном характере острого жидкостного скопления внутренняя структура образования была неоднородной, с эхопозитивными включениями на стенках или в его просвете. Учитывая то, что острые жидкостные скопления у больных ОДП возникают рано, в фазе токсемии, а пациенты поступали в стационар в разные сроки от начала заболевания, ультразвуковая картина изменений со стороны поджелудочной железы и окружающих тканей характеризовалась спектром изменений, характерных для некротической, инфильтративно-некротической форм и асептической секвестрации.
При панкреатическом некрозе гнойное расплавление тканей панкреатического инфильтрата сопровождалось появлением в его структуре большого количества мелких эхонегативных неправильно расположенных структур с нечеткими контурами. При динамическом наблюдении отмечалось их слияние с исходом в более крупные включения неоднородной плотности. Распространение процесса на окружающие ткани сопровождалось потерей четкости визуализации их структуры.
При абсцессах брюшной полости и забрюшинного пространства выявлялся единичный очаг неправильной формы и пониженной эхогенности. Внутренняя структура гнойника неоднородная с единичными, равномерно или беспорядочно рассеянными, мелкими эхопозитивными включениями. Позади очага имелась полоса отражений повышенной интенсивности.
При формировании кистозных образований в паренхиме железы или парапанкреатической клетчатке определялось кистозное образование с однородной гипоэхогенной структурой до 20–25 см в диаметре. Паренхима железы, окружающая кисту, имела неоднородную структуру.
Чувствительность, специфичность и диагностическая эффективность УЗИ составили 85,47%, 90,4% и 89,6% соответственно.
Следующим этапом диагностики у всех больных было проведение ТДП зон деструкции в поджелудочной железе, сальниковой сумке и забрюшинном пространстве. ТДП с целью ранней микробиологической и морфологической верификации природы очаговых изменений проводилась по диагностическим пункционным схемам[1]. Эти схемы заключались в последовательном применении различных игл и изменении кратности выполнения ТДП.
При статистической обработке результатов цитологического исследования аспирата из острых жидкостных скоплений выявлены различные сочетания элементов крови, воспаления, скопления некротических масс в зависимости от преобладания некротических, инфильтративно-некротических изменений или асептической секвестрации. В мазке-отпечатке аспирата гнойно-некротической формы наблюдались преимущественно некротические массы. Аспират, полученный из полости абсцессов, содержал в большом количестве элементы некротических масс и микробные тела, значительное количество элементов воспаления (нейтрофильные и разрушенные лейкоциты) и единичные измененные клеточные элементы крови. При кистозных образованиях в мазке-аспирате визуализировались элементы кистозной полости (слущенный неизмененный низкопризматический и уплощенный эпителий с дистрофическими изменениями) и жировой компонент в виде кристаллов на фоне умеренного количества элементов воспаления (макрофаги и многоядерные клетки) и некротических масс. Чувствительность, специфичность и диагностическая эффективность цитологического исследования в работе составили 87,7%, 95,4% и 91,6% соответственно.
У 126 (43%) пациентов бактериологический посев аспирата был отрицательным. У 167 (57%) пациентов результаты микробиологического исследования оказались положительными. В 75% случаев бактериальная флора была представлена условно-патогенными энтеробактериями грамотрицательного спектра, в 25% — грамположительными возбудителями. Чувствительность, специфичность и диагностическая эффективность микробиологического исследования, по нашим данным, составили 87,7%, 94,3% и 90,7% соответственно.
При проведении минимально инвазивной биоимпедансометрии у всех пациентов с ОДП наблюдалась зависимость величины импеданса от частоты переменного тока и глубины измерения. Величины импеданса зависели от структурной организации содержимого жидкостного образования. При проведении биоимпедансометрии аспирата при остром скоплении жидкости и псевдокисте со временем отмечается рост импеданса, а при абсцессе — вначале падение, а затем рост. Показатели биоимпеданса в зависимости от зоны очага (периферия, центр) статистически значимо различались при ложной кисте и панкреатогенном абсцессе железы. При остром скоплении жидкости наибольший рост импеданса отмечался до 20-й минуты после пункции, а при псевдокисте и абсцессе — после 20-й минуты. Цифры импеданса у аспирата из острого скопления жидкости в 2 раза выше по сравнению с псевдокистой. В результате была получена диагностическая система, позволяющая на раннем этапе дифференцировать характер очагового поражения при ОДП.
Кристаллографическая картина, структура и степень выраженности параметров зависит от характера биожидкости. Ложная киста, острое скопление жидкости и панкреатический абсцесс дают различающиеся изображения. У пациентов с панкреатогенным абсцессом среднее значение коэффициента Sбелк/Sобщ на 47,4% больше, чем в группах с острым скоплением жидкости и ложной кистой (φ*эмп = 2,78, р < 0,05). При исследовании аспирата, полученного у больных с острым скоплением жидкости и ложной кистой, коэффициент Sбелк/Sобщ в большинстве случаев (76,9% и 67,6% соответственно) находился в области минимальных значений, т. е. отношение было менее 0,4. У пациентов с панкреатогенным абсцессом установлены достоверные увеличение длины и уменьшение количества трещин по сравнению с данными при других экссудативных осложнениях ОДП (р < 0,05). При панкреатическом абсцессе у 37,5% больных количество трещин изменялось при повторном исследовании, тогда как у больных с ложной кистой и острым скоплением жидкости данный признак был стабильным. В группах больных с панкреатогенным абсцессом и ложной кистой преобладало деление кристаллов до ветвей 1-го порядка (68,7% и 61,8%), в фациях больных с острыми скоплениями жидкости деление кристаллов в большинстве случаев достигало 2-го порядка (69,2%). На основании анализа и сопоставления результатов кристаллографического исследования аспирата, клинической картины, результатов УЗТ, данных цитологического и бактериологического исследований полученного материала были выявлены наиболее информативные кристаллографические признаки фаций при ОДП, осложненном развитием различных экссудативных образований. Чувствительность, специфичность и точность кристаллографического метода исследования аспирата составили 91,8%, 93,3% и 92,3% соответственно.
Основой лечебных минимально инвазивных манипуляций при осложненном течении ОДП являлась комбинация диапевтических (пункционное лечение) и лечебных (установка дренажей) вмешательств. Точкой приложения для выполнения дренирующих вмешательств был ограниченный деструктивный процесс с преобладанием экссудативного компонента при наличии адекватного акустического окна. Всего выполнено 518 минимально инвазивных вмешательств с лечебной целью под контролем УЗТ и РТВ. В 92,8% случаев выполнение лечебных минимально инвазивных вмешательств на фоне активной комплексной консервативной терапии позволило купировать патологический процесс и избежать открытых оперативных вмешательств.
Трансабдоминальная УЗТ является быстрым и высокоинформативным неинвазивным методом прямой диагностики при развитии очаговых гнойно-некротических осложнений ОДП. Однако традиционные ультразвуковые признаки (контуры, размеры, эхогенность и т. д.) не несут принципиально новой информации о характере и динамике патологического процесса. При проведении эндокавитального УЗИ гнойной полости наблюдалось повышение информативности таких ультразвуковых признаков, как структура капсулы, эхоструктура стенки очага и его ультразвуковая пальпация, которые менее значимы при трансабдоминальной УЗТ. Качественно важной являлась комбинация традиционного и нового динамического признака: эхоструктура — подвижность; размер включения — степень фиксации к капсуле; эхооднородность содержимого — быстрота вымываемости из полости по дренажу. Именно они обладали минимальной вероятностью возникновения диагностической ошибки (–0,114; 0,098–0,12) по сравнению с трансабдоминальным ультразвуковым исследованием (0,876; 0,859–0,92).
ЗАКЛЮЧЕНИЕ
Острый деструктивный панкреатит (ОДП) в зависимости от фазы развития патологического процесса имеет полиморфную эхографическую картину. Диагностическая точность неинвазивной ультразвуковой томографии (УЗТ) в верификации стадии развития острого деструктивного панкреатита и характера его осложнений не превышает 89,6%, что определяет необходимость выполнения тонкоигольной диагностической пункции (ТДП). ТДП под контролем УЗТ с последующим микробиологическим и цитологическим исследованием аспирата является высокоинформативным методом диагностики характера поражения органа и детализации фазы развития патологического процесса. Минимально инвазивная биоимпедансометрия и кристаллография могут быть использованы для ранней уточняющей дифференциальной диагностики, прогнозирования течения экссудативных образований при ОДП и определения дальнейшей лечебной тактики. Перкутанные диапевтические технологии представляются эффективным минимально инвазивным методом лечения экссудативных и гнойных осложнений панкреонекроза. Использование эндокавитального ультразвукового исследования позволило оценить топографо-анатомические особенности органов в векторе изображения, направленном изнутри кнаружи, и провести сравнительный анализ ультразвуковой семиотики в комбинации количественных и динамических ультразвуковых признаков. Это дает качественно новую информацию о стадировании патологического процесса, что позволяет адекватно изменить дальнейшую диагностическую и лечебную тактику.








