Диспластические процессы шейки матки, а в последующем и рак шейки матки формируются на фоне эктопии, метаплазии. Это становится возможным вследствие бипотентных свойств резервных клеток эпителия шейки матки — их способности превращаться как в плоский, так и в цилиндрический эпителий. Именно резервные клетки служат резервуаром ВПЧ. ВПЧ является самой распространенной из всех урогенитальных инфекций, обладает значительной контагиозностью и высоким онкогенным потенциалом[6]. Этот вирус выявляют у 60% женщин с хроническими цервицитами, он нарушает структуру слизистой оболочки, поддерживает воспаление, вызывает (усиливает) супрессию иммунитета, как правило, сочетается с другими возбудителями, в 15–60% случаев ассоциируется с бактериальным вагинозом[1, 7].
У 70% молодых ВПЧ-инфицированных женщин ДНК вируса перестают обнаруживать на протяжении первых 24 месяцев наблюдения, в более старшем возрасте вирус может персистировать дольше[2]. У молодых женщин на фоне сопутствующих соматических и гинекологических заболеваний вирус активно функционирует, его репродукция в инфицированных клетках вызывает нарушение метаболизма эстрадиола с преобладанием 16α-гидроксиэстрона, который обладает самостоятельной канцерогенной активностью, стимулирует пролиферацию эпителия и экспрессию онкогенов вируса Е6 и Е7. Гиперэкспрессия онкобелка Е7 ВПЧ 16-го типа влияет на локальный гормональный статус и активирует процессы метилирования генов противоопухолевой защиты — супрессоров[3, 5]. Описаны более десяти генов-супрессоров опухолей (rb1, p15, p16, p21, p53, wt1 и др.), которые кодируют регуляторные белки, ингибирующие аномальный рост и трансформацию клеток[10]. Нарушение метилирования с аномалией гена-онкосупрессора р53 приводит к недостаточности апоптоза по отношению к пролиферации, что наблюдается при переходе цервикальной интраэпителиальной неоплазии (cervical intraepithelial neoplasia — CIN) I–II степени в СIN III и далее в рак шейки матки[4, 11].
Патогенез диспластического процесса и в последующем рака шейки матки схематично представлен на рисунке 1.
Рис. 1. Патогенез диспластического процесса при наличии вируса папилломы человека (ВПЧ) 16-го типа
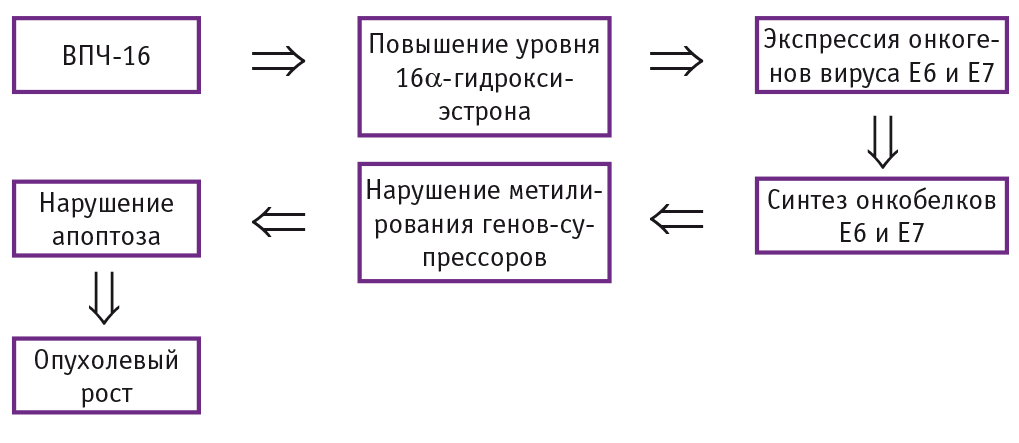
Очевидно, что предшествующие заболевания шейки матки и влагалища инфекционной и дисбиотической природы, нарушения гормонального гомеостаза у молодых женщин, инфицированных ВПЧ, способствуют развитию предраковых процессов шейки матки.
Цель исследования: оценка взаимосвязи нарушений репродуктивного здоровья и диспластических процессов шейки матки, определение их рациональной терапии.
МАТЕРИАЛЫ И МЕТОДЫ
В Клинике современной медицины г. Иваново (главный врач — к. м. н. О. А. Петрова) были обследованы 109 женщин в возрасте от 23 до 35 лет с дисплазией шейки матки: с CIN I — 28, с CIN II — 47 и с CIN III — 34 пациентки. Им проводили следующие диагностические мероприятия: расширенную кольпоскопию, цитологическое исследование, морфологическое исследование биопсийного материала, изучение микрофлоры влагалища с помощью системы ФЕМОФЛОР-17 и рН влагалища, молекулярно-биологическое тестирование на ВПЧ методом ПЦР, определение уровней гормонов сыворотки крови методом ИФА.
Статистическую обработку данных производили с помощью пакета прикладных программ Statistica 5.0 в системе Windows 2000. Статистически значимыми считали различия по критерию Стьюдента t > 2,0 при p < 0,05.
РЕЗУЛЬТАТЫ
В структуре вирусного инфицирования ВПЧ 16-го и 18-го типов составили 37,9% и 33,3% соответственно, другие онкогенные типы ВПЧ — 28,8%. Герпетическая инфекция была у 28,8% обследованных. Койлоцитоз в мазках обнаруживали у 88,1% участниц исследования, в том числе у 78,5% с CIN I, у 93,6% с CIN II и у 88,2% с CIN III. Дисбиоз влагалища диагностировали у 59,6% пациенток, при этом чаще при тяжелой стадии дисплазии, чем при легкой (76,5% и 50,0% соответственно).
Сопутствующие гинекологические заболевания имели место у 67 (61,5%) участниц исследования: остроконечные кондиломы влагалища и вульвы (38,5%), воспалительные заболевания матки (19,3%) и придатков матки (14,7%), мультифолликулярные яичники (14,7%), миома матки (8,2%), эндометриоз (9,1%), гиперпластические процессы эндометрия (25,0%), полипы цервикального канала (37,5%), диффузная мастопатия (56,2%). Диагноз мастопатии ставили на основании клинической картины и данных УЗИ. Бесплодие было у 12 (11,0%) женщин, в том числе первичное — у 8 (7,3%). Расстройства менструации выявлены у 59,4% обследованных, в том числе: дисменорея — у 53,0% из них, аномальные маточные кровотечения — у 18,8%. Их причинами стали хроническая ановуляция (у 28,1% женщин) и недостаточность лютеиновой фазы менструального цикла (у 31,3%), которые диагностировали на основании результатов тестов на овуляцию и фолликулометрии.
Клинические проявления андрогенозависимой дерматопатии и гирсутного синдрома наблюдали у 33,0% и 19,3% пациенток соответственно, галакторею — у 10,0%. Гиперандрогения по данным ИФА выявлена у 11,0% участниц исследования, гиперпролактинемия — у 9,2%. Проявления предменструального синдрома отмечали 14,7% женщин.
Сравнительная оценка частоты гинекологических заболеваний у пациенток с учетом степени развития у них диспластических процессов шейки матки показала, что частота нарушений репродуктивного здоровья возрастает по мере утяжеления степени дисплазии. Так, воспалительные болезни внутренних половых органов были выявлены у 17,8% женщин с CIN I, при умеренной дисплазии их частота возросла до 21,3%, при тяжелой дисплазии — до 55,9% (р < 0,01 для различия между пациентками с CIN III и с другими степенями CIN); миому матки обнаружили у 4,3%, 7,1% и 14,7% участниц исследования соответственно (р < 0,05 для различия между женщинами с CIN I и CIN III). Частота выявления миомы матки при легкой и умеренной, а также при умеренной и тяжелой степенях CIN статистически значимо не различалась.
Мастопатию несколько чаще диагностировали при CIN III (11,7%), чем при СIN I и CIN II (7,1% и 6,4% случаев соответственно, р > 0,05). Всех пациенток с CIN III перед выбором тактики лечения консультировал онколог.
НМФ отмечали у 14,3% обследованных с CIN I, у 25,5% с CIN II и у 41,2% c CIN III (р < 0,05 для различия между пациентками с CIN I и CIN III). Частота НМФ среди пациенток с легкой и умеренной, а также с умеренной и тяжелой степенями CIN статистически значимо не различалась. Гиперпластические процессы эндометрия развивались только у пациенток с умеренной и тяжелой дисплазией (у 12,7% и 29,4% соответственно). Бесплодие у женщин с CIN III диагностировали чаще, чем у пациенток с CIN II и СIN I (20,6%, 7,1% и 6,4% соответственно), однако выявленные различия не были статистически значимыми (р > 0,05).
На основании полученных данных были выбраны 66 женщин, лечение которым назначали с учетом степени диспластического процесса и дальнейших репродуктивных планов. В группе пациенток, планировавших беременность после лечения (n = 30), применяли дидрогестерон (Дюфастон) с 11–14-го или с 16-го дня цикла по 20 мг в день до наступления менструации. Cреди них CIN I была у 15, CIN II — у 8, CIN III — у 7 женщин. Пациентки, не планировавшие беременность (n = 36), использовали таргетную терапию в сочетании с комбинированными гормональными контрацептивами (КОК или вагинальным кольцом).
В обеих группах при наличии гиперпролактинемии в лечение включали препараты каберголина. При изменении содержания тиреотропного гормона и индекса инсулинорезистентности назначали консультацию эндокринолога для подбора дополнительной терапии. При проявлениях гирсутного синдрома и андрогенной дерматопатии лечение проводили совместно с дерматокосметологом.
При CIN I гормональную терапию осуществляли одновременно с местным противовоспалительным и противовирусным лечением. В качестве средства фотодинамической терапии применяли фотосенсибилизатор хлоринового ряда второго поколения на основе водорастворимой соли хлорина Е6. Для восстановления нормоценоза влагалища назначали терапию по следующей схеме: первый день — 1 таблетка аскорбиновой кислоты интравагинально для нормализации рН среды и повышения эффективности антимикробной терапии, затем курс противовоспалительной терапии (интерферон альфа-2b + метронидазол + флуконазол) в течение 10 дней, в последующие 5 дней — аскорбиновая кислота интравагинально по 1 таблетке для восстановления собственной микрофлоры влагалища и профилактики рецидивов.
При CIN II–III гормональное и противовирусное лечение (фотодинамическую терапию) начинали после деструктивного вмешательства на шейке матки — радиоволновой эксцизии.
Дидрогестерон выбран нами в связи с его самой высокой энергией связывания с прогестероновыми рецепторами и самой низкой энергией связывания с рецепторами к другим стероидам[8], возможностями подавления пролиферативных эффектов эстрогенов и эффективной подготовки к беременности. По данным отечественных и зарубежных авторов, дидрогестерон — высокоэффективное средство лечения аномальных маточных кровотечений, лютеиновой недостаточности, а также реабилитации поврежденного эндометрия[9, 12].
Через 6 месяцев оценивали эффективность лечения. Среди участниц исследования с легкой дисплазией нормальную кольпоскопическую картину наблюдали у 79,3%, признаки цервицита — у 13,8% женщин, неспецифические изменения диагностировали у 6,9%; цитограммы без особенностей были у 79,3%, воспалительные изменения в мазках — у 20,7% женщин. Результаты ПЦР-теста на онкогенные типы ВПЧ оказались отрицательными у всех пациенток с легкой дисплазией. Явления дисбиоза влагалища сохранялись у 9% женщин.
При умеренной и тяжелой дисплазии у большинства женщин (80,0% и 70,6% соответственно) наблюдалась нормальная кольпоскопическая картина. Признаки воспаления при CIN II и CIN III были выявлены соответственно у 20,0% и 29,4%, зоны ацетобелого эпителия — у 5,0% и 11,7% обследованных. У 75,0% пациенток с СIN II и у 76,5% с CIN III цитограмма была в норме, у остальных 25,0% и 23,5% участниц соответственно имели место признаки воспаления. У 10,0% пациенток с СIN II и у 17,6% с CIN III выявлены койлоциты. Выраженных аномальных цитограмм не обнаружено.
Положительные результаты ПЦР-теста получены у 5,0% пациенток при СIN II и у 5,8% при CIN III. Показатели кислотности влагалища нормализовались у большинства женщин с CIN II (85,0%) и CIN III (76,5%).
Частота расстройств менструации у выбранных нами 66 женщин до лечения составляла 75,6%, а через 6 месяцев после завершения лечения снизилась до 40,0% при использовании дидрогестерона (р < 0,05) и до 44,4% при применении гормональных контрацептивов (р < 0,05). Ановуляцию диагностировали до лечения у 63,6% из 66 пациенток, после лечения дидрогестероном она сохранялась у 20,0% (р < 0,01), после использования гормональной контрацепции — у 25,0% женщин (р < 0,01).
Мастопатия до лечения была у 81,8% пациенток, после лечения — у 48,5%: у 46,7% в группе дидрогестерона (р < 0,01) и у 50,0% в группе гормональной контрацепции (р < 0,05). Гиперпластические процессы эндометрия до лечения наблюдались у 53,3% пациенток, после терапии дидрогестероном — у 10,0% (р < 0,01), после применения гормональной контрацепции — у 5,6% (р < 0,01) (рис. 2).
Рис. 2. Частота сопутствующих гинекологических заболеваний у женщин с дисплазией шейки матки в динамике — до и после гормональной терапии, %.
Примечание. Отличия от исходных показателей статистически значимы: (*) — p < 0,05, (**) — p < 0,01
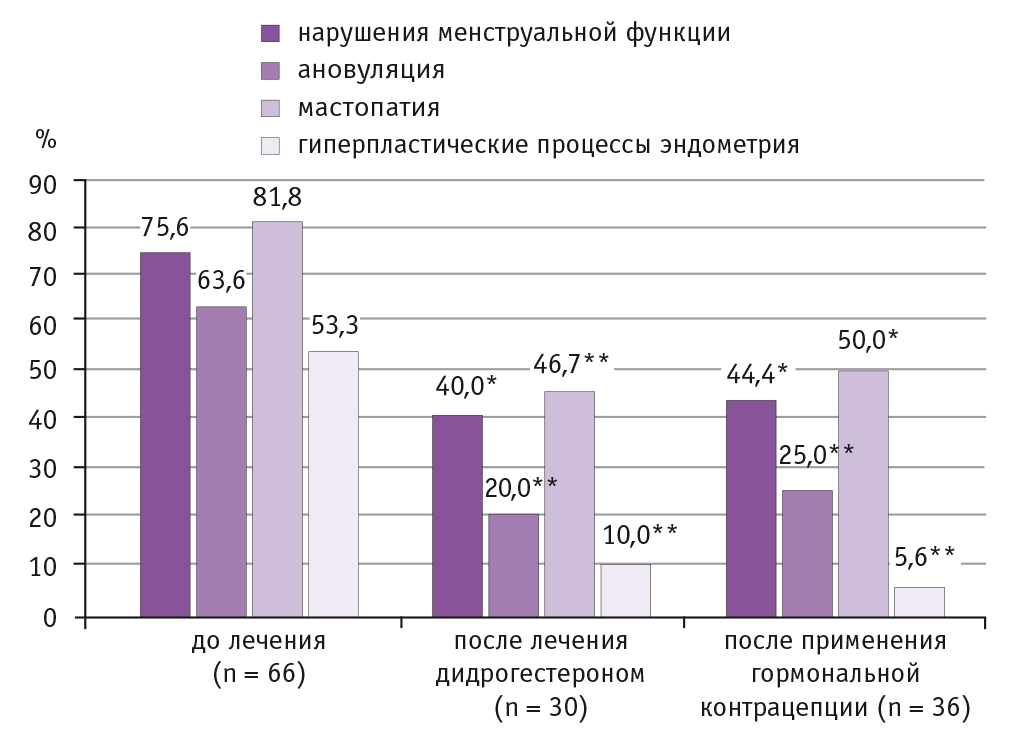
Результаты комплексного лечения у женщин с разной степенью тяжести поражения цервикального эпителия статистически значимо не различались. Улучшение показателей гинекологического здоровья наступало вне зависимости от степени CIN.
Анализ реализации репродуктивных планов у 30 женщин с СIN в течение 3 лет показал, что при использовании в составе комплексной терапии дидрогестерона беременность наступила у 25 (83,4%) из них: при CIN I — у 13 из 15, при СIN II — у 6 из 8, при CIN III — у 6 из 7 пациенток. В течение первого года после лечения беременность наступила у 8 из 30 женщин, принимавших дидрогестерон (26,7%), спустя 1,5 года и более — у 17 (56,7%). Бесплодие к концу третьего года наблюдения отмечено у 5 пациенток (16,7%).
Беременность завершилась родами у 17 (56,7%) женщин: своевременными — у 15, преждевременными — у 2. Роды per vias naturalis после лечения CIN I произошли у 8 из 10 женщин, при CIN II — у 3 из 4; при CIN III во всех случаях (n = 3) имело место оперативное родоразрешение. Самопроизвольный выкидыш в ранние сроки зафиксирован у 5 (16,7%) пациенток, в том числе у 3 женщин с CIN I, у одной с CIN II, у одной с CIN III. Медицинский аборт по желанию выполнен у 3 женщин (у одной с CIN II и у двух с CIN III).
ЗАКЛЮЧЕНИЕ
Высокая частота сопутствующих гинекологических заболеваний и гормональных нарушений у молодых женщин с развившимися диспластическими процессами шейки матки свидетельствует в пользу целесообразности использования в комплексном лечении гормональной терапии (дидрогестерона, КОК), что позволяет улучшить показатели гинекологического здоровья пациенток и в последующем способствовать успешной реализации их репродуктивных планов.








