Эндометриоз — широко распространенное гинекологическое заболевание, которым страдают до 10% женщин репродуктивного возраста[3, 8]. По данным эпидемиологических исследований, число больных эндометриозом достигает 176 млн[15]. Наибольшая частота выявления приходится на возраст от 25 до 34 лет, однако заболевание может дебютировать и гораздо раньше, вплоть до пубертата, что является предиктором тяжелого течения болезни[10]. Распространенность эндометриоза выше среди женщин с дисменореей (до 60%), бесплодием (до 50%) и хронической тазовой болью (до 75%)[1, 19, 28].
Эндометриоз — доброкачественное заболевание, субстратом которого является разрастание ткани, функционально и морфологически подобной нормальному эндометрию. Его отличают повышение локального образования эстрогенов и чувствительности к ним, а также резистентность к прогестерону. Сопутствующий воспалительный процесс, иммунологическая дисрегуляция, ингибирование апоптоза, активация ангиогенеза — патогенетические факторы, способствующие выживанию и росту эндометриоидных имплантов[14]. В большинстве случаев заболевание характеризуется прогрессирующим течением, при этом на фоне усиления клинической симптоматики (дисменорея, хроническая тазовая боль, диспареуния) при отсутствии эффективного лечения снижается качество жизни женщины[3, 7, 13, 21, 26].
Хотя клинические симптомы эндометриоза не являются патогномоничными, верификация диагноза с использованием современного диагностического оборудования не представляет существенных трудностей. «Золотой стандарт» диагностики эндометриоза — лапароскопия в сочетании с биопсией, однако эта инвазивная методика подходит не всем пациенткам. При наличии аденомиоза основной диагностический метод — сонография. Нехирургическая диагностика эндометриоза очень надежна[29]. При прогрессировании наружного эндометриоза на фоне пролиферации эндометриоидных гетеротопий в патологический процесс вовлекаются брюшина и соседние органы, что может приводить к формированию эндометриом, нарушению функций кишечника, мочевого пузыря и распространению спаечного процесса[15].
Ранняя диагностика эндометриоза — залог своевременного начала терапии, позволяющего предотвратить прогрессирование заболевания, снизить риск бесплодия и улучшить качество жизни женщины. Однако отсроченный период верификации диагноза в среднем составляет 6–7 лет[23].
Основная цель лечения — уменьшение объема эндометриоидных поражений[11, 13, 16]. Применяют сочетание хирургического и медикаментозного лечения, при этом глобального терапевтического подхода не выработано. Согласно определению Американского общества репродуктивной медицины, «эндометриоз стоит рассматривать как хроническое заболевание, требующее разработки стратегии длительного лечения, целью которого являются максимальное использование медикаментозной терапии и, по возможности, отказ от повторных хирургических вмешательств»[28]. Метод лечения должен определяться индивидуально. В связи с тем что ранний дебют влечет за собой более тяжелое течение заболевания и в большинстве случаев приводит к инвалидности, у таких пациенток особенно важно своевременное начало терапии[7, 20].
Обычно эндометриоз приводит к развитию относительной и/или абсолютной гиперэстрогении при количественном или качественном дефиците прогестерона. Поэтому патогенетической основой медикаментозной терапии является временное угнетение функции яичников, направленное на регресс очагов эндометриоза[5].
Для лечения могут применяться различные варианты медикаментозной терапии, однако наиболее эффективны агонисты гонадотропин-рилизинг-гормона (ГнРГ), даназол и некоторые прогестагены, рекомендованные для лечения эндометриоза. Гормональная терапия вызывает атрофию эндометриоидных очагов, воздействуя патогенетически, в том числе на рецепторном уровне[3, 7, 20].
Агонисты ГнРГ — «золотой стандарт» медикаментозной терапии эндометриоза; эти средства, бесспорно, высокоэффективны, однако их использование может быть ограничено сроком возможного применения и переносимостью ятрогенной псевдоменопаузы на фоне развивающегося дефицита эстрогенов[17]. При использовании агонистов ГнРГ более 6 месяцев (без «терапии прикрытия» эстрогенами) возникают нежелательные гипоэстрогенные эффекты, как то: приливы, сухость влагалища, снижение либидо, головная боль, — а также повышается риск уменьшения минеральной плотности костной ткани[1, 4, 6].
При тяжелой степени эндометриоза для преодоления бесплодия в большинстве ситуаций приходится прибегать к вспомогательным репродуктивным технологиям (ВРТ)[1]. Назначение агонистов ГнРГ при ассоциированном с эндометриозом бесплодии имеет ряд преимуществ ввиду того, что на фоне лечения не подавляется активность эндогенного ГнРГ, поэтому на этапе подготовки инфертильных пациенток к ВРТ этот класс препаратов традиционно рассматривают как приоритетный[5, 7, 9].
Даназол и прогестагены тоже оказывают центральное воздействие, подавляя активность системы «гипоталамус — гипофиз — яичники» и снижая тем самым секрецию эстрогенов. Их широкое применение насчитывает несколько десятков лет, однако даназол в последние годы практически не используется из-за серьезных побочных эффектов, а большинство прогестагенов не имеют соответствующих показаний[5, 7].
В зарубежных и отечественном руководствах в качестве средства специфической терапии эндометриоза указан диеногест[7, 18, 22]. Диеногест — хорошо изученный пероральный прогестаген, специально созданный для лечения эндометриоза[3, 27]. При непрерывном применении он воздействует непосредственно на очаги эндометриоза, вызывая децидуализацию стромальных клеток и атрофию железистого компонента гетеротопий. Умеренная выраженность антигонадотропного влияния диеногеста позволяет избежать клинически манифестных приливов и ятрогенного риска деминерализации костной ткани у большинства пациенток. Он также активирует фермент 17β-гидроксистероид-дегидрогеназа, преобразующий эстрадиол в слабый эстрон, что изменяет баланс эстрогенов на локальном уровне[12]; оказывает противовоспалительное действие, блокируя циклооксигеназу; подавляет неоангиогенез и нормализует иммунный баланс в перитонеальной жидкости[3, 5]. Благодаря антипролиферативному влиянию диеногеста эндометриоидные гетеротопии полностью исчезают или значительно уменьшаются[1, 3, 24, 26].
Данные клинических исследований, участницы которых получали диеногест, свидетельствуют, что этот препарат имеет благоприятный профиль безопасности, эффективен и хорошо переносится[2, 5, 21, 24]. При долгосрочном применении (сроком до 15 месяцев) благоприятные эффекты диеногеста после его отмены сохраняются в течение 24 недель наблюдения[26].
Эффективная, безопасная и хорошо переносимая терапия диеногестом, пригодная для долгосрочного применения, может не только преследовать чисто лечебные цели, но и быть резервом на этапе прегравидарной подготовки инфертильных пациенток к применению ВРТ[5].
Преодоление бесплодия, обусловленного эндометриозом, вызывает значительные трудности, поскольку до настоящего времени, несмотря на огромное число научных исследований, нет четкого представления о патофизиологических механизмах, препятствующих наступлению беременности, особенно при малых и умеренных формах заболевания. Долгое время не находили эффективного средства лечения эндометриоза, которое бы хорошо переносилось и предсказуемо влияло на овуляцию и сроки восстановления фертильности после прекращения его применения[6].
В литературе представлены данные о том, что у женщин с эндометриозом, особенно с рецидивами заболевания, подавление функции яичников агонистами ГнРГ в течение 3–6 месяцев увеличивает результативность экстракорпорального оплодотворения (ЭКО)[25]. Диеногест ингибирует овуляцию на период лечения, не оказывая негативного влияния на восстановление фертильности после отмены терапии. Поскольку существует очевидная взаимосвязь эндометриоза с бесплодием и значительное снижение индекса фертильности при нем — доказанный факт, представляется обоснованным проведение исследования по изучению эффективности применения диеногеста у женщин с эндометриозом и бесплодием перед проведением ЭКО.
Цели исследования: 1) разработать схемы и оценить эффективность терапии диеногестом при аденомиозе различной степени тяжести на этапе подготовки к лечению бесплодия методом ЭКО; 2) оценить эффективность преодоления бесплодного брака методом ЭКО после комплексной терапии с использованием диеногеста.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проведено в ООО «Клиника ВРТ "Дети из пробирки"» (директор клиники — д. м. н. Э. В. Вартанян) — на клинической базе кафедры акушерства, гинекологии и репродуктивной медицины факультета повышения квалификации медицинских работников Медицинского института РУДН (заведующий кафедрой — засл. деятель науки РФ, профессор В. Е. Радзинский) — в период с 01.07.2014 по 15.04.2015. В исследование включили 56 пациенток с аденомиозом различной степени тяжести (в том числе с сочетанными формами эндометриоза) в возрасте от 25 до 44 лет (средний возраст — 36,6 ± 4,2 года), получавших лечение бесплодия методом ЭКО. Все пациентки отмечали неэффективность проведенной ранее консервативной терапии эндометриоза, страдали бесплодием более 3 лет, имели в анамнезе попытки преодоления бесплодия методом ЭКО. У каждой четвертой из них (25,0%) имели место две и более неудачи ЭКО.
Критериями включения в исследование служили верифицированный эндометриоз, длительность заболевания свыше 3 лет, бесплодный брак. Критерии исключения: возраст младше 25 лет в сочетании с исходно сниженным овариальным резервом, наличие тяжелых экстрагенитальных заболеваний, а также указание в анамнезе на факт рецидива эндометриоидных кист яичников. По степени тяжести заболевания пациентки были стратифицированы на две группы: первая группа — 35 женщин с аденомиозом I–II степени тяжести, вторая группа — 21 пациентка с аденомиозом III степени тяжести.
Учитывая наличие бесплодного брака, все супружеские пары проходили обследование согласно алгоритму, разработанному в клинике ВРТ «Дети из пробирки». Алгоритм включал в себя:
- клинико-анамнестическое рутинное обследование: анамнез жизни (перенесенные заболевания, оперативные вмешательства, наличие профессиональных вредностей и привычных интоксикаций), анамнез фертильности пары, физикальное обследование, лабораторные исследования на наличие урогенитальной инфекции, гормональный скрининг, оценку менструального цикла и овариального резерва;
- обследование смежными специалистами при наличии экстрагенитальных заболеваний;
- инструментальное обследование: ультразвуковое исследование, доплерометрию сосудов матки в период предполагаемого окна имплантации, а также гистероскопию и лапароскопию по показаниям;
- генетическое обследование (кариотипирование): исследование Х-хромосомы, гена муковисцидоза и генов гемостаза;
- иммунологическое обследование женщин: определение антител к фосфолипидам, исследование спектра волчаночных и антиспермальных антител;
- иммуногенетическое обследование супружеской пары на определение HLA-совместимости II класса.
Разработанная схема терапии диеногестом включала в себя консервативное лечение аденомиоза в течение 4–6 месяцев (в зависимости от степени тяжести основного заболевания) с последующим применением препарата агониста ГнРГ в течение 14 дней в непрерывном режиме и с непосредственным переходом к протоколу ЭКО. Диеногест назначали в дозе 2 мг (пероральный прием) в непрерывном режиме: при аденомиозе I–II степени в течение 4 месяцев, а при аденомиозе III степени на протяжении 6 месяцев.
Для оценки эффективности лечения применяли двойной контроль. На первом этапе проводили анкетирование для уточнения характера жалоб и определение исходных показателей гемодинамики матки. Для динамической оценки интенсивности болевого синдрома (до начала терапии, далее ежемесячно до ее окончания) использовали визуальную аналоговую шкалу (ВАШ) в баллах: от 0 (нет боли) до 10 (нестерпимая боль). На втором этапе также оценивали изменения гемодинамики матки — по окончании терапии диеногестом перед переходом к протоколу ЭКО.
Особенности протокола ЭКО у пациенток с эндометриозом: непосредственно после окончания терапии диеногестом применяли длинный протокол с использованием агониста ГнРГ трипторелина ацетата в дозе 0,1 мг/сут. Всем женщинам также назначали противовоспалительную терапию нестероидными противовоспалительными препаратами: индометацин, суппозитории ректальные, в дозе 100 мг/сут в течение 10 дней. В посттрансферном периоде женщины получали медикаментозную поддержку дидрогестероном в дозе 20–40 мг/сут (пероральный прием).
Математическую обработку полученных результатов производили с использованием описательной статистики на персональном компьютере с помощью программы Exсel 2007. Доверительный интервал указан как M ± m, где M — медиана, а m = 2σ. Различия считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
Средний возраст в группах не различался и составил 36,6 ± 4,2 года, однако среди пациенток с аденомиозом III степени преобладали женщины 40 лет и старше: 42,8% против 17,1% пациенток с аденомиозом I–II степени (p < 0,05).
Длительность бесплодия в группах существенно различалась в зависимости от степени тяжести аденомиоза: 4,1 ± 0,7 года в первой группе против 11,6 ± 2,4 года во второй. Структура бесплодия имела особенности: во второй группе установлена более высокая частота длительного первичного бесплодия (76,2% наблюдений по сравнению с 25,7% в первой группе); вторичное бесплодие чаще было зарегистрировано у женщин первой группы (74,3% против 23,8% во второй группе). В обоих случаях различия были статистически значимы (p < 0,05).
Сочетание аденомиоза с наружным генитальным эндометриозом в первой группе имело место в 48,6% наблюдений против 14,3% во второй группе (p < 0,05). ЭКО было в анамнезе у 45,7% женщин из первой группы и у 52,4% из второй. Более высокая частота неудачных попыток ЭКО (две и более) отмечена у пациенток второй группы: 72,7% против 37,5% у женщин первой группы (р < 0,05).
Клиническое улучшение заключалось в уменьшении болезненности и продолжительности менструаций у 68,6% пациенток первой и у 61,9% женщин второй группы. Регресс тазовой боли (в баллах по ВАШ) к моменту окончания терапии отметили 74,3% участниц первой и 66,7% женщин второй группы (рис.).
Рис. Динамика регресса хронической тазовой боли у пациенток сравниваемых групп, баллы
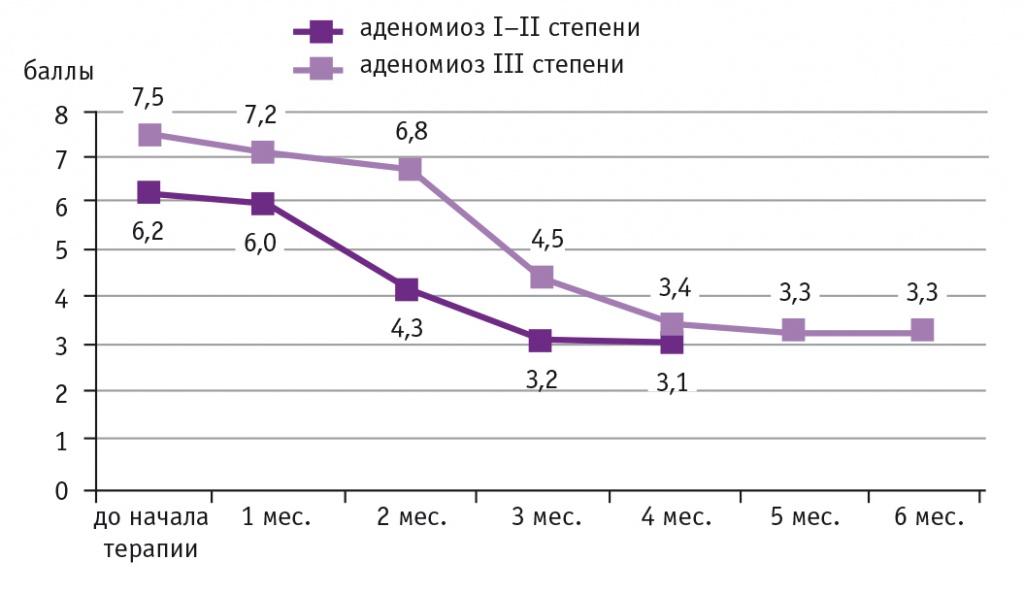
У половины (48,6%) женщин в первой группе и у каждой пятой (19,0%) во второй при динамической оценке маточной гемодинамики выявлена нормализация показателей кровотока в различных сегментах сосудистого дерева матки, что впоследствии сделало возможным успешное лечение бесплодия методом ЭКО (табл.).
Таблица
Индекс резистентности в сосудистом русле матки у пациенток сравниваемых групп, M ± m
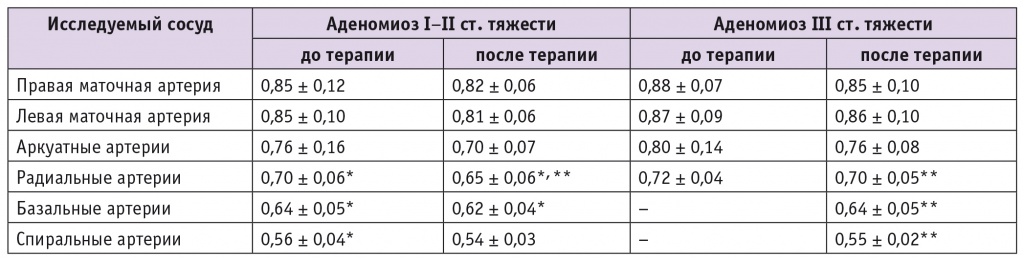
* Различия между группами статистически значимы (р < 0,05).
** Различия между показателями до и после лечения статистически значимы (р < 0,05).
Примечание. Прочерки стоят в тех случаях, когда цифровые величины получить не удалось, т. е. кровоток не зарегистрирован.
При анализе эффективности терапии диеногестом зафиксированы как внутригрупповые, так и межгрупповые статистически значимые различия в показателях индекса резистентности в разных сегментах сосудистой сетки матки. Что касается эффективности применения ЭКО, то в первой группе этот показатель составил 48,6%, во второй — 23,8% (p < 0,05).
ЗАКЛЮЧЕНИЕ
Полученные данные дополняют существующие теоретические положения о том, что диеногест при хорошей переносимости и минимальных метаболических эффектах обеспечивает стойкое клиническое улучшение, и, на наш взгляд, он может считаться препаратом выбора медикаментозной терапии эндометриоза у инфертильных пациенток на этапе подготовки к лечению бесплодия методом ЭКО.
Предпочтительно проводить консервативную терапию аденомиоза диеногестом в течение 4–6 месяцев на этапе подготовки к ЭКО. Продолжительность терапии зависит от степени тяжести эндометриоидного поражения: при аденомиозе I–II степени тяжести мы считаем целесообразным проводить терапию диеногестом в дозе 2 мг/сут в течение 4 месяцев, а при аденомиозе III степени — в течение 6 месяцев с непосредственным переходом к протоколу ЭКО.
Эффективная терапия диеногестом аденомиоза различной степени тяжести (в том числе при сочетании с наружными формами эндометриоза) повышает эффективность ЭКО, в том числе у пациенток с длительным бесплодием и неудачами ЭКО в анамнезе.








