ВВЕДЕНИЕ
Менопаузальная гормональная терапия остается «золотым стандартом» лечения климактерических симптомов, отдаленных последствий гипоэстрогении и ряда возраст-ассоциированных заболеваний[1]. При наличии противопоказаний к назначению эстрогенсодержащих препаратов, на этапе обследования или при нежелании пациенткой принимать гормональную терапию рекомендуется использовать альтернативные средства[1], в том числе растительного происхождения. Фитоэстрогены — соединения, которые образуются растениями путем фотохимического биосинтеза, способные связывать рецепторы эстрогенов (РЭ) млекопитающих и обладающие эстрогеноподобными свойствами.
Основными классами фитоэстрогенов, относящихся к полифенольным соединениям, являются флавоноиды, фенольные кислоты, лигнаны и стильбены. Наиболее известным и изученным фитоэстрогеном является ресвератрол (3,4,5-тригидрокси-транс(цис-)-стильбен), синтезируемый в качестве защитного вещества, повышающего устойчивость растений к неблагоприятным воздействиям, в том числе чрезмерному ультрафиолетовому излучению, экстремальным температурам, бактериям, грибам или механическим повреждениям. Первоначально ресвератрол был охарактеризован как фитоалексин из-за его фунгицидных свойств, но позднее подтвержден широкий спектр его биологической активности, значимой для профилактики и лечения различных заболеваний[2]. В настоящее время опубликовано более 17 тысяч научных отчетов о свойствах ресвератрола, охватывающих как фундаментальные, так и клинические исследования[3].
Потенциальными продуцентами ресвератрола являются более 72 видов растений. Его источниками могут служить ягоды красного, синего и темно-фиолетового цвета (малина, черника, шелковица и др.), фрукты (гранат и др.), бобы (какао) и орехи (арахис). Большинство растительных источников ресвератрола чрезвычайно богаты фруктозой, и их употребление в больших количествах неприемлемо при ряде заболеваний, в том числе при сахарном диабете или инсулинорезистентности. В фармацевтической промышленности транс-ресвератрол получают из лекарственного растительного сырья — корней и корневищ рейнутрии японской (лат. Polygonum сuspidatum). В данном растительном сырье содержание ресвератрола в 50–70 раз выше, чем в любом другом природном источнике. Такое производство позволяет получить эффективные и безопасные биологические активные добавки, содержащие транс-ресвератрол, которые возможно применять пациентам с метаболическими нарушениями.
ФАРМАКОКИНЕТИКА
Ресвератрол образуется из фенилаланина и существует в двух изомерных формах: цис-ресвератрола и более стабильной транс-формы. Короткий период полувыведения (около 1,5 ч) из-за быстрого всасывания в кишечнике и метаболизма в печени, низкая биодоступность и растворимость в воде являются одними из важнейших ограничений клинического применения ресвератрола. В последнее десятилетие для повышения биодоступности ресвератрола разработаны различные системы доставки, такие как инкапсуляция в липидные наноносители (липосомы), наноэмульсии, мицеллы, полимерные наночастицы, твердые дисперсии. Значительно повысить растворимость ресвератрола, обеспечивая медленное высвобождение действующего вещества, облегчая мембранный пассивный транспорт и клеточный захват, позволяют наноэмульсии[4].
После перорального приема ресвератрол абсорбируется кишечным эпителием путем пассивной диффузии или мембранными переносчиками и высвобождается в кровоток как в неизмененном виде, так и в виде метаболитов после глюкуронизации и сульфатной конъюгации фенольных групп и гидрирования алифатической двойной связи. В кровотоке ресвератрол связывается с транспортерами, в том числе альбуминами и липопротеинами низкой плотности, образуя комплексы, которые могут диссоциировать на клеточной мембране, где транспортеры взаимодействуют с соответствующими рецепторами и обеспечивают транспорт ресвератрола в клетки. Большинство метаболитов ресвератрола в плазме имеют низкую биологическую активность, а их период полувыведения и концентрация в плазме крови в 10 раз выше, чем нативного соединения. Основной метаболизм ресвератрола и его производных происходит в печени[5, 6].
ТЕРАПЕВТИЧЕСКИЕ СВОЙСТВА И КЛИНИЧЕСКОЕ ПРИМЕНЕНИЕ
Механизмы действия ресвератрола связаны со способностью модулировать множество сигнальных путей клеточного метаболизма и экспрессии генов. Наиболее значимыми мишенями реализации фармакологических эффектов ресвератрола, связанных с эстрогеноподобным, противовоспалительным, антиоксидантным, антипролиферативным действием, являются АМФ-активированная протеинкиназа и сиртуин-1[7, 8].
Эстрогеноподобные эффекты
Ресвератрол относится к семейству полифенольных соединений, которые структурно или функционально имитируют эффект эстрогена в репродуктивной системе млекопитающих[9]. В отличие от большинства фитоэстрогенов ресвератрол связывается как с α-, так и, с некоторым преимуществом, с β-эстрогеновыми рецепторами, что обеспечивает более широкий спектр действия по сравнению с другими фитоэстрогенами[10]. Кроме того, ресвератрол взаимодействует с мембранными рецепторами и модулирует негеномную эстрогенную активность.
Эстрогеноподобные эффекты ресвератрола зависят от уровня эндогенных эстрогенов. При сниженном уровне эстрадиола он проявляет агонистическую активность. Так, согласно данным рандомизированного контролируемого двойного слепого исследования L. Leo и соавт. сублингвальный транс-ресвератрол снижает количество и интенсивность умеренных и тяжелых вазомоторных эпизодов в период менопаузального перехода у 78,6% пациентов (р < 0,001)[11].
Эстрогеноподобное действие ресвератрола проявляется в позитивных эффектах как при ранних симптомах климакса, включая приливы, потливость, нарушение сна, так и поздних метаболических нарушениях, в том числе снижении минеральной плотности костной ткани[12]. Протективное действие на костную ткань связано с увеличением экспрессии остеопротегерина — белка, который ингибирует RANKL (лиганд рецептора-активатора ядерного фактора κB), противодействующего дифференцировке остеокластов на стадии предшественника и зрелых форм. Доклинические исследования показали, что ресвератрол может стимулировать пролиферацию и дифференцировку костных клеток и подавлять апоптоз хондроцитов за счет противовоспалительных механизмов.
Как фитоэстроген ресвератрол регулирует экспрессию рецепторов витамина D в остеобластоподобных клетках, влияя на костеобразование. По сравнению с монотерапией ресвератролом его комбинация с витамином D увеличивает внутриклеточную концентрацию фитоэстрогена, повышает активацию β-РЭ и экспрессию рецептора витамина D, что приводило к улучшению биодоступности как ресвератрола, так и витамина D, тем самым повышая их способность быстро проникать сквозь клеточную мембрану и достигать тканей-мишеней[13].
По данным R. Milia, применение трансресвератрола у женщин в постменопаузе в виде сублингвального спрея в течение 3 мес достоверно снижало выраженность вазомоторных симптомов, раздражительность, депрессивные расстройства, суставную и мышечную боль[14]. Результаты данного исследования подтвердили эффективность сублингвальной формы транс-ресвератрола для коррекции климактерического синдрома у женщин в постменопаузе.
В России данная форма транс-ресвератрола представлена сублингвальными таблетками и сублингвальным спреем, содержащими транс-ресвератрол в комбинации с витаминами D3 и E в форме наноэмульсии. Инновационная запатентованная технология доставки компонентов NANOEMULSION DELIVERY SYSTEM® обеспечивает наиболее высокую биодоступность транс-ресвератрола. «Транс-ресвератрол в форме сублингвальных таблеток применяется для профилактики и купирования менопаузальных симптомов в качестве базовой терапии. Транс-ресвератрол в форме сублингвального спрея эффективен в качестве скоропомощного средства при приливах жара как самостоятельно, так и в дополнение к любому виду терапии климактерических расстройств, в том числе менопаузальной гормональной терапии (рис. 1). Сублингвальный транс-ресвератрол возможно применять при климактерических проявлениях у женщин в период менопаузального перехода с эндометриозом в анамнезе. Данный порядок назначения был отражен в алгоритмах ведения пациенток с эндометриозом, где была широко рассмотрена тактика назначения терапии у пациенток с менопаузальными симптомами[15].
Рис. 1. Алгоритм выбора транс-ресвератрола в форме сублингвальных таблеток и сублингвального спрея для коррекции менопаузальных расстройств
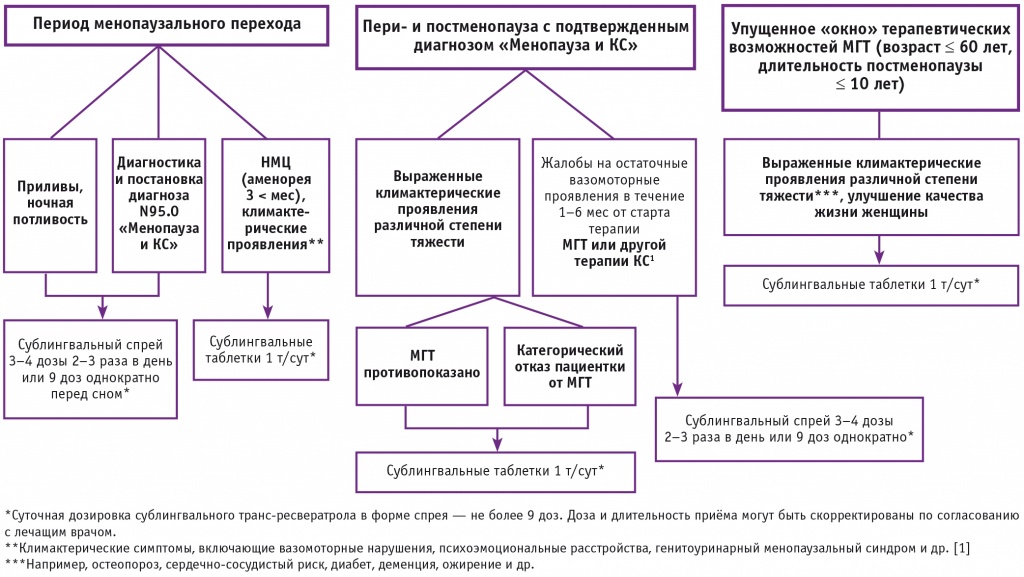
Основное преимущество сублингвального наноспрея заключается в скорости купирования вазомоторных эпизодов, именно поэтому его можно применять в тех ситуациях, когда требуется немедленное воздействие на приливы жара, — в момент приступа. Комбинация транс-ресвератрола, витамина D3 и витамина Е в виде сублингвальной эмульсии-спрея, приводит к статистически значимому снижению частоты и выраженности приливов[14]. При остаточных вазомоторных проявлениях целесообразно сочетание сублингвальных таблеток и сублингвального спрея. Дозы могут быть скорректированы с учётом выраженности симптомов и индивидуальных потребностей пациентки.
Целесообразно длительное применение ресвератрола. Согласно данным рандомизированных клинических исследований ресвератрол продемонстрировал благоприятный профиль эффективности при применении в течение 12, 24 мес[12].
Эффекты ресвератрола не ограничиваются влиянием на РЭ. Доказаны его антиоксидантные, противовоспалительные, противоопухолевые, антибактериальные, противогрибковые, противовирусные свойства, профилактический эффект в отношении развития метаболических, сердечно-сосудистых заболеваний, онкологической патологии, нейродегенеративных расстройств, в том числе болезни Альцгеймера, связанного с возрастом снижения тургора и эластичности кожи[16–19].
Антипролиферативное (противоопухолевое) действие
Ресвератрол как in vitro, так и in vivo показал эффективность при лечении рака, в том числе рака молочной железы в постменопаузе, в качестве дополнительного средства, усиливающего действие традиционной химиотерапии и сенсибилизирущего устойчивые опухолевые клетки к цитотоксичным препаратам (доцетакселу, паклитакселу, цисплатину, доксорубицину). Антипролиферативный эффект ресвератрола был установлен на клетках карциномы молочной железы человека и включал ингибирование клеточной пролиферации, снижение жизнеспособности клеток, инвазии и метастазирования. Ресвератрол подавлял рост как РЭ-позитивных, так и РЭ-негативных клеток, т.е. оказывал универсальный антипролиферативный эффект, активируя апоптоз и блокируя опосредованное 17β-эстрадиолом повреждение ДНК тканей молочной железы и эндометрия[20, 21].
Ресвератрол реализует противоопухолевые эффекты благодаря широкому спектру активности, включая антиоксидантные свойства и механизмы, регулирующие экспрессию проапоптотических белков, лежащих в основе развития опухоли. Антипролиферативная активность ресвератрола связана с активацией ряда внутриклеточных сигнальных путей, регулирующих рост и деление клеток, а также апоптоз.
Наиболее изученными внутриклеточными сигнальными механизмами ресвератрола являются:
-
индукция экспрессии опухолевого супрессора белка р53, регулирующего апоптоз и транскрипцию поврежденных ДНК;
-
активация каспаз 7 и 9;
-
торможение экспрессии или стимуляции расщепления белков, участвующих в канцерогенезе, таких как фосфолипидная скремблаза 1, каспаза-3, прокаспаза-8;
-
подавление фосфорилирования протеиназы mTOR (target of rapamycin) и многих других сигнальных путей опухолевого роста;
-
ингибирование сигнального пути синтазы жирных кислот (один из механизмов подавления пролиферации клеток рака молочной железы)[22–24].
В многочисленных исследованиях доказано влияние ресвератрола на некоторые биомаркеры рака. Так, ресвератрол подавляет плазменный инсулиноподобный фактор роста-1 и инсулиноподобный фактор роста, связывающий белок-3, которые являются белками сигнального пути инсулина, ответственными за онкогенез. Кроме того, ресвератрол снижает ДНК-связывающую активность ядерного фактора kВ, способствующего транскрипции генов, индуцирующих не только пролиферацию опухолевых клеток, но и экспрессию воспалительных цитокинов: интерлейкинов (ИЛ) -1, -6, -10 и фактора некроза опухоли-α (ФНО-α). Введение ресвератрола связано со значительным повышением уровня иммуномодулирующих Т-клеток и высоким антипролиферативным эффектом[25, 26].
Одним из механизмов противоопухолевой активности ресвератрола является активация аутофагии — протеолитического внутриклеточного процесса деградации в лизосомах продуктов клеточного метаболизма, агрегированных белков, поврежденных органелл (митохондрии, эндоплазматический ретикулум и др.). На раннем этапе онкогенеза аутофагия ингибирует рост опухоли. Однако нарушение механизмов аутофагии может привести к развитию различных заболеваний, таких как рак, нейродегенеративные расстройства, а также гибели клеток. Таким образом, ресвератрол, обладая модулирующими эффектами на процессы онкогенеза, может являться эффективной интервенционной стратегией противоопухолевой терапии с благоприятным профилем безопасности. Это позволяет рассмотреть опцию применения ресвератрола в качестве пищевой добавки женщинам высокой группы онкологического риска (например, с РМЖ в анамнезе)[26].
Противовоспалительное действие
Многочисленные клинические и экспериментальные исследования подтвердили мощный противовоспалительный эффект ресвератрола за счет значительного подавления провоспалительных реакций, маркеров воспаления и оксидантного стресса, в том числе циклооксигеназы-1, ФНО-α, ИЛ-6, ИЛ-8, p47hox, JNK1 и др.[27, 28]. Ресвератрол способен также подавлять нейровоспаление, опосредованное микроглией, и защищать нейроны от воспалительного повреждения, в том числе этанол-индуцированного[29–32].
Хроническое воспаление является патофизиологическим триггером многих метаболических заболеваний, включая ожирение, сахарный диабет 2 типа, нарушение толерантности к глюкозе и развитие резистентности к инсулину. Метаболические эффекты ресвератрола реализуются через сигнальный путь АМФ-активированной протеинкиназы стимуляцией липолиза, торможением биосинтеза холестерина и триглицеридов, активацией гликолиза в печени и мышцах, усилением выработки инсулина. В плацебо-контролируемом клиническом исследовании A. Movahed и соавт. результатом введения 1 г ресвератрола в течение 45 дней пациентам с сахарным диабетом 2 типа явились ключевые антидиабетические эффекты в виде снижения уровня глюкозы в крови натощак, гемоглобина A1c, уровня инсулина и резистентности к инсулину, а также значительного повышения уровня холестерина липопротеинов высокой плотности[33]. P. Brasnyó и соавт. доказали, что более низкие дозы ресвератрола (10 мг/сут), получаемые пациентами с сахарным диабетом в течение 4 нед, также снижают уровень гликемии и повышают чувствительность к инсулину. При этом повышение чувствительности к инсулину коррелировало со снижением маркера окислительного стресса орто-тирозина в моче и увеличением фосфорилирования протеинкиназы В, которая является ключевым сигнальным фактором инсулина[34]. Метаанализ K. Liu и соавт. показал, что ресвератрол более эффективен в борьбе с диабетом при введении в низких дозах[35].
Метаболические, противовоспалительные и антиоксидантные эффекты ресвератрола составляют основу протективного влияния на сердечно-сосудистую заболеваемость, связанную с гипертензией, гиперлипидемией, атеросклеротическим поражением сосудистой стенки и диабетом. Ресвератрол продемонстрировал терапевтический потенциал по снижению уровней сердечно-сосудистых факторов риска, в том числе аполипопротеина В, холестерина, липопротеинов низкой плотности. Прием пищевых добавок ресвератрола и продуктов с высоким содержанием ресвератрола связан со снижением риска сердечно-сосудистых событий, улучшением липидного профиля крови и уровня гликемии натощак[36–39].
Антиоксидантная активность
Окислительный стресс, вызванный накоплением активированных форм кислорода (АФК), лежит в основе многих возраст-ассоциированных заболеваний, включая сердечно-сосудистые, нейродегенеративные, рак и диабет. АФК вызывают воспаление, нарушение регуляции митохондрий и гибель клеток. Ресвератрол проявляет сильную антиоксидантную активность, главным образом за счет контроля основных антиоксидантных ферментов и блокирования повреждения ДНК свободными радикалами. Антиоксидантные эффекты ресвератрола связаны с наличием в его структуре трех гидроксильных групп, которые действуют как «ловушки» свободных радикалов, а также подавлением синтеза оксида азота. В фибробластах, астроглиальных и многих типах клеток ресвератрол уменьшает фрагментацию митохондрий, поддерживает потенциал митохондриальной мембраны, а также предотвращает ослабление окислительного фосфорилирования и гиперпродукцию АФК[40, 41].
Антивозрастные и дерматопротекторные эффекты
Продолжительность жизни организма в значительной степени определяется его способностью противостоять стрессовым воздействиям — как метаболическим, так и генотоксическим. Дефекты в механизмах противодействия метаболическим стрессам ведут к повреждению соматических клеток, а противодействия генотоксическим стрессам — к повреждениям генома и нарушению процессов обновления и пролиферации клеток. Регуляция клеточного апоптоза, системного метаболизма и мощный антиоксидантный эффект являются основой антивозрастного и дерматопротективного действия ресвератрола, опосредованного активацией сигнальных внутриклеточных мишеней, в том числе сиртуинов и АМФ-активированной протеинкиназы[42].
Сиртуины — это НАД-зависимые деацетилазы, которые контролируют апоптоз, клеточное репрограммирование, репарацию ДНК. Сиртуины также вовлечены в регуляцию прогрессии рака, старения яичников, окислительно-восстановительного гомеостаза и углеводно-липидного метаболизма. У млекопитающих идентифицированы 7 членов семейства сиртуинов (SIRT1-7), которые контролируют функции многих органов, в частности яичников. Ресвератрол является наиболее мощным природным лигандом SIRT1. Активированный SIRT1 связывает различные молекулярные мишени, включая NF-κB, p53, белки семейства FOXO (forkhead box O) -1, -3, -4, фактор, индуцируемый гипоксией, 2α (HIF-2α) и др. Активируя эти молекулы, ресвератрол регулирует энергетический гомеостаз, сайленсинг генов, стабильность генома и жизнеспособность клеток. FOXO являются транскрипционными факторами, контролирующими экспрессию генов, ответственных за пролиферацию, дифференцировку, апоптоз и реакцию клеток на внешние стрессы. Регулируя экспрессию генов-мишеней, FOXO защищают организм от неблагоприятных внешних воздействий, активируют защитные механизмы и тем самым замедляют процессы старения. Существуют и другие механизмы антивозрастных эффектов ресвератрола[43, 44].
Ингибирование NF-κВ под влиянием ресвератрола замедляет индуцированное повреждением ДНК старение и способствует повышению продолжительности жизни, что было показано в доклинических исследованиях на экспериментальных моделях на мышах. Полученные данные позволили предположить регулирующую роль этого транскрипционного фактора в процессах старения человека. Имеются данные и о тесной связи процессов старения с митохондриальной дисфункцией, обусловленной их морфологическими изменениями и мутациями в митохондриальной ДНК[45, 46].
Кожа является эндокринным органом, где клетки содержат биохимический аппарат, необходимый для выработки гормонов, влияющих на местную иммунную функцию. Существует несколько гормонов, вырабатываемых эндокринной системой, которые выделяют химические мессенджеры, связывающиеся со специфическими рецепторами в клетках/тканях для поддержания гомеостаза в организме, что влияет на здоровье кожи.
Наиболее распространенными дерматологическими регуляторными мессенджерами служат гормоны щитовидной железы, кортизол и эстрогены. Связываясь с рецепторами, тироксин модулирует пролиферацию клеток эпидермиса и их дифференцировку, заживление ран и увлажнение кожи, влияя на функцию дермальных фибробластов. Вызванный стрессом уровень кортизола может привести к тому, что сальные железы кожи будут вырабатывать больше кожного сала и вызывать вспышки акне, псориаза, экземы, кожной сыпи. Кроме того, высокий уровень кортизола может способствовать истончению чувствительной кожи и нарушению барьерной функции, замедлению заживления ран, появлению темных кругов вокруг глаз и увеличению тонких линий и морщин из-за распада коллагена и эластина[47, 48].
При гипоэстрогении, связанной в том числе с периодом менопаузального перехода и постменопаузой, кожа демонстрирует повышенную сухость, морщины, нарушение заживления ран, разрушение коллагена и эластина матриксными металлопротеиназами, снижение гидратации и антиоксидантной способности. При этом агонизм и активация β-РЭ ресвератролом обеспечивает химиопротекторное действие и способствует репарации кожи[49].
Ресвератрол защищает эпителиальные клетки от окислительного повреждения, вызванного АФК, благодаря различным механизмам, в том числе:
-
стимуляции ядерного фактора, связанного с эритроидом-2 — основным биофактором, который увеличивает выработку антиоксидантных и детоксицирующих ферментов;
-
активации сиртуинов-1 и -2;
-
стимуляции синтеза антиоксидантного фермента супероксиддисмутазы;
-
ингибирования матриксных металлопротеиназ, расщепляющих коллаген и эластин, и кальций-связывающих белков S100 A8 и A9, которые являются биомаркерами старения кожи, воспаления и фотостарения[50–54].
Проспективное клиническое исследование H. Hausenblas и соавт. показало, что при ежедневном пероральном приеме в течение 6 мес 100 мг ресвератрола женщинами в возрасте 36–76 лет с видимыми признаками старения кожи наблюдаются значительное повышение тонуса, снижение выраженности морщин и осветление ультрафиолетовых пятен[55]. A.S. Brinke и соавт. выявили, что применение 2% эмульсии транс-ресвератрола 2 раза в день в течение 8 нед у женщин в возрасте 30–35 лет привело к значительному улучшению количественных параметров эластичности кожи, барьерной функции и плотности без побочных эффектов[56].
Ресвератрол снижает синтез меланина, препятствует гиперпигментации и фотостарению кожи, вызывая в ряде случаев ее осветление, а также оказывает ингибирующий эффект на эластазу, гиалуронидазу и коллагеназу, активность которых повышается под влиянием ультрафиолетового излучения, воспаления и с возрастом. Кроме того, ресвератрол активирует антиоксидантные ферменты: каталазу, глутатионпероксидазу и супероксиддисмутазу. Благодаря своим антиоксидантным свойствам ресвератрол уменьшает содержание реактивных форм кислорода в кератиноцитах кожи под влиянием ультрафиолетового облучения и предупреждает повреждение и дистрофические изменения в эпидермисе, а также воспалительную реакцию[57, 58].
ЗАКЛЮЧЕНИЕ
Современным альтернативным подходом к купированию менопаузальных расстройств и профилактики системных метаболических нарушений, в том числе остеопороза, сахарного диабета, инсулинорезистентности и сердечно-сосудистой патологии является назначение фитоэстрогена транс-ресвератрола. Обладая высокой биодоступностью в транс-изомерной форме и высоким профилем безопасности, транс-ресвератрол в форме сублингвальных таблеток и сублингвального спрея является оптимальным негормональным средством коррекции менопаузальных симптомов, торможения некоторых процессов старения, а также имеет значимый потенциал предотвращения возраст-ассоциированных заболеваний.
Поступила: 21.07.2023
Принята к публикации: 25.08.2023








