ВВЕДЕНИЕ
В структуре заболеваемости злокачественными новообразованиями (ЗНО) женского населения России превалируют онкологические заболевания органов репродуктивной системы (40,1%)[1].
Современные методы диагностики и противоопухолевого лечения ассоциированы с увеличением безрецидивной и общей выживаемости у пациенток с ЗНО органов репродуктивной системы. Противоопухолевое лечение может оказывать негативные эффекты на ряд органов и систем, увеличивая риск сердечно-сосудистых заболеваний, сахарного диабета 2 типа, остеопороза и низкоэнергетических переломов. Кроме того, оно ассоциировано с развитием субфертильности, аменореи и наступлением преждевременной недостаточности яичников/ранней менопаузы. Климактерические симптомы (КС) при ятрогенной менопаузе значительно более выражены по сравнению с симптомами, возникающими при естественной менопаузе, особенно у пациенток с ЗНО органов репродуктивной системы, что приводит к резкому снижению качества их жизни[2–5].
Золотым стандартом лечения КС является менопаузальная гормональная терапия (МГТ), однако она противопоказана пациенткам с гормонпозитивными ЗНО, что требует поиска наиболее эффективной и безопасной негормональной терапии для данной категории пациенток. В соответствии с клиническими рекомендациями Министерства здравоохранения РФ к негормональным методам коррекции КС, рекомендованным к назначению пациенткам, имеющим противопоказания к МГТ, относятся антидепрессанты из группы селективных ингибиторов обратного захвата серотонина (СИОЗС) и селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН)[6], β-аланин и экстракт цимицифуги кистевидной (ЦК)[7].
СИОЗС и СИОЗСН
По данным метаанализов и рандомизированных клинических исследований, наиболее эффективными и безопасными лекарственными средствами из группы СИОЗС являются эсциталопрам и пароксетин[8]. Использование эсциталопрама в дозировке 10–20 мг/сут ассоциировано со значительным снижением количества и тяжести приливов и ночной потливости, улучшением сна и хорошим профилем переносимости[8]. Низкие дозы пароксетина (7,5 и 12,5 мг/сут) приводят к уменьшению количества и тяжести вазомоторных симптомов у женщин как с естественной, так и с хирургической менопаузой[8]. Установлено, что пароксетин является сильным ингибитором фермента цитохрома P-450 CYP2D6, который превращает тамоксифен в его активный метаболит эндоксифен. Одновременный прием пароксетина в дозировке 10 мг/сут в течение 4 нед и тамоксифена ассоциирован со снижением концентрации эндоксифена в плазме крови на 64%[9], в связи с чем пациенткам, получающим гормон-депривационную терапию тамоксифеном, прием пароксетина не рекомендован.
Антидепрессанты из группы СИОЗСН венлафаксин 75 мг/сут и десвенлафаксин 100 мг/сут также эффективны в лечении вазомоторных симптомов, однако одним из частых побочных эффектов является сухость во рту и слизистых, что ограничивает их назначение пациенткам с выраженными симптомами генитоуринарного менопаузального синдрома[10].
Из группы СИОЗС препаратом выбора для лечения КС у пациенток с гормонально-зависимыми ЗНО может рассматриваться эсциталопрам, обладающий высокой эффективностью, хорошей переносимостью и не оказывающий значимого влияния на метаболизм селективного модулятора эстрогеновых рецепторов тамоксифена, который используют в качестве адъювантной терапии при гормональнозависимых ЗНО молочной железы[11].
С целью минимизации побочных эффектов при приеме СИОЗС и СИОЗСН показано постепенное увеличение дозировки препарата. Учитывая возможность развития синдрома отмены, для которого характерны бессонница, тошнота, рвота, зрительные нарушения и тремор, отмена СИОЗС и СИОЗСН проводится с постепенным снижением дозировки[12].
В России лекарственные препараты СИОЗС и CИОЗСН не имеют зарегистрированных показаний к лечению менопаузальных симптомов, однако, учитывая их эффективность в лечении вазомоторных симптомов, согласно клиническим рекомендациям, могут быть рекомендованы для лечения вазомоторных симптомов вне утвержденных показаний (off-label) по решению врачебной комиссии[7].
Цимицифуга кистевидная
Основным компонентом ЦК, который связывается с рецепторами серотонина 5-HT1A, 5-HT1D и 5-HT7, принимающими участие в терморегуляции, является тритерпеновый гликозид[13]. Рецептор 5-НТ1А взаимодействует с переносчиком серотонина в гипоталамусе, регулируя обратный захват серотонина. Препараты ЦК указаны в клинических рекомендациях для терапии женщин с КС легкой и средней степени тяжести при наличии у них противопоказаний к МГТ или иных факторов, препятствующих ее назначению[7].
Цель исследования — при помощи специализированных опросников оценить тяжесть КС и качество жизни пациенток с менопаузой ятрогенного генеза в зависимости от получаемой негормональной терапии антидепрессантом эсциталопрамом или экстрактом ЦК.
Дизайн — открытое проспективное, рандомизированное исследование в параллельных группах.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводили на базе ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, набор пациентов осуществляли в отделении гинекологической эндокринологии.
С сентября 2019 г. по ноябрь 2021 г. в исследование были включены 60 пациенток с менопаузой ятрогенного генеза после двусторонней овариэктомии, имевшие в анамнезе ЗНО органов репродуктивной системы. Все пациентки были информированы о содержании и терапии исследования и подписали информированное добровольное согласие на участие. Проведение исследования было рассмотрено и одобрено комиссией по этике биомедицинских исследований ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
В соответствии с целью исследования методом простой рандомизации (метод конвертов) пациентки были распределены в следующие группы:
- группа 1 — 34 пациентки, получавших терапию препаратом эсциталопрам;
– подгруппа 1а — 23 пациентки, доза препарата которых оставалась неизменной на протяжении терапии;
– подгруппа 1б — 11 пациенток, доза препарата которых была увеличена через 3 нед с момента начала терапии в связи с низкой эффективностью проводимой терапии
- группа 2 — 26 пациенток, получавших терапию экстрактом ЦК — препаратом BNO 1055.
Эсциталопрам назначали по схеме: 5 мг 1 раз в день — 7 дней, 10 мг 1 раз в день — 2 нед, в дальнейшем по 10 мг/сут (подгруппа 1а) или 20 мг/сут (подгруппа 2а) — 12 нед. Дозу 20 мг/сут использовали при отсутствии снижения количества и тяжести КС более чем на 50% за 3 нед приема препарата в дозе 10 мг/сут. BNO 1055 назначали в дозе 6,5 мг/сут (по 1 таблетке 1 раз в день) в течение 15 нед.
Критерии включения в исследование:
-
ЗНО органов репродуктивной системы (рак молочной железы, рак яичников, рак тела матки и рак шейки матки) в анамнезе с ожидаемой продолжительностью жизни не менее 12 мес;
-
возраст 18–45 лет;
-
наличие КС;
-
оперативное лечение, объём которого включал двустороннюю овариэктомию;
-
наличие регулярных менструаций до проведения оперативного лечения;
-
наличие противопоказаний для назначения МГТ;
-
категорический отказ от применения МГТ;
-
подписанное информированное согласие на участие в исследовании.
Критерии невключения в исследование:
-
наступление естественной менопаузы;
-
наличие заболеваний желудочно-кишечного тракта и сердечно-сосудистой системы в стадии декомпенсации, некомпенсированной эндокринологической патологии, почечной и печеночной недостаточности, острого тромбофлебита;
-
в анамнезе предшествующий серотониновый синдром, биполярное расстройство личности, неконтролируемые судороги, суицидальные мысли и суицидальные попытки, органические поражения головного мозга с церебростеническим синдромом (последствия черепно-мозговой травмы, инсульта), эндогенные психические расстройства;
-
прием ингибиторов моноаминоксидазы (и период менее 2 нед после их отмены), пимозида, добавок льняного семени, сои и мелатонина в течение 30 дней до включения в исследование;
-
использование локальной и системной гормональной терапии в течение последних 6 мес.
Критерии исключения из исследования:
-
отсутствие возможности продолжить проведение всех мероприятий, запланированных в исследовании со стороны пациента;
-
развившиеся нежелательные побочные и аллергические реакции на фоне проводимой терапии;
-
желание пациентки добровольно прекратить участие в исследовании.
В исследовании оценивали количество приливов в сутки, а также использовали опросники:
-
анкетирование для оценки тяжести КС по шкале Грина, которая включает в себя 21 симптом-вопрос для оценки психоэмоционального состояния, в частности симптомов депрессии (1–6 вопросы) и тревоги (7–11 вопросы), соматических проявлений (12–18 вопросы), вазомоторного (19 и 20 вопросы) и сексуального (21 вопрос) статусов[14].
-
анкетирование для оценки качества жизни (SF-36)[15]. Данный опросник состоит из 36 вопросов, сгруппированных в 8 шкал: физическое функционирование, ролевая деятельность, телесная боль, общее здоровье, жизнеспособность, социальное функционирование, эмоциональное состояние и психическое здоровье. Показатели каждой шкалы составлены таким образом, что чем выше значение показателя (от 0 до 100), тем лучше оценка по избранной шкале. Из них формируют два параметра: психологический и физический компоненты здоровья.
-
анкетирование для оценки субъективных характеристик сна или индекс выраженности бессонницы (ISI)[16]. Опросник для оценки тяжести бессонницы разработан канадским сомнологом Ч. Морином как инструмент для психотерапевтов. С его помощью можно интерпретировать выраженность проблем со сном.
Для статистической обработки данных и построения графиков использовали электронные таблицы «Microsoft Excel» и пакет программ GraphPad Prism 6 (GraphPad Software). Для определения нормальности распределения использовали обобщенный тест Д'Агостино–Пирсона. При анализе параметрических данных рассчитывали среднее значение и среднеквадратичное отклонение, использовали ANOVA. При анализе непараметрических данных рассчитывали медиану и интерквартильный размах, использовали тест Краскела–Уоллиса. При анализе качественных данных (абсолютные значения и доля в процентах) использовали точный тест Фишера, для межгруппового сравнения — апостериорные тесты. Различия считали значимыми при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
На первом этапе исследования мы провели оценку сопоставимости клинико-антропометрических данных пациенток в обеих группах. Возраст и индекс массы тела пациенток были сопоставимыми (табл. 1).
Таблица 1
Исходные клинико-антропометрические характеристики пациенток
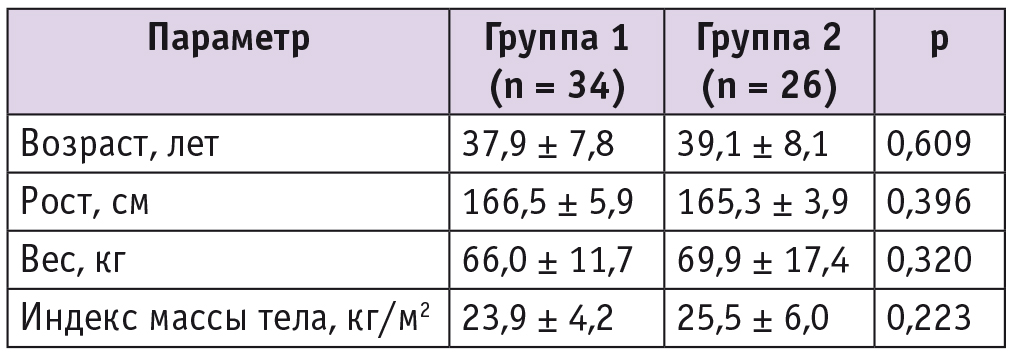
На момент включения пациенток в исследование с момента оперативного лечения (двусторонней овариэктомии) в среднем прошло 130 (67–540) дней у пациенток группы 1 и 223 (98–470) дней у пациенток группы 2, статистически значимых различий не выявлено (p = 0,612).
Далее мы проанализировали особенности образа жизни пациенток, включенных в исследование. Подавляющее большинство пациенток имели высшее образование. Курили 9 (15,0%) пациенток, регулярно употребляли алкоголь — 3 (5,0%), регулярно занимались спортом или иной физической активностью — 15 (25,0%). Статистически значимых различий между изучаемыми группами не выявлено.
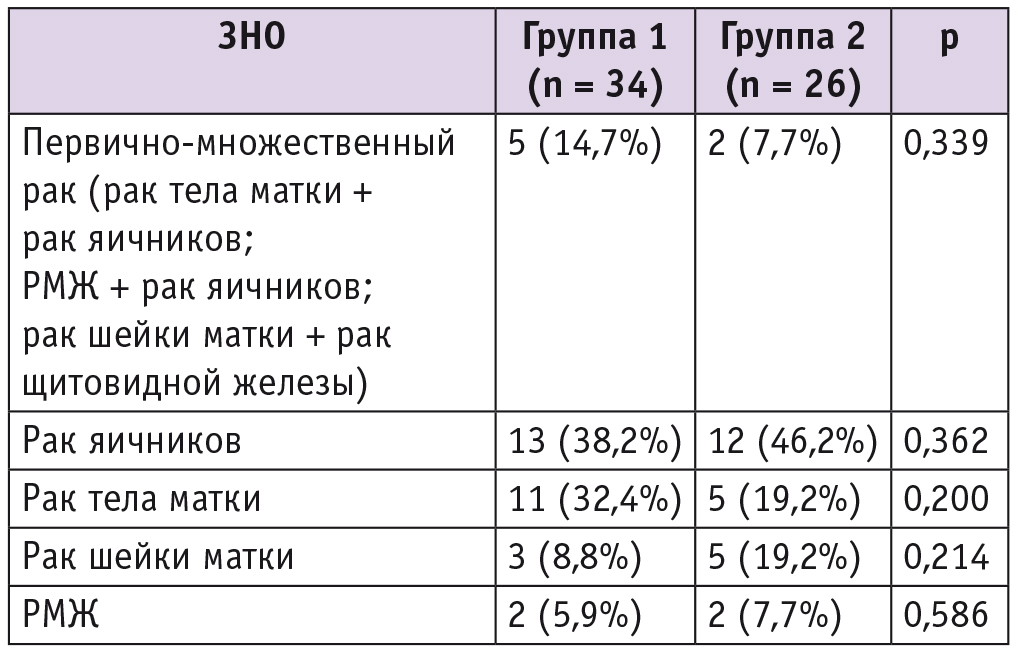
В структуре ЗНО, по поводу которых в рамках хирургического лечения была произведена двусторонняя овариэктомия, первое место занимал рак яичников, второе — рак тела матки (табл. 2). Реже встречались рак шейки матки и рак молочной железы (РМЖ). У больных РМЖ билатеральная риск-редуцирующая операция выполнялась в случае выявления мутации генов BRCA. Значимых различий структуры онкологической патологии у пациенток групп 1 и 2 не выявлено.
Таблица 2
Структура ЗНО в исследуемых группах женщин с ятрогенной менопаузой, имеющих в анамнезе ЗНО органов репродуктивной системы
В нашей работе мы оценили количество приливов до терапии и через 15 нед терапии изучаемыми препаратами. Как следует из данных табл. 3, количество приливов снизилось во всех группах терапии, однако статистически достоверным оно было только у пациенток подгруппы 1а.
Таблица 3
Количество приливов исходно и через 15 нед терапии в исследуемых группах женщин с ятрогенной менопаузой, имеющих в анамнезе ЗНО органов репродуктивной системы, Me (Q1–Q3)
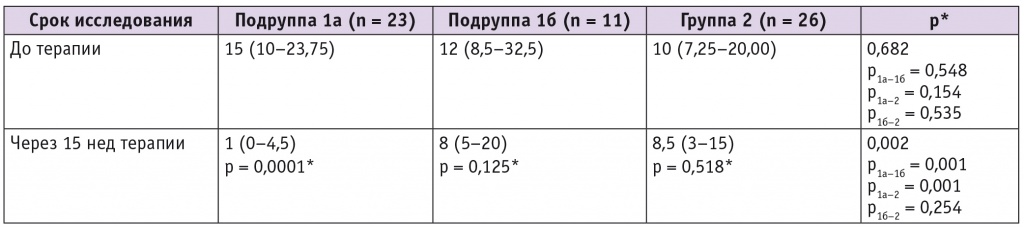
*По сравнению с показателем до терапии.
Далее мы проанализировали степень выраженности КС по шкале КС Грина. Результаты опросников были объединены в 5 кластеров с целью оценки симптомов тревоги и депрессии, соматических, вазомоторных и сексуальных проявлений. Исходно пациентки исследуемых групп были сопоставимы по показателям шкалы КС Грина (табл. 4). В подгруппе 1а через 15 нед терапии установлено значимое снижение выраженности КС, симптомов тревоги и депрессии, улучшение соматических проявлений, снижение тяжести вазомоторных симптомов, улучшение либидо. Для пациенток подгруппы 1б характерно достоверное снижение выраженности КС и тревожного компонента. Пациентки группы 2 отметили значимое снижение выраженности КС и депрессии. При межгрупповом сравнении наиболее выраженный эффект на КС, симптомы тревоги, депрессии и тяжести вазомоторных симптомов был выявлены в подгруппе 1а по сравнению с подгруппой 1б и группой 2.
Таблица 4
Оценка КС по шкале Грина исходно и через 15 нед терапии у женщин с ятрогенной менопаузой, имеющих в анамнезе ЗНО органов репродуктивной системы, Me (Q1–Q3)
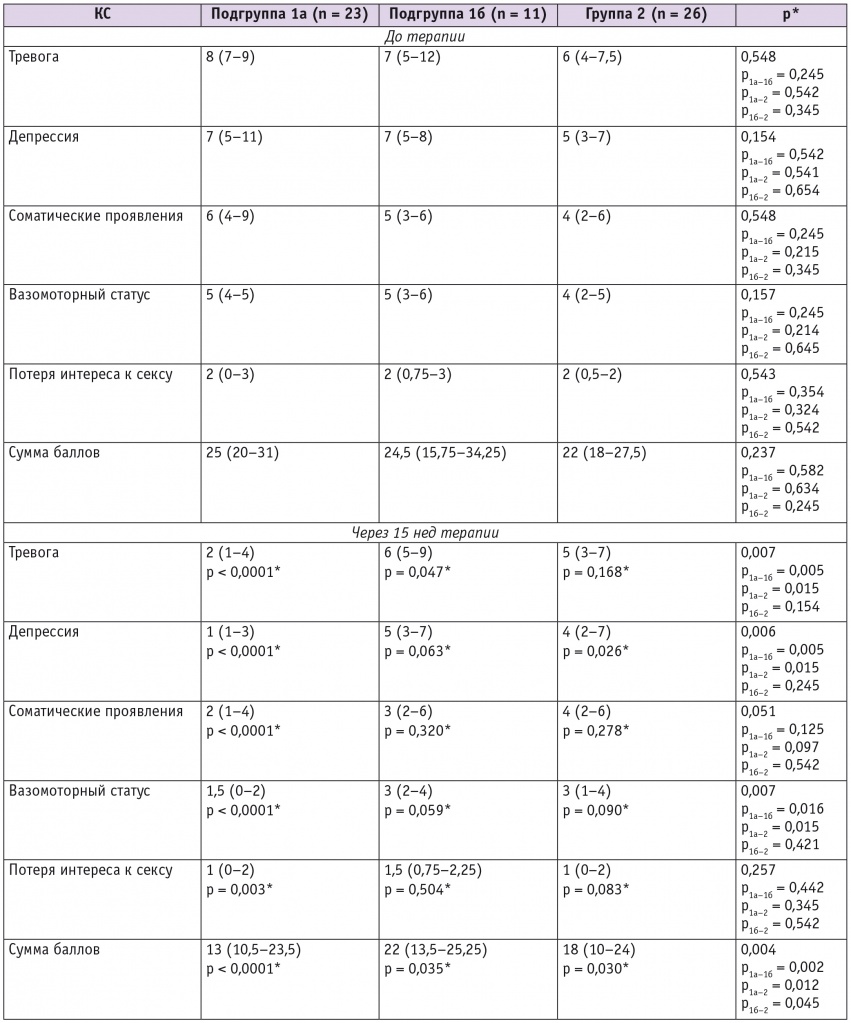
*По сравнению с показателем до терапии.
Оценку качества жизни проводили по опроснику SF-36, который включает в себя оценку физического и психологического компонентов здоровья. Физический компонент здоровья был оценен по следующим параметрам: физическое функционирование, ролевое функционирование, обусловленное физическим состоянием, интенсивность боли и общее состояние здоровья. Психологический компонент здоровья складывается из таких параметров, как жизненная активность, социальное функционирование, ролевое функционирование, обусловленное эмоциональным состоянием, и психическое здоровье.
До начала терапии физический и психологический компоненты здоровья в группах сравнения были сопоставимы (табл. 5). В процессе лечения отмечено значимое улучшение физического компонента здоровья у пациенток группы 2, психологического компонента здоровья — в подгруппе 1а через 15 нед терапии. В то же время у пациенток подгруппы 1б этот показатель качества жизни в результате лечения практически не изменился.
Таблица 5
Оценка по опроснику SF-36 «Оценка качества жизни» исходно и через 15 нед терапии у женщин с ятрогенной менопаузой, имеющих в анамнезе ЗНО органов репродуктивной системы, Me (Q1–Q3)
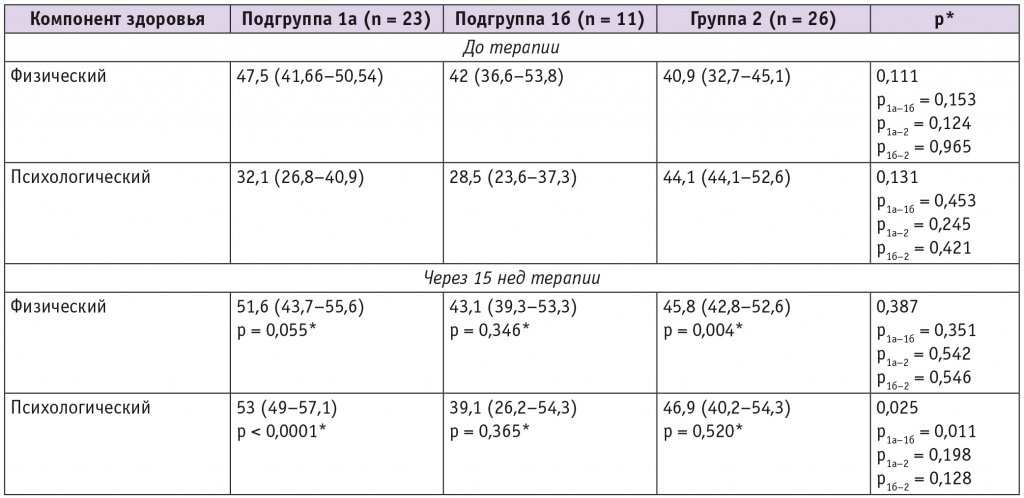
*По сравнению с показателем до терапии.
Индекс выраженности бессонницы исходно был сопоставим в группах сравнения (табл. 6). Через 15 нед лечения у пациенток подгруппы 1а индекс выраженности бессонницы значительно снизился, тогда как у пациенток подгруппы 1б и группы 2 он снижался незначимо.
Таблица 6
Индекс выраженности бессонницы, Me (Q1–Q3)

*По сравнению с показателем до терапии.
Нежелательными явлениями на фоне терапии эсциталопрамом были головная боль — 3 (8,8%) и яркие сновидения — 1 (2,9%), которые нивелировались к 2–3-й неделе терапии. Пациентки, получающие BNO1055, отмечали тошноту — 3 (11,5%), которая проходила в течение 1 нед.
ОБСУЖДЕНИЕ
В нашем исследовании установлено, что у пациенток репродуктивного возраста с ятрогенной менопаузой, имеющих ЗНО органов репродуктивной системы, эффективной дозой эсциталопрама для коррекции КС является 10 мг/c. Использование эсциталопрама в дозе 10 мг/c в течение 15 нед ассоциировано со снижением выраженности КС, количества и тяжести приливов, улучшением соматических показателей, улучшением качества жизни за счет психологического компонента здоровья, психоэмоционального состояния и сна. В исследовании E.W. Freeman и соавт. также показано, что терапия эсциталопрамом в дозе 10–20 мг/c ассоциирована со значительным снижением частоты приливов (р = 0,004) и их тяжести (р = 0,003)[17]. K.E. Ensrud и соавт. также выявлено снижение количества и тяжести вазомоторных симптомов, что, в свою очередь, было связано с улучшением сна (р < 0,001)[18]. При анализе полученных данных мы оценили эффективность терапии эсциталопрамом по его влиянию на вазомоторные симптомы в группе 2. Нам удалось установить, что увеличение дозировки эсциталопрама до 20 мг/c не оказало значимого влияния на вазомоторные симптомы у 67% пациенток, что может быть ассоциировано с генетическими особенностями пациенток, в том числе полиморфизмом гена ABCB1, который является АТФ-зависимым мембранным транспортером и участвует в выведении из клетки лекарственных препаратов. Такое же предположение было выдвинуто A.B. Singh и соавт., показавшими, что однонуклеотидные полиморфизмы в rs1045642 ABCB1 могут влиять на биодоступность эсциталопрама, что может объяснить индивидуальный ответ пациенток на различные дозировки эсциталопрама[19]. В связи с этим можно сделать вывод, что если через 3 нед приема эсциталопрама снижение количества и тяжести вазомоторных симптомов составляет менее 50%, то необходимо увеличить дозировку препарата вдвое и провести оценку эффективности через 2 нед терапии, и в случае его неэффективности решить вопрос о смене лекарственного средства.
В нашем исследовании терапия лекарственным препаратом BNO 1055 в дозе 6,5 мг/сут привела к значимому снижению выраженности КС и тяжести приливов, снижению тревожного компонента, а также повышению качества жизни за счет физического компонента здоровья. В исследовании С. Wang и др. было также показано достоверное снижение выраженности КС при использовании ЦК у больных РМЖ, получающих эндокринную терапию агонистами гонадотропин-рилизинг-гормона[20]. В метаанализе 2023 г., включающем более 2000 женщин, установлено, что использование экстракта ЦК было ассоциировано со значительным снижением тяжести КС (95% ДИ 0,283–0,867; р < 0,001), в том числе снижением вазомоторных проявлений (95% ДИ 0,107–0,524; р = 0,003) и улучшением соматического состояния пациенток (95% ДИ 0,165–0,670; р = 0,001). При этом ЦК не оказывала существенного влияния на симптомы тревоги и депрессии, в отличие от результатов нашего исследования, где было получено достоверное снижение выраженности тревожного компонента[21].
ЗАКЛЮЧЕНИЕ
У пациенток с гормонально-зависимыми ЗНО с целью улучшения качества их жизни, лечения КС, коррекции психоэмоционального состояния и улучшения сна показана негормональная терапия антидепрессантом эсциталопрамом из группы СИОЗС либо растительным лекарственным препаратом из экстракта ЦК.
На основании полученных результатов можно сделать вывод об эффективности и хорошей переносимости негормональной терапии эсциталопрамом и экстрактом ЦК проявлений КС у пациенток с ЗНО. Терапия эсциталопрамом способствовала значительному повышению качества жизни пациенток за счет клинически значимого улучшения психологического компонента здоровья и снижения тяжести КС. Эсциталопрам оказал положительный эффект на все компоненты КС: вазомоторные, психоэмоциональные, соматические и сексуальные. Терапия лекарственным препаратом ЦК была ассоциирована с достоверным улучшением качества жизни за счет физического компонента здоровья и значимого снижения выраженности КС за счет преимущественного воздействия на вазомоторные симптомы и тревогу. Учитывая вышесказанное, подбор лекарственной терапии КС у пациенток с ЗНО органов репродуктивной системы должен носить персонифицированный характер с учетом индивидуальных потребностей пациентки.
Поступила: 09.06.2023
Принята к публикации: 10.07.2023








