Хроническая тазовая боль (ХТБ) при перитонеальном эндометриозе (ПЭ), как правило, обретает статус самостоятельного заболевания, истощая силы организма, снижая сопротивляемость к внешним воздействиям, оказывая выраженное влияние на эмоциональное состояние, что приводит к снижению качества жизни у больных ПЭ. Сложность и многогранность этих взаимосвязанных патологических состояний очевидна, но способы их реальной терапии все еще недостаточно эффективны [17, 18]. В патогенез связанной с ПЭ тазовой боли могут быть вовлечены все три возможных патофизиологических компонента боли, а именно ноцицептивный, невропатический и психогенный.
Появляется все больше доказательств того, что при ПЭ в основе генерации боли на всех этапах ее передачи лежит тесное взаимодействие между периферическими тазовыми нервами, провоспалительным перитонеальным микроокружением и ЦНС [12, 15, 16]. Возникающая ноцицептивная боль за счет иммунного воспаления постепенно приводит к формированию невропатической боли, конечный этап которой — центральная сенситизация — является самым важным механизмом ХТБ. При наличии характерного для эндометриоидных поражений персистирования болевого раздражителя в течение длительного времени локальные воспалительные процессы могут вызывать и поддерживать феномен периферического нейровоспаления, взаимосвязанного с активацией клеток микроглии и астроцитов, называемых «иммуноцитами ЦНС» (центральное нейровоспаление) [5, 16, 20].
Значимым фактором формирования ХТБ является несостоятельность эндогенных анальгетических систем, в том числе антиноцицептивной серотонинергической [13]. Серотонин относится к соединениям, воздействующим на ноциогенные зоны и провоцирующим боль. Высвобождаясь тучными клетками, а также тромбоцитами при действии на них активирующего фактора, он вызывает чувство боли в зоне повреждения как непосредственно, так и потенцируя эффект брадикинина (ноцицептивный компонент боли) [19–21]. Причиной наличия невропатической составляющей боли считают нарушение центрального торможения ноцицептивных нейронов. При условии персистенции раздражающего фактора возникают изменения пластичности периферической и центральной нервной системы, что способствует сохранению боли независимо от интенсивности раздражения. Нисходящее супраспинальное торможение также реализуется через серотонин-, норадреналин- и опиоидергические нейротрансмиттерные системы [4]. Серотониновой нейротрансмиттерной системе придают существенное значение и в деятельности антиноцицептивной центральной регуляции болевой чувствительности [6–9] и регуляции эмоций человека. Снижение уровня эндогенного серотонина доказано при депрессиях. Нарушение обмена серотонина является важным биохимическим фактором формирования и поддержания хронического болевого синдрома с развитием эмоциональных нарушений, которые поддерживают болевую доминанту в надсегментарных структурах ЦНС, формируя психогенный компонент боли [1].
По статистике ВОЗ, ХТБ страдают около 15% женщин репродуктивного возраста. Согласно данным Международного общества по тазовой боли (International Pelvic Pain Society), ХТБ является поводом для 10% всех обращений к гинекологу, 20% всех лапароскопий и 10–15% гистерэктомий. Эндометриоз — одна из наиболее частых причин ХТБ: он поражает 10% женщин репродуктивного возраста в целом и до 70% женщин и девочек-подростков с тазовой болью, охватывая период жизни женщины от менархе до постменопаузы. ПЭ остается одной из наиболее распространенных локализаций эндометриоза, ведущим проявлением которого является ХТБ [2, 12, 19, 21].
В литературе имеются единичные исследования по изучению серотонинового статуса у пациенток с ХТБ при генитальном эндометриозе, посвященные исходной гипофункции гуморального звена серотониновой системы у больных эндометриозом и потому о низкой физиологической активности церебрального (нейронального) ее звена [14]. Однако далеко не у всех пациенток манифестация симптоматики ПЭ патогенетически обусловлена функциональной недостаточностью (гипофункцией) серотониновой системы. Возможно, именно наличие болевого синдрома вызывает истощение серотонинергической церебральной системы в условиях ее высокой антиноцицептивной активности при длительном существовании ХТБ. Все вышеизложенное обосновывает актуальность изучения серотонинового и цитокинового статуса у пациенток с различным течением и интенсивностью ХТБ при ПЭ, расширение представлений о котором открывает перспективы совершенствования подходов к терапии данной коморбидной патологии.
Цель исследования: изучить состояние серотонинового и цитокинового статуса при ХТБ у пациенток с ПЭ.
МАТЕРИАЛЫ И МЕТОДЫ
Обследованы 195 пациенток с ХТБ (код по МКБ-10: R10.2), обусловленной ПЭ, и 30 практически здоровых женщин (группа контроля) в возрасте от 25 до 42 лет. Исследование проведено на базе Перинатального центра ГБУЗ «Краевая клиническая больница № 2» г. Краснодара и МБУЗ «Родильный дом № 4» г. Краснодара базы кафедры акушерства, гинекологии и перинатологии ГБОУ ВПО КубГМУ Минздрава России (заведующая кафедрой — И. И. Куценко) в 2012–2015 гг.
У всех пациенток ПЭ II или III стадии был диагностирован при лапароскопии, выполненной по поводу синдрома тазовых болей, и подтвержден результатами гистологического исследования. У 109 (55,9%) пациенток ПЭ диагностировали впервые, у 86 (44,1%) имел место рецидив ранее выявленного ПЭ. Интенсивность тазовой боли определяли по визуальной аналоговой шкале (ВАШ).
Пациентки были стратифицированы по интенсивности боли и особенностям течения заболевания (впервые выявленный ПЭ или рецидив): 1-я группа (n = 53) — интенсивность боли по ВАШ 4–6 баллов, ПЭ выявлен впервые; 2-я группа (n = 56) — ВАШ 7–10 баллов, ПЭ также диагностирован впервые; 3-я группа (n = 45) — ВАШ 4–6 баллов, рецидив ПЭ; 4-я группа (n = 41) — ВАШ 7–10 баллов, также наблюдался рецидив ПЭ; 5-я группа (n = 30) — контроль (практически здоровые женщины, пришедшие на профилактический осмотр к гинекологу). Группы были статистически сопоставимы.
Содержание про- и противовоспалительных цитокинов в периферической крови (ИЛ-1β, ИЛ-2, ИЛ-4, ИЛ-6, ИЛ-8, ИЛ-10, рецепторного антагониста ИЛ-1 — РАИЛ-1) в динамике до лечения и на фоне терапии у всех пациенток определяли методом ИФА (ASCENT, Финляндия) с использованием соответствующей панели моноклональных антител (ЗАО «Вектор-Бест», г. Ростов-на-Дону). Рассчитывали провоспалительный индекс, отражающий баланс цитокинов в семействе ИЛ-1 (отношение ИЛ-1β/РАИЛ-1).
Исследование серотонина в периферической крови проводили с помощью иммуноферментного метода. Для повышения точности и упрощения объективизации интенсивности боли применяли способ регистрации интенсивности хронической невропатической боли, разработанный А. А. Шутовым, Ю. В. Каракуловой, Т. В. Завалиной (патент № 2254574, 2005 г.).
Поскольку изучение патогенетических факторов формирования болевого синдрома необходимо проводить с применением корреляционного анализа, в работе использован подход, направленный на выявление характера и степени взаимосвязей между факторами, участвующими в формировании компонентов болевого синдрома, с применением множественного корреляционного анализа.
Статистическую обработку полученных данных производили, используя характеристики описательной статистики: выборочное среднее, медиану (Me). При статистической обработке применяли статистический программный пакет Statistica v. 8 (StatSoft, США). Корреляционный анализ проводили с помощью коэффициента корреляции Спирмена. Достоверными считали различия при р < 0,05.
РЕЗУЛЬТАТЫ
У всех пациенток имели место жалобы на тазовую боль. Следует отметить, что интенсивность боли ни у одной пациентки не превышала 9 баллов по ВАШ. В группах обследованных с впервые выявленным ПЭ длительность боли составляла 1–2 года (их доля в выборке — 63,3%). Среди пациенток с рецидивом ПЭ было больше всего женщин с длительностью боли 3–5 лет (52,3%) и 6–8 лет (47,7%).
Цитокиновый профиль обследованных свидетельствовал в пользу воспалительного компонента в патогенезе ХТБ любой интенсивности и при любом течении ПЭ. У больных 1-й и 2-й групп наблюдали достоверное увеличение концентрации провоспалительных интерлейкинов в периферической крови по сравнению с группой контроля (табл.). Это в достаточной мере компенсировалось виражом противовоспалительного профиля, хотя и сопровождалось небольшим отставанием в нарастании последнего. Достоверные различия в интерлейкиновом профиле наблюдали и в группах с разной выраженностью болевого синдрома, т. е. между 1-й и 2-й и между 3-й и 4-й группами (см. табл.).
Таблица. Цитокиновый профиль периферической крови у пациенток с хронической тазовой болью, ассоциированной с перитонеальным эндометриозом, пкг/мл (М ± m)
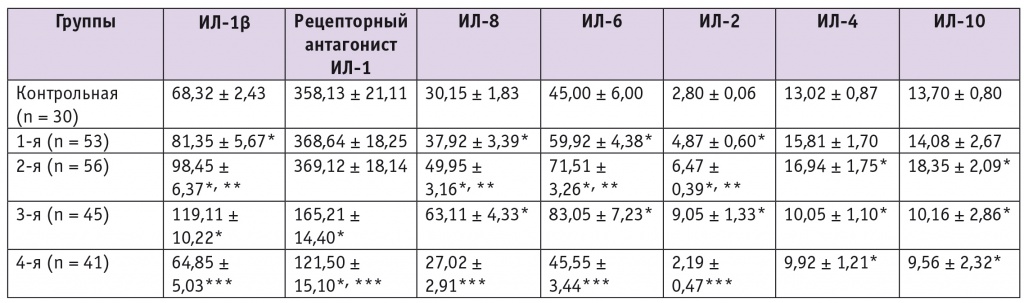
Примечание. Знаком (*) отмечены достоверные отличия: (*) — от группы контроля (p < 0,01); (**) — от 1-й группы (р > 0,05); (***) — от 3-й группы (р < 0,05).
Выявленные различия наглядно демонстрирует провоспалительный индекс в группах исследования (рис. 1). У пациенток 3-й группы (рецидив, умеренная ХТБ) наблюдали максимально выраженное превалирование провоспалительного цитокинового звена с некоторым угнетением противовоспалительного, что подтверждалось провоспалительным индексом — 0,72 ± 0,05 (p < 0,05) (см. рис. 1).
Рис. 1. Отношение про- и противовоспалительных цитокинов (провоспалительный индекс) периферической крови у пациенток с хронической тазовой болью, ассоциированной с перитонеальным эндометриозом.
Примечание. Знаком (*) отмечены достоверные отличия: (*) — от группы контроля (p < 0,05); (**) — от 1-й, 2-й и 4-й групп (p < 0,05).
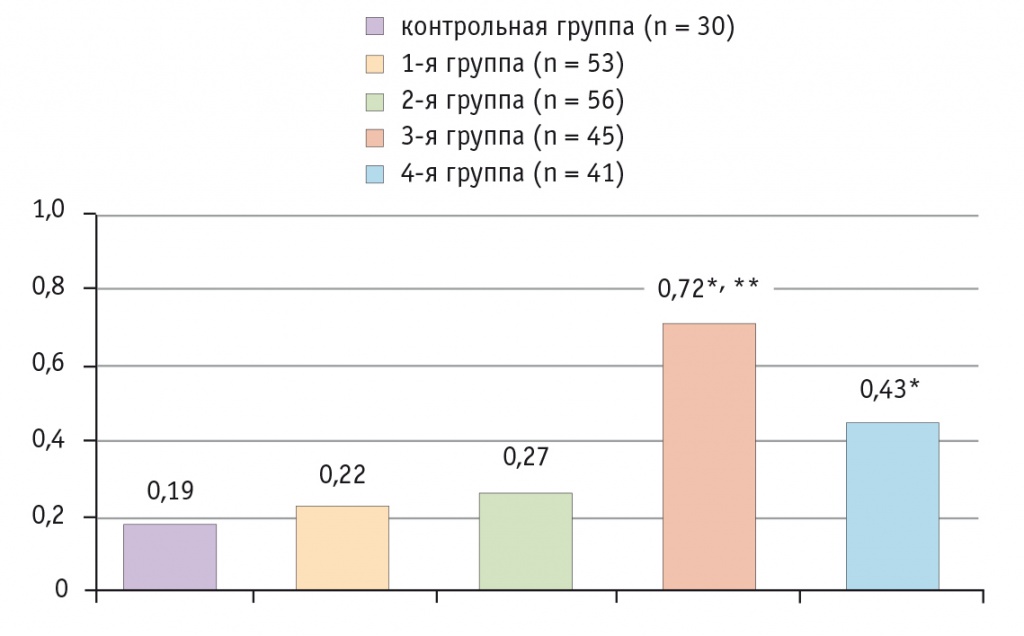
В 4-й группе (рецидив, сильная ХТБ) отмечено выраженное снижение уровней про- и противовоспалительных цитокинов с уменьшением абсолютных показателей интерлейкинов, что трактуется как «ложная стабилизация» и указывает на срыв адаптивных возможностей. Однако даже в условиях срыва адаптации провоспалительный индекс свидетельствовал о превалировании провоспалительного компонента в цитокиновом профиле: 0,43 ± 0,02 против 0,19 ± 0,03 в группе контроля (p < 0,05) (см. рис. 1).
Полученные данные позволяют использовать провоспалительный индекс как адекватный маркер эффективности проводимой терапии ХТБ при ПЭ.
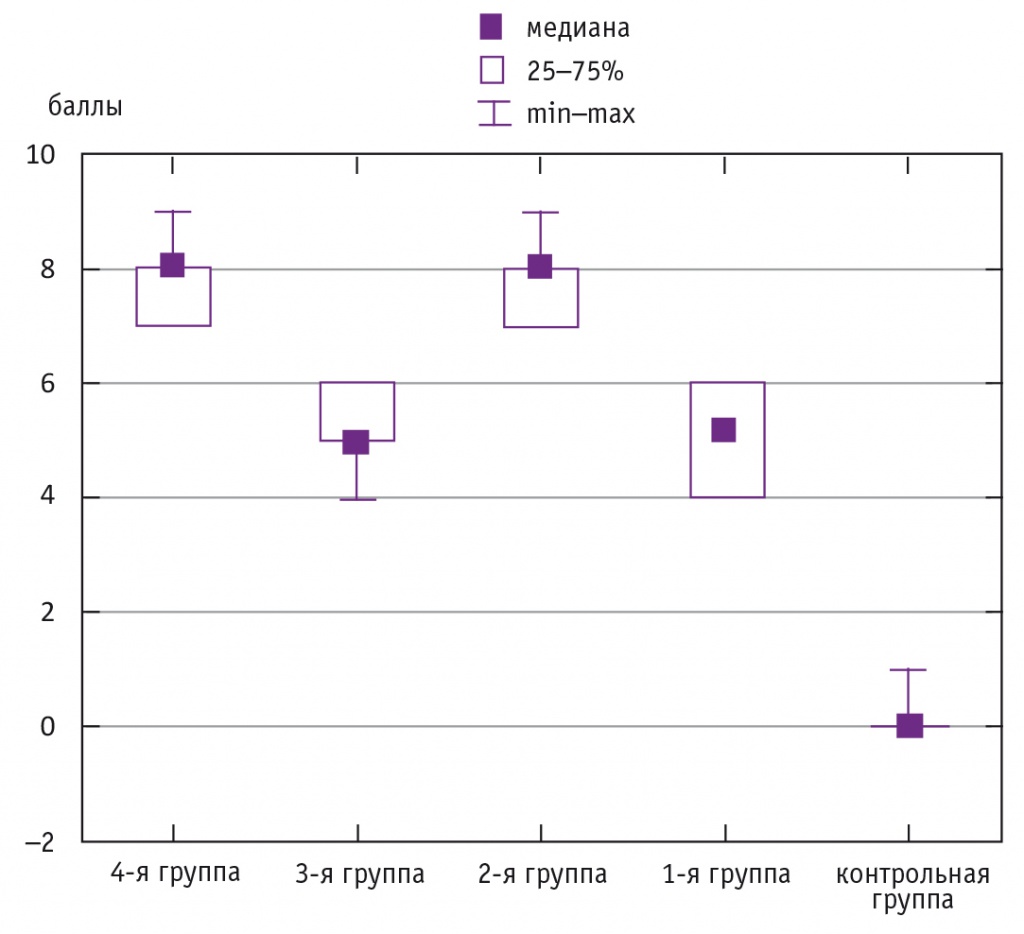
Анализ серотонинового статуса во всех группах исследования показал достоверное снижение содержания серотонина в периферической крови по сравнению с контролем (р < 0,05). Уровни серотонина у пациенток 1-й и 3-й групп соответствовали градациям данного показателя при объективной регистрации хронической невропатической боли умеренной степени (4,9 ± 0,1 и 5,0 ± 0,1 балла соответственно; р > 0,05), а во 2-й и 4-й группах находились в пределах показателей при регистрации выраженной хронической невропатической боли (7,7 ± 0,1 и 7,9 ± 0,1 балла; р > 0,05), что соответствовало субъективной оценке боли по ВАШ.
Во 2-й и 4-й группах уровни серотонина периферической крови составили соответственно 110,4 ± 1,4 нг/мл (Me = 109) и 96,1 ± 1,7 нг/мл (Me = 95), что существенно ниже в сравнении с показателями у пациенток 1-й и 3-й групп (р < 0,05). При этом содержание серотонина у женщин 4-й группы было достоверно ниже (р < 0,05), чем у больных 2-й группы. Однако субъективно по ВАШ пациентки 2-й и 4-й групп оценивали боль идентично — как выраженную (7,7 ± 0,1 и 7,9 ± 0,1 балла соответственно) (рис. 2, 3).
Рис. 2. Содержание серотонина в периферической крови у обследованных пациенток, нг/мл.
Примечание. Знаком (*) отмечены достоверные отличия: (*) — от 1-й и 3-й групп (p < 0,05); (**) — от 2-й группы (p < 0,05)
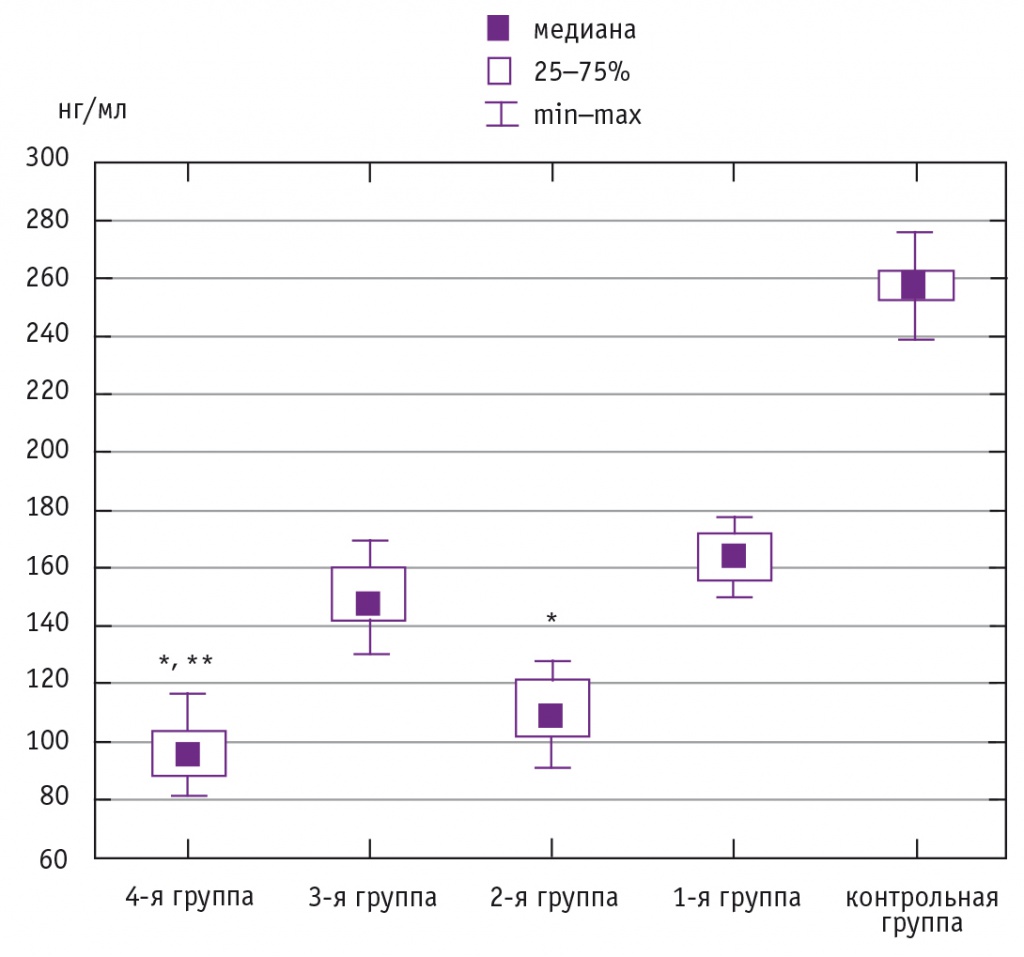
Рис. 3. Выраженность хронической тазовой боли по визуальной аналоговой шкале у обследованных пациенток, баллы
Патогенез ХТБ при ПЭ является сложно организованным и многокомпонентным. При этом в полном объеме определить и охарактеризовать факторы, формирующие компоненты боли, при раздельном изучении каждого элемента не представляется возможным, поскольку длительность и степень выраженности болевого синдрома тесно связаны с их уровнем сопряженности.
Проведенный корреляционный анализ показателей цитокинового и серотонинового статуса подтвердил существование определенных закономерностей, позволяющих считать взаимовлияние изучаемых факторов значимым для формирования ХТБ при ПЭ.
Особый интерес представляют результаты корреляционного анализа взаимосвязи между уровнями регуляторного ИЛ-2 и серотонина, значениями провоспалительного индекса при ХТБ, обусловленной ПЭ различной интенсивности и разного течения.
При впервые выявленном ПЭ, сопровождавшемся умеренной и выраженной ХТБ, а также при умеренно выраженной ХТБ при рецидиве ПЭ коэффициент корреляции указывал на сильную положительную связь между уровнем ИЛ-2 и провоспалительным индексом, которая снижалась до средней степени (r = 0,56) в 4-й группе. Коэффициент корреляции 4-й группы достоверно отличался от таковых во всех остальных группах (р < 0,001) (рис. 4), что косвенно подтверждало процессы дисрегуляции в цитокиновом статусе у пациенток с длительно текущим ПЭ, сопровождавшимся выраженной ХТБ.
Рис. 4. Значения коэффициента корреляции уровня интерлейкина 2 с показателями провоспалительного индекса и серотонина в группах исследования
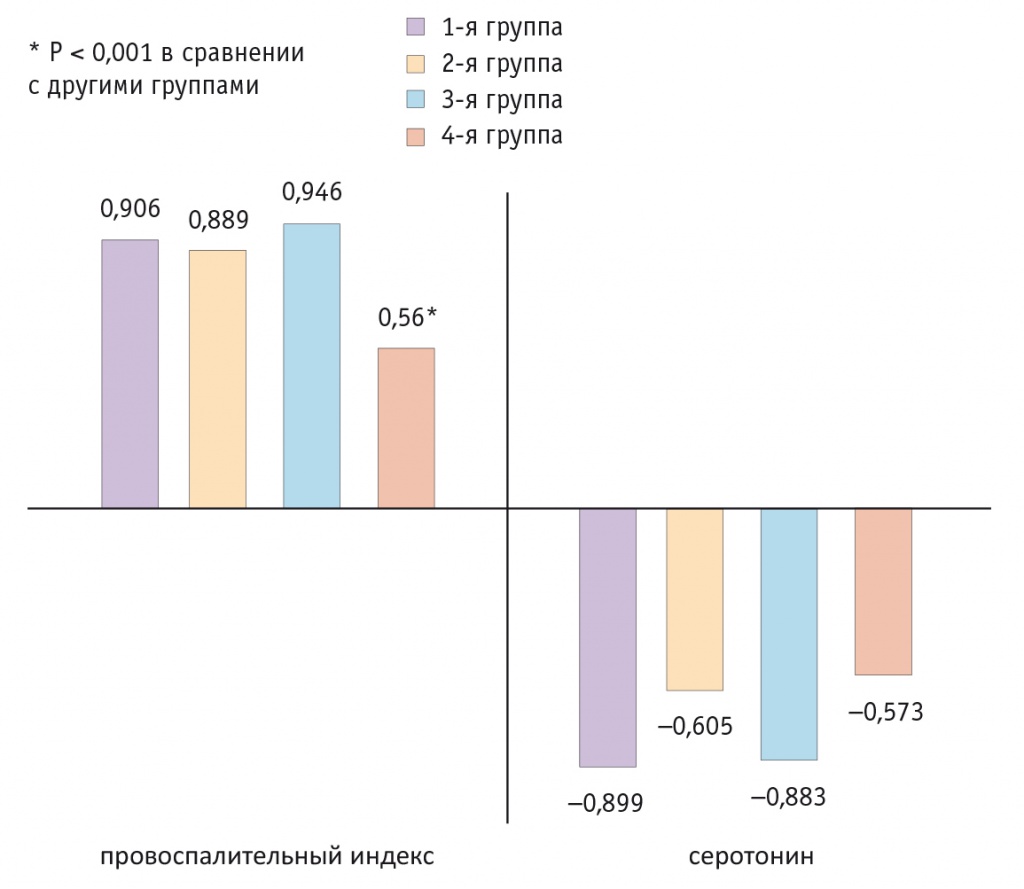
Умеренная ХТБ при впервые выявленном заболевании и при рецидиве характеризовалась сильной отрицательной взаимосвязью между содержанием ИЛ-2 и уровнем серотонина. Напротив, при выраженной ХТБ независимо от характера течения ПЭ мы обнаружили ослабление корреляционных связей между уровнями серотонина и ИЛ-2 до средних значений, коэффициенты корреляции во 2-й и 4-й группах достоверно не различались (р > 0,05) (см. рис. 4). Вероятно, это свидетельствует о снижении активности антиноцицептивных механизмов формирования боли и об отрыве процессов формирования болевого синдрома от первичного (ноцицептивного) компонента на фоне дефицитарности нейротрансмиттерной (серотониновой) системы.
ЗАКЛЮЧЕНИЕ
Проведенное исследование показывает, что наличие иммунного воспаления с хронизацией воспалительного процесса вызывает персистирование боли и способствует длительной гипервозбудимости ноцицептивной системы, приводящей к снижению уровня серотонина при любой интенсивности болевого синдрома и независимо от характера течения заболевания. При нарастании интенсивности хронической тазовой боли (ХТБ) имеющиеся дисфункции достоверно усиливаются. Однако при ХТБ при перитонеальном эндометриозе (ПЭ) при идентичной интенсивности боли на фоне достоверно более длительного иммунного воспаления, наряду с ноцицептивным механизмом возникновения тазовой боли, наиболее значимо усугубляется неврогенный компонент.
Вопрос о дифференцированной медикаментозной терапии ПЭ должен решаться с учетом этих патогенетических особенностей. Поскольку обычно необходимо долгосрочное лечение, по возможности следует применять наиболее безопасные из существующих препаратов. В связи с ключевой ролью иммунной системы в патогенезе ХТБ при ПЭ большой интерес представляют иммуномодулирующие эффекты лекарственных средств, используемых в комплексном лечении болевого синдрома, что созвучно мнению большинства авторов [3, 10, 11]. Важным условием успешной терапии ХТБ при ПЭ является способность препаратов купировать иммунное воспаление как фактор, формирующий ХТБ.








