Создание новых оральных антикоагулянтов (НОАК), обладающих весомыми преимуществами перед варфарином и гепаринами, привело к тому, что все больше пациентов, в том числе с сочетанием различных заболеваний (коморбидностью), их получают. В связи с этим необходимо рассматривать антикоагулянтную терапию с мультидисциплинарной точки зрения.
Цель обзора: осветить проблему применения антикоагулянтов у коморбидных больных, оценить желудочно-кишечную переносимость оральных антикоагулянтных препаратов и определить наиболее рациональную гастропротективную терапию.
В настоящее время в России зарегистрированы три НОАК: дабигатрана этексилат, ривароксабан, апиксабан. Их объединяет отсутствие необходимости в подборе дозы, мониторинге параметров коагулограммы, соблюдении диеты. Они обладают минимальным спектром лекарственных взаимодействий, дозирование не зависит от пола, возраста, этнической принадлежности, веса пациента. Все эти НОАК в клинических исследованиях либо были так же эффективны, как препараты сравнения (антагонисты витамина К и эноксапарин), либо превосходили их в предотвращении тромбоэмболических событий. Применение НОАК способствовало снижению риска тяжелых кровотечений, особенно таких как внутричерепное и фатальное. Кроме того, эти препараты значительно более удобны в использовании, чем антагонисты витамина К. Так, при их применении не требуется постоянный контроль МНО, а при отмене происходит быстрое восстановление нормальной свертываемости крови[4]. Однако вопросы желудочно-кишечной безопасности антикоагулянтов остаются на повестке дня в связи с ростом распространенности клинически значимых желудочно-кишечных кровотечений (ЖКК).
КОМОРБИДНОСТЬ У ПАЦИЕНТОВ С ЗАБОЛЕВАНИЯМИ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
Проблема ведения коморбидных больных в настоящее время является предметом обсуждения на медицинских форумах различных уровней: от ежедневных утренних врачебных конференций до всемирных научных площадок. Причина этого — рост смертности от ЖКК. Среди людей старше 65 лет 10–20% регулярно принимают НПВП. По данным Комитета по контролю за лекарственными препаратами США, НПВП-гастропатия — эрозивно-язвенное поражение гастродуоденальной слизистой — ежегодно становится причиной 100–200 тыс. госпитализаций и 10–20 тыс. смертельных исходов[3].
Очевидно, что рост распространенности фатальных ЖКК, связанных с приемом НПВП, антикоагулянтов и их сочетаний, неслучаен: отмечается увеличение количества пожилых коморбидных пациентов. В исследовании Л. Б. Лазебника и В. Н. Дроздова, проведенном более 10 лет назад, при обследовании 564 пациентов с заболеваниями ЖКТ в возрасте от 60 до 85 лет только остеоартроз диагностировали у 55,5% больных с хроническим холециститом, у 39% — с хроническим гастритом, у 25% — с хроническим панкреатитом, немного реже — при наличии язвенной болезни и цирроза печени (16,6% и 12,6% соответственно), а количество болезней на одного человека составило 5,1–5,8[5].
По данным А. Л. Вёрткина и А. В. Наумова (2007), выполнивших анализ 3239 протоколов аутопсий умерших в крупном многопрофильном стационаре, причинами смерти у 48,4% были острые и хронические сердечно-сосудистые заболевания. При этом частота фибрилляции предсердий (ФП) у этих пациентов составила 27,0% (n = 423). Таким образом, каждый третий сосудистый больной страдал ФП. Дальнейший анализ показал, что в 66% (n = 279) случаев ФП была у женщин; ФП сопутствовали ожирение (n = 63; 14,9%), сахарный диабет 2 типа (n = 118; 27,9%), ХОБЛ (n = 207; 49,0%), доброкачественная гиперплазия предстательной железы (n = 72; 17,0%), АГ (n = 351; 83,0%), желчнокаменная болезнь (n = 97; 22,9%). Приведенные цифры свидетельствуют, что пациенты с ФП коморбидны, причем общее число заболеваний более четырех[2].
Это значит, что такой больной — с наличием язвенного кровотечения в анамнезе, с ФП и риском тромбоэмболических осложнений, с болью в суставах, гипертонической болезнью и ожирением — не редкость в практике гастроэнтеролога. Для врача очень важно верно определить баланс между эффективностью и безопасностью применяемых препаратов.
Крайне актуальным сегодня является вопрос о рациональной антикоагулянтной терапии. О важности тщательно собранного лекарственного анамнеза у всех пациентов, и особенно у коморбидных больных, не устает напоминать профессор А. Л. Вёрткин. Его настойчивость ставится понятной, когда докладывают о летальных исходах вследствие ЖКК у больных трудоспособного возраста. Приведем один из таких примеров.
Пациент Р., 56 лет, был госпитализирован в стационар с диагнозом «Массивное ЖКК. Острая постгеморрагическая анемия». При поступлении больной предъявлял жалобы на многократный черный стул, одышку, слабость. Из анамнеза известно, что 2 года назад он перенес инфаркт миокарда, после чего постоянно принимал ацетилсалициловую кислоту (АСК), метопролол. Год назад стал ощущать перебои в работе сердца. Больному поставили диагноз ФП, в связи с чем был назначен варфарин в дозе 7,5 мг (3 таблетки), о подборе дозы информации нет.
Последнее значение МНО (6 месяцев назад) — 3,3. Диету не соблюдал. Со слов жены, периодически злоупотреблял алкоголем. Последнюю неделю много работал, из-за чего плохо питался. Два дня назад почувствовал слабость, появились одышка, головокружение, затем пациент отметил жидкий черный стул, который связывал с употреблением большого количества кофе. Слабость нарастала, и больной был госпитализирован по «03».
При первичном осмотре: состояние тяжелое, кожа бледная, пастозность голеней. В легких хрипов нет. Тоны сердца приглушенные, неритмичные. ЧСС — 120 уд/мин, АД — 90/55 мм рт. ст., ЧДД — 22 в минуту. Живот при пальпации мягкий, умеренно болезненный в эпигастрии и по ходу толстой кишки. Симптомов раздражения брюшины нет. Печень не увеличена. При ректальном исследовании — мелена.
В анализах крови: анемия (гемоглобин — 61 г/л, гематокрит — 24, эритроциты — 2,7 × 1012/л), МНО — 12,7.
При ЭГДС обнаружилось, что желудок заполнен большим количеством крови. После отмывания ледяной водой выявлен острый эрозивный пангастрит, сохранялось капиллярное кровотечение (слизистая оболочка «плачет» кровью).
Была начата инфузионная терапия с введением эритроцитарной массы, плазмозамещающих растворов, менадиона натрия бисульфита, ИПП.
Несмотря на проводившуюся терапию, состояние пациента быстро ухудшалось. Его готовили к гастрэктомии. Сохранялись гипотензия, признаки продолжающегося кровотечения, на фоне которых пациент скончался.
На секции — массивное ЖКК из эрозий желудка и практически всей поверхности тонкой кишки, признаки постгеморрагической анемии.
Такие случаи, может быть, не столь трагичные, есть в практике многих врачей.
Предоставляют ли НОАК какие-либо преимущества в уменьшении риска ЖКК? Ответ неоднозначен. Так, в метаанализе D. Capodanno и соавт. (2013) при безусловно более высокой эффективности НОАК по сравнению с варфарином параметры их безопасности выглядят неоднородно: отмечается статистически значимое снижение риска геморрагического инсульта и внутричерепного кровотечения при некотором увеличении частоты ЖКК. Последний параметр характеризуется высокой гетерогенностью в анализируемых исследованиях, что требует дополнительной индивидуальной оценки каждого препарата. Интересно, что, несмотря на неоднозначные результаты по безопасности, авторы указывают на НОАК как на препараты первой линии при выборе антикоагулянтного лечения у пациентов с ФП[8].
Другой метаанализ (L. Loffredo и соавт., 2015), в который был также включен эдоксабан(1), показал, что по сравнению с варфарином суммарно НОАК статистически значимо увеличивают риск ЖКК (ОР = 1,23; 95%-й ДИ: 1,03–1,46; p = 0,01). Риск ЖКК повышали ривароксабан (ОР = 1,46; 95%-й ДИ: 1,2–1,8; p < 0,001), высокие дозы эдоксабана (ОР = 1,22; 95%-й ДИ: 1,01–1,47; p = 0,038) и дабигатрана этексилата (ОР = 1,50; 95%-й ДИ: 1,20–1,88; p < 0,001). Не влияли на риск ЖКК эдоксабан и дабигатрана этексилат в низких дозах (что в некоторой степени снизило их эффективность). Апиксабан оказался единственным препаратом, для полной дозы которого не зафиксировано увеличение риска подобного кровотечения (ОР = 0,89; 95%-й ДИ: 0,70–1,15; р = 0,37), при превосходящей эффективности в профилактике инсульта[14]. Аналогичные результаты получены при изучении его применения по другим показаниям (лечение острой венозной тромбоэмболии, первичная и вторичная профилактика в ортопедии)[11].
Оценивая увеличение частоты кровотечения из ЖКТ при применении антикоагулянта, необходимо прежде всего учитывать локализацию кровотечения и его объем. Невозможно сопоставлять незначительные, или «минорные», кровотечения из десен (которые также являются кровотечениями из пищеварительного тракта!) и массивные, приводящие к необходимости хирургического вмешательства. Слишком разную клиническую значимость они имеют. С другой стороны, необходимо принимать во внимание дополнительные факторы, такие как язвенный анамнез и сопутствующая терапия АСК.
Эффекты варфарина в условиях клинического исследования и в реальной жизни достаточно сильно различаются. Приведенный клинический случай демонстрирует, что отсутствие должного контроля со стороны врача и настороженности пациента в отношении кровотечения применение АСК, несоблюдение режима приема лекарств приводят к серьезным последствиям и даже к смерти. Такое вряд ли произошло бы при клиническом исследовании. Набирающее популярность изучение реальной практики позволит оценить истинный риск ЖКК при применении варфарина и НОАК.
ЖЕЛУДОЧНО-КИШЕЧНАЯ ПЕРЕНОСИМОСТЬ АНТИКОАГУЛЯНТОВ
В целом частота желудочно-кишечной диспепсии при приеме НОАК составляет 1/100 случаев и более. Этот показатель необходимо рассматривать прежде всего как фактор, влияющий на приверженность пациента предписанной терапии. По данным исследования RE-LY, лечение дабигатрана этексилатом пациенты прекращали статистически значимо чаще, чем терапию варфарином, из-за диспепсии (110 мг дабигатрана этексилата — 2,2%, 150 мг дабигатрана этексилата — 2,1%; варфарин — 0,6%). Основная причина этого побочного эффекта дабигатрана этексилата — наличие винной кислоты в лекарственной форме, которая введена туда для улучшения всасывания. В литературе также имеются клинические примеры возникновения эрозивных поражений ЖКТ на фоне приема дабигатрана этексилата[16]. Ни апиксабан, ни ривароксабан таким эффектом не обладают[9, 10, 15].
Итак, как помочь пациенту с язвенной болезнью в анамнезе (в период ее обострения НОАК противопоказаны) избежать нежелательных явлений со стороны ЖКТ при необходимости приема оральных антикоагулянтов? Прежде всего, надо знать современные возможности гастропротекции и иметь представление о вероятных лекарственных взаимодействиях у коморбидных больных.
ИПП и антациды являются наиболее часто используемыми препаратами у подобных пациентов. Исследования I фазы НОАК показали минимальное влияние на биодоступность и другие параметры фармакокинетики при использовании ИПП[11]. Антациды не влияют на кинетику ингибиторов Ха-фактора, однако у дабигатрана этексилата, для всасывания которого требуется кислая среда, возможна вариабельность биодоступности. Современные же ИПП, вероятно, могут уменьшить риск диспепсии и кровотечений. Запланированные исследования дадут ответ на этот вопрос в будущем.
ИПП обладают самым мощным эффектом среди всех антисекреторных средств, которые применяются в лечении кислотозависимых заболеваний желудка. Эти препараты дозозависимо подавляют базальную и стимулированную секрецию соляной кислоты клетками слизистой оболочки желудка за счет блокирования Н+/К+-АТФазы — протонной помпы париетальной клетки[12]. ИПП широко используются для профилактики стрессовых и НПВП-индуцированных язв[13, 17]. На сегодняшний день в клинической практике как в России, так и за рубежом используются несколько ИПП — омепразол, лансопразол, пантопразол, эзомепразол, рабепразол, декслансопразол.
Можно заключить, что у коморбидных больных при необходимости применения НОАК с целью гастропротекции предпочтение следует отдавать ИПП с наименьшим лекарственным взаимодействием (пантопразолу) и современным ИПП с модифицированным высвобождением (декслансопразолу с технологией двойного высвобождения, обеспечивающему гастропротективный уровень рН желудочного сока в течение более длительного времени по сравнению с традиционной формой лансопразола)[1].
ПРИМЕНЕНИЕ АНТИКОАГУЛЯНТОВ ПРИ ГИПОКОАГУЛЯЦИИ, СВЯЗАННОЙ С ЗАБОЛЕВАНИЯМИ ПЕЧЕНИ
При тяжелых заболеваниях печени (гепатите, циррозе) в первую очередь происходит уменьшение синтеза факторов свертывания крови, что является важнейшей причиной геморрагического синдрома. Вначале снижается синтез фактора VII, затем II, IX, X, при тяжелой печеночноклеточной недостаточности также уменьшается синтез факторов I, V и XIII. Кроме того, возможно повышенное потребление факторов свертывания. Выделение из поврежденных клеток печени в кровь тромбопластических веществ ведет к диссеминированному внутрисосудистому свертыванию крови с фибринолизом и образованием тромбоцитарных тромбов. Эти процессы требуют повышенного количества I, II, V, VII, IX–XI факторов свертывания, в результате чего развивается коагулопатия потребления. Для дифференцировки первично нарушенного синтеза факторов свертывания и коагулопатии потребления существенное значение имеет повторное исследование коагулограммы: быстрое падение уровней факторов свертывания свидетельствует о коагулопатии потребления[6].
Уменьшение количества тромбоцитов также играет важную роль в развитии геморрагического диатеза при заболеваниях печени; наиболее частыми причинами тромбоцитопении являются гиперспленизм и диссеминированное внутрисосудистое свертывание крови, иногда снижается тромбопластическая активность.
Ксимелагатран в фиксированной дозе был изначально изучен как средство первичной тромбопрофилактики у ортопедических пациентов, затем, учитывая полученные доказательства эффективности, — в аспекте профилактики инсульта при неклапанной фибрилляции предсердий в клиническом исследовании SPORTIF III (2003). Результаты исследования показали, что частота развития инсульта и системных тромбоэмболий, а также геморрагических осложнений при его применении сходна с таковой при использовании варфарина, это дало возможность считать ксимелагатран весьма перспективным для профилактики тромбоэмболических осложнений[7]. Однако выявленная в последующем гепатотоксичность препарата стала причиной его отзыва с фармацевтического рынка.
У всех НОАК обязательно прицельно изучают влияние на функцию печени. В уже упомянутом метаанализе D. Capodanno и соавт. (2013) приводятся данные по печеночной безопасности новых антикоагулянтов[8]. Ни один из них не демонстрирует какого-либо значимого влияния на уровень печеночных ферментов.
Варфарин и ингибиторы Ха-фактора преимущественно метаболизируются в печени. Нарушение ее функции может приводить к увеличению их концентрации и повышению риска кровотечений. Дабигатрана этексилат, который в большей степени выводится почками, теоретически мог бы быть более безопасным, однако клинические исследования не показали каких-либо его отличий от других НОАК.
Следующий аспект применения антикоагулянтов — это возможность их использования у пациентов с различной степенью печеночной недостаточности.
Не рекомендуется применение НОАК при заболеваниях печени, сопровождающихся нарушениями в системе свертывания крови и клинически значимым риском развития кровотечений, например больным с циррозом печени класса С по Чайлду — Пью. При более легких формах цирроза (классов А и В), при сохраненной синтетической функции антикоагулянт может быть назначен. При гипокоагуляции на фоне заболевания печени применение антикоагулянта, особенно с длительным периодом полувыведения (таким как у варфарина), способно привести к фатальному кровотечению. Больные циррозом печени с тяжелой гепатоцеллюлярной недостаточностью — самая сложная группа с неблагоприятным прогнозом, требующая интенсивного мониторинга показателей гемостаза.
При особых ситуациях у таких пациентов, например при тромбозе центрального катетера, возможно применение гепаринов парентерально.
СВЯЗЬ АНТИКОАГУЛЯНТОВ С ПРИЕМОМ ПИЩИ И ДИЕТОЙ
Среди множества факторов, влияющих на терапевтическую эффективность лекарств, существенное место занимает пища. Взаимодействие препарата с различными продуктами иногда влияет не только на развитие фармакологического эффекта, но и на возникновение нежелательных лекарственных реакций. Сочетание лекарств с пищевыми продуктами может повысить их эффективность или же оказаться опасным или бесполезным. Имеет значение не только правильное назначение препаратов по отношению к приему пищи, но и ее качественный состав — необходим учет особенностей воздействия тех или иных продуктов на функциональное состояние органов пищеварения, от которого в значительной мере зависит выраженность действия лекарств.
При взаимодействии препаратов, их метаболитов и пищи в организме происходят сложные процессы, однако они подчиняются общим закономерностям.
Проблема взаимодействия лекарственных средств и пищи имеет несколько аспектов:
- влияние компонентов пищи на терапевтическую эффективность лекарств;
- влияние компонентов пищи на их токсичность;
- влияние препаратов на физиологические процессы пищеварения и на состояние ЖКТ.
Можно выделить несколько этапов взаимодействия лекарственных средств и пищи: всасывание, распределение и выведение из организма. Наиболее часто взаимодействие возникает на этапе всасывания. Всасывание лекарства начинается уже в ротовой полости, но в основном происходит в кишечнике. На абсорбцию в кишечнике большое влияние оказывает скорость опорожнения желудка. В зависимости от состава пища оказывает различное действие на перистальтику желудка.
Жиры, особенно содержащие высшие жирные кислоты, уменьшают выделение желудочного сока и замедляют перистальтику желудка. В ЖКТ жирная пища вызывает перераспределение липофильных и гидрофильных лекарственных препаратов между просветом кишечника и химусом, что изменяет скорость и степень их абсорбции. Под влиянием пищи, богатой жирами, значительно снижается эффективность антигельминтных препаратов, нитрофуранов, фенилсалицилата, сульфаниламидов, диданозина, индинавира, зидовудина. В то же время обогащенную жирами пищу следует рекомендовать в тех случаях, когда требуется повысить всасывание жирорастворимых лекарств — антикоагулянтов, витаминов А, D, Е, метронидазола, транквилизаторов-бензодиазепинов, гризеофульвина, итраконазола. Углеводы также замедляют опорожнение желудка, в результате чего может нарушаться всасывание сульфаниламидов, цефалоспоринов и макролидов[7].
Что касается взаимодействия антикоагулянтов и пищи, то эта проблема в большей степени относится к антагонисту витамина К варфарину. Витамин К — витамин естественного происхождения, содержащийся в основном в зеленых листовых овощах (шпинате, брокколи, латуке) и попадающий в организм с пищей. Кроме того, витамин K синтезируется бактериями в кишечнике. Суточная потребность в нем — 0,03–1,5 мкг/кг/сут (до 105 мкг/сут).
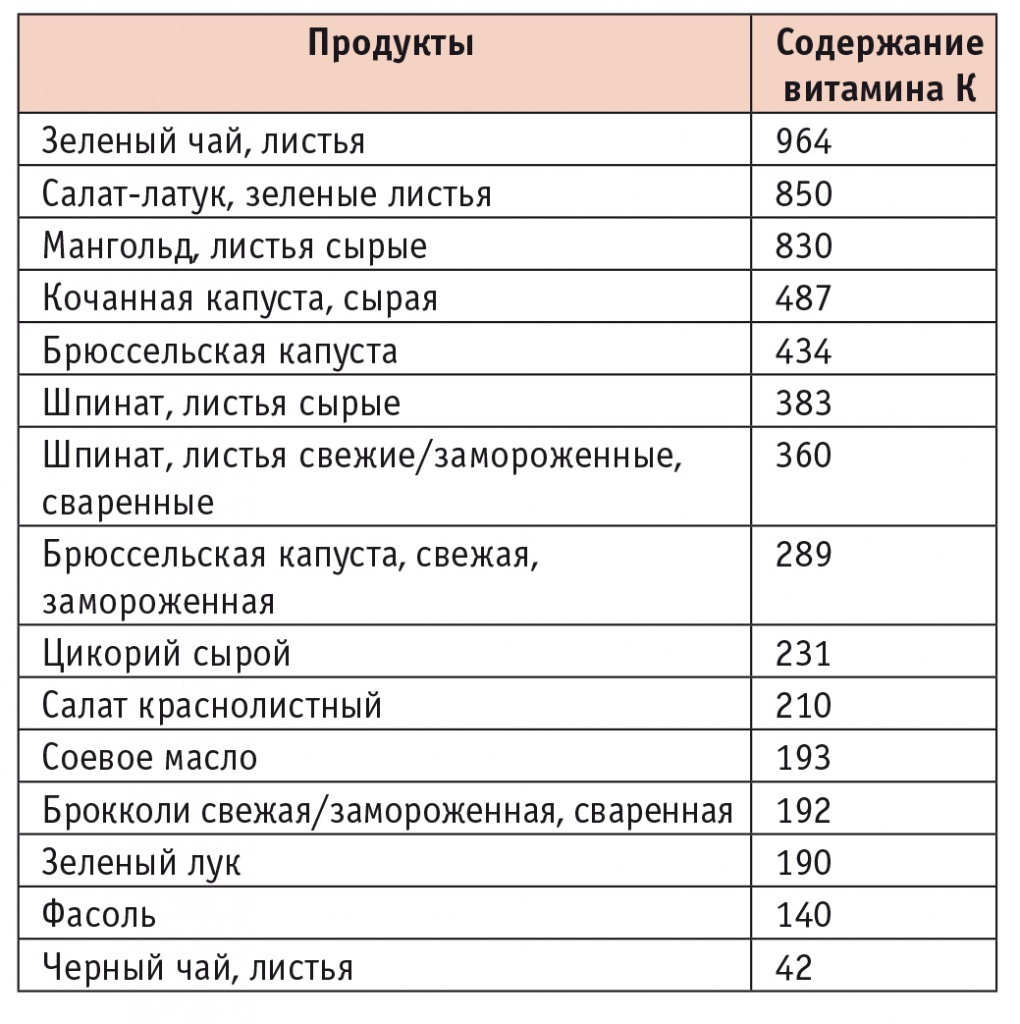
Пациенты, принимающие варфарин, должны соблюдать строгую диету, поскольку, как видно из таблицы, витамин К в большом количестве содержится в определенных продуктах питания и несложно пополнить его запасы в организме, что может привести к недостаточной эффективности препарата.
Таблица
Содержание витамина К в некоторых продуктах, мкг/100 г[7]
Для НОАК заявлено минимальное взаимодействие с продуктами питания. Однако может иметь значение прием НОАК с пищей или натощак. Прием пищи не влияет на абсорбцию дабигатрана этексилата, таким образом, данный препарат можно применять независимо от него. Поскольку прием пищи может влиять на абсорбцию и биодоступность ривароксабана (увеличение на 39% площади под кривой зависимости концентрации в плазме от времени[11]), ривароксабан следует принимать с пищей, что обеспечивает практически полную абсорбцию и почти 100%-ю биодоступность. Но это может вызывать трудности у пациента и снижать комплаенс из-за дополнительных условий лечения. Значимого взаимодействия апиксабана с пищей не отмечено, поэтому его возможно применять независимо от приема пищи, что дает ему преимущества благодаря простой схеме применения.
ТАКТИКА ПРОВЕДЕНИЯ ЭНДОСКОПИЧЕСКОГО ИССЛЕДОВАНИЯ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА НА ФОНЕ ПРИЕМА АНТИКОАГУЛЯНТОВ
Как показали клинические исследования НОАК, большинству пациентов требовалась приостановка приема препарата в связи с различными манипуляциями или оперативными вмешательствами[9–11, 15].
Согласно рекомендациям European Heart Rhythm Association (EHRA, 2013), хирургические вмешательства классифицируют по степени риска кровотечения[11].
- Низкий риск: эндоскопия с биопсией; биопсия простаты, пузырная биопсия; электрофизиологическое исследование, радиочастотная аблация; ангиография, чрескожное коронарное вмешательство; имплантация электрокардиостимулятора, кардиовертера-дефибриллятора; холецистэктомия, гистерэктомия; операция пластики грыж, малая пластическая хирургия; малая ортопедическая хирургия/артроскопия. В первые 48 часов вероятность серьезного кровотечения составляет 0–2%.
- Высокий риск: осложненная аблация; спинальная или эпидуральная анестезия; люмбальная пункция, биопсия печени, почек; абдоминальная хирургия; сосудистая хирургия; трансуретральная резекция простаты; большие ортопедические операции; имплантация электрокардиостимулятора, кардиовертера-дефибриллятора в сложных случаях. В первые 48 часов вероятность серьезного кровотечения ≥ 2–4%.
- Очень высокий риск: нейрохирургические операции (внутричерепные и на позвоночнике); кардиохирургия (коронарное шунтирование и операции на клапанах).
Таким образом, эндоскопические исследования — ЭГДС, колоноскопию и другие со взятием биопсийного материала — стоит рассматривать как вмешательства с низким риском кровотечения. Они требуют прекращения приема антикоагулянта в соответствии с рекомендациями EHRA. При определении сроков отмены необходимо принимать во внимание почечную функцию. Апиксабан и ривароксабан следует отменить за 24 часа до процедуры при клиренсе креатинина выше 30 мл/мин и за 36 часов при 15–30 мл/мин. Учитывая преимущественно почечную экскрецию дабигатрана этексилата, у здоровых пациентов с клиренсом креатинина ≥ 80 мл/мин препарат отменяют как минимум за 24 часа, при клиренсе креатинина 50–80 мл/мин — за 36 часов и более, 30–50 мл/мин — за 48 часов и более. При клиренсе креатинина менее 30 мл/мин дабигатрана этексилат противопоказан.
Возобновить прием НОАК возможно через 6–8 часов при условии достигнутого гемостаза.
Так как опыт перипроцедурального применения НОАК ограничен, а рекомендации основаны в большей степени на некотором допущении, необходимо соблюдать принцип разумности: индивидуально оценивать риск кровотечения и тромбоэмболических событий, в том числе на основании известных шкал расчета их рисков HAS-BLED и CHA2DS2-VASC.
ЗАКЛЮЧЕНИЕ
Рост числа фатальных желудочно-кишечных кровотечений связан не только с приемом нестероидных противовоспалительных препаратов и антикоагулянтов, но и с увеличением количества коморбидных сосудистых больных пожилого возраста. Прием новых оральных антикоагулянтов (НОАК) ассоциируется с меньшей частотой геморрагических осложнений по сравнению с варфарином, при этом только апиксабан среди всех НОАК не увеличивает риск желудочно-кишечных кровотечений. Не рекомендуется применение НОАК при заболеваниях печени, сопровождающихся нарушениями в системе свертывания крови и клинически значимым риском развития кровотечений. У коморбидных больных при необходимости применения НОАК с целью гастропротекции предпочтение следует отдавать ингибиторам протонной помпы с наименьшим лекарственным взаимодействием.
(1) Эдоксабан в России пока не зарегистрирован. Международные клинические исследования этого НОАК проводились с участием РФ. — Примеч. авт.








