Цистатин С представляет собой негликозилированный белок с молекулярной массой 13 кДа, который состоит из 122 аминокислот и является членом семейства ингибиторов цистеиновых протеиназ. Цистатин С — продукт гена «домашнего хозяйства» CST3, экспрессирующегося во всех ядерных клетках с постоянной скоростью. Цистатин С обладает основными свойствами (изоэлектрическая точка pI = 9,0)[28]. Благодаря малому размеру и основным свойствам он свободно фильтруется в почечных клубочках. Цистатин С не секретируется, но реабсорбируется эпителием проксимальных почечных канальцев и впоследствии катаболизируется, так что не возвращается обратно в кровоток[28].
Ингибируя активность протеиназ, цистатин С замедляет деградацию внеклеточного матрикса и участвует в патогенезе атеросклероза, ремоделировании миокарда, инвазии злокачественных опухолей. Нарушение баланса между активностью протеиназ и их ингибитора — цистатина С — ведет к атерогенезу[22, 24]. Показано, что чем выше концентрация цистатина С в сыворотке крови, тем ниже она в артериях и тем чаще наблюдаются неблагоприятные кардиоваскулярные исходы. Выявлено также, что плазменные уровни катепсина S и цистатина С у пациентов со стенокардией выше, чем в контрольной группе здоровых пациентов с нормальным уровнем цистатина С. Содержание цистатина С положительно коррелирует с размером, количеством и распространенностью нестабильных атеросклеротических бляшек[12, 21].
Найдена линейная связь между увеличением концентрации цистатина С и тяжестью ишемии миокарда: повышенные его уровни независимо от других факторов связаны с тяжестью индуцируемой ишемии[7, 9, 25]. Повышенное содержание цистатина С — независимый предиктор кардиальных событий у больных с ОКС без подъема ST-сегмента[39].
У пациентов с атеросклерозом сосудов мозга риск инсульта коррелирует с концентрацией цистатина С[41]. При этом снижение скорости клубочковой фильтрации (СКФ) — это сильный и независимый предиктор неблагоприятного исхода инсульта[15, 40, 43].
В некоторых исследованиях показано, что цистатин С не является причиной повышения риска сердечно-сосудистых заболеваний, а увеличение его концентрации у пациентов с ИБС сопряжено с сопутствующим ухудшением функции почек[27, 38].
Уровень цистатина С в крови почти не зависит от возраста человека и практически постоянен с 1 года до 50 лет жизни. Его концентрация не зависит и от пола[2, 10, 11]. У детей расчет СКФ по цистатину С более точен, чем по креатинину, не связан с полом и наличием дистрофии[10, 11].
Основное преимущество цистатина С перед креатинином для определения СКФ — независимость от телосложения пациента (от веса и мышечной массы)[2, 4, 29, 35]. Благодаря отсутствию связи между концентрацией цистатина С и тощей (безжировой) массой пациента этот показатель оказался более надежным, чем креатинин, маркером СКФ у пациентов с нервной анорексией[2, 10, 11]. Показано, что он превосходит креатинин крови при определении малых нарушений почечной функции у лиц пожилого возраста[30].
Во многих исследованиях сравнивали диагностическую ценность цистатина С и других маркеров. В большинстве работ выявлено, что цистатин С и уравнения на его основе превосходят методы определения СКФ по креатинину крови[10, 11, 13, 29, 32, 34, 36, 37, 42]. Кроме того, что цистатин С позволяет более точно измерять СКФ, чем креатинин, он оказался более чувствительным к малым изменениям СКФ[2, 14, 32, 34, 36]. Концентрацию в крови цистатина С считают лучшим индикатором СКФ, чем концентрацию креатинина, у пациентов со спинальной травмой и циррозом печени[14]. У больных сахарным диабетом 1 и 2 типов цистатин С не только является более надежным, чем креатинин, маркером СКФ, но и лучше коррелирует с изменениями СКФ (происходящими со временем) по мере прогрессирования хронической почечной недостаточности (ХПН)[31, 33].
У реципиентов почки, несмотря на то что СКФ, рассчитанная по цистатину С, занижается на 14%, цистатин С более чувствителен к нарушению функции почек, чем креатинин крови и клиренс креатинина, и не дает ложноотрицательных результатов[20].
Однако на концентрацию цистатина С (как и на концентрацию креатинина крови) независимо от почечной функции влияет функция щитовидной железы. В противоположность содержанию креатинина уровень цистатина С ниже при гипотиреоидизме и выше при гипертиреоидных состояниях по сравнению с нормой. В целом содержание цистатина С может изменяться на 30% при явных заболеваниях щитовидной железы и на 15% — при субклинических состояниях. В связи с данной проблемой для определения СКФ у пациентов с нарушением функции щитовидной железы рекомендуют использовать концентрацию креатинина и формулу Cockcroft — Gault[6]. Нежелательно применять концентрацию цистатина С для определения СКФ, не имея данных о функции щитовидной железы[6].
Известно, что использование глюкокортикоидов дозозависимо повышает уровень цистатина С в крови в результате усиления его синтеза, приводя к занижению рассчитанной СКФ[2, 4].
Влияние на концентрацию цистатина С в крови злокачественных опухолей однозначно не определено. С одной стороны, продемонстрировано повышение его содержания при некоторых злокачественных опухолях[16] и при лейкемиях[5]. С другой — показано, что уровень цистатина С не связан с наличием или отсутствием опухолей[26].
Концентрация цистатина С сильно коррелирует с воспалительными маркерами, фибриногеном, альбумином, D-димером, антитромбином III[18, 27].
Ввиду полного катаболизма невозможен расчет клиренса цистатина С по концентрации в моче. Для оценки СКФ используют его содержание в крови по тому же принципу, что и концентрации мочевины или креатинина в крови[19].
Первый метод определения уровня цистатина С был предложен в 1979 г., его чувствительность составляла 30 мкг/л, чего более чем достаточно для здоровых лиц[23]. Сейчас разработаны методы его определения на основе радиоактивного, флуоресцентного и ферментного анализов, которые дают чувствительность от 0,13 до 1,9 мкг/л[19].
Индивидуальная изменчивость концентрации цистатина С меньше или такая же, как у креатинина[1].
Лишь отдельные исследования показали очень малые половые различия для цистатина С, поэтому референсные значения не зависят от пола[19].
Содержание цистатина С выше в первый год жизни, после чего оно снижается. Поэтому у детей старше года используются референсные значения для взрослых[28]. В целом они действуют для лиц от 1 года до 50 лет. У пожилых людей концентрация цистатина С растет в связи с ухудшением почечной функции[8].
Референсные значения цистатина С зависят от метода его определения и могут различаться на 20–30%[19]. В большинстве исследований обнаружено, что референтный интервал концентраций цистатина С в сыворотке крови (5-й и 99-й процентили) составляет 0,52–0,90 мг/л со средним значением 0,71 мг/л для женщин и 0,56–0,98 мг/л для мужчин, общее среднее значение для мужчин и женщин — 0,77 мг/л. В недавнем широкомасштабном исследовании, включавшем 7596 человек из общей популяции, референтный интервал цистатина С (1-й и 99-й процентили) составлял 0,57–1,12 мг/л для женщин и 0,60–1,11 мг/л для мужчин[3, 17].
Целью данной работы стало сравнение концентраций цистатина С у пациентов с почечной недостаточностью, ОКС и острым нарушением мозгового кровообращения.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось в 2010 и 2013 гг. на базе Центральной клинической больницы с поликлиникой Управления делами Президента РФ. Для выявления различий между концентрациями цистатина С у пациентов с почечной, кардиальной и нейропатологией были отобраны 84 человека: с ХПН (получавшие программный гемодиализ), ОКС, ишемическим инсультом и транзиторными ишемическими атаками мозга. Участники исследования были разделены на три группы: 1-ю составили больные ХПН на программном гемодиализе, 2-ю — пациенты с заболеваниями сердца и 3-ю — пациенты с заболеваниями мозга (табл. 1).
Таблица 1
Клиническая характеристика обследованных больных
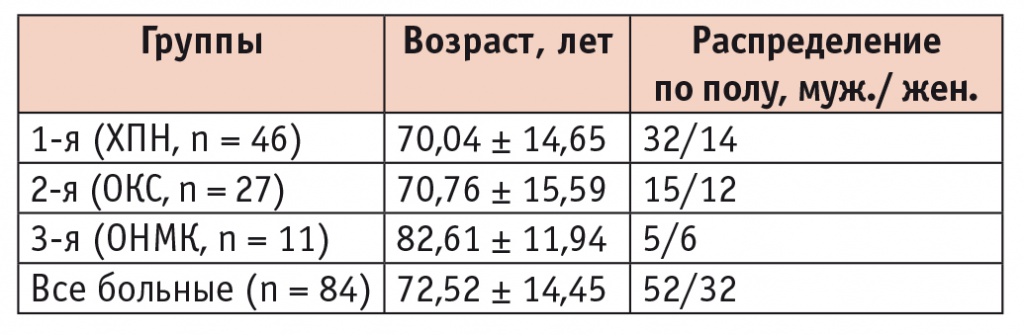
Примечание. ОНМК — острое нарушение мозгового кровообращения; ОКС — острый коронарный синдром; ХПН — хроническая почечная недостаточность.
У всех участников определяли концентрации цистатина С в крови одновременно двумя методами: турбидиметрическим и иммуноферментным. У пациентов 1-й группы уровень цистатина С измеряли перед проведением сеанса гемодиализа.
В первой части работы дополнительно делали анализ соответствия значений цистатина С, определенных двумя лабораторными методами, рассчитывали степень корреляции и формулу, связывавшую полученные значения. Данный анализ позволил оценить, насколько сильно методика определения уровня цистатина С в крови может влиять на полученные показатели. В литературе уже было отмечено, что для каждого метода используются различные референсные значения.
При измерении концентрации цистатина С в крови методом ИФА использовался набор RD191009100 Human Cystatin C ELISA (BioVendor Laboratory Medicine, Inc., Чехия). Он основан на «сэндвич»-методе и предназначен для количественного определения цистатина С в биологических жидкостях человека: в сыворотке и плазме крови, в моче, спинномозговой жидкости и культуральной среде.
Измерение концентрации цистатина С в крови проводили согласно протоколу, предложенному производителем набора. Разведенные образцы, контроли и стандарты вносили в лунки микропланшета, покрытые поликлональными специфическими антителами к цистатину С человека. Цистатин С в нашей пробе связывался с иммобилизованными антителами. Не связавшиеся белки удалялись при тщательной промывке. Затем в лунки с иммобилизованным комплексом «антитело — цистатин С» добавляли антитела к цистатину С человека, меченные ферментом пероксидазой хрена. После второй инкубации и процедуры промывки в лунки добавляли раствор субстрата (перекись водорода и тетраметилбензидин), с которым связавшиеся, конъюгированные с пероксидазой хрена антитела вступали в реакцию, давая голубое окрашивание. Реакцию останавливали, добавляя раствор кислоты, абсорбцию получившегося желтого раствора определяли спектрофотометрически при длине волны 450 нм. Параметры поглощения полученного раствора были прямо пропорциональны концентрации цистатина С, связавшегося с антителами на первом этапе инкубирования образцов. Калибровочная кривая строилась по значениям оптической плотности, полученным для стандартов цистатина С, поставляемых с набором, с использованием четырехпараметрической регрессии.
Турбидиметрический метод основан на связывании специально подготовленных иммуночастиц, содержащих антитела к цистатину С.
Исследования концентрации цистатина С проводились согласно протоколу, поставляемому производителем набора для исследования BÜHLMANN (Швейцария). Образцы сыворотки или плазмы крови смешивали с иммуночастицами, антитела которых связывались с цистатином С, содержавшимся в образцах. Образовавшиеся комплексы частиц поглощали свет, и абсорбция раствора была пропорциональна концентрации цистатина С, которую вычисляли по калибровочной кривой, построенной с помощью стандартов. Значения стандартов специфичны для каждого лота, и при использовании каждого нового лота стандартов строилась новая калибровочная кривая. При использовании набора BCYC-CASET (BÜHLMANN, Швейцария) калибровочная кривая строилась по шести точкам согласно инструкции к анализатору.
Турбидиметрический метод позволяет измерять уровень цистатина С в диапазоне приблизительно 0,4–8,0 мкг/л. Точные значения зависят от значений стандартов, которые специфичны для каждого лота. Предел определения (фактическая чувствительность) турбидиметрического метода набором Cystatin C Immunoassay (BÜHLMANN, Швейцария) составляет 0,031 мкг/л, минимальная определяемая концентрация — 0,33 мкг/л. По инструкции производителя, результаты тестирования, проведенного с использованием данного набора на анализаторе Architect ci8200 (Abbott Diagnostics, США), линейны в диапазоне 0,3–8,8 мкг/л. Референсные значения цистатина С крови для взрослых, согласно руководству BioVendor Laboratory Medicine, Inc. (Чехия), находятся в диапазоне 0,7–1,5 мкг/л.
Поскольку референсные значения цистатина С крови хорошо охарактеризованы и внесены в рекомендации производителей наборов для определения его концентрации, выбор групп пациентов с кардиальной и нейропатологией был произведен для дифференциального контроля, так как учеными описаны изменения уровня цистатина С при этих заболеваниях[38, 40, 41, 43], которые часто с разной степенью выраженности присутствуют у одних и тех же пациентов. Данный анализ позволил нам качественно охарактеризовать диагностическую значимость цистатина С при терминальной почечной недостаточности и интерферирующую роль сосудистой патологии сердца и мозга, широко распространенной среди пожилых больных.
РЕЗУЛЬТАТЫ
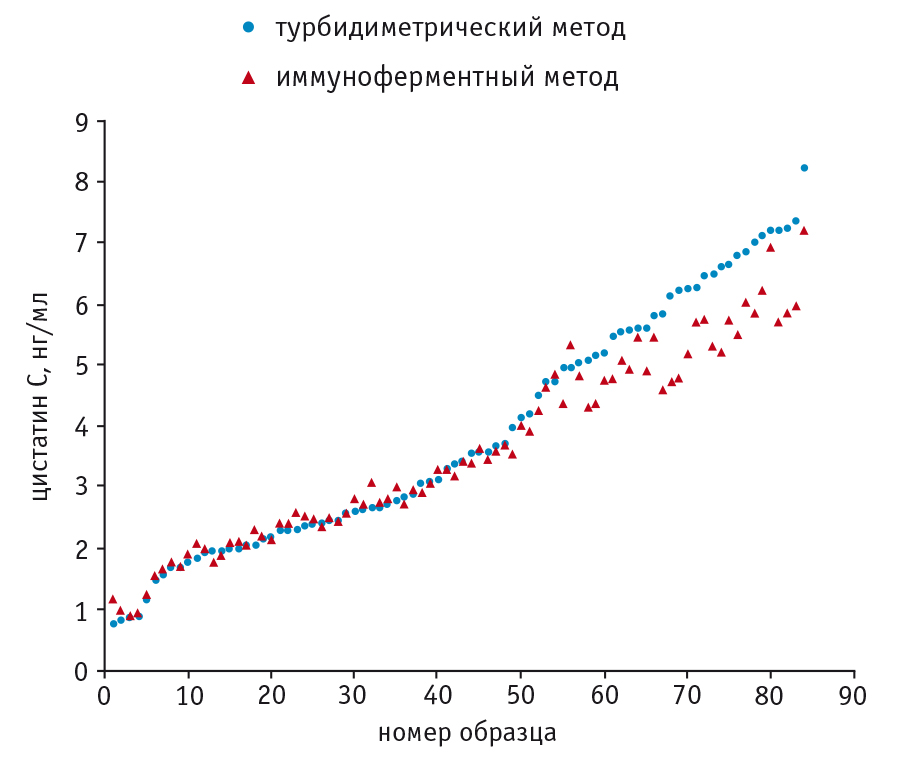
Концентрации цистатина С, определенные турбидиметрическим методом и посредством ИФА, графически отображены на рисунке 1. Как видно из графика, существует взаимосвязь этих значений. При статистическом анализе получена высокая корреляция (r = 0,984, p < 0,0001).
Рис. 1. Результаты определения уровня цистатина С иммуноферментным и турбидиметрическим методами в одних и тех же образцах крови, нг/мл
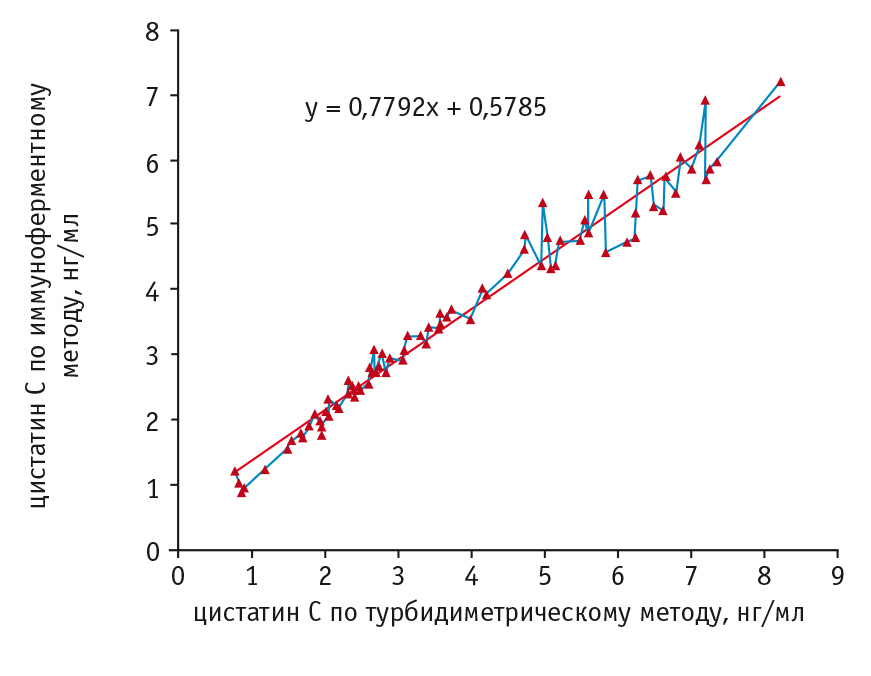
Для выявления зависимости между уровнями цистатина С, измеренными разными методами, был построен график зависимости определенных значений (рис. 2). В результате аппроксимации значений на графике получена зависимость:
у = 0,7792х + 0,5785,
где:
y — концентрация цистатина C, выявленная методом ИФА;
х — концентрация цистатина С, определенная турбидиметрическим методом.
Рис. 2. Зависимость значений цистатина С, определенных иммуноферментным методом, от значений, полученных турбидиметрическим методом
Обнаруженная зависимость практически линейна, однако с увеличением значений на графике отмечается увеличение разброса. Для объективизации отклонений в зависимости показателей цистатина С, определенных методом ИФА, от показателей, определенных турбидиметрическим методом, был произведен расчет ожидаемых значений ИФА по приведенной выше формуле, полученной в результате аппроксимации зависимости значений. Затем было рассчитано процентное отклонение реальных значений цистатина С, определенных посредством ИФА, от его ожидаемых значений (рис. 3).
Рис. 3. Отклонение значений цистатина С, определенных иммуноферментным методом, от ожидаемых, которые были рассчитаны по формуле зависимости от показателей, полученных турбидиметрическим методом, %
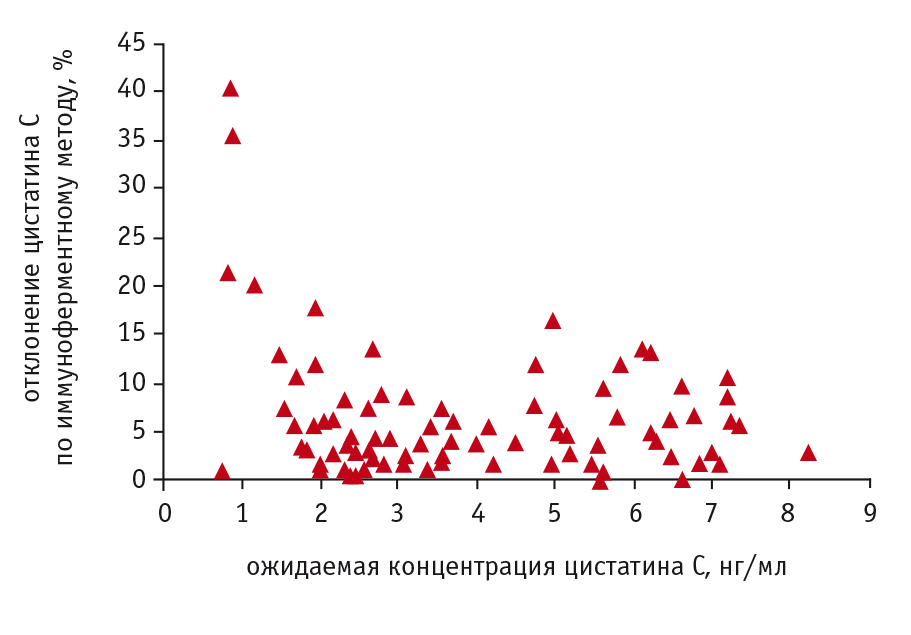
При визуализации реальных и ожидаемых значений цистатина С, полученных методом ИФА и путем расчета по формуле, отмечается большой их разброс при минимальных уровнях цистатина С (около 1 нг/мл), что соответствует верхней границе нормы. Такие показатели практически не встречаются у пациентов с нарушенной функцией почек, и, следовательно, этот разброс не имеет значения в данной группе больных. В целом наблюдается высокая корреляция значений, определенных двумя методами.
На втором этапе исследования мы провели сравнительный анализ концентраций цистатина С, полученных турбидиметрическим методом, у 14 больных, впервые поступивших на программный гемодиализ, и у пациентов 2-й и 3-й групп. Определение уровней цистатина С у пациентов до начала программного гемодиализа представляет больший интерес, чем после проведения сеанса, поскольку процедура гемодиализа сама по себе изменяет концентрацию цистатина С.
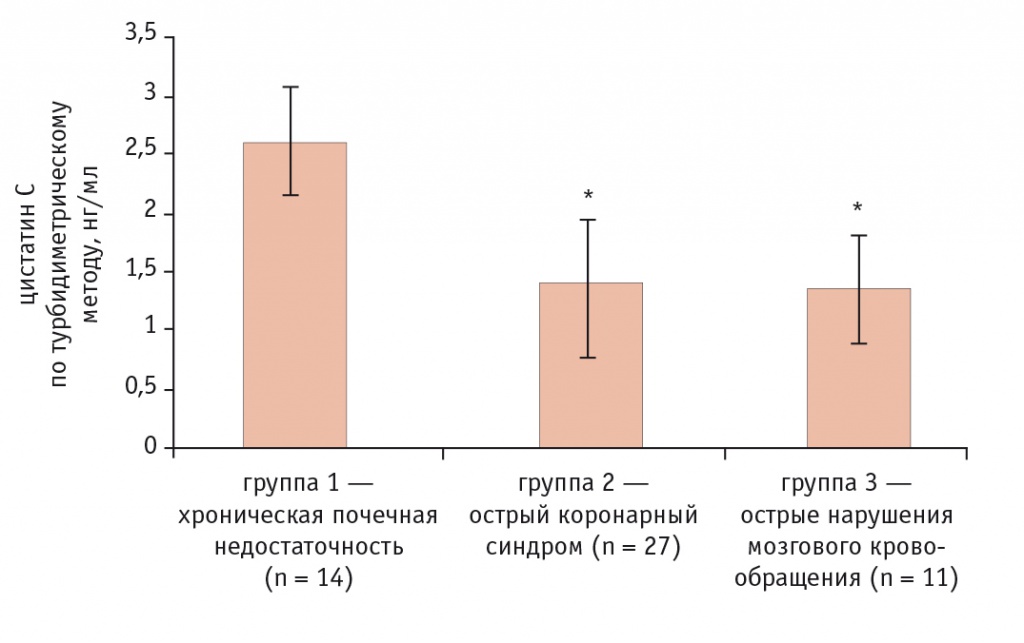
Средние значения и стандартные отклонения для каждой из групп отображены на рисунке 4. При анализе полученных данных были выявлены статистически значимые различия между содержанием цистатина С у пациентов с ХПН и у больных с ишемией сердца и мозга. Уровни цистатина С у пациентов с ишемией миокарда и ишемией мозга практически не различались и превышали норму приблизительно в 1,5 раза. У пациентов с ХПН, впервые поступивших на программный гемодиализ, уровень цистатина С в среднем превышал норму в 2–2,5 раза.
Рис. 4. Средние значения концентрации цистатина С, определенные турбидиметрическим методом, у обследованных пациентов, нг/мл.
* Отличие от группы 1 статистически значимо (p < 0,01)
ЗАКЛЮЧЕНИЕ
В представленной работе показана высокая корреляция между двумя распространенными методами определения концентрации цистатина С.
На небольших сериях также проанализированы уровни цистатина С в разных группах пациентов, в которых их измерение теоретически оправданно для диагностики и стратификации тяжести почечной, кардиальной и нейропатологии. Выявлено, что лишь при почечной недостаточности концентрация цистатина С изменяется значительно и достаточно пропорционально степени нарушения функции почек (скорости клубочковой фильтрации), чтобы служить надежным диагностическим инструментом. В случае ишемических заболеваний сердца и мозга интерферирующим фактором является частое наличие сниженной функции почек; изменения содержания цистатина С при этом неоднозначны и невелики, что соответствует данным литературы.








