Интерес к изучению влияния погоды на течение сердечно-сосудистых заболеваний (ССЗ) значительно возрос после европейской волны жары августа 2010 г., когда смертность от болезней системы кровообращения в Москве возросла более чем на 50%, преимущественно вследствие ИБС [4].
Ранее в различных регионах мира, включая Москву, было отмечено сезонное увеличение смертности от ИБС и заболеваемости ОКС зимой и ее снижение летом [3, 6, 17]. По данным ряда крупных исследований, а также в соответствии с нашими собственными результатами, полученными при анализе динамики госпитализаций по поводу ОКС в Москве в 2009-2012 гг., наиболее значимым метеорологическим фактором для коронарной патологии является температура воздуха [3, 6, 10, 20].
Среднесуточная температура, соответствующая минимальной сердечно-сосудистой и коронарной смертности в Москве, составляет, по данным Б. А. Ревича, около 20 °С [4]. Увеличение и снижение температуры воздуха относительно оптимального диапазона сопровождается увеличением смертности от ССЗ, в частности от ИБС. Волны холода и жары в Москве приводят к большему приросту смертности по сравнению с отдельными холодными и жаркими днями (понятия «холодный» и «жаркий» традиционно определяются через нижние и верхние процентили многолетнего распределения среднесуточных, максимальных или минимальных значений температуры воздуха в данном регионе). Вместе с тем имеющиеся сведения о связи жары с заболеваемостью ОКС противоречивы: в различных исследованиях на фоне высокой температуры воздуха показаны как ее прирост, так и уменьшение [29]. В частности, в Москве достоверных данных об увеличении заболеваемости ОКС во время волн жары нет [3, 6].
Цель исследования: изучить влияние изменения погодных факторов на частоту развития сердечно-сосудистых осложнений (ССО) и динамику некоторых лабораторно-инструментальных показателей у пациентов с ИБС.
МАТЕРИАЛЫ И МЕТОДЫ
В работе представлены результаты 3-летнего наблюдения за состоянием 100 пациентов со стабильной ИБС в зависимости от времени года и метеоусловий в Москве в 2012-2015 гг.
В исследование были включены мужчины старше 40 лет и женщины старше 50 лет с ИБС (верифицированная ишемия миокарда, или инфаркт миокарда (ИМ) либо операция реваскуляризации в анамнезе, или наличие по данным коронароангиографии стенозирующего атеросклероза коронарных артерий — стеноза ствола левой коронарной артерии более 50% или любой другой коронарной артерии более 70%). Больные наблюдались в Российском кардиологическом научно-производственном комплексе (РКНПК), получали оптимальную медикаментозную терапию в соответствии с современными рекомендациями Российского кардиологического общества.
В исследование не включали пациентов, перенесших сосудистое событие или реваскуляризацию в течение последних 3 месяцев до начала наблюдения, а также готовившихся к реваскуляризации; больных с выраженной клиникой недостаточности кровообращения (НК) (III-IV ФК по NYHA), жизнеугрожающими желудочковыми нарушениями ритма сердца, аритмиями и тромботическими состояниями, требующими назначения антикоагулянтов; пациентов с имплантируемыми антиаритмическими устройствами; гемодинамически значимыми пороками сердца, тяжелой сопутствующей патологией, способной оказывать самостоятельное влияние на прогноз.
Наблюдение продолжалось с осени 2012 г. до осени 2015 г. Всем пациентам проводилось амбулаторное обследование в РКНПК, включавшее врачебный осмотр со сбором анамнеза и заполнением специально разработанного опросника самочувствия, регистрацию стандартной ЭКГ, суточное мониторирование ЭКГ по Холтеру (ХМ-ЭКГ), клинический и биохимический анализы крови, а также определение уровней маркеров воспаления и гемостаза: D-димера, фактора Виллебранда, фибриногена, высокочувствительного СРБ (вчСРБ).
Визиты в РКНПК больные совершали регулярно планово, три в холодное (ноябрь-март) и три в теплое (май-сентябрь) время года. Дополнительно посетили РКНПК 23 пациента во время волны жары в июле 2014 г.
Все участники вели дневники АД и ЧСС. Осенью, весной и в периоды жары проводился телефонный опрос пациентов о самочувствии с заполнением опросника. В случае необходимости больные имели возможность связаться с лечащим врачом по телефону в любое время, при наличии показаний проводились коррекция лечения, а также обследование и лечение амбулаторно и в условиях стационара РКНПК.
В качестве порога жары летом нами была принята среднесуточная температура воздуха +22,7 °С, весной в качестве жарких рассматриваются дни с превышением климатической нормы на 5 °С [4].
48 больным были выданы приборы для дистанционной регистрации одноканальной ЭКГ AATOS (Mega Electronics Ltd., Финляндия). Система регистрации ЭКГ состоит из компактного электрокардиографа, смартфона и сервера. Регистрация ЭКГ проводилась пациентами самостоятельно, в амбулаторных условиях, планово регулярно, в одно и то же время суток дважды в неделю (по средам и субботам), в покое в положении лежа, а также при ухудшении самочувствия и при наступлении экстремальных метеоусловий. Полученные фрагменты ЭКГ были в дальнейшем проанализированы на предмет вариабельности ритма сердца (ВРС): рассмотрена динамика временных и спектральных показателей, а также аритмий в сопоставлении со среднесуточной температурой воздуха (по данным ФГБУ «Гидрометцентр России»). С учетом погодных условий, имевших место в дни регистрации фрагментов ЭКГ, включенных в анализ, диапазон зарегистрированных в период мониторирования температур был разбит на четыре категории: -(2-10) °С, +(2-10) °С, +(11-17) °С, выше +21 °С.
Статистический анализ производился с использованием пакета программ Statistica 13.0. Статистическую значимость различий дихотомических показателей оценивали с помощью Q-критерия Кохрена. При сопоставлении парных измерений с непараметрическим распределением применялся тест Вилкоксона.
При анализе показателей ВРС, полученных при дистанционном мониторировании, использовали тест Манна — Уитни. Уровень статистической значимости был принят равным 0,05.
РЕЗУЛЬТАТЫ
Характеристика пациентов, включенных в исследование, представлена в таблице 1.
Таблица 1
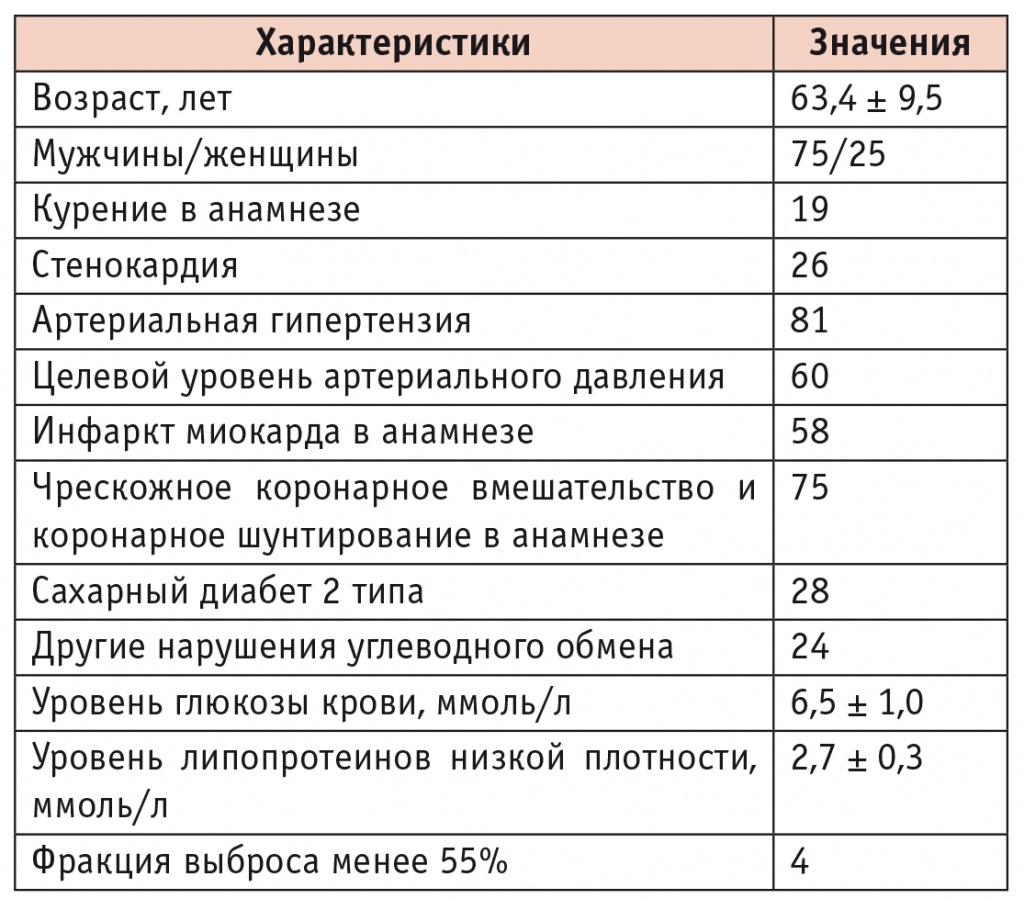
Клиническая характеристика пациентов, включенных в исследование (n = 100)
Ацетилсалициловая кислота и статины были назначены всем больным, β-блокаторы — 92 из них, нитраты — 26, антагонисты кальция — 41, ингибиторы АПФ/сартаны — 80, диуретики — 19. К моменту окончания исследования из 100 больных наблюдаться продолжали 96 человек. Состояние 48 из них оставалось стабильным, у других 48 отмечалось ухудшение, вызванное дестабилизацией АД (100,0%), развитием симптомов НК (4,2%), пароксизма фибрилляции предсердий (ФП) (29,2%), ОКС (20,8%), появлением или учащением приступов стенокардии (33,4%)1.
Погодные условия в 2012-2015 гг. Абсолютные значения температуры воздуха в Москве в 2012-2015 гг. варьировали в диапазоне от -28,5 °C до +32,7 °C, среднесуточная температура воздуха составляла от -21,4 °C до +26,4 °C.
Изучаемый период охватил три холодных сезона, в целом сходных по температурному режиму, и три теплых. Из теплых сезонов наиболее жаркими были май 2013 г. и лето 2014 г. (средняя температура — +17,0 °C и +18,8 °C соответственно), самыми прохладными — май и лето 2015 г. (+14,2 °C и +17,9 °C соответственно). Согласно принятому определению волн жары, в изучаемый период имели место четыре волны жары продолжительностью не менее 5 дней: 7-20 мая и 26-30 июня 2013 г., 18-27 мая и 26 июля — 6 августа 2014 г.
При рассмотрении сезонного распределения основных сердечно-сосудистых событий и жалоб больных, имевших место в период наблюдения (табл. 2, 3), отчетливо выделяются три времени года: лето вне жары, жара (весенняя и летняя), холодное время года (осень, зима, весна вне жары). Летом вне жары ССО в изучаемой группе больных не отмечено, число жалоб было минимальным. Большинство жалоб со стороны сердечно-сосудистой системы (преимущественно на учащение приступов стенокардии и повышение АД) пришлось на холодное время года. 54,2% жалоб на учащение ангинозных приступов зафиксировано зимой, 20,8% — осенью. 5 из 10 случаев ОКС также распределились между осенью (2), зимой (2) и весной вне волн жары (1).
Таблица 2
Сезонное распределение основных сердечно-сосудистых событий за период наблюдения (количество случаев)
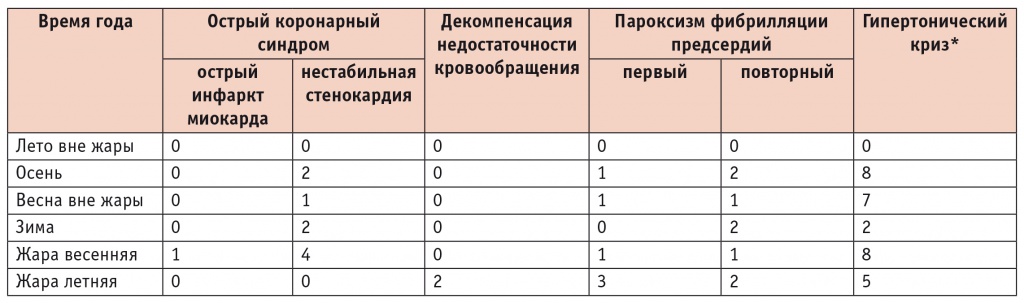
* Различия в количестве гипертонических кризов между всеми сезонами были статистически значимыми (p < 0,05).
Таблица 3
Сезонное распределение жалоб пациентов за период наблюдения (количество случаев)
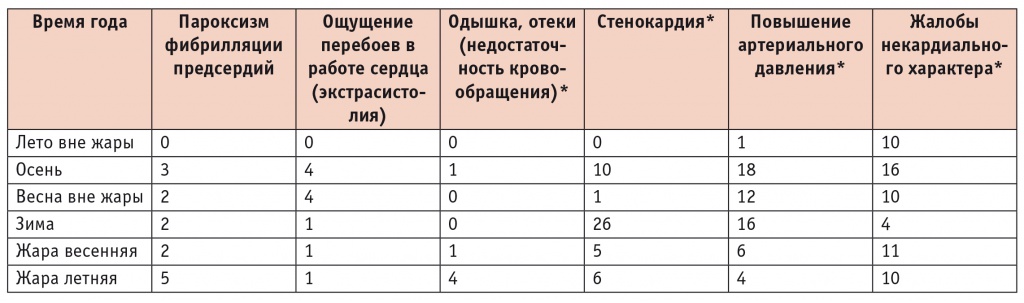
* Различия в количестве жалоб на одышку и отеки, стенокардию, повышение артериального давления, а также некардиальных жалоб между всеми сезонами были статистически значимыми (p < 0,05).
Во время волн жары имели место оба случая декомпенсации НК, потребовавшие госпитализации, и бо́льшая часть жалоб, связанных c НК, а также 4 из 6 впервые развившихся пароксизмов ФП. Кроме того, на жару пришлись половина от общего числа случаев ОКС (5 из 10, включая 1 верифицированный ИМ) и 22,9% жалоб на учащение приступов стенокардии, причем пациенты отмечали первый день повышения температуры воздуха.
У некоторых больных наблюдалось повышение АД в жару, в том числе кризовое, однако оно было спровоцировано физической работой на загородных участках либо снижением качества и нарушением ритма сна в некондиционируемых помещениях. В целом по группе в теплое время года и в жару отмечалась тенденция к снижению АД, имел место один эпизод гипотонии.
Динамика лабораторно-инструментальных показателей также была проанализирована с учетом изменений самочувствия пациентов в холодное время года, летом вне жары и в жару.
В холодное время года по сравнению с теплым во всей изучаемой группе больных отмечалось увеличение уровней гематокрита на 0,2% (р < 0,005), тромбокрита — на 0,01% (р = 0,01) и гемоглобина — на 0,8 г/л (p = 0,006), среди пациентов со стенокардией напряжения также наблюдались выраженная тенденция к повышению содержания вчСРБ (на 0,2 мг/дл; p = 0,06) и статистически значимый рост коэффициента анизотропии эритроцитов (на 0,3; p = 0,03).
При ХМ-ЭКГ статистически значимой сезонной динамики числа эпизодов преходящей ишемии миокарда и их продолжительности не обнаружено, однако выраженность ишемической депрессии сегмента ST в холодное время года была статистически значимо больше, чем в теплое (3,0 ± 1 мм против 1,0 ± 0,5 мм, р = 0,01).
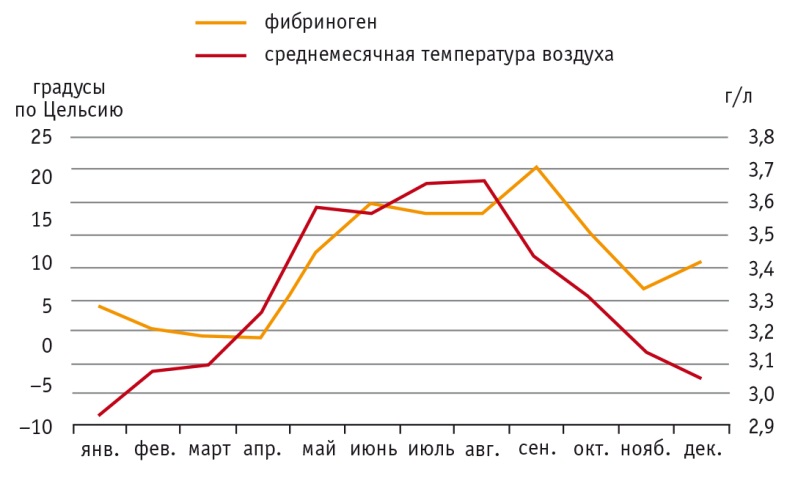
При сравнении уровней фибриногена и фактора Виллебранда в крови пациентов в жару и в умеренные периоды лета 2014 г. статистически значимых различий не выявлено, однако жарким летом 2014 г. концентрация обоих факторов была значимо выше, чем относительно прохладным летом 2013 и 2015 гг., в среднем на 9% (р < 0,0005) и 15% (р = 0,009). У обследованных больных уровень фибриногена статистически значимо коррелировал со среднемесячной температурой воздуха (r = 0,7; p < 0,05) (рис. 1).
Рис. 1. Динамика среднемесячной температуры воздуха и концентрации фибриногена плазмы (r = 0,7; p < 0,05)
Кроме того, в теплое время года по сравнению с холодным и в жару по сравнению с просто теплым временем года в крови пациентов отмечалось статистически значимое снижение концентрации калия и хлора; уровни натрия и креатинина плазмы при этом увеличивались. В группе больных с нарушениями углеводного обмена связь концентрации креатинина со временем года была выражена значимо меньше, а уменьшение концентраций калия и хлора плазмы в жару было сильнее, чем у лиц без нарушений углеводного обмена (p < 0,05 для всех показателей).
При самостоятельной дистанционной регистрации ЭКГ с помощью приборов AATOS в течение изучаемого периода было получено 4250 фрагментов ЭКГ, содержащих не более 10% эктопических комплексов, пригодных для анализа ВРС. При сопоставлении динамики ВРС со среднесуточной температурой воздуха отмечено статистически значимое снижение показателей pNN50, RMSSD, HF (отражающих активность парасимпатической нервной системы) в крайних диапазонах температур: ниже -2 °С и выше +21 °С (рис. 2). В холод и в жару показатели ВРС соответственно снизились: pNN50 на 85,9% и на 79,1%, RMSSD — на 25,5% и на 19,2%, HF — на 40,8% и на 30,5%.
Рис. 2. Параметры вариабельности ритма сердца в зависимости от среднесуточной температуры воздуха
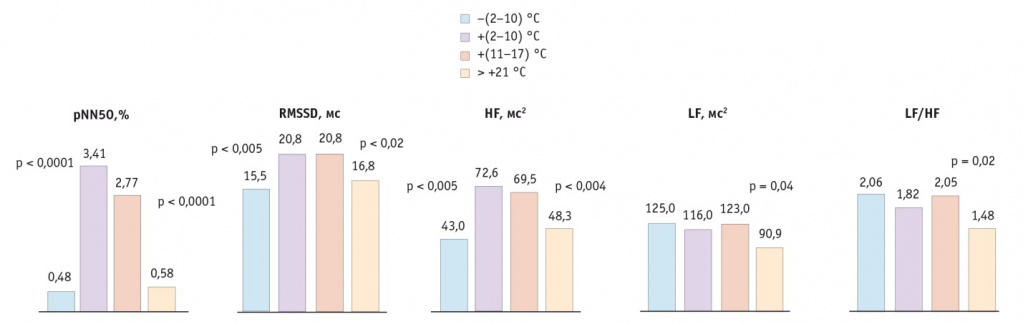
Кроме того, при температуре выше +21 °С имело место статистически значимое уменьшение показателей LF (90,9 [46,4; 150,0] мс2 против 123 [51,2; 238,0] мс2, p = 0,04) и LF/HF (1,48 [0,82; 2,84] против 2,05 [1,02; 3,58], p = 0,02), что может рассматриваться как проявление ослабления дыхательного компонента ВРС и чувствительности барорефлекса в жару [13]. Статистически значимой динамики ЧСС, SDNN не зафиксировано.
ОБСУЖДЕНИЕ
Состояние наших пациентов было оптимальным при умеренной температуре летом. Отмеченное нами увеличение числа жалоб на повышение АД и учащение приступов стенокардии (в рамках стабильной ИБС) в холодное время года соответствует мировым данным [5]. В жару по сравнению с холодным периодом в целом было меньше жалоб, однако большинство проблем, связанных с декомпенсацией НК, развитием пароксизмов ФП, пришлось именно на это время. По результатам ряда эпидемиологических исследований, наиболее частыми кардиальными причинами роста смертности, а также увеличения числа госпитализаций во время волн жары в США, Великобритании, Германии, Чехии явились нарушения ритма сердца и декомпенсация НК; у пациентов, получавших амбулаторную помощь во время волны жары августа 2010 г., также преимущественно отмечались аритмии и проявления сердечной недостаточности [1, 5, 7, 12, 18, 26]. Повышение заболеваемости ОКС во время волн жары подтверждается не во всех исследованиях и не является основной причиной увеличения числа госпитализаций и показателей смертности от ССЗ. В нашем исследовании на периоды волн жары пришлось наибольшее число случаев ОКС, включая один острый ИМ, однако отличие от других периодов не было статистически значимым.
Таким образом, как в холодное время года, так и в жару состояние пациентов с ИБС ухудшалось по сравнению с умеренным летом, но причины ухудшения различаются.
Изменения, происходящие в организме под воздействием холода, объясняются в литературе активацией симпатоадреналовой системы с повышением в крови концентрации катехоламинов и ангиотензина, что, в свою очередь, приводит к повышению тонуса артерий большого круга кровообращения и коронарных. При этом закономерно возрастает АД и учащаются приступы стенокардии. Кроме того, в результате транссудации плазмы в межклеточное вещество развивается гемоконцентрация, которая может предрасполагать к тромботическим осложнениям [16].
В изучаемой нами группе пациентов действительно наблюдалось повышение уровней гемоглобина, гематокрита и тромбокрита. У больных с наиболее тяжелым поражением коронарного русла, у которых сохранялись приступы стенокардии напряжения, в холодное время года повышались также содержание вчСрб и коэффициент анизотропии эритроцитов, являющиеся доказанными предикторами ССО [2, 9, 15]. Возможно, это наблюдение отражает большую предрасположенность к ССО в холодное время года у больных очень высокого риска.
В жару в исследуемой группе пациентов мы отметили снижение почечной функции и изменения электролитного баланса (рост концентрации натрия и снижение концентраций калия и хлора). Подобные наблюдения были сделаны и другими авторами [1, 5]. Описанные изменения соответствуют физиологической адаптации в жару, механизмы которой направлены на сохранение объема циркулирующей крови на фоне перераспределения кровотока и усиленного потоотделения. При этом происходят уменьшение системного АД, ослабление почечного кровотока со снижением скорости клубочковой фильтрации (СКФ), активация симпатоадреналовой системы и РААС [23]. Кроме того, альдостерон и вазопрессин способствуют усилению реабсорбции натрия в почечных канальцах.
Умеренное уменьшение СКФ, повышение концентрации натрия плазмы и снижение содержания калия (за счет усиленного потоотделения и потерь с мочой) у наших пациентов не выходили за пределы нормальных значений, однако в популяции эти изменения в жару могут быть выражены в большей степени и приводить к осложнениям. Так, в Калифорнии в числе частых причин осложнений в жару были дегидратация, нарушения функции почек и электролитного баланса [18].
Описанные изменения концентрации электролитов плазмы способны вносить свой вклад в развитие аритмических осложнений и декомпенсации НК, а также способствовать тромбообразованию [1, 14]. Другим предрасполагающим фактором к нарушениям ритма сердца и иным ССО в жару может быть снижение активности парасимпатической нервной системы, отмеченное нами при дистанционном мониторировании ЭКГ.
Физиологические изменения, связанные с воздействием внешних факторов, опосредованы механизмами вегетативной регуляции. Возможно, именно поэтому у больных с нарушениями углеводного обмена нарастание концентрации креатинина плазмы в жару выражено меньше, чем у пациентов без нарушений углеводного обмена: в связи с развитием полинейропатии вегетативная регуляция у больных этой группы ослабевает. Однако в среднем вследствие поражения почек на фоне сахарного диабета 2 типа уровень креатинина плазмы в данной группе выше, чем у лиц без нарушений углеводного обмена. Усиленное потоотделение, характерное для пациентов с сахарным диабетом 2 типа, может объяснять бо́льшую степень снижения концентрации электролитов плазмы (калия и хлора) во время волн жары.
В жару мы отметили у наших пациентов повышение уровней фибриногена и фактора Виллебранда, связанное, очевидно, именно с усилением их биосинтеза, а не с гемоконцентрацией, учитывая отсутствие статистически значимой динамики гематокрита в жару в исследуемой группе больных. Повышение концентраций фибриногена и фактора Виллебранда, которые в настоящее время рассматриваются в качестве предикторов ССО и маркеров эндотелиальной дисфункции, может увеличивать риск тромбообразования в жару [11, 13, 21].
В данном исследовании мы также обнаружили связь содержания фибриногена плазмы с уровнем среднемесячной температуры воздуха. Максимальным уровень фибриногена был летом и в сентябре, в зимние месяцы также отмечалось некоторое повышение его концентрации в крови пациентов.
Ранее была описана сезонная динамика содержания маркеров гемостаза и воспаления, в том числе фибриногена, с повышением их концентрации зимой и снижением летом [21, 24]. V. L. S. Crawford и соавт. показали рост уровня фибриногена плазмы летом и его положительную связь со среднемесячной температурой воздуха и температурой тела, измерявшейся во внутреннем ухе [8]. R. W. Stout и V. L. S. Crawford отметили максимальный уровень фибриногена плазмы зимой и его отрицательную корреляцию со среднемесячной температурой воздуха и температурой тела [25]. Возможно, в действительности оба приведенных наблюдения отражают U-образную связь температуры тела с уровнем белков острой фазы.
При анализе данных дистанционного мониторирования ЭКГ мы не могли оценить динамику показателей ВРС, отражающих активность симпатического отдела вегетативной нервной системы, так как практически все пациенты получали лечение β-блокаторами. Однако динамика показателей ВРС, описывающих активность парасимпатической нервной системы, выглядела симметрично U-образной кривой (см. рис. 2).
Аналогичный характер связи RMSSD с температурой воздуха был обнаружен E. B. Wassermann и соавт. Они также отметили различия в лаговой структуре теплового и холодового воздействия: при повышении температуры воздуха летом RMSSD снижается быстрее, чем при ее снижении зимой [27]. Вероятно, динамика маркеров ответа острой фазы подчиняется тем же законам.
Возможно, описанный U-образный характер связи физиологических показателей с температурой воздуха определяет аналогичную форму температурных кривых: в частности, U-образно выглядит связь сердечно-сосудистой смертности с температурой воздуха.
Снижение чувствительности барорефлекса, отмеченное нами у пациентов со стабильной ИБС в жару, может лежать в основе ортостатических реакций [28]. Кроме того, по результатам ряда исследований, ослабление чувствительности барорефлекса и дыхательного компонента ВРС может рассматриваться в качестве предиктора ССО [19, 22]. Таким образом, снижение указанных показателей также способно участвовать в генезе ССО в жару.
В рамках данной работы мы не учитывали экспозицию — продолжительность воздействия факторов внешней среды на каждого участника исследования. Ограничением настоящего исследования явилось и отсутствие данных об изменениях внутренней температуры тела участников. Данный показатель коррелирует с температурой окружающей среды [8, 25, 27]. Возможно, дальнейшее изучение связи, существующей между динамикой факторов внешней среды и изменениями внутренней температуры тела, позволит подойти ближе к индивидуальной оценке риска ССО пациентов при различных метеоусловиях и разработке персональных рекомендаций.
ЗАКЛЮЧЕНИЕ
Для пациентов с ишемической болезнью сердца лето вне жары является наиболее благоприятным временем года. В холодное время года и при наступлении волн жары число жалоб и сердечно-сосудистых осложнений увеличивается. Использование методов дистанционного контроля с помощью приборов ААТОС позволяет получать дополнительную информацию о состоянии пациентов.
Notes
- [←1]
-
Возобновление или учащение исходно наблюдавшихся приступов стенокардии, имевшие место у 16 больных, рассматриваются в рамках стабильной ИБС, т. к. пациенты предъявили жалобы более чем через месяц от начала ухудшения.








