Вагинальные инфекции, к числу которых относят бактериальный вагиноз (БВ), кандидозный вульвовагинит (КВВ), трихомониаз, аэробный (неспецифический) вагинит, являются основной причиной патологических вагинальных выделений. Вагинальные инфекции не только существенно снижают качество жизни женщины, но также ассоциированы с рядом воспалительных заболеваний репродуктивного тракта и становятся одной из частых причин развития инфекционных осложнений беременности.
Самые частые инфекционные заболевания влагалища — БВ и КВВ, которые в совокупности отвечают за большинство случаев патологических вагинальных выделений [1]. БВ — это полимикробный клинический синдром, для которого характерно замещение физиологической лактобациллярной микрофлоры влагалища другими микроорганизмами, главным образом анаэробными. Несмотря на то что с БВ ассоциирован целый спектр бактерий, результаты многих работ показали, что важнейшими маркерами БВ являются Gardnerella vaginalis и Atopobium vaginae [2].
КВВ вызывается дрожжеподобными грибами рода Candida. До 85% случаев КВВ обусловлены C. albicans, еще около 15% — C. glabrata, остальные виды встречаются гораздо реже [3].
В значительном числе случаев имеет место сочетание БВ и КВВ [4]. В связи с этим комплексная терапия указанных инфекций с использованием комбинированных препаратов представляется оптимальным подходом.
В настоящее время предлагается ряд комбинированных антимикробных препаратов, которые отличаются высокой клинической эффективностью и могут с успехом применяться в терапии инфекций влагалища смешанной этиологии. К их числу относится Метрогил Плюс (Unique Pharmaceutical Laboratories, Индия) — комбинированный препарат в виде геля для интравагинального применения, оказывающий антибактериальное, антимикотическое и противопротозойное действие. Препарат включает в себя метронидазол (10 мг в 1 г геля) и клотримазол (20 мг в 1 г геля), входящие в стандарты терапии БВ и КВВ соответственно.
Метронидазол является основным препаратом группы нитроимидазолов — синтетических антимикробных препаратов с высокой активностью в отношении анаэробных бактерий и возбудителей протозойных инфекций. Механизм действия заключается в биохимическом восстановлении 5-нитрогруппы метронидазола внутриклеточными транспортными белками анаэробных микроорганизмов и простейших. Восстановленная нитрогруппа метронидазола взаимодействует с ДНК клетки микроорганизмов, ингибируя синтез их нуклеиновых кислот, что ведет к гибели микроорганизмов.
Метронидазол активен в отношении большинства анаэробов, как грамотрицательных, так и грамположительных: бактероидов, клостридий, фузобактерий, G. vaginalis. К метронидазолу чувствительны простейшие: трихомонады, лямблии, лейшмании, амебы, балантидии.
Клотримазол — синтетический противогрибковый препарат из группы производных азола для местного (в том числе интравагинального) лечения кандидоза и других микозов. Азолы обладают преимущественно фунгистатическим эффектом, который связан с ингибированием цитохром Р-450-зависимой 14α-деметилазы, катализирующей превращение ланостерола в эргостерол — основной структурный компонент грибковой мембраны. Сообщается об умеренной активности клотримазола в отношении некоторых бактерий (стрептококков, стафилококков, бактероидов) и трихомонад, однако действие препарата на эти микроорганизмы в достаточной мере не изучено [5].
Целью данного исследования было определение in vitro чувствительности микроорганизмов, выделенных из влагалища, к комбинированному препарату местного действия на основе метронидазола и клотримазола.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось в октябре 2017 года в лаборатории микробиологии ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта». В работе использовали клинические изоляты микроорганизмов (всего 421 изолят), выделенных из влагалища женщин репродуктивного возраста: дрожжеподобных грибов рода Candida (C. albicans, C. glabrata), БВ-ассоциированных бактерий (G. vaginalis, A. vaginae), грамотрицательных бактерий (Escherichia coli, Klebsiella pneumoniae, Enterobacter spp.), грамположительных бактерий (Streptococcus agalactiae, Enterococcus spp.), лактобацилл (Lactobacillus iners, L. jensenii, L. gasseri, L. crispatus).
Бактерии культивировали на плотных питательных средах: агаре Сабуро для дрожжеподобных грибов, 5% кровяном агаре для факультативно анаэробных бактерий, агаре Шедлера с 5% бараньей кровью для анаэробных бактерий. Идентификацию микроорганизмов проводили методом MALDI-TOF на масс-спектрометре Microflex (Bruker, Германия).
Для определения чувствительности микроорганизмов к препарату использовали агар Мюллера — Хинтона (Oxoid, Великобритания) без добавления или с добавлением 3% донорской эритроцитарной массы и 2% сыворотки крупного рогатого скота, в зависимости от потребности микроорганизмов в дополнительных питательных веществах.
Для тестирования чувствительности микроорганизмов к изучаемому препарату 0,5 мл взвеси каждого изолята в изотоническом растворе (мутность доводили до 0,5 по МакФарланду) наносили на поверхность плотной питательной среды и равномерно с помощью шпателя распределяли по поверхности. Затем калиброванной петлей объемом 10 мкл наносили исследуемый препарат (без разведения). Чашки Петри инкубировали в течение 24 ч при температуре 37°С. Культуры гарднерелл и лактобацилл инкубировали в анаэростате с газогенерирующими пакетами (Oxoid, Великобритания) в течение 24 ч при температуре 37°С.
Учет результатов чувствительности микроорганизмов к препарату проводили визуально, замеряя диаметр зоны задержки роста. Чувствительной к данному препарату считали культуру микроорганизма с диаметром задержки роста для дрожжеподобных грибов более 18 мм, для других микроорганизмов — более 17 мм.
Статистическая обработка результатов включала определение частоты (%) чувствительных и резистентных изолятов по отношению к общему числу протестированных изолятов.
РЕЗУЛЬТАТЫ
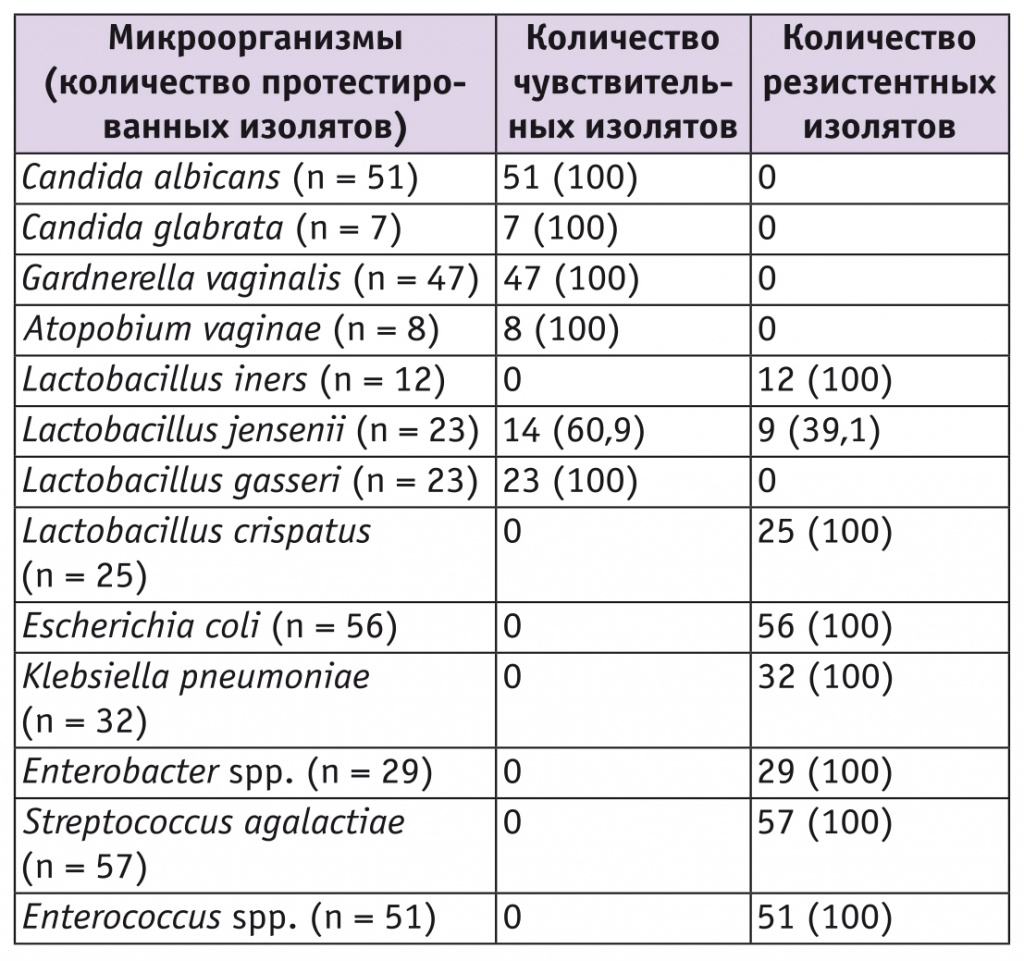
Результаты тестирования чувствительности микроорганизмов, выделенных из влагалища, представлены в таблице. Все протестированные изоляты Candida spp. были чувствительны к препарату. Среди протестированных изолятов G. vaginalis и A. vaginae также не выявлено ни одного резистентного. Показатели чувствительности разных видов лактобацилл существенно варьировали. Все протестированные изоляты L. iners и L. crispatus были резистентны к препарату, тогда как все изоляты L. gasseri чувствительны к нему. Из 23 протестированных изолятов L. jensenii 14 (60,9%) ингибировались препаратом, 9 (39,1%) нет. Все исследованные изоляты грамотрицательных (E. coli, K. pneumoniae, Enterobacter spp.) и грамположительных бактерий (S. agalactiae, Enterococcus spp.) были резистентны к изучаемому препарату.
Таблица
In vitro чувствительность микроорганизмов влагалища к интравагинальному антимикробному препарату Метрогил Плюс, n (%)
ОБСУЖДЕНИЕ
Среди женщин репродуктивного возраста наиболее распространенными гинекологическими инфекционными заболеваниями являются БВ и КВВ. Факторы, предрасполагающие к развитию этих заболеваний, во многом похожи. К ним относятся нарушения системного и местного иммунитета, эндокринная патология, неадекватная контрацепция, изменения нормального микробиоценоза влагалища вследствие нерационального применения антибактериальных препаратов. Несмотря на то что оба заболевания не относятся к числу ИППП, сексуальное поведение имеет определенное значение в их трансмиссии.
Основное направление в лечении БВ — элиминация повышенного количества анаэробных микроорганизмов, что достигается применением метронидазола или клиндамицина (интравагинально или внутрь) или тинидазола (внутрь) [1, 6, 7]. При КВВ используют клотримазол, миконазол, итраконазол, бутоконазол или натамицин интравагинально или флуконазол либо итраконазол (внутрь) [1, 6, 7]. В связи с тем, что C. glabrata и некоторые другие так называемые non-albicans виды рода Candida имеют высокий уровень резистентности к системному антимикотику флуконазолу, а также в связи с ростом резистентности к флуконазолу C. albicans при лечении острого урогенитального кандидоза рекомендуется назначать местнодействующие лекарственные средства [1, 6, 7].
Поскольку роль смешанных вульвовагинальных инфекций в инфекционной патологии женских половых органов существенна, для достижения оптимальных терапевтических результатов представляется целесообразным использование комбинированных антимикробных препаратов. Согласно международным и отечественным рекомендациям, интравагинальные метронидазол и клотримазол относятся к препаратам первой линии при лечении БВ и КВВ соответственно. В связи с этим основное внимание в нашей работе было уделено микроорганизмам, вовлеченным в развитие указанных заболеваний. Необходимо отметить, что, несмотря на высокую антипротозойную активность метронидазола, мы не тестировали чувствительность к данному препарату Trichomonas vaginalis (возбудителя еще одной вагинальной инфекции — трихомониаза). Связано это с тем, что лечение трихомониаза местнодействующими формами метронидазола не рекомендовано ни международными, ни отечественными стандартами терапии [1, 6, 7].
Все протестированные нами изоляты C. albicans (n = 51) и C. glabrata (n = 7) были чувствительны к антимикотическому компоненту исследуемого препарата клотримазолу. Данные литературы относительно показателей резистентности дрожжеподобных грибов рода Candida к клотримазолу существенно разнятся, что может быть обусловлено как региональными различиями в стандартах терапии кандидоза, так и методологическими различиями между исследованиями. Так, в работе S. Khadka и соавт. (2017) 7,2% протестированных изолятов C. albicans и 14,2% изолятов C. glabrata, выделенных у женщин в Непале, были резистентны к клотримазолу [8]. В работе F.J. Wang и соавт. (2016) количество резистентных изолятов C. albicans и C. glabrata, выделенных у женщин в Китае, составило 3,1% и 50,5% соответственно [9]. D.S. ElFeky и соавт. (2016) в популяции женщин из Египта не выявили резистентные к клотримазолу изоляты C. albicans и C. glabrata [10].
Наши данные о высокой активности клотримазола в отношении самых распространенных при КВВ видах рода Candida согласуются с данными Е.И. Касихиной и соавт. (2012), также свидетельствующими о том, что подавляющее большинство штаммов Candida spp. в популяции российских женщин чувствительны к клотримазолу [11].
Метронидазол является эффективным препаратом для эрадикации большинства анаэробных микроорганизмов и на протяжении многих лет считается препаратом выбора, наряду с клиндамицином, для лечения БВ. Согласно результатам нашего исследования, метронидазол высокоактивен в отношении G. vaginalis и A. vaginae, которые рассматриваются как ключевые бактерии, вовлеченные в развитие БВ. Наши данные в значительной мере разнятся с данными литературы, свидетельствующими о достаточно высоких показателях in vitro резистентности G. vaginalis и в большей степени A. vaginae к этому антибиотику.
Так, в недавнем исследовании D.M. Knupp de Souza и соавт. (2016) в экспериментах in vitro показатели резистентности G. vaginalis к метронидазолу, тинидазолу и секнидазолу составляли 59,8%, 60,3% и 71,6% соответственно [12].
Необходимо отметить, что, несмотря на низкую in vitro эффективность метронидазола в отношении некоторых бактерий, ассоциированных с БВ, лечение метронидазолом пациенток с манифестным БВ имеет те же показатели эффективности, что и терапия клиндамицином, обладающим более широким спектром антимикробной активности [13]. Возможное объяснение этому заключается в том, что метронидазол изменяет микрофлору влагалища путем эрадикации чувствительных к нему бактерий, а также воздействием на невосприимчивые к нему бактерии его гидроксильных метаболитов, которые могут быть эффективны in vivo [14].
Особого внимания заслуживает вопрос о действии исследуемого препарата на физиологическую (лактобациллярную) микрофлору влагалища. В нашем исследовании препарат не оказывал антибактериальное действие на рост L. iners и L. crispatus. Около 40% протестированных изолятов L. jensenii также были резистентны к препарату. В то же время Метрогил Плюс ингибировал рост всех изолятов L. gasseri.
Известно, что метронидазол не действует на лактобациллы. Так, M. Petrina и соавт. (2017) при тестировании чувствительности изолятов L. crispatus, L. jensenii, L. gasseri и L. iners к нитроимидазолам (метронидазолу, тинидазолу и секнидазолу) не обнаружили ни одного чувствительного к данным препаратам изолята [15]. В работе C. Neut и соавт. (2015) при тестировании чувствительности трех штаммов вагинальных лактобацилл (L. crispatus, L. jensenii и L. gasseri) к интравагинальным антимикробным препаратам все три вида лактобацилл были резистентны как к метронидазолу, так и к клотримазолу и большинству других азолов, входящих в состав изучаемого препарата в виде единственного компонента [16].
Тем не менее при использовании некоторых комбинированных препаратов, включая комбинации метронидазола с антимикотиками, наблюдали подавление роста того или другого вида лактобацилл [16]. Резистентность L. iners — самого распространенного наряду с L. crispatus вида лактобацилл — к исследуемому препарату представляется нам важным результатом. Этот вид известен своими высокими адаптивными характеристиками, благодаря которым, как полагают, он первым заселяет влагалище после излечения от инфекции и создает условия для роста других видов лактобацилл [17].
Ингибирование роста всех изолятов L. gasseri и некоторых изолятов L. jensenii препаратом метронидазола/клотримазола, показанное в нашей работе, возможно, происходило за счет клотримазола, который оказывает умеренное антибактериальное действие. В то же время ни один из протестированных нами изолятов грамотрицательных (E. coli, K. pneumoniae, Enterobacter spp.) и грамположительных бактерий (S. agalactiae, Enterococcus spp.) не был чувствителен к данному препарату.
ЗАКЛЮЧЕНИЕ
В данной работе показаны высокая in vitro активность интравагинального антимикробного препарата Метрогил Плюс в отношении ключевых микроорганизмов, вызывающих бактериальный вагиноз (БВ) (G. vaginalis и A. vaginae) и кандидозный вульвовагинит (КВВ) (C. albicans и C. glabrata), и отсутствие влияния на основные виды лактобацилл — L. iners и L. crispatus. В совокупности с хорошими фармакокинетическими свойствами, такими как высокая биодоступность и низкая системная абсорбция, это позволяет рассматривать препарат как предпочтительное средство для лечения двух самых распространенных инфекционных заболеваний влагалища — БВ и КВВ.








