Синдром Ретта сопровождается нарушениями нервно-психического развития пациентов с нормальной динамикой до 6–18 месяцев и последующей утратой сформированных ранее навыков самообслуживания и целенаправленных движений рук. Последние замещаются стереотипными «моющими» движениями, сочетающимися с полной потерей речи. Распространенность среди лиц женского пола составляет 1 : 10 000 — 1 : 15 000, у мальчиков встречается крайне редко [1].
Консорциум экспертов в 2010 г. при поддержке Международного фонда синдрома Ретта пересмотрел диагностические критерии заболевания и пришел к новому соглашению. Согласно ему для диагностики типичного варианта синдрома Ретта при наличии регрессии нервно-психического развития достаточно четырех основных критериев [6, 7].
К обязательным диагностическим критериям относятся:
1) частичная или полная утрата приобретенных целенаправленных движений рук;
2) частичная или полная утрата приобретенных навыков экспрессивной речи;
3) аномалии походки: нарушенная походка (диспраксия) или отсутствие способности ходить;
4) стереотипные движения рук, такие как сжатие/сдавливание, хлопки/постукивание, сосание пальцев, «моющие» движения/автоматическое трение рук.
Критерии исключения:
1) повреждение головного мозга в результате травмы (в пери- или постнатальном периоде), нейрометаболических болезней или тяжелой инфекции, которые обусловливают формирование неврологических проблем;
2) нарушение психомоторного развития в первые 6 месяцев жизни.
Постнатальное замедление роста головы было исключено из числа критериев диагностики синдрома Ретта, так как наблюдалось не у всех лиц с типичной формой болезни, хотя данный симптом является клиническим признаком и предупреждает специалиста о возможности развития заболевания [6].
Случаи болезни, удовлетворяющие всем обязательным критериям, получили название классических, практически все они наблюдаются у девочек [8].
В 1999 г. была определена генетическая причина синдрома Ретта. Этиология болезни связана с мутациями в гене МЕСР2, расположенном на длинном плече хромосомы X в участке Xq28 и кодирующем метил-CpG-связывающий белок 2 (МЕСР2); этот ген играет ключевую роль в эпигенетической регуляции активности генов ЦНС [1]. Мутации гена MЕCP2 выявляются у большинства (35–90%) индивидуумов c клиническими признаками классической формы синдрома Ретта [4, 7, 9–11].
Специального лечения к настоящему времени не разработано. Симптоматическая и поддерживающая терапия необходима при дыхательных расстройствах, нарушениях сна (мелатонин), возбуждении (атипичный антипсихотик рисперидон), мышечной ригидности (карбидопа, леводопа); для контроля эпилептических приступов применяются антиэпилептические препараты (АЭП).
Прогноз неблагоприятный, зависит от тяжести течения заболевания: некоторые пациенты умирают в детском или юношеском возрасте, в то время как другие доживают до 20–30 лет и даже более.
Самым распространенным заболеванием, ассоциированным с синдромом Ретта, является эпилепсия: она встречается в 50–80% случаев [12]. Дебют эпилептических приступов приходится преимущественно на II и III стадии синдрома Ретта, возраст больных при этом может варьировать в диапазоне от 4 месяцев до 28 лет. Описаны случаи дебюта синдрома Ретта с эпилептических приступов с последующим развертыванием типичных клинических симптомов. Согласно большинству наблюдений, типы эпилептических приступов различны: 60% случаев являются фокальными, из них до 70% — с вторичной генерализацией; есть данные и о преобладании генерализованных приступов (эпилептический миоклонус и абсансы) [2]. Эпилептические приступы возникают с различной частотой; особой характеристикой при синдроме Ретта является их резистентное течение: приступы не купируются или плохо поддаются противосудорожной терапии (но по мере развития заболевания их частота может снижаться). Для синдрома Ретта также типичны рефлекторные приступы, провоцируемые едой, стрессом, гипервентиляцией; нередко отмечается аутоиндукция [13, 14]. В 40% случаев наблюдается развитие эпилептического статуса [14].
Изменения на ЭЭГ могут быть различными, регистрируются как с появлением эпилептических приступов, так и задолго до их дебюта и включают региональную, мультирегиональную и диффузную эпилептиформную активность, а также медленноволновую (тета-) активность (частотой 4–6 Гц) в центральных, главным образом лобно-центральных, отделах [15]. В отдельных случаях развивается гипсаритмия [16]. Региональная эпилептиформная активность, выявляемая в центральных отделах в виде комплексов «острая — медленная волна», «пик — волна», по морфологии нередко соответствует доброкачественным эпилептиформным паттернам детства (ДЭПД) с нарастанием представленности во сне [2]. Наиболее часто отмечается сочетание диффузной и региональной активности с преобладанием в центральных отведениях [15]. Диффузная активность имеет тенденцию к нарастанию в фазе медленного сна. Иногда регистрируется электрический эпилептический статус во время фазы медленного сна, особенно при раннем дебюте эпилепсии [16].
Изменения на ЭЭГ могут быть связаны с длительностью течения и отражают стадийность синдрома Ретта: постепенное уменьшение индекса эпилептиформной активности и нарастание тета- и дельта-замедления по мере прогрессирования заболевания в IV стадии [2]. В то же время применение антиэпилептической терапии может уменьшать представленность эпилептиформных изменений на ЭЭГ. Анализ данных видео-ЭЭГ-мониторинга у 82 пациенток с синдромом Ретта в возрасте 2–30 лет показал наличие изменений на ЭЭГ в 100% случаев [17]. Максимум эпилептиформной активности был зарегистрирован в фазу медленного сна (97%). Пароксизмальные эпизоды отмечались в 28% случаев, причем в 16,8% наблюдений выявлялись эпилептические приступы, а 11,2% эпизодов расценивались как неэпилептические пароксизмы. У 36% пациентов в ходе видео-ЭЭГ-мониторинга эпилептические приступы были выявлены впервые. Показано, что не все пароксизмальные состояния при синдроме Ретта являются эпилептическими приступами, этим обусловливается необходимость проведения видео-ЭЭГ-мониторинга с включением периода сна у пациентов с синдромом Ретта, поскольку он позволяет разграничивать состояния эпилептической и неэпилептической природы [17].
Цель исследования: изучить клинические особенности эпилепсии при синдроме Ретта в детском возрасте.
МАТЕРИАЛЫ И МЕТОДЫ
В клиническом исследовании приняли участие 11 девочек в возрасте от 2 до 14 лет, которые обследовались и получали лечение на кафедре психиатрии Южно-Уральского государственного медицинского университета (г. Челябинск). Пациентки имели диагноз синдрома Ретта, подтвержденный генетическим верифицирующим обследованием и выявленной мутацией гена MECP2 и отвечавший критериям рубрики F84.2 «Синдром Ретта» МКБ-10.
Были применены следующие методы:
1) клинико-анамнестический, клинико-психопатологический и клинико-динамический с оценкой симптомов согласно диагностическим критериям МКБ-10;
2) нейрофизиологический — видео-ЭЭГ-мониторинг в состоянии бодрствования и сна;
3) нейрорадиологический — КТ головного мозга.
Оценку степени выраженности аутистических проявлений и поведенческих нарушений проводили с использованием Рейтинговой шкалы детского аутизма (англ. Childhood Autism Rating Scale, CARS). Шкала включает в себя 15 позиций, описывающих все значимые для обследования области проявлений ребенка, по каждому параметру дается оценка от 1 до 4 баллов. Итоговая оценка от 15 до 29 баллов соответствует отсутствию аутизма, от 30 до 36 — легкому/умеренно выраженному аутизму, от 37 до 60 баллов — тяжелому аутизму. В диапазоне тяжелого аутизма в ряде случаев выделяют крайне тяжелый — от 42 до 60 баллов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Клинико-психопатологические характеристики. В основу клинической оценки выявленных симптомов были положены стадии течения заболевания. По данным литературы [2], стадия «аутистического регресса» (I) наблюдается в возрасте 6–18 месяцев и характеризуется остановкой развития, аутистическими формами поведения. В стадии «быстрого регресса» (II) в возрасте от 1,5 года до 3 лет появляются специфические двигательные стереотипии в руках и нарастают неврологические нарушения. В «псевдостационарной» стадии (III) в возрасте 3–8 лет отмечаются стабилизация психопатологических симптомов, появление эпилепсии. На стадии «поздних двигательных нарушений» (IV) после 8 лет жизни развивается полная обездвиженность больных и формируются вторичные костные деформации.
В процессе проведенного исследования было выявлено, что все пациентки в возрасте от 12 до 24 месяцев перенесли «аутистический регресс» с остановкой речевого, психомоторного развития и замедлением роста окружности головы.
На момент обследования у 3 пациенток была II стадия течения синдрома Ретта, характеризующаяся «быстрым регрессом» (табл.). В клинической картине отмечались регресс развития с потерей целенаправленного мануального праксиса, который замещался патогномоничными стереотипиями, напоминающими мытье рук, потирание рука об руку, с периодическим касанием рта рукой и облизыванием рук. Оценка проявлений аутизма по шкале CARS соответствовала тяжелому и крайне тяжелому уровню — 37, 42 и 60 баллов.
Таблица
Клинические характеристики обследованных пациенток с синдромом Ретта
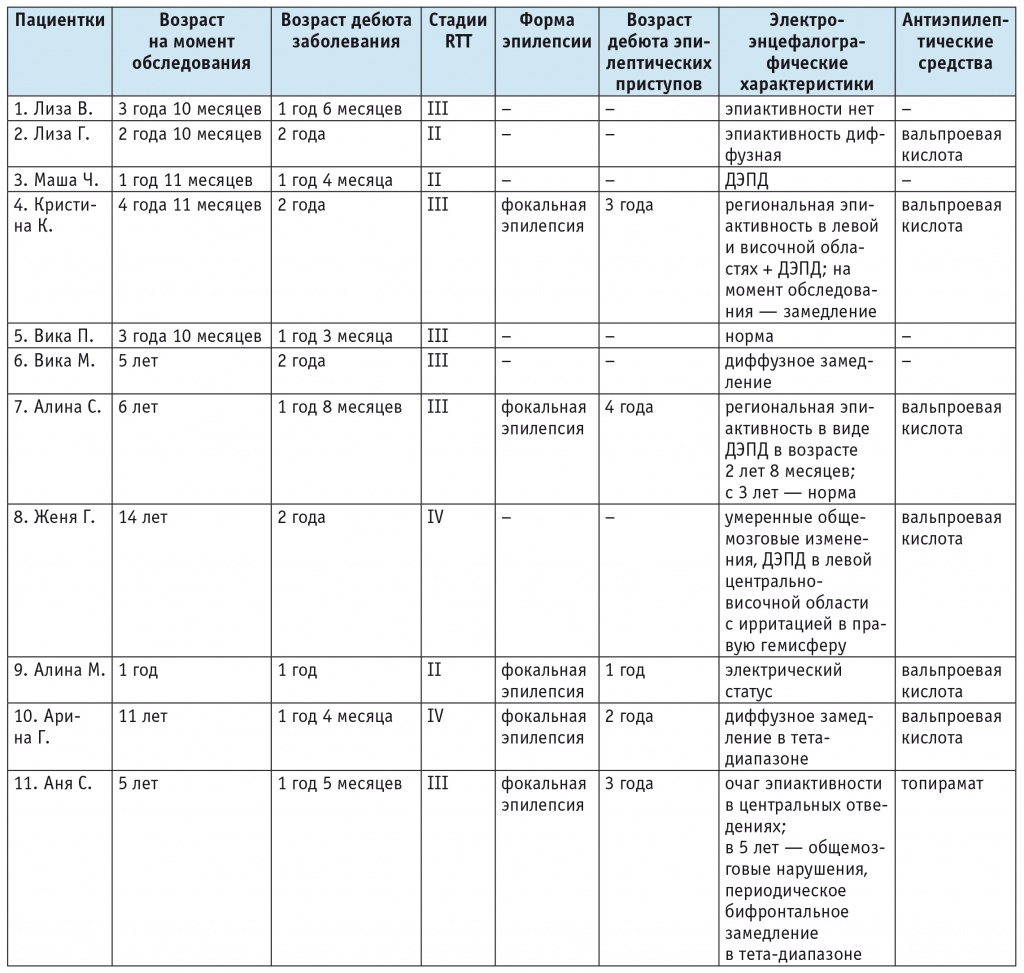
Примечание. ДЭПД — доброкачественные эпилептиформные паттерны детства; RTT — синдром Ретта.
В 6 случаях наблюдалась III, или «псевдостационарная», стадия заболевания (см. табл.), возраст пациенток варьировал от 3 лет 10 месяцев до 6 лет. Состояние больных характеризовалось стабилизацией процесса с наличием тяжелой умственной отсталости, аутизмом. На этой стадии пациентки приобретали навыки социального общения, у них увеличивалась двигательная активность, но продуктивного контакта не происходило из-за отсутствия речи. Экспрессивная речь была представлена отдельными звуками, сенсорное восприятие речи практически отсутствовало. Пациентки были безучастны в поведении, со стереотипными движениями в виде сосания пальцев, «моющих» движений руками, с бруксизмом и беспричинным смехом, при ходьбе нуждались в посторонней поддержке. Проявления аутизма по шкале CARS оценивались как крайне тяжелые — от 42 до 60 баллов. На этой же стадии обычно развивалась эпилепсия.
У 2 пациенток болезнь перешла в IV стадию (см. табл.). У одной из пациенток развились контрактуры голеностопных суставов с возможностью передвигаться только на коленях. У другой больной в клинической картине отмечалась стабилизация состояния: она стала спокойнее, улучшилась осанка, появилось больше социальных навыков (научилась петь, читать стихи с помощью матери), пациентка занимается плаванием, катается на лыжах. В интеллектуальном развитии этих больных сформировался умственный дефект, в речи отмечались эхолалии, оценка по шкале CARS составила 42 и 50 баллов (крайне тяжелый аутизм).
Клинико-эпилептические, нейрофизиологические и нейрорадиологические характеристики. Из 11 обследованных пациенток с синдромом Ретта у 5 была зафиксирована эпилепсия, что составило 45,5% (см. табл.). У всех больных отмечалась фокальная форма эпилепсии, в том числе у одной пациентки имел место электрический эпилептический статус в фазе медленноволнового сна. Приступы, соответственно, носили фокальный характер: наблюдались атипичные абсансы, моторные, вторично-генерализованные приступы. Возраст дебюта приступов варьировал от 1 года до 4 лет.
Как показано в таблице, нормальная картина ЭЭГ имелась только у 2 девочек, в остальных случаях были обнаружены следующие феномены: диффузная эпилептиформная активность (n = 1), региональная эпиактивность (n = 2), ДЭПД (n = 4), региональное или диффузное замедление (n = 4), электрический статус (n = 1). Следует отметить, что характер изменений на ЭЭГ был связан со стадией заболевания. Так, как правило, при II стадии регистрировались различные виды эпилептиформной активности с высоким индексом представленности, электрический статус (при раннем дебюте эпилепсии), а при III и IV — диффузное и региональное замедление при снижении индекса эпилептиформной активности, что могло свидетельствовать о снижении функциональной активности головного мозга и стабилизации частоты приступов.
КТ головного мозга проведена всем пациенткам с эпилепсией. У трех из них выявлена гидроцефалия, у 2 больных патологии не обнаружено.
Терапия АЭП проводилась у 5 девочек с эпилепсией и у двух без эпилепсии (см. табл.). В первом случае назначение АЭП было обусловлено дебютом эпилептических приступов, рекомендовались вальпроаты в дозе 30–40 мг/кг и топирамат в дозе 3 мг/кг. При этом во всех наблюдениях отмечено снижение частоты приступов на 50%, у пациентки с электрическим статусом снизился индекс эпиактивности. У 2 пациенток без эпилепсии вальпроаты назначались в связи с высокой представленностью эпиактивности на ЭЭГ. У одной девочки в возрасте 14 лет при длительном применении вальпроата и выраженных изменениях на ЭЭГ в виде ДЭПД эпиприступы отсутствовали.
ЗАКЛЮЧЕНИЕ
Согласно результатам проведенного исследования, у 45,5% девочек с синдромом Ретта наблюдалась эпилепсия, отмечались фокальные формы с атипичными абсансами, моторными и вторично-генерализованными приступами. Эпилепсия дебютировала на I, II и III стадиях заболевания. Эпилептиформная активность как при эпилепсии, так и без нее определялась стадией синдрома Ретта и зависела от применения антиэпилептических препаратов. Не исключено, что использование вальпроевой кислоты снижало риск возникновения эпилептических приступов у пациенток с синдромом Ретта.








