ВВЕДЕНИЕ
Ишемический инсульт остается ведущей причиной инвалидизации трудоспособного населения во всем мире. В последнем опубликованном международном исследовании эпидемиологии острых нарушений мозгового кровообращения, охватившем период с 1990 по 2019 год, отмечено ежегодное увеличение общего числа инсультов и показано, что ишемические инсульты преобладают в числе новых случаев инсульта (в 2019 году их доля составляла 62,4%). При этом значительная часть бремени болезни приходится на страны с низким и средним уровнем валового национального дохода, в том числе на Российскую Федерацию[1, 2].
В подавляющем большинстве случаев при инсульте развивается двигательный дефицит, структура которого неоднородна и представляет собой синдромокомплекс, включающий снижение силы мышц, изменение их тонуса, а также координаторные нарушения. Степень выраженности составляющих может различаться, но в конечном счете они приводят к значительной дезадаптации пациента. Существенный вклад в этот процесс вносят нарушения ходьбы и равновесия, которые развиваются у многих пациентов и связаны как со слабостью нижней конечности, так и с нефизиологичным восстановлением движения в ней[3].
В последние годы достигнут значительный прогресс в лечении постинсультных двигательных нарушений: активно применяются не только традиционные методы, такие как кинезио- и эрготерапия, но и высокотехнологичные инновационные технологии, например мультимодальная стимуляция. Благодаря одновременной афферентации по нескольким сенсорным каналам у пациентов возникает целостная картина необходимого движения и эффективнее восстанавливается требуемый навык.
Одним из способов включения дополнительных модальностей является виртуальная реальность (ВР). Иммерсивная ВР, то есть ВР с полным погружением, достаточно успешно применяется в качестве самостоятельного реабилитационного метода для коррекции движений паретичной руки, а также зрительно-пространственных нарушений у пациентов с ишемическим инсультом[4, 5]1. Как самостоятельный метод используют также неиммерсивную ВР, в том числе для коррекции постинсультных нарушений ходьбы[6, 7]. Но несколько чаще ВР применяется в комплексе с другими методами реабилитации, например с роботизированными тренажерами[8] или неинвазивной нейромодуляцией[9].
Перспективной методикой, в которую имплементируют ВР, является, в частности, подошвенная стимуляция, достаточно давно назначаемая пациентам с ишемическим инсультом[10]. Проведено исследование применения мультимодальной стимуляции (подошвенная стимуляция в виртуальной среде) у пациентов в остром периоде ишемического инсульта. Оно показало, что такая стимуляция оказывает определенное позитивное влияние в отношении двигательных нарушений, но остались недостаточно изученными лечебные эффекты в более поздние сроки, не были определены факторы, влияющие на общую результативность данной методики[11].
Цель исследования: оценка влияния мультимодальной стимуляции в виртуальной реальности на восстановление ходьбы и равновесия у пациентов в остром и раннем восстановительном периодах ишемического инсульта.
МАТЕРИАЛЫ И МЕТОДЫ
Работа выполнена на клинической базе филиала № 3 «Многопрофильная клиника медицинской реабилитации» Московского научно-практического центра медицинской реабилитации, восстановительной и спортивной медицины Департамента здравоохранения города Москвы (ГАУЗ МНПЦ МРВСМ ДЗМ). Клиническое исследование одобрено локальным этическим комитетом ГАУЗ МНПЦ МРВСМ ДЗМ (протокол № 1 от 17.03.2022) и проводилось при добровольном информированном согласии участников.
В него включались пациенты с первичным ишемическим инсультом любой локализации давностью не более 6 месяцев, осложнившимся гемипарезом или монопарезом нижней конечности (1–4 балла по шкале оценки мышечной силы Британского совета по медицинским исследованиям — англ. Medical Research Council Scale, MRCS), с сохранными когнитивными функциями (26 баллов и выше по Монреальской шкале оценки когнитивных функций — англ. Montreal Cognitive Assessment, MoCA).
Не включались лица с выраженными речевыми нарушениями, онкологическими заболеваниями, перенесшие инфаркт миокарда менее 6 месяцев назад, имевшие пароксизмальную или персистирующую форму фибрилляции предсердий, а также пациенты с эпилепсией или иными пароксизмальными нарушениями сознания. Кроме того, в число исследуемых не входили больные с контрактурами нижних конечностей (в связи с невозможностью проведения подошвенной стимуляции) и с тромбозами вен нижних конечностей (в связи с противопоказанием к применению подошвенной стимуляции).
В результате отбора в исследование вошли 67 пациентов (47 мужчин и 20 женщин) в возрасте от 44 до 75 лет. У 21 пациента (31,3%) ранее диагностировали сахарный диабет (СД), у 13 пациентов (19,4%) — хроническую сердечную недостаточность (ХСН), в 19 случаях (28,3%) — ишемическую болезнь сердца.
Методом случайного распределения больные были разделены на две группы: основную и контрольную. Основную группу составили 36 пациентов (22 мужчины и 14 женщин), возраст — 62,50 [56,75; 65,00] года, время от начала инсульта — 16,50 [12,75; 67,75] дня. В контрольной группе был 31 пациент (25 мужчин и 6 женщин), возраст — 61,00 [59,00; 66,00] года, время от начала инсульта — 17,00 [13,00; 44,50] дня. Группы были сопоставимы по возрасту, факторам риска, степени выраженности неврологических нарушений и давности развития инсульта.
Все пациенты получали базисную реабилитационную программу, включавшую занятия лечебной физкультурой, физиотерапевтические процедуры и лекарственную терапию. Лицам основной группы дополнительно проводили
10 занятий на мультисенсорном тренажере ВР ReviVR («Ревайвер») (Россия), состоящем из программно-аппаратного комплекса, шлема ВР и специальных сандалий с пневматическими камерами. В процессе занятия пациент совершает «виртуальную прогулку» в шлеме, одновременно пневматические камеры создают давление на подошву, имитируя прикосновение к опоре. Движения в ВР синхронизированы с пневмостимуляцией, пациент перемещается в виртуальной среде, получая визуальные, слуховые и тактильные сигналы. Суммарная длительность пребывания в виртуальной среде за одно занятие составляла 15 минут.
Пациентов обследовали до начала реабилитации и после ее окончания. Для оценки выраженности когнитивных и аффективных нарушений использовали шкалу МоСА[12] и госпитальную шкалу тревоги и депрессии (англ. Hospital Anxiety and Depression Scale, HADS)[13], для оценки тяжести инсульта применяли шкалу тяжести инсульта Национальных институтов здоровья США (англ. National Institutes of Health Stroke Scale, NIHSS)[14]. Степень пареза нижней конечности определяли с использованием MRCS. Функциональную независимость оценивали с помощью индекса мобильности Ривермид, а нарушения ходьбы и равновесия — с помощью шкалы Тинетти. В ходе исследования осуществлялся мониторинг нежелательных явлений.
Для статистического анализа полученных данных использовали программу StatTech v. 3.1.5 (ООО «Статтех», Россия). Для ненормально распределенных параметров рассчитывали медиану и квартили (Me [Q1; Q3]). Различия считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
После завершения курса медицинской реабилитации у пациентов обеих групп были зафиксированы положительные изменения, выражавшиеся в увеличении силы мышц нижней конечности, уменьшении выраженности нарушений ходьбы и равновесия, однако в основной группе динамика этих показателей оказалась существенно выше.
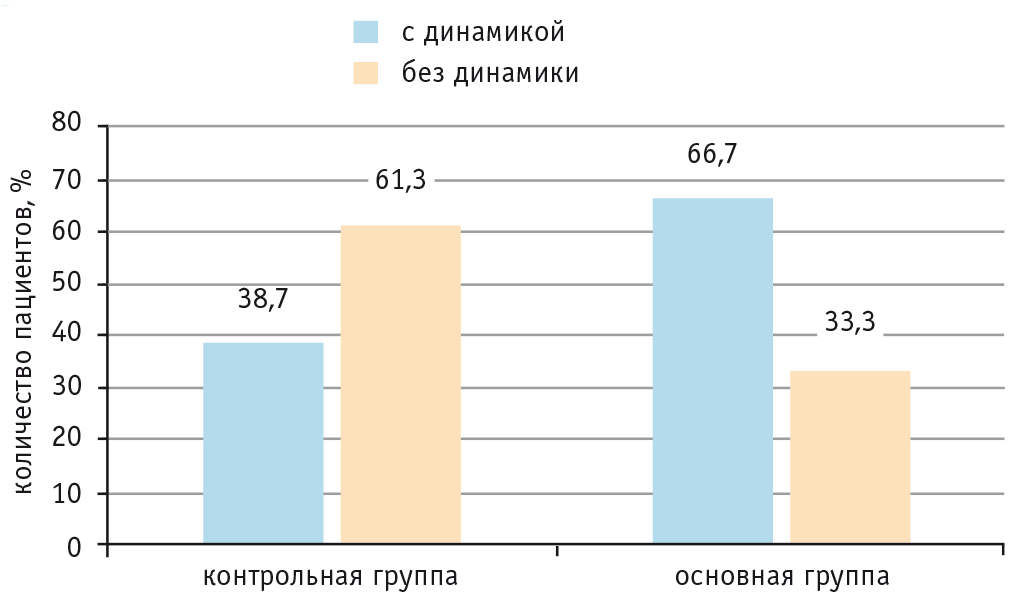
В основной группе увеличение силы мышц нижней конечности по MRCS составило 0,7 [0,3; 0,9] балла, в то время как в контрольной — лишь 0,4 [0,2; 0,7] балла (p = 0,046; U-критерий Манна — Уитни). При этом в основной группе выше был процент пациентов, у которых сила мышц увеличилась более чем на 0,5 балла: 66,7% против 38,7% в контрольной группе (рис. 1, 2).
Рис. 1. Прирост силы мышц нижней конечности в исследуемых группах по MRCS, баллы
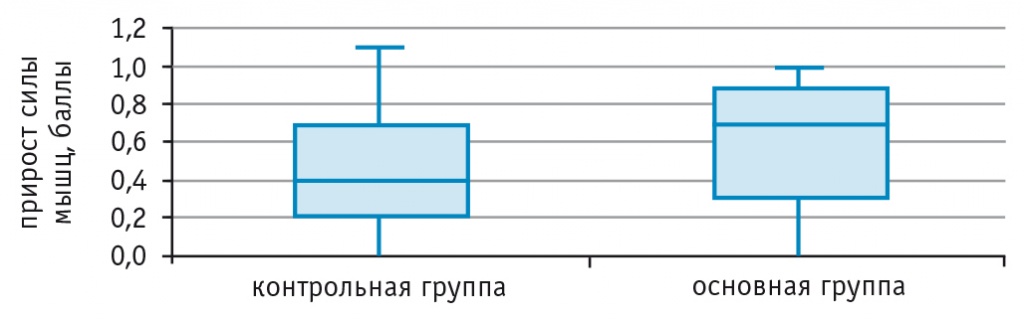
Рис. 2. Соотношение пациентов с наличием и отсутствием положительной динамики по MRCS в исследуемых группах, %.
Примечание. Положительную динамику регистрировали при увеличении силы мышц в нижней конечности более чем на 0,5 балла по MRCS
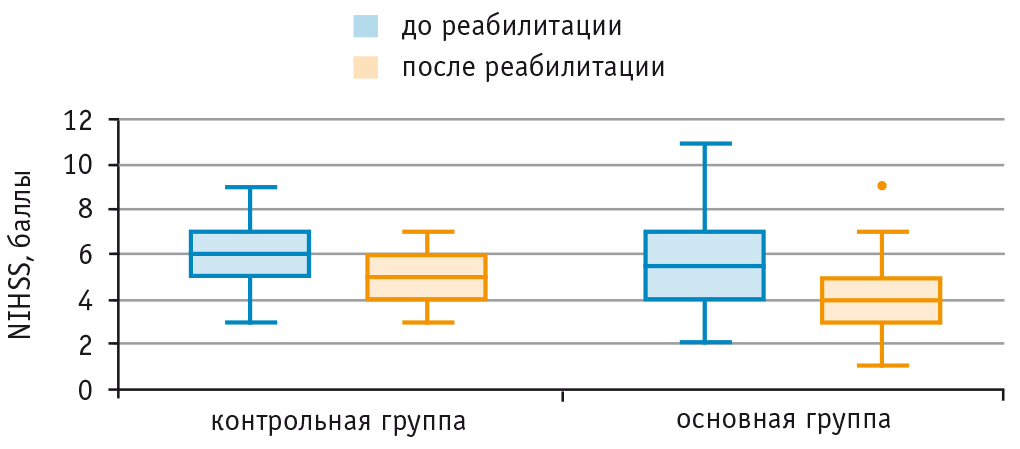
При анализе динамики по NIHSS после курса реабилитации отмечено уменьшение выраженности симптомов у больных основной и контрольной групп: суммарный балл снизился с 5,5 [4,0; 7,0] до 4,0 [3,0; 5,0] и с 6,0 [5,0; 7,0] до 5,0 [4,0; 6,0] соответственно (рис. 3). У пациентов основной группы положительная динамика была более выраженной (p = 0,019; U-критерий Манна — Уитни).
Рис. 3. Динамика по NIHSS в исследуемых группах, баллы
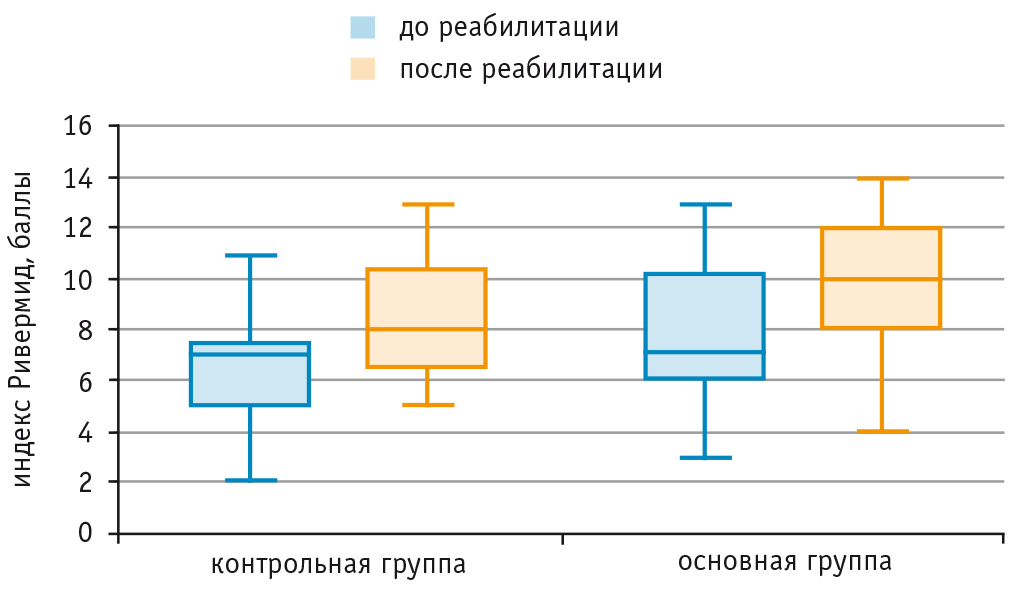
Аналогичные различия были выявлены при сравнении динамики функциональной независимости, оцениваемой с помощью индекса Ривермид. В основной группе отмечено увеличение индекса с 7,0 [6,0; 10,2] до 10,0 [8,0; 12,0] балла, в группе контроля прирост был ниже — с 7,0 [5,0; 7,5] до 8,0 [6,5; 10,5] балла (p = 0,049; U-критерий Манна — Уитни) (рис. 4).
Рис. 4. Динамика индекса мобильности Ривермид в исследуемых группах, баллы
В ходе анализа полученных данных были выявлены факторы, влияющие на степень восстановления двигательных функций. Так, у пациентов с сопутствующим СД статистически значимо хуже восстанавливалась сила мышц паретичной конечности: прирост составил 0,3 [0,2; 0,6] балла против 0,7 [0,3; 0,9] балла у пациентов без СД (p = 0,02; U-критерий Манна — Уитни). Аналогичная корреляция наблюдалась у пациентов с сопутствующей ХСН: сила мышц у таких больных увеличилась на 0,3 [0,1; 0,6] балла против 0,6 [0,3; 0,9] балла у пациентов без ХСН (p = 0,034; U-критерий Манна — Уитни).
Функциональная независимость по индексу Ривермид после курса реабилитации также была ниже при сопутствующем СД: индекс Ривермид у пациентов без СД составил 10,0 [8,0; 12,0] балла, в то время как у лиц с СД — 8,0 [6,0; 11,0] балла (p = 0,045; U-критерий Манна — Уитни).
При оценке других факторов, таких как выраженность когнитивных и аффективных нарушений, статистически значимых различий между исследуемыми группами выявлено не было.
ОБСУЖДЕНИЕ
Мультимодальная стимуляция активно применяется в медицинской реабилитации пациентов с различными неврологическими нарушениями, в том числе постинсультными. Наиболее часто используются визуальные, слуховые и тактильные модальности. Для обеспечения первых двух модальностей оптимальной представляется иммерсивная ВР. Притом что ВР находит применение в медицинской реабилитации как самостоятельный метод[6, 15], ее включение в существующие технические средства в качестве дополнительного инструмента обладает существенным терапевтическим потенциалом[16]. Одна из основных стратегий восстановления двигательных функций при ишемическом инсульте — активация системы зеркальных нейронов. Чем больше афферентных путей возможно задействовать, тем точнее внутренняя картина движения у конкретного пациента и эффективнее реабилитация в целом.
Обнаруженное нами после курса реабилитации уменьшение выраженности неврологического дефицита по шкале NIHSS сопоставимо с результатами T.-H. Ho и соавт., которые показали улучшение по NIHSS у пациентов после семи занятий в виртуальной среде[17]. В то же время другие исследователи статистически значимой разницы в оценках по NIHSS у больных, занимавшихся в ВР и проходивших традиционное лечение, не обнаружили (p = 0,072)[18]. Различия в полученных результатах можно объяснить тем, что в первом случае ВР входила в комплекс мультимодальной стимуляции, а во втором применялась изолированная неиммерсивная ВР.
В группе мультимодальной стимуляции нами выявлено более заметное улучшение функциональной независимости согласно индексу Ривермид, что разнится с данными литературы. В проведенных ранее исследованиях статистически значимого влияния на степень самообслуживания у больных с ишемическим инсультом как изолированной ВР[19], так и ВР, сочетающейся с робот-ассистивной технологией[20], выявлено не было. Полученные нами результаты, вероятно, связаны с характеристикой выборки: в нашей работе испытуемые находились в остром и раннем восстановительном периодах ишемического инсульта, тогда как в указанных исследованиях пациенты начинали курс реабилитации в позднем восстановительном периоде, когда реабилитационный потенциал значительно снижается. Это свидетельствует о необходимости как можно более ранней инициации реабилитации у пациентов с инсультом.
Как в начале, так и по завершении нашего исследования группы пациентов были сопоставимы по выраженности пареза нижней конечности (медианный балл по MRCS). Тем не менее абсолютный прирост силы в основной группе в среднем был статистически значимо выше, что согласуется с данными литературы[21].
Анализ полученных результатов позволил выявить два негативных предиктора восстановления двигательных функций — СД и ХСН. Негативное влияние на динамику восстановления двигательных функций сопутствующего СД согласуется с результатами последнего систематического обзора[22]. СД является сердечно-сосудистым фактором риска и одновременно вызывает целый ряд неврологических осложнений. Как с СД, так и с ХСН связаны нарушения макро- и микроциркуляции, что в свою очередь замедляет процессы репарации и нейрогенеза.
При анализе остальных показателей статистически значимых различий между исследуемыми группами выявлено не было. В обеих группах отмечено уменьшение выраженности нарушений ходьбы и равновесия, оцениваемой по шкале Тинетти, однако в основной группе все же прослеживалась тенденция к более выраженному улучшению. Когнитивные и аффективные показатели за период наблюдения не изменились, что связано в первую очередь с критериями включения в исследование.
За время наблюдения нежелательных явлений у участников исследования отмечено не было. Не зарегистрировано случаев специфического для ВР кинетоза, проявляющегося головокружением и некоторыми вегетативными симптомами. Данный кинетоз возникает, как правило, при активных движениях аватара и быстрой смене сцены в виртуальной среде, из-за чего происходит десинхронизация зрительной, вестибулярной и проприоцептивной систем. В случае мультимодальной стимуляции аудиовизуальные сигналы синхронизированы с проприоцептивными, а движения в ВР достаточно плавны и не сопровождаются резким изменением самой виртуальной среды.
ЗАКЛЮЧЕНИЕ
Полученные нами результаты показывают, что мультимодальная стимуляция является действенным адъювантным методом реабилитации пациентов в остром и раннем восстановительном периодах ишемического инсульта.
Имплементация дополнительных модальностей с помощью виртуальной среды позволяет повысить результативность ранее внедренных методик, в частности подошвенной стимуляции. Стимуляция, включающая зрительную, слуховую и тактильную модальность, дает дополнительный терапевтический эффект в части коррекции двигательных нарушений, в том числе нарушений ходьбы и равновесия, а также улучшает функциональную независимость пациентов.
Поступила: 22.05.2023
Принята к публикации: 26.06.2023
________
1 Всероссийское общество неврологов; Национальная ассоциация по борьбе с инсультом; Ассоциация нейрохирургов России; Межрегиональная общественная организация «Объединение нейроанестезиологов и нейрореаниматологов»; Общероссийская общественная организация «Союз реабилитологов России». Ишемический инсульт и транзиторная ишемическая атака у взрослых: клинические рекомендации. M.; 2021. URL: https://cr.minzdrav.gov.ru/schema/171_2 (дата обращения — 26.07.2023).








