1) повышенная частота сочетания пароксизмов разных типов у одного и того же больного в сравнении с популяционными показателями (проблема коморбидности пароксизмальных проявлений головного мозга) — это закономерность или случайность?
2) выделение в каждом из заболеваний, сопровождающихся приступом (пароксизмом), двух противоположных механизмов: патогенных (болезненных) и саногенных (защитных).
I. ПРОБЛЕМА КОМОРБИДНОСТИ
Г. Н. Крыжановский в своих многолетних экспериментальных исследованиях (1960–1990) убедительно показал наличие общих патофизиологических механизмов двигательных и болевых пароксизмов в виде детерминантных очагов, специфически преобразующих деятельность мозга. Н. П. Бехтерева (1978), анализировавшая свойства эпилептического очага, резюмировала результаты во фразе: «Эпилептический очаг управляет функциональным состоянием мозга». То обстоятельство, что у одного и того же пациента достоверно чаще, чем в популяции, имеет место сочетание разных пароксизмов (эпилептических и мигренозных, эпилептических и вегетативных и др.), позволило нам и А. М. Вейну еще более 25 лет назад независимо друг от друга выдвинуть проблему пароксизмального мозга (Карлов В. А., 1991; Вейн А. М., 1991).
Данная работа является результатом 50-летних экспериментальных и клинических исследований. Экспериментальные исследования проводились на кафедре нормальной физиологии Первого Московского государственного медицинского университета им. И. М. Сеченова (ранее — Первый МОЛМИ), клинические — на кафедре нервных болезней Московского государственного медико-стоматологического университета им. А. И. Евдокимова (ранее — ММСИ), на базах Научно-исследовательского института скорой помощи им. Н. В. Склифосовского и Московской ГКБ № 6.
Один из наименее исследованных клинических аспектов проблемы коморбидности — эпилепсия и синкоп. Совместно с терапевтом, д. м. н. А. В. Певзнером (Институт клинической кардиологии им. А. Л. Мясникова РКНПК Минздрава России) было изучено состояние 52 пациентов с приступами, у которых после осмотра опытным терапевтом и анализа суточной ЭКГ по Холтеру и после осмотра опытным неврологом и анализа рутинной ЭЭГ диагноз не мог быть установлен. В ходе проведенного исследования характер приступов удалось идентифицировать у 47 из 52 человек, т. е. у 90,4% обследуемых.
Были выделены три группы пациентов: I (n = 23) — с нейрокардиогенными обмороками, II (n = 11) — с эпилептическими припадками (ЭП) и III (n = 13) — с сочетанием нейрокардиогенных обмороков и ЭП. Методы исследования представлены на рисунках 1, 2.
Рис. 1. Пассивная ортостатическая проба (Tilt-test): видеоэлектроэнцефалографический мониторинг (ВЭМ); депривация сна (ДС); длительная пассивная ортостатическая проба (ДПОП), %
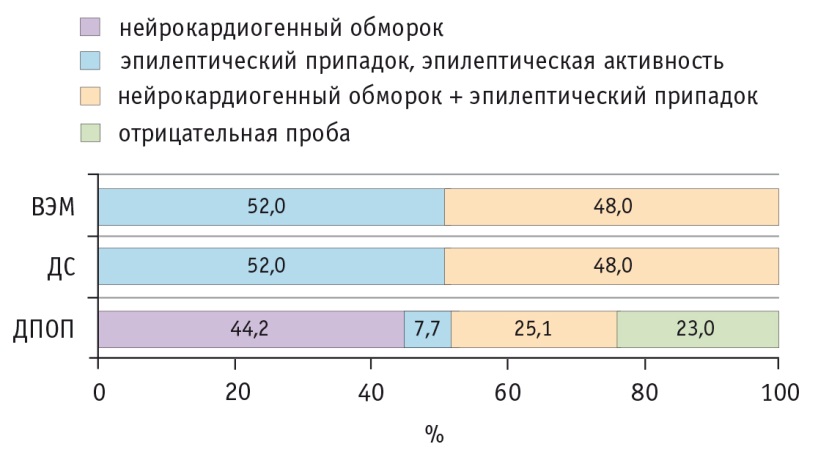
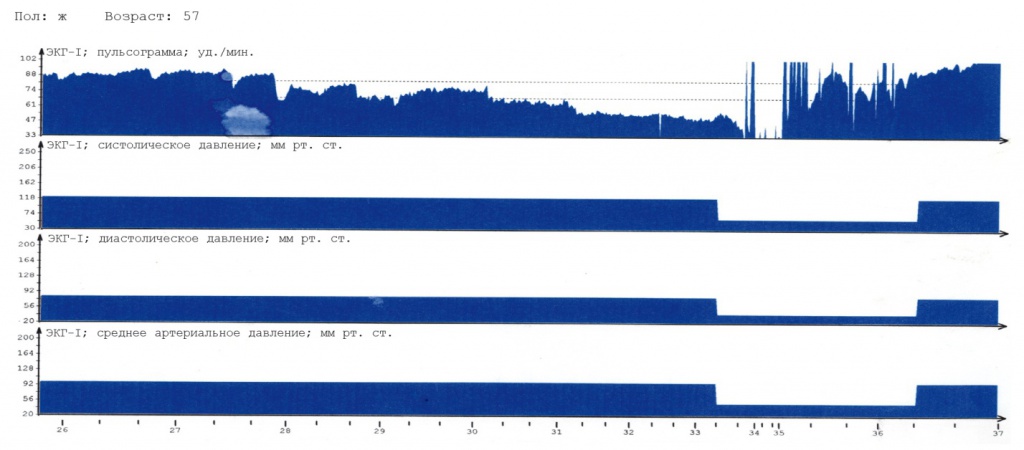
Рис. 2. Динамика физиологических показателей. Асистолия
Пациенты с сочетанием нейрокардиогенных обмороков и ЭП отличались высокой частотой наследственного отягощения по синкопальным приступам, наличием перинатальной патологии, присутствием других видов пароксизмов, возникновением заболевания в пубертатном периоде, дебютом с бессудорожного обморока с последующим присоединением ЭП. Характерно отсутствие пароксизмов, развивающихся во сне. Таким образом, была выделена клиническая форма пароксизмальности — синкоп-эпилепсия.
Нами изучались также пациенты с сочетанием ЭП и панических атак, эпилепсии и мигрени, ЭП и альтернативных дисфорий, по результатам этой работы дано определение сущности припадка. Но прежде чем остановиться на сущности припадка, следует поставить вопрос: такие сочетания — это случайность или закономерность?
Очевидные пароксизмальность, более частое сочетание «эпилепсия + мигрень» и нередкий запуск одного патологического состояния другим (что особенно демонстративно для сочетания «мигрень + эпилепсия»), общее функциональное состояние мозга (сон или бодрствование), ответ на одни и те же лечебные средства (невралгия тройничного нерва (НТН) и эпилепсия — карбамазепин; мигрень и эпилепсия — топирамат; панические атаки и эпилепсия — бензодиазепины) позволяют сделать вывод о том, что в данных случаях коморбидность является закономерностью и, по-видимому, связана с определенными патофизиологическими механизмами.
Наиболее сложен вопрос о механизмах пароксизмальных состояний. Очевидно, что механизмы пароксизмальности могут быть различными и реализовываться на разных уровнях. Рассмотрим два конкретных примера.
Пациентка Н. С., 34 года, мать троих детей. Два с половиной года назад возник приступ головной боли с фотопсиями и левосторонней гемианопсией. Четыре месяца назад перенесла операцию по удалению каверномы правой затылочной доли. С тех пор часто страдает подобными приступами, вызываемыми ярким светом (если это световой пучок, то при засвечивании им нижнего квадранта левого глаза) или решетчатым паттерном (обычно черной решеткой белой кухонной плиты). Приступов не бывает, когда левый глаз закрывает черной повязкой.
Со стороны психики и неврологического статуса изменений нет. КТ: киста правой затылочной доли. ЭЭГ: асимметрия альфа-ритма, усвоение ритма в диапазоне частот от 6 до 12 Гц, эпилептиформная активность не выявляется. Компьютерная периметрия: левосторонняя гомонимная парциальная (в левом глазу за счет верхневисочного сектора, в нижнем есть скотомы) гемианопсия. Зрительные вызванные потенциалы (ЗВП) на шахматный паттерн: латентность Р100 слева в отведении O1-Fz меньше, чем в отведении О2-Fz, на 4,75 мс — значимая межполушарная асимметрия по латентностям коркового ответа. Приступ во время исследования не возникал.
Особенности случая. Приступы имеют органическую основу (постоперационная киста правой затылочной доли), возникают у пациентки с отсутствием отягощения как по мигрени, так и по эпилепсии, вызываются с левого глаза. Они исключительно зрительные (яркие вспышки, молнии, пульсирующее раскаленное пятно), и их можно избежать, если надеть темные очки или, что абсолютно надежно, закрыть левый глаз черной повязкой.
Существенное улучшение возникло на фоне приема леветирацетама, антимигренозные средства оказались неэффективны. В противоположность бытовым факторам провокации, адекватные лабораторные методы воздействия ответа не вызывали.
Трудности дифференциальной диагностики между эпилептическим и мигренозным характером приступов очевидны. Триггером является световое воздействие на нижний квадрант сетчатки левого глаза, в котором, согласно данным периметрии, есть слепые и зрячие участки. Это указывает на то, что сохранившиеся нейроны в соответствующей зоне проекционной зрительной коры являются в той или иной степени денервированными, т. е. лишенными нормальных афферентных импульсов. Таким образом, они подчиняются закону денервационной сверхчувствительности, продуцируя чрезмерный и искаженный ответ на стимулы, что подтверждается уменьшением латентного коркового ответа ЗВП Р100. Остается неясным, почему приступы провоцируются именно бытовыми, а не лабораторными воздействиями. Этот вопрос требует специального исследования.
Второй аспект рассматриваемой проблемы — пароксизмальная боль. В качестве модели для изучения была избрана НТН.
Пациент П. М., 62 года. В течение последних нескольких лет страдает артериальной гипертензией с умеренным повышением артериального давления. Церебральных, коронарных кризов не было. Год назад во время утреннего умывания возник левосторонний приступ острой боли — «прострел» в верхней челюстно-скуловой области. В течение нескольких дней развернулась картина невралгии второй и третьей ветвей левого тройничного нерва с приступами, провоцировавшимися умыванием, жеванием, разговором, бритьем. На фоне комплексной терапии, включавшей применение сосудистых препаратов, антиоксидантов и противоэпилептического препарата (800 мг карбамазепина в сутки), а также орошения курковых зон анестетиком, наступила ремиссия. В дальнейшем пациент принимал поддерживающую комплексную терапию, включавшую противоэпилептический препарат (300 мг карбамазепина в сутки).
Срыв наступил на фоне переохлаждения лица при работе на сквозняке. При осмотре: выражение лица страдальческое, пациент небрит, объясняется жестами. Характерен паттерн приступа, который был спровоцирован попыткой выполнения трехфаланговой пробы: пациент замер, в мимических мышцах лица на стороне боли возникли клонические подергивания и гиперемия, появилось слезотечение. Разбор заболевания не является сейчас нашей задачей, однако нельзя не проанализировать ЗВП больного.
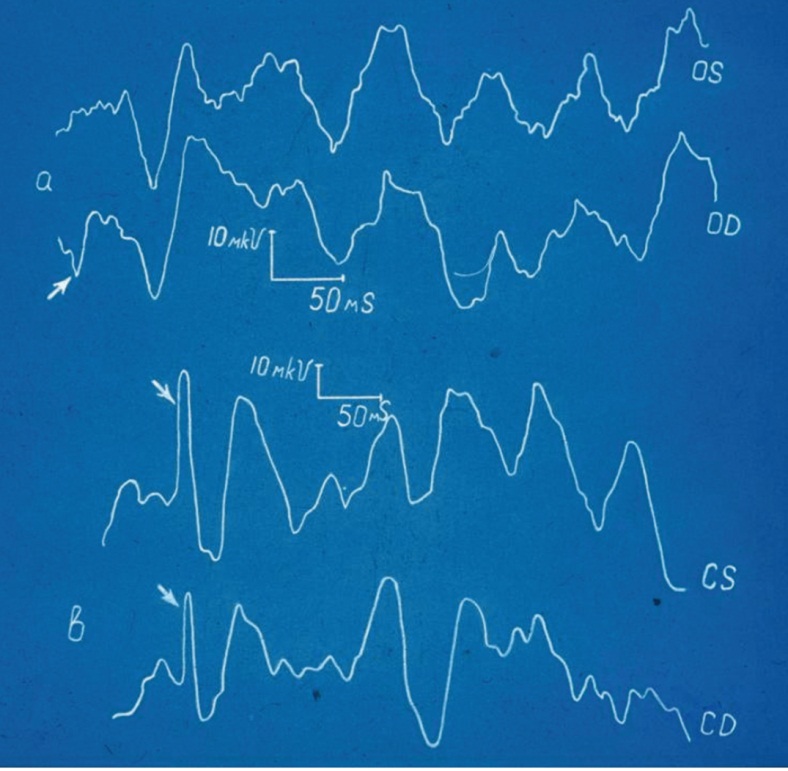
Нами был обнаружен уникальный феномен — перестройка ЗВП по характерному для эпилепсии спайк-волновому типу не в проекционной зрительной коре, а в центральной области (рис. 3). Тем самым было показано, что важнейшим механизмом пароксизмальности при НТН является центральная сенситизация роландической (сенсомоторной) области (Карлов В. А., Поманцев В. А., Петренко С. Е., 1983). Посредством этого была установлена схожесть механизмов центрального звена патогенеза НТН с иктальными механизмами при эпилепсии и объяснена эффективность при НТН не анальгетиков, а ряда противоэпилептических препаратов.
Рис. 3. Зрительные вызванные потенциалы при невралгии тройничного нерва в стадии обострения.
Примечание. OS — левая и OD — правая затылочная кора; CS — левая и CD — правая роландическая (центральная) кора
Как известно, эпилептогенными обычно являются корковые поражения. Согласно упомянутым выше исследованиям, ядром гипервозбужденной болевой системы при НТН также является кора, а именно проекционная роландическая кора. Установление этого факта дало возможность объяснить старое название НТН, данное одним из первоописателей этого заболевания Дж. Фозергиллом (John Fothergill): «болевой тик» (франц. le tic de douleur). В связи с этим уместно вспомнить, что все экспериментальные модели пароксизмальных синдромов отрабатывались на животных позднего филогенетического уровня, т. е. обладающих развитой корой. В то же время кора головного мозга, подобно заднему рогу спинного мозга, обладает релейными свойствами, но значительно более сложными, являясь высшим уровнем, по сути, психической интеграции функций проекционных и неспецифических систем, а также вегетативных функций. В связи с этим она стала ключевым элементом ряда защитных мозговых систем, в частности противоболевой и противоэпилептической. При отказе противоболевой системы приступы НТН трансформируются в status neuralgicus. Пароксизмальность здесь — свойство именно краниальных невралгий, которые разыгрываются в регионе лица, имеющем для человека особую социальную и биологическую значимость.
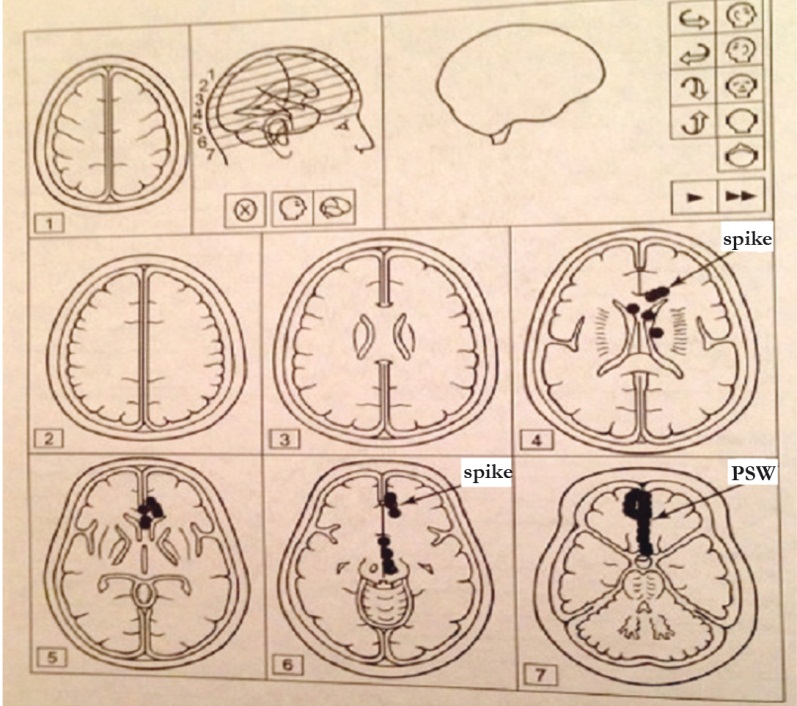
Особой заслугой отечественной эпилептологической школы является учение об эпилептических и противоэпилептических системах (Окуджава В. М., 1969; Степанова Т. С., Грачёв К. В., 1976; Карлов В. А., 1980). В наших исследованиях установлена локализация ингибиторной постспайковой медленной волны в медиобазальных отделах лобной доли головного мозга (Карлов В. А., Гнездицкий В. В., 2000), которая выступает ключевым элементом системы противоэпилептической защиты (рис. 4).
Рис. 4. Данные многошаговой дипольной локализации пациентки М. 34 лет с абсансной эпилепсией, дебютировавшей в 14 лет: спайк локализован справа в медиальной части лобной доли, постспайковая волна — слева в орбитальной коре.
Примечание. PSW — постспайковая волна
Нами совместно с В. В. Гнездицким (Научный центр неврологии РАН) впервые было проведено исследование функционального состояния надсегментарного звена вегетативной нервной системы с помощью регистрации кожного симпатического вызванного потенциала (КСВП) у пациентов с эпилепсией (группа Э), паническими атаками (группа ПА) и сочетанием ЭП и панических атак (группа Э+). В каждую группу входили по 30 человек. Исследовались качество вегетативного регулирования посредством регистрации КСВП и сопоставления данных с результатами ЭЭГ (индексом пароксизмальности, динамикой медленной активности — фоновой и в ответ на гипервентиляцию) и качество жизни больных согласно опроснику Quality of Life 31.
Во всех группах пациентов выявлены существенные отклонения изученных показателей от нормы. Повышение индекса пароксизмальности и нарастание медленной активности были ранжированы по группам: Э, Э+, ПА. Показатели качества вегетативного регулирования оказались ранжированы несколько иначе: Э+, ПА, Э. Эти изменения объединяют больных всех исследованных групп. При их максимальной выраженности у одного и того же больного реализуются оба вида пароксизмов — эпилептические и панические атаки. В то же время имеются и различия: наибольшее снижение качества вегетативного регулирования максимально сближает группы Э+ и ПА, а нарастание индекса пароксизмальности — Э+ и Э. Указанные различия могут объяснить разницу в адресности клинических проявлений — панических атак в первом случае и ЭП во втором.
Установлены недостаточность симпатического (эрготропного) обеспечения при эпилепсии и крайнее напряжение парасимпатической системы стабилизации гомеостаза при панических атаках и их сочетании с ЭП (Гнездицкий В. В., Карлов В. А., Кудрявцева С. В., 2007; Карлов В. А., Гнездицкий В. В., Деряга И. Н., 2008).
II. СУЩНОСТЬ ПРИПАДКА
Вторым слагаемым эпилепсии является нарушение психики. Последнее обычно рассматривается в рамках коморбидности, однако есть и другой аспект их взаимоотношений. Г. Ландольт в 1960-х годах описал феномен «насильственной нормализации» ЭЭГ, отражающий кардинальное изменение в клинической картине заболевания: либо припадки, либо психоз. Поскольку психозы относятся к компетенции психиатров, мы рассматривали эту проблему на модели альтернативных дисфорий. Но все же приведем одно наблюдение продромы альтернативного психоза, поскольку оно в значительной степени уникально.
Пациентка 15 лет, страдает аутизмом и шизофренией, но в то же время полноценно общается путем переписки. Удивительно, что человек, который не говорит, пишет пронзительные стихи. Обращение за неврологической помощью было связано с генерализованными судорожными припадками (ГСП), которыми девочка страдает в течение 4 лет; в конечном счете удалось подобрать эффективную терапию. Через 1,5 года мама с девочкой приходят на прием, и по выражению их лиц видно, что что-то случилось. Мама объясняет: «Психотика пошла» (т. е. у девочки случились два острых психотических эпизода). Растерянная мама спрашивает: «Что же делать?» А девочка пишет: «Может быть, уменьшить дозу противоэпилептических препаратов?»
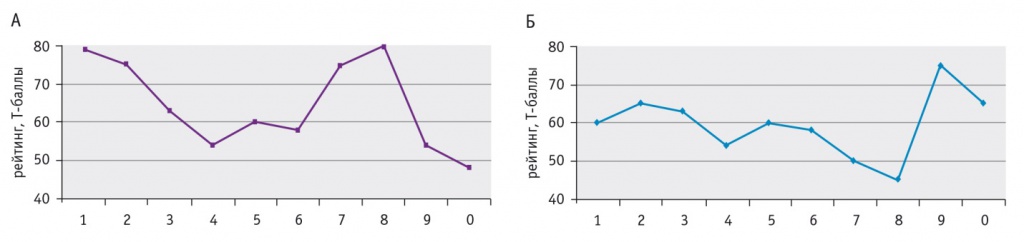
Этот случай возвращает нас к проблеме: что есть ЭП? Нами наблюдались 10 мужчин с ГСП (частота приступов — один раз в месяц). Приступ устранял у этих пациентов дисфорию и возвращал их в социум, но затем постепенно снова возникали и нарастали дисфорические проявления и больные как избавления ожидали очередного приступа. Эти клинические данные нашли подтверждение при исследовании по Миннесотскому многоаспектному личностному опроснику (англ. Minnesota Multiphasic Personality Inventory) (рис. 5А, Б).
Рис. 5. Результаты исследования по Миннесотскому многоаспектному личностному опроснику (наибольший сдвиг по шкалам ипохондрии, депрессии, истерии, психопатии и шизоидности) у четырех пациентов с мезотемпоральной эпилепсией и периодическими приступами за день до (А) и после (Б) генерализованного судорожного припадка, Т-баллы
ЗАКЛЮЧЕНИЕ
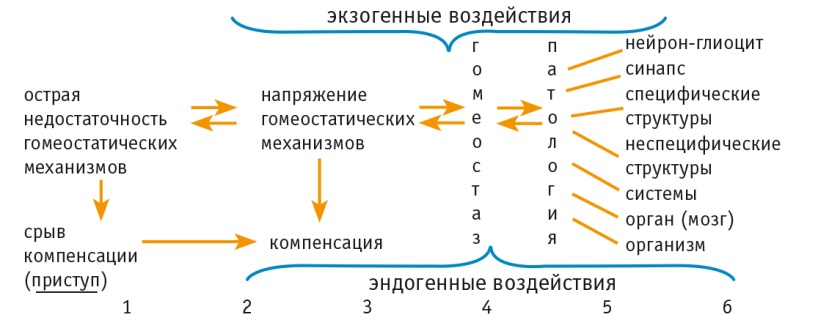
Представленные материалы дополняют известные сведения о применении генерализованных судорожных припадков для лечения ряда патологических состояний: шизофрении, невралгии тройничного нерва и даже суперрефрактерного эпилептического статуса. Они послужили основанием для определения пароксизма с точки зрения его биологической сущности, а именно как срыва перенапряженной системы стабилизации гомеостаза, в результате чего могут быть мобилизованы витальные резервы, не только выводящие пациента из приступа, но и компенсирующие его межприступное состояние (рис. 6).
Рис. 6. Патогенетическая схема развития пароксизмального состояния при заболеваниях нервной системы