Наследственная геморрагическая телеангиэктазия (НГТ) — редкое заболевание, известное также как болезнь Рандю — Ослера — Вебера, наследуемое по аутосомно-доминантному типу. Для него характерны сосудистая дисплазия с образованием телеангиэктазии на коже, слизистых оболочках респираторного, пищеварительного трактов и артериовенозные мальформации (АВМ) во внутренних органах[22, 25].
Цель обзора: изучить литературные данные по применению препарата бевацизумаб для лечения рецидивирующих носовых кровотечений у пациентов с НГТ.
Рецидивирующие носовые кровотечения различной степени интенсивности являются основным симптомом болезни. В статье представлены сведения об использовании препарата бевацизумаб — рекомбинантных моноклональных антител, ингибирующих фактор роста эндотелия сосудов (vascular endothelial growth factor — VEGF), для лечения рецидивирующих носовых кровотечений у пациентов с НГТ.
В 1864 г. Н. Sutton впервые описал рецидивирующие кровотечения у мужчины с телеангиэктазиями на коже и слизистых оболочках. К сожалению, нельзя было проследить наследственный характер симптомов, этот человек оказался сиротой[28]. В 1896 г. вышла статья Н. Rendu, в которой автор описал случай рецидивирующих носовых кровотечений и телеангиэктазий у 52-летнего мужчины, которые стали беспокоить его c 12 лет. У отца этого пациента были желудочно-кишечные кровотечения, мелена и сосудистые «звездочки» на носу, языке, верхней губе[24].
Термин «наследственная геморрагическая телеангиэктазия» был введен в 1909 г. F. Hanes[12]. Стоит отметить, что интерес к этому заболеванию вновь возрос после открытия генетической природы болезни и механизмов ее развития.
ЭПИДЕМИОЛОГИЯ
Болезнь встречается во всех этнических группах, с одинаковой частотой у мужчин и у женщин. Заболеваемость — 1 : 5000–10 000[17]. Имеются данные, что в Северо-Восточной Англии эти цифры несколько меньше и составляют 1 : 40 000[24], тогда как среди скандинавской популяции — 1: 6000[17].
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
В настоящее время выявлено четыре генетические формы НГТ. При первом варианте имеется мутация гена эндоглина. Он располагается на длинном плече 9 хромосомы (9q33-q34). Второй вариант вызван мутацией гена активин-рецептороподобной киназы 1-го типа (activin-receptorlike kinase 1 — ALK-1), который располагается на 12 хромосоме (12q11-q19). Эндоглин и ALK-1 представляют собой клеточные поверхностные рецепторы, участвующие в сигнальных механизмах, опосредованных трансформируемым фактором роста. Мутации генов эндоглина и ALK-1 приводят к снижению концентрации рецепторов на поверхности эндотелия сосудов[2].
Описан и третий вариант — мутация, связанная с геном, расположенным на 5 хромосоме. Четвертый вариант — редкая форма, вызываемая мутацией в гене SHAD4[2].
В основе патогенеза НГТ лежат анатомические и функциональные изменения сосудистого русла[5]. При этом заболевании происходит поражение кровеносных сосудов различного калибра с дегенерацией и гипоплазией мышечного и эластического слоев. В результате развивается очаговое истончение стенок, затем расширение просвета микрососудов. Кровоточивость объясняется чрезвычайно легкой ранимостью сосудистой стенки в месте ангиоэктазии.
Сосудистые мальформации представляют собой прямые артериовенозные соединения через тонкостенные аневризмы и варьируют от небольших телеангиэктазий до огромных АВМ, располагающихся во внутренних органах.
На ранней стадии патологического процесса возникает локальная дилатация, вовлекающая все слои стенки посткапиллярной венулы. Затем это растяжение распространяется на артериолу, что в итоге приводит к формированию прямого их соединения без образования промежуточной капиллярной сети. Результатом данного процесса является снижение давления крови и скорости ее тока (рис. 1).
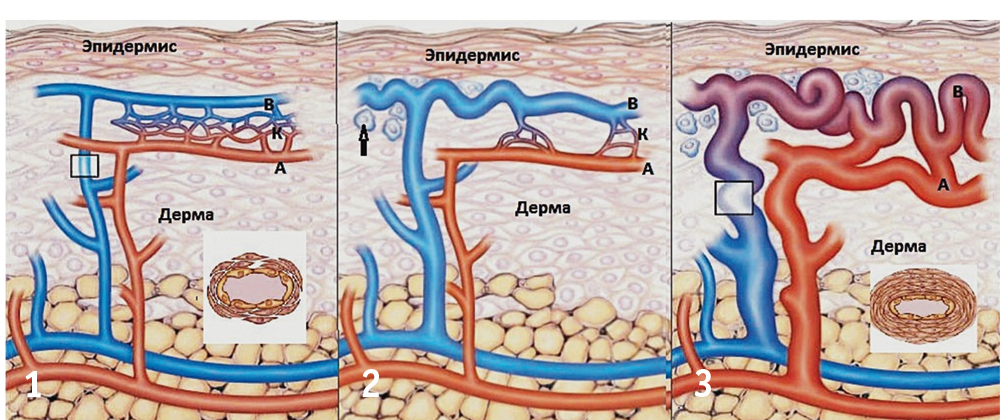
Рис. 1. Формирование кожного телеангиэктаза при наследственной геморрагической телеангиэктазии.
Примечание. (1) — норма, (2) — ранняя стадия формирования телеангиэктазии, (3) — «зрелая» телеангиэктазия.
Нормальная кожа пронизана артериолами (А), которые соединяются с венулами (В) через капилляры (К). Ультраструктура нормальной посткапиллярной венулы (показана в разрезе) состоит из просвета, эндотелиальных клеток второго и третьего рядов перицитов. На ранней стадии формирования телеангиэктазий единичные венулы расширяются, но все еще соединяются с артериолами посредством единичных капилляров. Появляется периваскулярная лимфоцитарная инфильтрация (показана стрелкой). При «поздних» талеангиэктазах венулы и их ветви резко расширены, удлинены и извиты. Артериолы не соединяются посредством расширенных коммуникант, минуя капилляры. Периваскулярная инфильтрация нарастает. Увеличивается толщина сосудистой стенки (по данным[5, 10])
При гистологическом исследовании обнаруживают синусообразные расширения сосудов неправильной формы, истонченные стенки которых образованы эндотелиальными клетками и рыхлой соединительной тканью.
КЛИНИЧЕСКАЯ КАРТИНА
НГТ начинается как доброкачественное состояние, но прогрессирует с возрастом, вызывая серьезные осложнения. У большинства пациентов диагноз устанавливают в подростковом или уже зрелом возрасте. У новорожденных проявления HГT обычно отсутствуют.
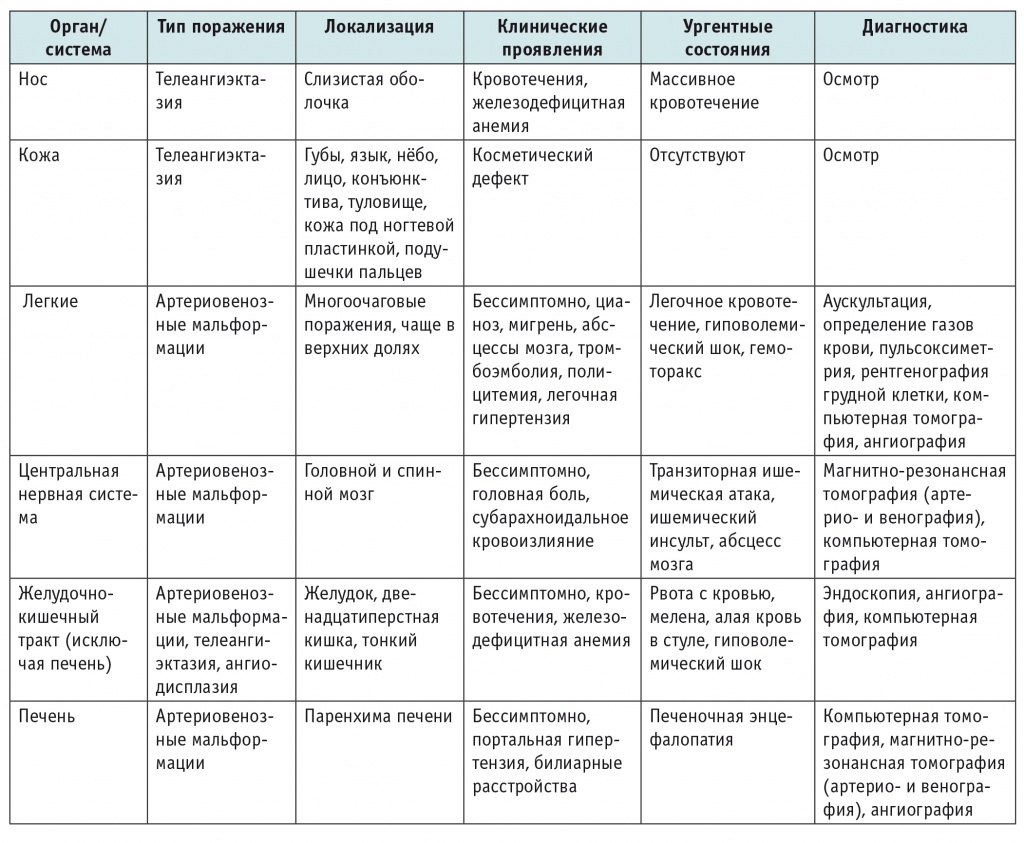
Основными симптомами заболевания являются носовые кровотечения, телеангиэктазии на коже и слизистых оболочках, а также АВМ внутренних органов (табл.).
Таблица
Клинические проявления наследственной геморрагической телеангиэктазии
Носовые кровотечения — наиболее частое проявление НГТ. В 95% случаев они начинаются в возрасте 12 лет, их периодичность в среднем составляет 18 эпизодов в месяц. В большинстве случаев частота и тяжесть кровотечений увеличиваются к зрелому возрасту[3, 23].
Телеангиэктазии, появляясь на слизистых оболочках и коже, обычно ярко-красного цвета, достигают 3–10 мм в диаметре, не пульсируют, бледнеют при надавливании, их количество медленно увеличивается с возрастом. В классическом описании W. Osler выделяет три типа телеангиэктазий:
- ранний — небольшие неправильной формы пятнышки;
- промежуточный — по типу сосудистых «паучков»;
- поздний или узловатый — ярко-красные или пурпурно-фиолетовые округлые узелки диаметром 5–7 мм, выступающие над поверхностью кожи или слизистой оболочки на 1–3 мм.
У больных старше 25 лет часто обнаруживают телеангиэктазии двух или всех трех типов. Они могут располагаться на слизистой оболочке носа, губах, деснах, языке, на коже волосистой части головы, лица, конечностей. Особенно патогномоничны телеангиэктазии на крыльях носа и мочках ушей[21]. На коже они вызывают лишь небольшие косметические дефекты. Однако при поражении слизистых оболочек, особенно полости носа и ЖКТ, телеангиэктазии могут вызывать значительные кровотечения, вплоть до развития железодефицитной анемии, гиповолемии и гипотензии. При коррекции постгеморрагических анемий необходим пероральный или парентеральный прием препаратов железа, а в тяжелых случаях — переливания эритроцитарной массы.
Клиническая картина АВМ различна в зависимости от их расположения во внутренних органах. При поражении легких возникает сброс крови, минующий микроциркуляторное русло, что приводит к низкому уровню оксигенации артериальной крови и увеличению сердечного выброса. Возрастает также риск венозной эмболии, инфарктов легких. При локализации мальформаций в головном мозге имеют место ишемические или геморрагические инсульты, абсцессы мозга.
Возможны портальная гипертензия, поражение билиарного тракта, высокий риск сердечных осложнений при внутрипеченочном расположении шунтов[4, 11, 19].
ДИАГНОСТИКА
Заподозрить НГТ возможно при правильной оценке жалоб больного, данных осмотра и семейного анамнеза. Генетические методы диагностики не являются основными, поскольку лишь в 70–90% случаев удается обнаружить мутации генов эндоглина и АLK-1[18, 20].
Большее значение придают диагностическим критериям Curasao, сформулированным в 1999 г.:
- рецидивирующие спонтанные носовые кровотечения;
- множественные телеангиэктазии на коже и слизистых оболочках;
- артериовенозные аневризмы внутренних органов (легких, головного и спинного мозга, печени, ЖКТ);
- наличие родственника 1-й линии родства, соответствующего первым трем критериям.
Диагноз считается подтвержденным, если у пациента имеются три или четыре критерия, возможным — при наличии двух критериев, сомнительным — менее двух критериев[26].
В соответствии с международными рекомендациями, при явном и возможном диагнозе НГТ показано обследование: МРТ-ангиография головного мозга, ЭхоКГ для исключения легочной гипертензии, КТ или МРТ брюшной полости и грудной клетки с обязательным внутривенным контрастированием для исключения поражения легких и печени.
В настоящее время разработана специальная шкала оценки степени тяжести носового кровотечения (Epistaxis Severity Score — ESS) в баллах. Она включает в себя шесть простых вопросов о частоте, длительности, интенсивности кровотечений, необходимости медицинской помощи, коррекции постгеморрагической анемии, трансфузионной зависимости (рис. 2)[13].
Рис. 2. Опросник для оценки тяжести носовых кровотечений у пациентов с наследственной геморрагической телеангиэктазией[13]

Ответ на каждый из вопросов оценивают в баллах, результаты суммируют при помощи специальной формулы (рис. 3)[13].
Рис. 3. Формула подсчета нормализованного показателя оценки тяжести носовых кровотечений (Epistaxis Severity Score)[13], баллы
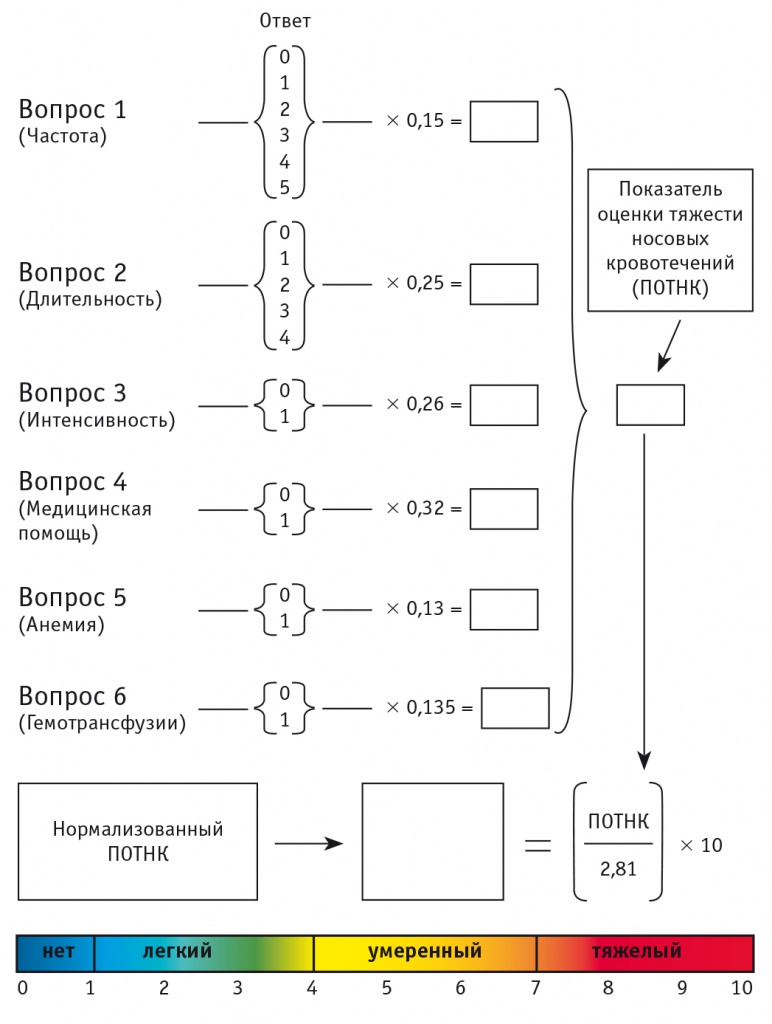
Носовое кровотечение классифицируется как легкое при 1–4 баллах, умеренное — от 5 до 7 баллов, тяжелое — при более чем 7 баллах[13].
ЛЕЧЕНИЕ
В лечении НГТ используют два основных принципа:
- контроль местных и общих симптомов (кровотечений различной локализации и их последствий);
- предотвращение осложнений, связанных с наличием АВМ в различных органах.
Лечение НГТ требует междисциплинарного подхода с привлечением гематолога, оториноларинголога, пульмонолога, интервенционного хирурга, невролога, нейрохирурга, генетика, кардиолога.
У пациентов с НГТ первой линией терапии рецидивирующих носовых кровотечений с уровнем доказательности А могут быть увлажнители воздуха в доме, носовой душ солевыми растворами, тампонада носа, дермопластика области перегородки носа. Уровню доказательности В соответствуют лигирование сосудов, крио- и электрокаутеризация, коагуляция при помощи аргонового, диодного лазера, эмболизация ветвей наружной сонной артерии, топические вазоконстрикторы, антиэстрогеновый противоопухолевый препарат тамоксифен. Описаны единичные случаи эффективности резекции пораженной слизистой оболочки полости носа в пределах подслизистого слоя (уровень доказательности С)[6].
В настоящее время ни один из перечисленных выше методов лечения не позволяет обеспечить должного уровня контроля носовых кровотечений. Разработка альтернативных методов терапии НГТ активно ведется во всем мире. Появилось большое количество научных работ, где достижения генной инженерии используются в терапии рецидивирующих носовых кровотечений.
Бевацизумаб — препарат рекомбинантных моноклональных антител, ингибирующих VEGF. Его применяют при злокачественных новоообразованиях ЖКТ, легких и бронхов, молочной железы. В настоящее время проводят исследования эффективности, безопасности препарата и разрабатывают рекомендации для лечения им носовых кровотечений у больных НГТ[14].
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
S. Dupuis-Girod и соавт. одними из первых сообщили о применении коротких курсов внутривенных инъекций бевацизумаба у пациентов с высоким сердечным выбросом при печеночной форме НГТ. В работу вошли данные о применении препарата у 24 больных, средний возраст которых составил 57 лет. Пациентам проводили лечение бевацизумабом в дозе 5 мг/кг в виде внутривенных инъекций каждые две недели, курс включал 6 введений. Период наблюдения — 6 месяцев со времени первой инъекции препарата. Исходный уровень сердечного выброса составил 5,0 л/мин/м2. Из 24 пациентов 23 завершили курс, один прервал лечение после двух введений.
Полный ответ на терапию, то есть нормализация сердечного выброса, отмечена у 5 больных. Частичный ответ (любое снижение сердечного индекса) наблюдали у 15 человек. Неэффективной терапия оказалась у 3 пациентов.
Авторы измеряли длительность эпизодов носовых кровотечений в течение каждого месяца, она снизилась с 221 до 134 минут в течение первых трех месяцев и составляла в среднем 43 минуты через полгода от начала лечения. Среднее число эпизодов кровотечения в месяц уменьшилось с 26 до 20 случаев через три месяца от начала лечения и составляло по истечении полугода 11 случаев ежемесячно. При помощи специального опросника оценивали качество жизни пациентов, его показатели на фоне лечения бевацизумабом улучшились[7].
Научные исследования были направлены на поиск новых методов введения препарата, учитывая большое количество осложнений при внутривенном использовании. J. Simonds и соавт. одними из первых интраназально стали применять VEGF и опубликовали ретроспективное исследование. Основной группе пациентов с рецидивирующими носовыми кровотечениями (n = 10) проводили коагуляцию источника кровотечения при помощи аргонового лазера и подслизистое введение бевацизумаба в дозировке 100 мг, в группе контроля (n = 9) выполняли только коагуляцию источника кровотечения. По данным авторов, основные показатели оценки тяжести носовых кровотечений, такие как переливания эритроцитарной массы, экстренные госпитализации, прием пероральных и парентеральных препаратов железа, в течение года после лечения у больных обеих групп статистически значимо не различались[27].
T. Karnezis и соавт. в 2011 г. представили результаты своей работы по лечению носовых кровотечений. В исследование вошли 32 пациента, из которых 17 использовали бевацизумаб в виде спрея, 10 пациентам выполнили подслизистое введение препарата в стандартной дозировке 100 мг, 5 получали комбинированное лечение в виде спрея и подслизистого введения. Среднее по группам значение ESS снизилось с 7,0 до 2,9 балла в последующие 4 месяца (p < 0,0001)[15].
В 2012 г. эти же авторы опубликовали данные о лечении 19 пациентов, получавших интраназальные инъекции бевацизумаба в дозе 100 мг, с ретроспективным наблюдением в течение 12 месяцев. У 6 пациентов дополнительно использовали бевацизумаб в виде спрея в той же дозировке. ESS в среднем снизился с 8,15 до 3,50 балла в течение года[16]. К сожалению, тяжело оценить, какой способ введения препарата способствует максимальному снижению индекса ESS.
R. Guldmann и соавт. опубликовали результаты небольшого проспективного исследования с участием 6 пациентов, применявших бевацизумаб в виде назального спрея в дозе 50 мг. ESS оценивали ежемесячно, побочные эффекты лечения не отмечены. Курс интраназального применения бевацизумаба давал статистически значимое снижение ESS в течение первых двух месяцев лечения (р < 0,001 и р < 0,005 соответственно). В течение третьего месяца снижение ESS уже не было статистически значимым. Показатель степени тяжести носовых кровотечений не снижался у пациента с его исходным уровнем более 7 баллов. Авторы делают вывод, что применение препарата дает значимое снижение показателя тяжести носовых кровотечений в первые два месяца введения при его значении до начала лечения менее 7 баллов, т. е. при носовых кровотечениях умеренной тяжести[9].
ОСЛОЖНЕНИЯ ЛЕЧЕНИЯ БЕВАЦИЗУМАБОМ
Бевацизумаб, являясь противоопухолевым препаратом, обладает рядом побочных действий, таких как перфорации ЖКТ, кровоизлияния и кровотечения, артериальная тромбоэмболия. Эти осложнения встречаются при распаде опухоли на фоне лечения. Наиболее часто пациентов беспокоят АГ, слабость, астения, диарея, боли в животе, повышение температуры тела. Очень редко в постмаркетинговых исследованиях отмечают гипертензивную энцефалопатию, синдром обратимой поздней лейкоэнцефалопатии, головную боль, психические нарушения. Стоит отметить, что все эти осложнения наблюдали при парентеральном введении препарата.
Исследование, проводившееся во Франции S. Dupuis-Girod и соавт., показало, что у 21 пациента возникли 89 различных состояний, которые могли быть связаны с применением препарата бевацизумаб при НГТ. У одного больного развилась гипертоническая болезнь с АГ 3-й степени через месяц после инъекции препарата. В период трехмесячного наблюдения отмечены случаи головной боли (n = 52), тошноты и рвоты (n = 12), астении (n = 9), боли в животе (n = 4), миалгии (n = 4), диареи (n = 6), сыпи (n = 1). Ни у одного пациента не было кровотечений, тромбоэмболических осложнений, перфораций ЖКТ или лейкоэнцефалопатий[7].
Было проанализировано применение препарата в форме назального спрея (n = 26), подслизистого введения (n = 34) в дозировке от 25 до 100 мг вместе с коагуляцией при помощи аргонового лазера. В 5 случаях сформировалась стойкая перфорация перегородки носа. Данные о формировании перфорации перегородки носа только при подслизистых инъекциях или использовании спрея авторы не приводят[13, 15, 17].
Международное руководство по лечению НГТ 2006 г. не рассматривает применение бевацизумаба в лечении НГТ как основную ветвь терапии[8]. Это положение было сформировано до выхода серии научных исследований терапии данным препаратом. Вероятно, эффективность и преобладание пользы над вероятным риском осложнений даст возможность широкого использования его в лечении носовых кровотечений. Особый интерес представляют малоинвазивные способы применения бевацизумаба (подслизистые инъекции или интраназальный спрей), возможные в амбулаторных условиях.
Первый опыт подслизистого введения бевацизумаба для терапии рецидивирующих носовых кровотечений у детей с НГТ был опубликован в России в 2014 г. Пятилетней девочке был проведен курс из двух подслизистых инъекций, что позволило снизить показатель тяжести носовых кровотечений с 7,8 до 2,0 баллов[1]. Таким образом, первое применение бевацизумаба в лечении носовых кровотечений у пациентки свидетельствует о его эффективности, но требуется накопление клинического опыта для взвешенной оценки результатов лечения и определения оптимального метода введения препарата.
ЗАКЛЮЧЕНИЕ
Хочется отметить, что у многих пациентов имеет место тяжелое течение наследственной геморрагической телеангиэктазии с массивными кровотечениями, требующими приема препаратов железа, трансфузий эритроцитарной массы. В настоящее время ни один из методов лечения не позволяет обеспечить должного контроля носовых кровотечений. Использование бевацизумаба может снизить частоту, тяжесть и продолжительность кровотечений, повысить качество жизни пациентов и уменьшить материальные затраты на их лечение.








