Ювенильный идиопатический (ревматоидный) артрит (ЮИА) — хроническое иммуновоспалительное заболевание детей и подростков с преимущественным поражением суставов, имеющее неизвестную этиологию и сложный патогенез. Оно характеризуется неуклонно прогрессирующим течением, которое приводит к деструкции суставов, нарушению роста и развития ребенка, ранней инвалидизации[1, 3, 4].
Терапия базисными противоревматическими препаратами у детей с ЮИА часто является недостаточной. У ряда больных назначение метотрексата, сульфасалазина и циклоспорина вызывает развитие побочных эффектов. Несмотря на улучшение клинической картины, у значительной части пациентов продолжается прогрессирование заболевания. По данным литературы, 20–40% пациентов с полиартикулярным вариантом ЮИА нуждаются в усилении терапии генно-инженерными биологическими препаратами[1, 3, 5, 9].
С 2008 г. в арсенале врача-ревматолога появился новый генно-инженерный биологический препарат — абатацепт (Оренсия). Он представляет собой растворимую гибридную белковую молекулу, состоящую из внеклеточного домена человеческого CTLA4 (англ. Cytotoxic T-Lymphocyte-associated Antigen 4 — цитотоксического Т-лимфоцит-ассоциированного антигена 4), сцепленного с модифицированным Fc-фрагментом (области CH2 и CH3) человеческого IgG1. Абатацепт модулирует ключевой костимуляторный сигнал, который требуется для полной активации Т-лимфоцитов с экспрессирующимися на них CD28. Т-лимфоциты обнаруживаются в синовиальной оболочке у пациентов с ЮИА. Активированные Т-лимфоциты являются важным звеном патогенеза этого заболевания. Для полной активации Т-лимфоцитов требуются два сигнала, которые реализуются с участием антигенпредставляющих клеток: идентификация специфического антигена рецепторами Т-клеток и костимуляторный сигнал, который обеспечивается за счет взаимодействия рецептора CD28 на Т-лимфоцитах и СD80/СD86 на антигенпредставляющих клетках. Абатацепт специфически связывается с СD80/СD86, ингибируя этот костимуляторный путь, в результате чего блокируется активация Т-клеток[1, 4, 8, 11].
В клинических исследованиях показано, что абатацепт в дозе приблизительно 10 мг/кг ингибирует активацию Т-лимфоцитов, уменьшает продукцию макрофагов, фибробластоподобных синовиоцитов и В-клеток, а также подавляет острую фазу реактивации воспаления. Наблюдалось уменьшение содержания в сыворотке крови растворимого рецептора ИЛ-2 — маркера активации Т-лимфоцитов; ИЛ-6 — продукта активации макрофагов и фибробластоподобных синовиоцитов; ревматоидного фактора — антитела, продуцирующегося плазменными клетками; С-реактивного белка. Кроме того, отмечалось снижение сывороточного уровня матриксной металлопротеиназы-3, которая вызывает деструкцию хряща и тканевые структурные изменения[1, 8]. Наблюдалось также уменьшение сывороточного содержания ФНО-α[4].
В педиатрической практике использование абатацепта для лечения больных с полиартикулярным вариантом ЮИА разрешено с 6 лет. В работах по изучению применения препарата при ЮИА он назначался в дозе 10 мг/кг внутривенно в течение 30 минут, после первой инфузии последующие осуществлялись через 2 и 4 недели, в дальнейшем — каждые 4 недели[2, 7].
В ряде исследований, проведенных среди пациентов с ревматоидным артритом, доказан усиливающийся с течением времени ответ на терапию абатацептом. Так, в исследовании AGREE у пациентов с ранним ревматоидным артритом на втором году терапии абатацептом отмечено более существенное замедление рентгенологического прогрессирования заболевания, чем на первом году. Частота наступления ремиссии у больных, получавших лечение абатацептом 2 года, возросла с 46,1% на первом году до 55,2% к концу второго года терапии[10]. В исследовании AIM 72% пациентов, имевших ответ по критериям Американской коллегии ревматологов (англ. American College of Rheumatology — АСR) на терапию абатацептом к концу первого года, сохраняли этот ответ вплоть до 5 лет непрерывного лечения. Среди пациентов, достигших на первом году терапии 70%-го улучшения по критериям ACR, 62,6% сохраняли такой ответ на лечение к 5 годам терапии[4, 6, 8].
Наиболее масштабным клиническим исследованием эффективности и безопасности абатацепта у детей с ЮИА является рандомизированное двойное слепое плацебо-контролируемое исследование, выполненное под руководством профессора N. Ruperto. Оно проводилось в 45 медицинских центрах и включало 190 детей в возрасте от 6 до 17 лет с активным ЮИА, характеризовавшимся поражением не менее пяти суставов и неэффективностью предшествующей терапии одним базовым болезньмодифицирующим противоревматическим препаратом и более. Абатацепт назначался в стандартных дозировках. К окончанию открытой фазы исследования (через 4 месяца лечения) 30%-е улучшение по педиатрическим критериям ACR (ACR Pedi) было зарегистрировано у 65% пациентов, 50%-е — у 50%, 70%-е — у 28%, 90%-е — у 13%. Через 6 месяцев лечения в группе детей с положительным ответом на терапию абатацептом 30%-е улучшение было зарегистрировано у 82% пациентов, 50%-е — у 77%, 70%-е — у 53%, 90%-е — у 40%. Серьезных нежелательных явлений на фоне приема абатацепта отмечено не было. По результатам проведенного исследования можно сделать вывод о высокой эффективности и хорошей переносимости этого препарата[7].
М. Ф. Дубко и соавт. проведено ретроспективное исследование, целью которого была оценка эффективности и безопасности абатацепта у детей с ЮИА, ранее не получавших терапии генно-инженерными биологическими препаратами. В исследование вошли 20 пациентов в возрасте от 3 до 17 лет. Все больные характеризовались большой продолжительностью заболевания (в среднем 6,5 года) и высокими показателями его клинико-лабораторной активности. Через 8 месяцев от начала исследования 70% пациентов достигли как минимум 30%-го улучшения по ACR Pedi. Из различных подтипов ЮИА самыми чувствительными к лечению оказались системный вариант (без системных проявлений на момент инициации терапии абатацептом), при котором на лечение ответили все трое больных, и полиартикулярный вариант — при нем ответ был получен у 9 из 11 человек. Среди факторов, приведших к отмене терапии, наиболее часто отмечали отсутствие эффекта или недостаточную эффективность — у 4 детей. Кроме того, у одного ребенка лечение было отменено из-за некомплаентности и у одного — из-за побочных реакций (головная боль, боль в животе, рвота и обмороки)[2]. Вышеизложенное подтверждает высокую эффективность и безопасность абатацепта у детей с ЮИА.
Цель статьи: демонстрация клинического случая успешного использования абатацепта у ребенка с высокой активностью полиартикулярного варианта ювенильного идиопатического артрита.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Пациентка П. с 6 лет (с мая 2011 г.) находится под наблюдением в детском ревматологическом отделении Университетской детской клинической больницы Первого Московского государственного медицинского университета имени И. М. Сеченова (УДКБ Первого МГМУ им. И. М. Сеченова). Девочка от третьей беременности, протекавшей на фоне железодефицитной анемии легкой степени тяжести на протяжении всего срока гестации. Роды вторые, самостоятельные, на 40-й неделе, без особенностей. Вес при рождении составил 3250 г, рост — 51 см. Оценка по шкале Апгар — 8/9 баллов. В периоде новорожденности наблюдалась неврологом с диагнозом мышечной дистонии. На первом году жизни сохранялись признаки перинатального поражения ЦНС, по поводу чего проводились повторные курсы лечебного массажа. Кроме того, девочка в течение первого года жизни 4 раза перенесла ОРВИ, однократно — лакунарную ангину с проведением антибактериальной терапии амоксициллином в возрастной дозировке. Далее отмечались ОРВИ до 3–4 раз в год, в 3 года — ветряная оспа. До 2 лет вакцинация осуществлялась согласно национальному календарю профилактических прививок без развития нежелательных реакций. Реакция Манту проводилась ежегодно, в 2007 г. — отрицательная. Под наблюдением фтизиатра не состояла. Аллергологический анамнез без особенностей. Наследственный анамнез: у бабушки по отцовской линии в возрасте 14 лет была диагностирована острая ревматическая лихорадка.
С сентября 2007 г. (с 2 лет) мать пациентки начала обращать внимание на повышенную раздражительность ребенка. Девочка с трудом вставала по утрам с кровати. Продолжительность утренней скованности в среднем составляла 25–30 минут. В октябре 2007 г. у ребенка без видимых причин появились боль, припухлость и ограничение подвижности в правом коленном суставе. Спустя 3 дня стало отмечаться повышение температуры тела до 39 °С, преимущественно в утренние часы. Девочка была госпитализирована в стационар по месту жительства с диагнозом реактивного артрита. При осмотре обращали на себя внимание бледность кожных покровов, повышение температуры тела до 37,6 °С, микрополиадения. Патологических изменений внутренних органов выявлено не было. Поражение суставов было представлено артритом правого коленного сустава с выраженными экссудативными изменениями и ограничением функции. В анализах крови отмечались ускорение СОЭ до 33 мм/ч, увеличение количества лейкоцитов до 15,8 × 109/л, сдвиг лейкоцитарной формулы влево. Девочке были проведены антибактериальная терапия ампициллином и мидекамицином в течение 7 дней, лечение НПВП per os и местно. На фоне терапии удалось купировать лихорадку, уменьшились воспалительные изменения в крови и интенсивность артралгий в правом коленном суставе. Однако в дальнейшем сохранялась утренняя скованность в пораженных суставах до 15 минут, наблюдались эпизоды артралгий в коленном суставе на фоне физической нагрузки и ОРВИ.
В марте 2008 г. у девочки без видимой причины произошло повторное обострение заболевания с вовлечением в патологический процесс новых суставов. Наросли экссудативные изменения и ограничение подвижности в коленных суставах, лучезапястных, проксимальных и дистальных межфаланговых, пястно-фаланговых суставах рук, локтевых и плечевых суставах. В анализах крови отмечались повышение СОЭ до 28–40 мм/ч, увеличение количества лейкоцитов до 12,8 × 109/л. По месту жительства был поставлен диагноз: «Ювенильный ревматоидный артрит, суставная форма, полиартикулярный вариант, активность III степени». С апреля 2008 г. была начата базисная иммуносупрессивная терапия метотрексатом 12 мг/м2 в комбинации с НПВП (диклофенак (Вольтарен) 5 мг/кг/сут), проводились внутрисуставные пункции коленных и лучезапястных суставов с введением глюкокортикоидов (метилпреднизолон (Депо-Медрол)). На фоне лечения состояние девочки улучшилось: уменьшились артралгии, увеличился объем движений в суставах. В дальнейшем эффективность терапии постепенно нарастала. Однако каждые 3–5 месяцев девочка нуждалась во внутрисуставных введениях глюкокортикоидов в связи с нарастанием экссудативных изменений в суставах. В ноябре 2010 г. при очередном выраженном обострении заболевания терапия была усилена за счет увеличения дозы метотрексата до 15 мг/м2 и добавления циклоспорина в дозе 5 мг/кг/сут. Несмотря на массивную иммуносупрессивную терапию двумя базисными болезньмодифицирующими противоревматическими препаратами, заболевание у ребенка продолжало прогрессировать (в патологический процесс вовлекались новые суставы), нарастала инвалидизация.
В детское ревматологическое отделение УДКБ Первого МГМУ им. И. М. Сеченова девочка впервые поступила в мае 2011 г. При поступлении состояние ребенка было тяжелым по основному заболеванию. У девочки отмечались боли и ограничение подвижности в суставах. При осмотре обращали на себя внимание выраженные признаки интоксикации: субфебрильная лихорадка, бледность кожных покровов, «тени» под глазами, общая дистрофия, полиадения. Наблюдалось генерализованное поражение суставов с вовлечением в патологический процесс височно-нижнечелюстных суставов, шейного отдела позвоночника, плечевых, локтевых, лучезапястных, пястно-фаланговых, проксимальных и дистальных межфаланговых суставов рук, тазобедренных, коленных и голеностопных суставов. В суставах отмечались экссудативно-пролиферативные изменения с нарушением функции и болезненностью при движении. Лабораторное обследование выявило ускорение СОЭ до 40 мм/ч, повышение уровня С-реактивного белка до 3,5 мг/дл, увеличение количества лейкоцитов до 14,7 × 109/л и тромбоцитоз до 719 × 109/л. Был получен положительный прокальцитониновый тест. Рентгенологическое исследование пораженных суставов позволило обнаружить выраженный регионарный остеопороз, субхондральное уплотнение крыш вертлужных впадин. На основании клинической картины и данных лабораторно-инструментального обследования диагноз ЮИА был подтвержден. В связи с выраженными признаками интоксикации, лейкоцитозом, сдвигом лейкоцитарной формулы влево и положительным прокальцитониновым тестом девочке был назначен курс внутривенного введения иммуноглобулина в дозе 0,5 г/кг в течение 3 дней. После проведенной терапии самочувствие ребенка улучшилось, купировалась субфебрильная лихорадка, повторный прокальцитониновый тест — отрицательный.
С учетом длительного стажа заболевания, неуклонно прогрессировавшего течения суставного синдрома с нарастанием инвалидизации, а также отсутствия должного ответа на массивную комбинированную иммуносупрессивную противоревматическую терапию было принято решение о назначении девочке генно-инженерного биологического препарата — абатацепта. Первое внутривенное введение абатацепта было проведено 10 мая 2011 г. в дозе 10 мг/кг. После первой инфузии последующие осуществляли через 2 и 4 недели, а в дальнейшем введение препарата повторяли 1 раз в 4 недели. Ребенок переносил инфузии хорошо, нежелательных реакций отмечено не было.
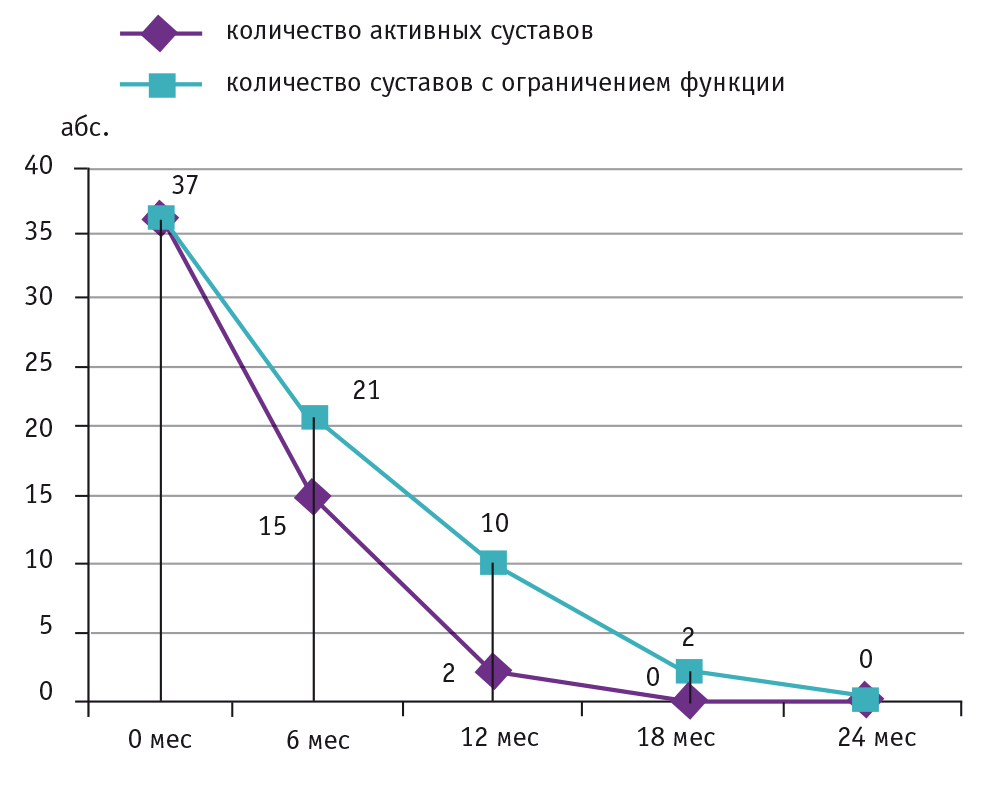
После выписки из стационара девочка продолжала получать метотрексат 15 мг/м2, циклоспорин 5 мг/кг/сут, диклофенак (Вольтарен) 2 мг/кг/сут, абатацепт 10 мг/кг 1 раз в 4 недели. На фоне терапии ее состояние улучшилось: значительно уменьшились артралгии, возрос объем движений в суставах. При повторном осмотре через 6 месяцев от начала терапии абатацептом нормализовались показатели крови, примерно в 2 раза снизилось количество активных суставов и суставов с ограничением функции, купировалась утренняя скованность (рис. 1, табл.). При комплексной оценке эффективности абатацепта было получено 50%-е улучшение по ACR Pedi. Однако на фоне массивной иммуносупрессивной терапии у девочки отмечался рецидивирующий афтозный стоматит, с целью купирования которого доза метотрексата была снижена до 10 мг/м2.
Рис. 1. Динамика количества пораженных суставов у ребенка с ювенильным идиопатическим артритом на фоне терапии абатацептом, абс.
Таблица
Динамика показателей активности заболевания и изменение медикаментозного лечения у ребенка с полиартикулярным вариантом ювенильного идиопатического артрита на фоне терапии абатацептом
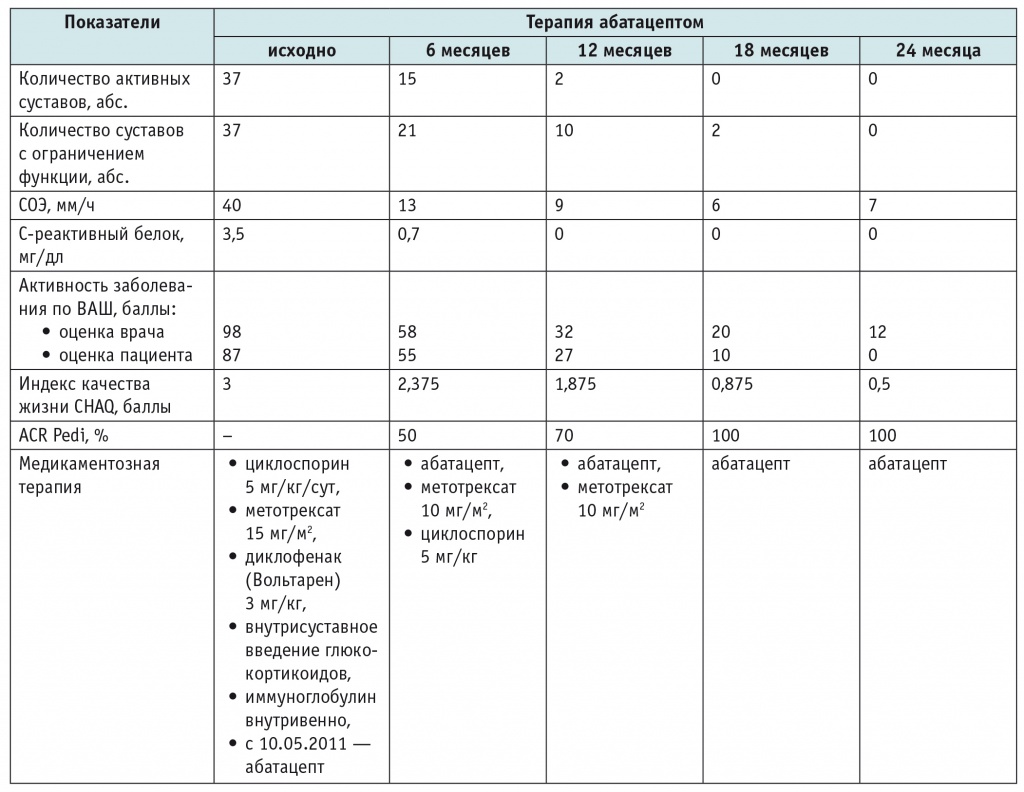
Примечание. ACR Pedi — педиатрические критерии Американской коллегии ревматологов; CHAQ (англ. Childhood Health Assessment Questionnaire) — опросник для оценки общего состояния здоровья у педиатрических пациентов.
При дальнейшем наблюдении сохранялась положительная динамика на фоне терапии абатацептом. Через 12 месяцев нормализовались показатели СОЭ и С-реактивного белка (рис. 2, см. табл.). Количество активных суставов уменьшилось до 2, суставов с ограничением функции — до 10. Активность заболевания, оцененная со стороны врача и пациента по ВАШ, показатели индекса качества жизни CHAQ (англ. Childhood Health Assessment Questionnaire — опросник для оценки общего состояния здоровья у педиатрических пациентов) также продолжали снижаться (рис. 3, см. табл.). При комплексной оценке эффективности абатацепта было получено 70%-е улучшение по ACR Pedi (рис. 4, см. табл.). К году от начала использования генно-инженерного биологического препарата девочке был отменен циклоспорин, продолжена комбинированная терапия метотрексатом 10 мг/м2 и абатацептом.
Рис. 2. Динамика лабораторных показателей активности заболевания у ребенка с ювенильным идиопатическим артритом на фоне терапии абатацептом.
Примечание. СОЭ — скорость оседания эритроцитов; СРБ — С-реактивный белок
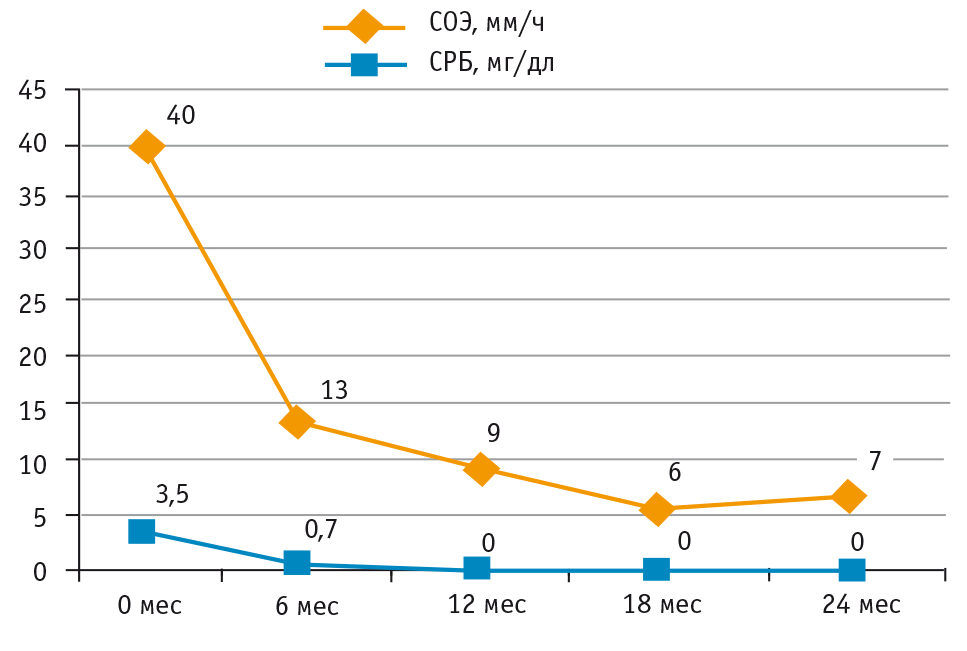
Рис. 3. Динамика показателей визуальной аналоговой шкалы (ВАШ) со стороны врача и пациента у ребенка с ювенильным идиопатическим артритом на фоне терапии абатацептом, баллы
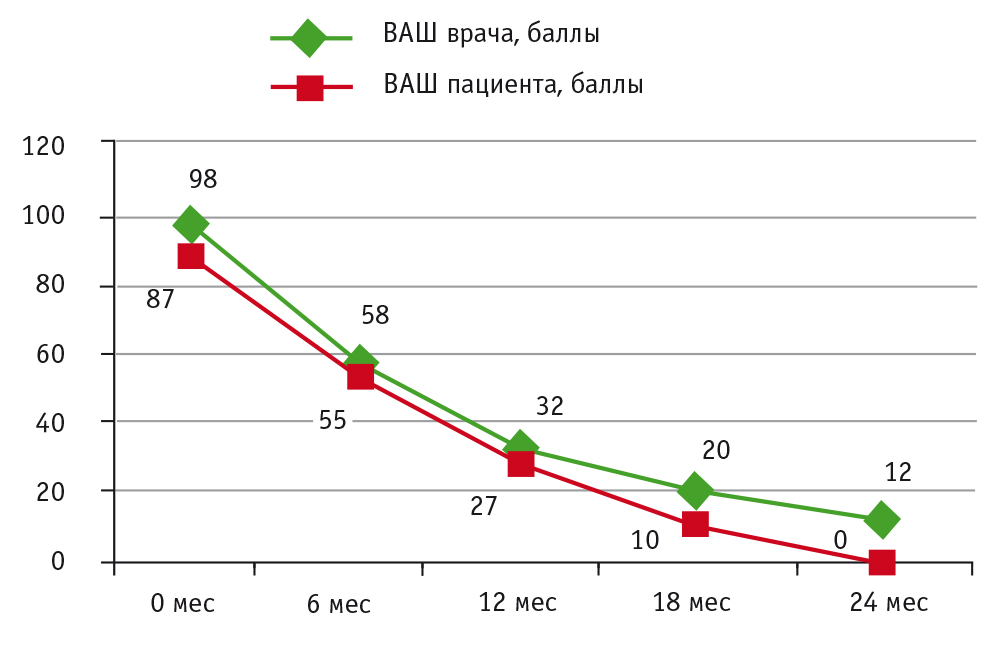
Рис. 4. Эффективность лечения согласно педиатрическим критериям Американской коллегии ревматологов (ACR Pedi) у ребенка с ювенильным идиопатическим артритом на фоне терапии абатацептом, %
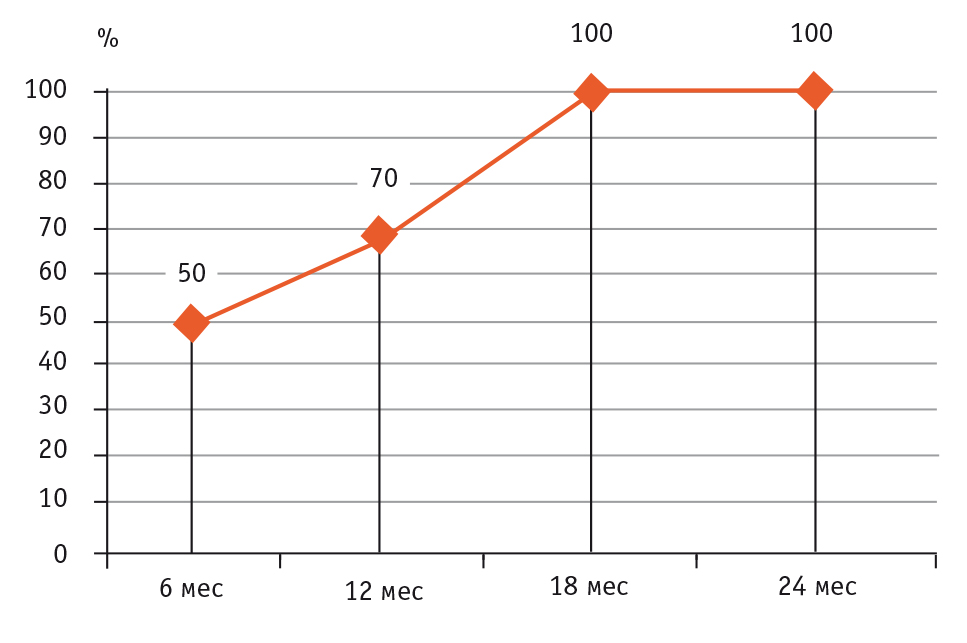
В дальнейшем состояние девочки продолжало улучшаться. К 18 месяцам удалось полностью купировать утреннюю скованность и суставной синдром. Зарегистрировано развитие стойкой клинико-лабораторной медикаментозной ремиссии. Учитывая полученный результат, девочке с успехом осуществлена попытка отмены метотрексата. В течение последующих 8 месяцев ребенку была продолжена терапия абатацептом по указанной выше схеме. За этот период лабораторные показатели оставались в пределах возрастной нормы, артралгии и утренняя скованность не беспокоили. По данным рентгенологического исследования, деструктивные изменения не прогрессировали. Лечение абатацептом оказало позитивное влияние на физическое и психоэмоциональное состояние ребенка. Оценка функционального статуса девочки по критериям CHAQ сравнялась с показателями практически здоровых сверстников.
ЗАКЛЮЧЕНИЕ
Анализ представленного клинического случая демонстрирует тяжелое, быстропрогрессирующее течение ювенильного идиопатического (ревматоидного) артрита (ЮИА) с генерализованным поражением суставов, неуклонной инвалидизацией ребенка, несмотря на массивную комбинированную стандартную иммуносупрессивную терапию метотрексатом и циклоспорином, а также регулярные внутрисуставные введения глюкокортикоидов. На фоне терапии абатацептом уже к 6 месяцам от начала терапии удалось полностью отказаться от проведения внутрисуставных пункций, к 12 месяцам — отменить циклоспорин, к 18 — метотрексат. Через полтора года от начала терапии абатацептом достигнута стойкая клинико-лабораторная медикаментозная ремиссия заболевания. Полученные результаты свидетельствуют о правильности выбора препарата и подтверждают высокую эффективность абатацепта у детей с полиартикулярной формой ЮИА, торпидной к стандартной противоревматической терапии.








