В связи с развитием современных методов аналитической биохимии и молекулярной генетики возможность заподозрить и диагностировать орфанные заболевания у детей биохимическим методом появилась и в областных центрах. Более 70% из них манифестируют в раннем возрасте, приводя к тяжелым инвалидизирующим расстройствам (у 65% детей) и являясь причиной смерти пациентов на первом году жизни в 35% случаев [7]. Благодаря развитию молекулярной медицины сформировались новые представления о патогенезе различных заболеваний. Лекарственное воздействие на конкретные молекулы, молекулярные комплексы или субклеточные структуры, дефекты которых обуславливают развитие болезни, в последние годы получило название «таргетная терапия» [9].
Лизосомные болезни накопления — группа наследственных метаболических заболеваний, связанных с нарушением активности лизосомных гидролаз или системы транспорта белков и субстратов в лизосомы [3]. Гликогенозы представляют собой группу заболеваний, в основе которых лежит нарушение распада гликогена, приводящее к накоплению его в различных органах. Тип наследования аутосомно-рецессивный, ген картирован на хромосоме 17q25. Распространенность гликогенозов варьирует от 1 : 14 000 до 1 : 300 000 [11]. Истинная частота встречаемости в России неизвестна [6].
Гликогеноз II типа (болезнь Помпе) — это генерализованный гликогеноз, возникающий в результате мутации в гене GAA, кодирующем фермент кислую альфа-глюкозидазу (кислую мальтазу). Его дефицит ассоциирован со значительным спектром клинических проявлений: от тяжелого и стремительного течения с выраженной мышечной гипотонией и гипертрофической кардиомиопатией (с летальным исходом на первом году жизни) до медленно прогрессирующей миопатии с поражением дыхательной мускулатуры. В зависимости от возраста больного на момент дебюта болезни выделяют две формы заболевания — младенческую (инфантильную) и форму болезни с поздним началом. Клинические симптомы при инфантильной форме проявляются практически с рождения (чаще в возрасте 1‒2 месяцев) в виде мышечной гипотонии, макроглоссии, гепатомегалии, кардиомиопатии с прогрессирующей сердечной недостаточностью, приводящей к смерти на первом году жизни [2, 4]. В биохимическом анализе крови характерно повышение уровней трансаминаз, КФК и ЛДГ. При проведении ЭКГ выявляются укорочение интервала PQ (гликоген стимулирует процессы проводимости), гипертрофия левого желудочка, высокий вольтаж комплекса QRS, при ЭхоКГ — нарастающая гипертрофия миокарда [1]. Для подтверждения заболевания используют определение активности кислой альфа-D-глюкозидазы в различных тканях (кровь, мышцы). Снижение активности фермента в крови является ведущим доказательством диагноза. Разработана молекулярно-генетическая диагностика болезни Помпе, к настоящему моменту известно более 200 мутаций гена [5]. Дифференциальная диагностика проводится с миопатиями, заболеваниями ЦНС, кардиомиопатиями другой этиологии [8].
Долгое время оказание медицинской помощи пациентам с болезнью Помпе ограничивалось симптоматической терапией. На сегодняшний день единственным специфическим физиологическим способом лечения является таргетное воздействие, или ферментозаместительная терапия (ФЗТ). За рубежом этот способ лечения используется с 2006 г., доказаны его эффективность и целесообразность применения с максимально ранних стадий болезни. Алглюкозидаза альфа (Санофи Джензайм, США) — рекомбинантная кислая глюкозидаза — применяется для лечения всех форм гликогеноза II типа (инфантильной и формы болезни с поздним началом). Наиболее благоприятные результаты достигаются при начале терапии в раннем возрасте, до развития значительного повреждения скелетной мускулатуры [10]. В России одними из первых лечение рекомбинантной кислой глюкозидазой по витальным показаниям получили четыре ребенка с инфантильной формой болезни Помпе в кардиологическом отделении Научного центра здоровья детей РАМН (далее — НЦЗД РАМН) с 2011 по 2013 г. [1, 2].
Цель статьи: поделиться опытом ведения ребенка с орфанным заболеванием — болезнью Помпе.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Вася Т. — ребенок от третьей беременности, протекавшей с угрозой прерывания на всем ее протяжении, вторых срочных родов. Родился с весом 2930 г, ростом 51 см, с оценкой по шкале Апгар 7/8 баллов. За первый месяц прибавил в весе 1200 г, вырос на 5 см. К концу первого месяца жизни появилась одышка при кормлении и беспокойстве. Мальчик впервые лечился в отделении детей раннего возраста детского стационара в детской городской клинической больнице г. Оренбурга (далее — МАУЗ «ДГКБ» г. Оренбурга) в возрасте полутора месяцев (январь 2011 г.) с диагнозом: Гипертрофическая симметричная (концентрическая) кардиомиопатия без обструкции выводного тракта левого желудочка. Врожденный порок сердца — умеренная коарктация аорты; вторичный дефект межпредсердной перегородки 5,5 мм. Умеренная легочная гипертензия. Недостаточность кровообращения IIА степени. Перинатальное поражение ЦНС, синдром мышечной гипотонии. Получал лечение: спиронолактон, пропранолол, гопантеновую кислоту, ИФН-α-2b, триметазидин. В 2 месяца ребенка консультировали в Научном центре сердечно-сосудистой хирургии им. А. Н. Бакулева. Было рекомендовано продолжить лечение спиронолактоном и триметазидином.
В 4 месяца мальчик повторно поступил в МАУЗ «ДГКБ» г. Оренбурга в связи с ухудшением состояния: наросла сердечная недостаточность, присоединился коронарный синдром. При осмотре состояние тяжелое, бледен, пониженного питания, отмечены пастозность голеней, макроглоссия, мышечная гипотония. Вес 5630 г, рост 57 см. Голову держал плохо, переворачивался с трудом. Одышка смешанного характера до 68 в минуту, втяжение уступчивых мест грудной клетки при дыхании. Границы относительной сердечной тупости расширены влево — на 3‒3,5 см кнаружи от левой срединно-ключичной линии. Тоны сердца громкие, выслушивался систолический шум вдоль левого края грудины без иррадиации. ЧСС до 160 в минуту. Нижний край печени выступал на 3 см ниже края реберной дуги.
Результаты лабораторного и инструментального обследования. Биохимический анализ крови: АЛТ — 117 Eд/л, АСТ — 232 Ед/л, ЛДГ — 949 Ед/л, КФК — 796 Ед/л. ЭКГ: синусовая брадиаритмия с ЧСС 103‒142 в минуту, укорочение интервала PQ до 0,07 секунды, комбинированная гипертрофия желудочков и левого предсердия, признаки субэндокардиальной ишемии. ЭхоКГ: гипертрофическая симметричная (концентрическая) кардиомиопатия с утолщением межжелудочковой перегородки до 11 мм, задней стенки левого желудочка до 10 мм, передней стенки правого желудочка до 5 мм; фракция выброса — 78%, давление в правом желудочке — 32 мм рт. ст. УЗИ внутренних органов: увеличение размеров печени, повышение эхогенности печени, почек. Рентгенография грудной клетки: усиление легочного рисунка в прикорневых зонах, увеличены все отделы сердца, кардиоторакальный индекс — 64%.
Проведено лечение: цефтриаксон, ИФН-α-2b, спиронолактон, триметазидин, пропранолол, изосорбида динитрат, ацетилсалициловая кислота, левокарнитин, бифидобактерии бифидум, мельдоний внутривенно.
С учетом поражения сердца, мышечной гипотонии, увеличения печени, повышенной активности ферментов в сыворотке крови (АЛТ — в 3, АСТ — в 5, ЛДГ и КФК — в 4 раза) выполнялся дифференциальный диагноз с митохондриальными заболеваниями (содержание лактата в крови оказалось в пределах нормы) и гликогенозом.
Положительный результат исследования крови на кислую мальтазу методом сухих пятен свидетельствовал в пользу болезни Помпе. Для дальнейшего лечения ребенок в возрасте 4,5 месяца был направлен в кардиологическое отделение НЦЗД РАМН с диагнозом: Гипертрофическая симметричная (концентрическая) кардиомиопатия без обструкции кровотока, осложненная коронарным синдромом. Врожденный порок сердца: гипоплазия перешейка аорты, аномалия строения аортального клапана, укорочение правой коронарной створки. Умеренная легочная гипертензия. Недостаточность кровообращения IIА степени. Группа риска по синдрому внезапной смерти. Последствия перинатального поражения ЦНС, синдром нарушения мышечного тонуса. Риск гипотиреоза. Гипотрофия I степени, пре-, постнатальная, смешанной этиологии. Болезнь Помпе (?)
Энзимодиагностика проведена в лаборатории наследственных болезней обмена веществ Медико-генетического научного центра (г. Москва). Выявлено снижение альфа-D-глюкозидазы до 0,4 нмоль/мг/ч (при норме 13,00‒53,66 нмоль/мг/ч), что было подтверждено в Университетском медицинском центре г. Гамбурга (ФРГ). Получены отрицательные результаты анализов крови на органические аминоацидурии и наследственные аминоацидопатии. Диагноз болезни Помпе был подтвержден генетически: обнаружена мутация в гене GAA в гетерозиготном состоянии — p.Cys103Gly/c.1030_1039del. Данная мутация описана в международной базе данных и ассоциирована с потенциально менее тяжелым течением заболевания [2]. Окончательный диагноз: Гипертрофическая кардиомиопатия, специфическая, необструктивная форма. Недостаточность аортального клапана. Гипоплазия перешейка аорты. Феномен укороченного интервала PQ. Недостаточность кровообращения IIА степени. Болезнь Помпе. Вторичная миопатия. Задержка моторного развития. Риск синдрома внезапной смерти.
С 4,5 до 9 месяцев жизни (с апреля по сентябрь 2011 г.) ребенок периодически находился в кардиологическом отделении НЦЗД РАМН, получал только симптоматическую терапию: каптоприл, пропранолол, спиронолактон, ацетилсалициловую кислоту, триметазидин, урсодезоксихолевую кислоту. К 8 месяцам наросла мышечная гипотония, мальчик перестал переворачиваться, возникли проблемы с глотанием, отмечалась потеря в весе. На ЭКГ сохранялись признаки гипертрофии обоих желудочков и выраженные нарушения процессов реполяризации, появились признаки гипертрофии межжелудочковой перегородки. При проведении ЭхоКГ также наблюдалась отрицательная динамика: толщина задней стенки левого желудочка увеличилась до 12 мм, межжелудочковой перегородки — до 14 мм, передней стенки правого желудочка — до 11 мм, фракция выброса возросла до 80%. При КТ грудной клетки и брюшной полости данных за сужение аорты получено не было.
Только с 9-месячного возраста в кардиологическом отделении НЦЗД РАМН был начат курс ФЗТ алглюкозидазой альфа в дозе 20 мг/кг с кратностью введения 1 раз в 14 дней. До 1 года 5 месяцев данное лечение проводилось в Москве. В дальнейшем (с мая 2012 г.) ребенок получал ФЗТ в условиях палаты интенсивной терапии МАУЗ «ДГКБ» г. Оренбурга, с августа 2013 г. — через инфузионную порт-систему. Тем не менее для проведения полного обследования и коррекции терапии мальчик регулярно (с интервалом в 3‒6 месяцев) госпитализировался в кардиологическое отделение НЦЗД РАМН. Помимо ФЗТ пациент постоянно получал бета-адреноблокаторы (бисопролол), антиагреганты (ацетилсалициловую кислоту), урсодезоксихолевую кислоту, ангиопротекторы (пентоксифиллин); курсами — препараты кардиометаболического действия, нейропептиды, сосудистые лекарственные средства и ноотропы (триметазидин, тиоктовую кислоту, пиридоксин + тиамин + цианокобаламин + лидокаин (раствор для внутримышечного введения), Кортексин, этилметилгидроксипиридина сукцинат, гопантеновую кислоту). В питание была включена лечебная смесь «Педиашур», проводились ЛФК, массаж, занятия с логопедом. За время наблюдения (с 1 года 5 месяцев до 3 лет 3 месяцев) ребенок 5 раз перенес ОРВИ, в 2 года — обструктивный бронхит.
На фоне таргетной терапии (начатой с 9-месячного возраста) у пациента к полутора годам по результатам инструментальных исследований сохранялась кардиомегалия (рис. 1, 2), хотя было отмечено уменьшение толщины задней стенки левого желудочка с 12 мм до 7 мм и межжелудочковой перегородки сердца с 14 мм до 7 мм. Клинические признаки сердечной недостаточности уменьшились, двигательная активность увеличилась: мальчик стал самостоятельно сидеть с 1 года; ходил с поддержкой с 1 года 10 месяцев, самостоятельно — с 2 лет; бегал, забирался по лестнице с 3 лет. Уменьшились признаки задержки нервно-психического развития: ребенок с 2 лет говорил отдельные слова, с 3 лет играл с детьми, у него имелись все навыки самообслуживания.
Рис. 1. Эхокардиограммы больного Васи Т. в возрасте 1 года 2 месяцев на фоне получаемой в течение 5 месяцев ферментозаместительной терапии (слева) и здорового ребенка в возрасте 1 года (справа). Фото Н. М. Лаптевой, 2012 г.
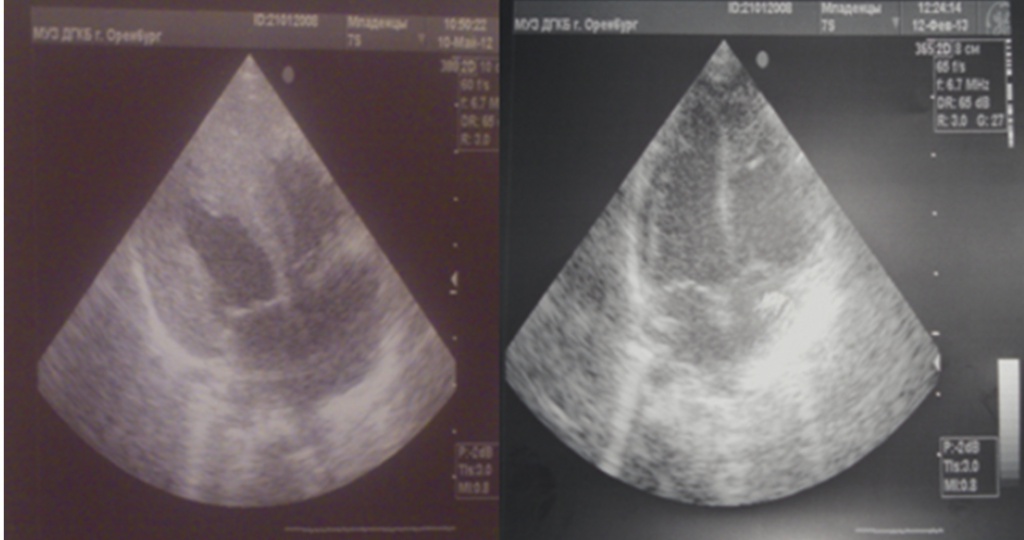
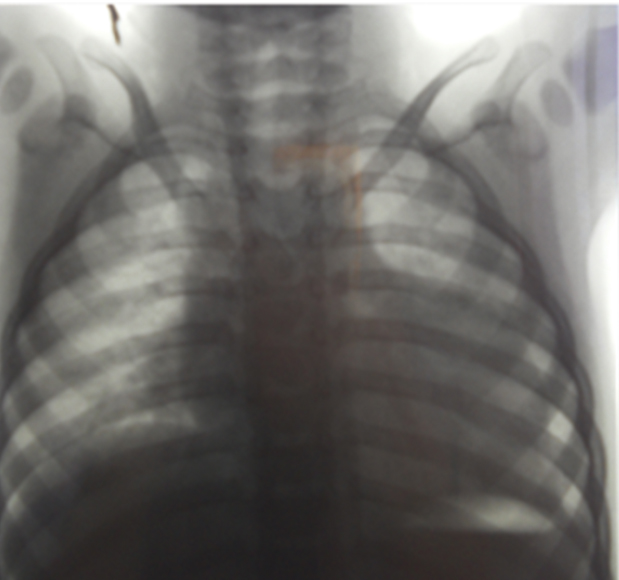
Рис. 2. Рентгенограмма грудной клетки больного Васи Т. на фоне получаемой в течение 5 месяцев ферментозаместительной терапии. Усиление легочного рисунка в прикорневых зонах, увеличение всех отделов сердца. Фото Н. М. Лаптевой, 2012 г.
При осмотре в 3 года 1 месяц: вес 13,7 кг, рост 96 см, несколько пониженного питания. Отмечались бледность кожных покровов, периоральный цианоз, макроглоссия, гиперсаливация, признаки мышечной гипотонии, псевдогипертрофии икроножных мышц, выраженная эквиноварусная деформация правой и плосковальгусная деформация левой стопы. Границы относительной сердечной тупости не расширены. Тоны сердца средней громкости, выслушивался короткий систолический шум, не проводившийся за пределы сердца. Частота дыхания и ЧСС в пределах возрастной нормы. Исчезла гепатомегалия.
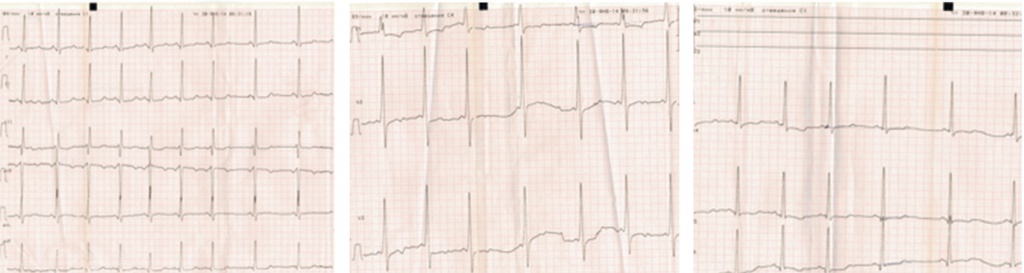
В биохимическом анализе крови сохранялось повышение активности ферментов: АЛТ — в 5, АСТ — в 10, ЛДГ — в 9 раз. На ЭКГ — гипертрофия обоих желудочков, левого предсердия, выраженные нарушения процессов реполяризации, укорочение интервала PQ до 0,08‒0,10 секунды (рис. 3). На ЭхоКГ сохранялись признаки гипертрофической симметричной кардиомиопатии без признаков обструкции выходных отделов; толщина межжелудочковой перегодки 7‒8 мм (норма — 3‒4 мм), задней стенки левого желудочка — 7‒8 мм (норма — 3‒4 мм), передней стенки правого желудочка — 5 мм (норма); фракция выброса — 66%. Рентгенография грудной клетки: очаговоподобные тени до 5 мм, кардиоторакальный индекс — 61%.
Рис. 3. Электрокардиограмма больного Васи Т. в возрасте 3 лет. Гипертрофия обоих желудочков и левого предсердия, выраженные нарушения процессов реполяризации, укорочение интервала РQ до 0,08‒0,10 секунды. Фото Н. М. Лаптевой, 2014 г.
В 3 года 2 месяца ребенку проводилась правосторонняя ахиллотомия по поводу эквиноварусной деформации стопы.
В 3 года 3 месяца мальчик заболел ОРВИ, лечился амбулаторно (цефтазидим внутримышечно, ацетилцистеин, ИФН-α-2b). На 6-й день болезни произошло резкое ухудшение состояния, наросла дыхательная недостаточность. Машиной скорой помощи ребенок был доставлен в стационар МАУЗ «ДГКБ» г. Оренбурга в крайне тяжелом состоянии: конечности холодные, диффузный цианоз, самостоятельное дыхание затруднено, выраженная мышечная гипотония. Проведены интубация трахеи и подключение к аппарату ИВЛ. В легких ослабленное дыхание с мелкопузырчатыми влажными хрипами. Тоны сердца средней громкости, ритмичные, выслушивался короткий систолический шум, не проводившийся за пределы сердца. Нижний край печени выступал на 2 см ниже края реберной дуги. Центральная гемодинамика нестабильная, ЧСС — 180 в минуту, частота дыхания — 40 в минуту, артериальное давление — 108/64 мм рт. ст., SaO2 — 52‒100%.
В биохимическом анализе крови уровень АЛТ повышен в 4, АСТ — в 8 раз. Проведено микробиологическое исследование мокроты, выделен Acinetobacter calcoaceticus в титре более 106. Рентгенография грудной клетки: по всем легочным полям определялись множественные очаговые тени, местами сливного характера. ЭКГ: синусовая аритмия — 118‒185 в минуту, интервал PQ 0,09 секунды, гипертрофия правого и левого желудочков, выраженное нарушение процессов реполяризации. ЭхоКГ: снижение фракции выброса до 60%; в динамике появилось эхосвободное пространство в области верхушки (7 мм) и по задней стенке левого желудочка (7 мм). УЗИ внутренних органов: диффузные изменения печени, поджелудочной железы, почек.
В связи с диагностированной внебольничной двусторонней полисегментарной пневмонией тяжелой степени, наличием токсикоза III степени и дыхательной недостаточности III степени была проведена антибактериальная терапия (цефтазидим, амикацин, ванкомицин, меропенем, ципрофлоксацин); ребенок получал глюкозо-солевые растворы внутривенно капельно, препараты калия, дексаметазон, фуросемид, дигоксин, амиодарон, альбумин, свежезамороженную плазму; ему проводили ИВЛ (505 часов). Несмотря на лечение, состояние прогрессивно ухудшалось: угнетение сознания до комы III степени, появились ДВС-синдром, полиорганная недостаточность. Гемодинамика оставалась стабильной только на дофаминовой поддержке. На 23-й день госпитализации произошла остановка сердечной деятельности. Секционного исследования не проводилось по просьбе родителей.
Обсуждение
Наличие у ребенка при повторной госпитализации в 4 месяца полисистемного поражения в виде гипертрофической кардиомиопатии с прогрессирующей сердечной недостаточностью, симптомов мышечной гипотонии, макроглоссии, гепатомегалии, гипотрофии в сочетании с повышением уровней трансаминаз, ЛДГ и КФК, а также положительный результат анализа крови на кислую мальтазу заставили заподозрить гликогеноз II типа.
В последующем в кардиологическом отделении НЦЗД РАМН диагноз был подтвержден биохимическим (снижение активности альфа-D-глюкозидазы) и генетическим методами. Там же с 9-месячного возраста по витальным показаниям начата таргетная терапия рекомбинантной человеческой кислой альфа-глюкозидазой. Помимо ФЗТ, ребенок постоянно получал бета-адреноблокаторы, антиагреганты, урсодезоксихолевую кислоту, ангиопротекторы; курсами — нейропептиды, ноотропы, сосудистые лекарственные средства и препараты кардиометаболического действия; проводились ЛФК, массаж, занятия с логопедом. В результате у пациента уменьшились признаки сердечной недостаточности, увеличилась двигательная активность, однако сохранялись поражение скелетной мускулатуры (псевдогипертрофия икроножных мышц) и макроглоссия.
Особенностью данного случая является ранняя диагностика гликогеноза II типа, позволившая начать ФЗТ с возраста 9 месяцев. Выявленные мутации гена GAA, характерные для болезни Помпе, в гетерозиготном состоянии ассоциированы с потенциально менее тяжелым течением заболевания. Несмотря на эффективность таргетной терапии, развившаяся двусторонняя пневмония у данного пациента привела к летальному исходу в возрасте 3 лет 3 месяцев.
ЗАКЛЮЧЕНИЕ
Болезнь Помпе — редкая генетическая патология, ранняя диагностика которой затруднена в связи с многообразием клинической картины. Распространение информации об этом заболевании во врачебной среде и использование биохимических методов диагностики позволяют выявить его на ранних стадиях. Таргетная терапия является единственным специфическим методом лечения. Раннее начало терапии — способ повысить ее эффективность. В связи с полисистемным характером заболевания пациенты нуждаются в комплексном лечении и динамическом наблюдении.








