ВВЕДЕНИЕ
Первичные иммунодефициты (ПИД) — это тяжелые, генетически детерминированные заболевания, в основе которых лежат молекулярно-генетические дефекты, приводящие к нарушениям каскада иммунных реакций, пролиферации, дифференцировки и функций иммунокомпетентных клеток, характеризующиеся тяжелыми инфекционными процессами, аутоиммунными, аутовоспалительными проявлениями и склонностью к развитию злокачественных новообразований[1]. Отмечено, что диагноз ПИД может быть поставлен не только на 1-м году жизни, но и в подростковом возрасте, и все годы ребенок может быть компенсирован либо страдать различными заболеваниями[2, 3].
Самую распространенную форму ПИД (около 60% случаев заболеваний) представляют агаммаглобулинемии (АГГ) — группа врожденных дефектов антителопродукции, характеризующаяся резким снижением концентрации сывороточных иммуноглобулинов всех классов и количества циркулирующих В-клеток. Частота встречаемости АГГ, по данным разных авторов, составляет от 1 : 100 000 до 1 : 200 000[4]. Данная патология имеет различный характер наследования: сцепленный с Х-хромосомой или аутосомно-рецессивный. X-сцепленный вариант АГГ XLA (X-Linked Agammaglobulinemia) носит название болезни Брутона и составляет более 80% всех наследственных вариантов АГГ[5].
XLA описана O. Bruton в 1952 г. у мальчика с рецидивирующими бактериальными инфекциями, но только в 1993 г. был идентифицирован ген, мутации которого приводят к развитию заболевания. Этот ген, расположенный на длинном плече Х-хромосомы (Xq21.3-Xq22), кодирует B-клеточную тирозинкиназу (ВКТ), которая является ключевой молекулой в активации и дифференцировке пре-B-клеток[6]. При болезни XLA в результате генетического дефекта нарушается синтез ВКТ, что приводит к остановке дифференцировки В-лимфоцитов на стадии пре-В-клеток в костном мозге и, как следствие, к отсутствию зрелых В-лимфоцитов в периферическом кровообращении и серьезному снижению концентрации в сыворотке иммуноглобулинов всех классов[7].
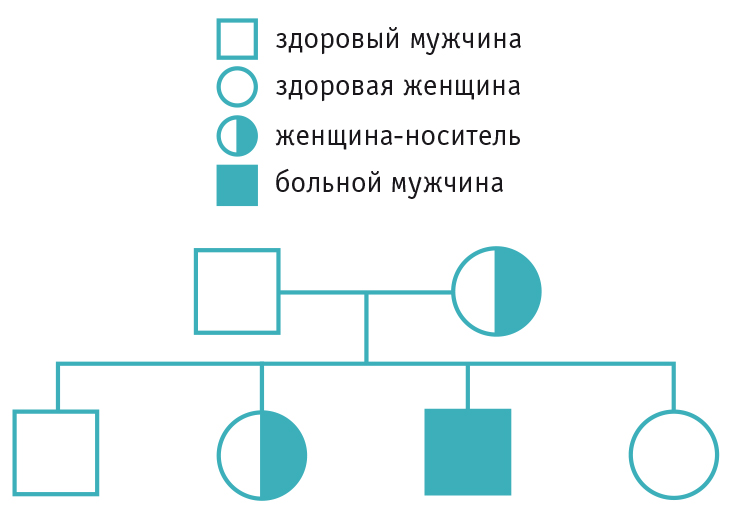
Болезнь Брутона наследуется по Х-сцепленному рецессивному типу: признаки заболевания проявляются только у мальчиков (рис. 1). Дочери больных XLA являются облигатными носителями мутации, но остаются клинически здоровыми[2].
Рис. 1. Схема наследования АГГ от матери-носителя
Начало клинических проявлений при XLA, как правило, относится ко второму полугодию жизни (после исчезновения из циркуляции трансплацентарно переданных материнских антител). Чаще всего заболевание манифестирует с инфекционных поражений респираторного и гастроинтестинального трактов. Дефекты антителопродукции приводят к повышенной чувствительности к инфекциям, вызванным инкапсулированными бактериями, особенно Streptococcus pneumoniae и Haemophilus influenzae. У подавляющего большинства пациентов с АГГ развиваются повторные или хронические инфекции, вызванные вышеуказанными микроорганизмами, такие как пневмонии, отиты, синуситы, конъюнктивиты, энтероколит. Несколько реже встречаются более тяжелые инфекции: менингит, остеомиелит, деструктивная плевропневмония, сепсис, септический артрит, пиодермия и гнойные инфекции подкожной клетчатки.
Маркером АГГ с дефицитом B-клеток является гипоплазия лимфатических узлов и миндалин. Частое осложнение этого заболевания — артрит. Как правило, развиваются неинфекционные моноартриты, поражающие крупные суставы, однако возможно и формирование деформирующего полиартрита, аналогичного ревматоидному или псориатическому артриту[6, 8].
В диагностике АГГ ведущее место занимают вышеперечисленные клинические проявления, но они не являются патогномоничными только для АГГ. При иммунологическом обследовании выявляется снижение содержания в сыворотке крови иммуноглобулинов всех классов, лимфоцитов (содержание СD19+-В-клеток менее 2%). Достоверно подтверждает диагноз генетическое обследование, направленное на поиск мутаций в гене ВКТ. На данный момент в практику внедряется неонатальный скрининг, заключающийся в количественном определении методом полимеразной цепной реакции в режиме реального времени в сухих пятнах крови новорожденных уровня TREC (T-cell receptor excision circle — кольцевые участки, вырезанные из ДНК в Т-лимфоците при его созревании) и KREC (kappa recombining excision circle — кольцевые участки ДНК, вырезанные при созревании В-клеток из локуса, кодирующего каппа-цепь), позволяющий на доклиническом этапе заподозрить дефекты Т- и В-клеточного звеньев иммунитета[5, 9].
Основой лечения АГГ является заместительная терапия иммуноглобулином для внутривенного введения. Регулярная поддерживающая терапия проводится 1 раз в 3–4 нед в дозе 0,4–0,6 г/кг. Претрансфузионный уровень IgG должен составлять не менее 700 мг/дл. В настоящее время широкое распространение получило использование подкожного иммуноглобулина, ежемесячная доза которого в 1,3 раза выше, чем внутривенного, и обычно делится на 4 введения (1 раз в неделю). Рано начатая адекватная заместительная терапия иммуноглобулином позволяет избежать формирования хронических инфекций и значительно уменьшает количество эпизодов острых инфекций и частоту развития аутоиммунных осложнений[6, 10].
КЛИНИЧЕСКИЙ СЛУЧАЙ
О пациентах: в семье из 5 человек 3 детей (мальчики) страдают X-сцепленным вариантом АГГ. Генеалогический анамнез: имеются случаи смерти новорожденных детей у бабушки по линии матери.
Ребенок 1, средний брат, возраст при обследовании 1 год 8 мес
Анамнез жизни: ребенок от 3-й нормально протекавшей беременности, 2-х срочных родов. При рождении масса 4000 г, рост 55 см, оценка по Апгар — 9/10 баллов. Период новорожденности протекал без особенностей. На 1-м году жизни прививался по национальному календарю, поствакцинальный период — без осложнений. Находился на грудном вскармливании до 1 года 2 мес, в этот период не болел. Физическое, нервно-психическое развитие ребенка на 1-м году жизни соответствовало возрасту. Аллергоанамнез не отягощен.
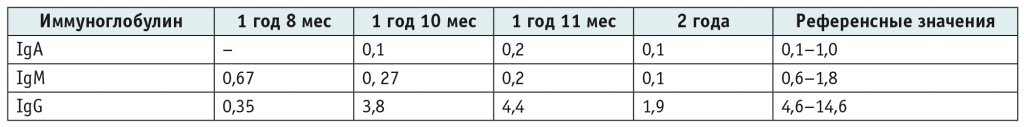
Анамнез заболевания: после окончания грудного вскармливания наблюдались частые острые респираторные вирусные заболевания (6 раз в год), отит, в 1 год 7 мес перенес острый бронхит. Заболевания протекали с высокой температурой, длительно, тяжело, всегда требовали длительного назначения антибиотиков. В анамнезе — несколько эпизодов кратковременного разжиженного стула без повышения температуры. Эндокринологом диагностированы тиромегалия и тимомегалия. В возрасте 1 год 8 мес консультирован пульмонологом, когда впервые проведено иммунологическое обследование, по результатам которого выявлено снижение показателей гуморального иммунитета. Получил два курса Immunoglobullini humoros по 3,0 № 3 внутримышечно. В динамике уровень иммуноглобулина сохранялся низким (табл. 1).
Таблица 1. Показатели уровня иммуноглобулинов у ребенка 1 в динамике, г/л
Физикальная диагностика: при обращении (1 год 8 мес) физическое развитие ниже среднего, дисгармоничное. Белково-энергетическая недостаточность легкой степени. Общее состояние средней степени тяжести, самочувствие страдает умеренно. Шейные лимфатические узлы пальпируются 1 степени, мягкие, безболезненные, не спаянные с окружающими тканями, печень, селезёнка не увеличены. Внутренние органы без особенностей.
Предварительный диагноз: первичный иммунодефицит, АГГ/гипогаммаглобулинемия.
Для верификации диагноза первичного иммунодефицита пациент в возрасте 2 года 5 мес направлен в Российскую детскую клиническую больницу (РДКБ) ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России.
Результаты лабораторной диагностики: при обследовании выявлена АГГ — IgA 0,06 г/л (норма 0,3–1,5 г/л), IgG 0,46 г/л (норма 8,8–15,4 г/л), IgM 0,08 г/л (норма 0,8–1,6 г/л). По данным иммунофенотипирования лимфоцитов CD19 — 1%. Поствакцинальные антитела к краснухе и гепатиту В не определяются. Проведено генетическое исследование: обнаружена мутация в гене ВКТ с.862C>Т (p.288Arg>Trp) в экзоне 10.
Клинический диагноз: на основании дебюта заболевания на 2-м году жизни, наличия рецидивирующих тяжелых длительно текущих бактериальных процессов (бронхолегочная система, ЛОР-органы) в сочетании со значительным снижением всех классов иммуноглобулинов и лимфоцитов СD19+, обнаружением мутации в гене ВКТ в экзоне 10 ребенку был выставлен диагноз: Первичный иммунодефицит: XLA с дефицитом В-клеток (мутация в гене ВКТ с.862C>Т (p.Arg288Trp) в экзоне 10) (код по МКБ: D80.0).
Учитывая генетическую детерминированность патологии, проведено обследование братьев.
Ребенок 2, младший брат, возраст при обследовании 1 год 3 мес
Анамнез жизни: ребенок от 4-й нормально протекавшей беременности, 3-х срочных родов. При рождении масса 3820 г, рост 55 см, оценка по шкале Апгар 9/10 баллов. Находился на грудном вскармливании до 1 года 3 мес. Аллергоанамнез не отягощен. Физическое, нервно-психическое развитие ребенка на 1-м году жизни соответствовало возрасту. Профилактические прививки проведены по национальному календарю.
Анамнез заболевания: до 1 года ребенок не болел, в возрасте 1 год и 1 год 1 мес переболел острыми респираторными вирусными заболеваниями, получал антибактериальную терапию с положительным эффектом. В 1 год 3 мес по месту жительства мальчику проведено иммунологическое обследование, выявлено снижение содержания иммуноглобулинов: IgA — 0,2 г/л (норма 0,1–1,0 г/л); IgM — 0,2 г/л (норма 0,6–1,8 г/л); IgG — 3,6 г/л (норма 4,6–14,6 г/л).
Физикальная диагностика: жалоб активных нет, состояние стабильное, самочувствие удовлетворительное. Физическое развитие среднее, гармоничное. Кожные покровы розовые, нормальной влажности, чистые. Ногти и волосы не изменены. Лимфатическая система: шейные, подчелюстные, подмышечные, паховые лимфоузлы до 1 см, безболезненные, не спаяны между собой и с окружающими тканями. Печень у края реберной дуги, безболезненная, эластичная. Селезенка не пальпируется. По внутренним органам — без особенностей.
Предварительный диагноз: первичный иммунодефицит, ХLA.
С целью проведения обследования и уточнения диагноза ребенок в возрасте 1 год 4 мес госпитализирован в отделение клинической иммунологии РДКБ ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России.
Результаты лабораторной диагностики: снижение всех фракций иммуноглобулинов: IgA — 0,06 г/л (норма 0,1–1,0 г/л), IgM — 0,13 г/л (норма 0,6–1,8 г/л), IgG — 2,43 г/л (норма 4,6–14,6 г/л). По данным иммунофенотипирования лимфоцитов CD19 — 3%. Генетическое исследование: обнаружена мутация в гене ВКТ c.862С>Т в экзоне 10.
Подтвержден клинический диагноз: Первичный иммунодефицит: ХLA с дефицитом В-клеток (мутация в гене ВКТ с.862С>Т (p.Arg288Trp) в экзоне 10) (код по МКБ: D80.0).
Ребенок 3, старший брат, возраст при обследовании 8 лет 6 мес
Анамнез жизни: ребенок от 1-й беременности, протекавшей с угрозой прерывания в 24 нед, 1-х срочных родов. При рождении масса 3470 г, рост 52 см, оценка по шкале Апгар 9/10 баллов. Находился на грудном вскармливании до 1 года 6 мес. Профилактические прививки проведены по национальному календарю. Аллергоанамнез не отягощен. Нервно-психическое развитие по возрасту.
Физикальная диагностика: жалоб активных нет, состояние стабильное, самочувствие удовлетворительное. Физическое развитие среднее, гармоничное. Кожные покровы розовые, нормальной влажности, чистые. Ногти и волосы не изменены. Лимфатическая система: шейные, подчелюстные, подмышечные, паховые лимфоузлы до 1 см, безболезненные, не спаяны между собой и с окружающими тканями. Печень пальпируется у края реберной дуги. Селезенка не пальпируется. По внутренним органам без особенностей.
Анамнез заболевания: диагностирована пиелоэктазия в 9 мес. Болел инфекционно-воспалительными заболеваниями редко (1–3 раза в год), лечился амбулаторно, не всегда получал антибактериальную терапию. В 8 лет 6 мес определены уровни иммуноглобулинов: IgA — 0,63 г/л (норма 0,9–1,9 г/л), IgM — 0,43 г/л (норма 0,8–1,9 г/л), IgG — 5,28 г/л (норма 9,7–11,7 г/л).
В возрасте 9 лет 6 мес мальчик обследован в РДКБ ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России.
Результаты лабораторной диагностики: уровень сывороточных иммуноглобулинов: IgA — следы (норма 0,9–2,9 г/л); IgG — 2,32 г/л (норма 9,4–16,6 г/л), IgM — 0,53 г/л (норма 0,6–2,0 г/л). По данным иммунофенотипирования лимфоцитов CD19 — 3%. Проведено молекулярно-генетическое обследование и также обнаружена мутация в гене ВКТ с. 862C>Т в экзоне 10.
Верифицирован клинический диагноз: Первичный иммунодефицит: ХLA с дефицитом В-клеток (мутация в гене ВКТ с.862С>Т (p.288Arg>Trp) в экзоне 10) (код по МКБ: D80.0).
Обнаружение одинакового типа мутации гена у всех трех братьев послужило основанием для генетического обследования матери, в результате которого у нее обнаружена мутация в гене в гетерозиготном состоянии (ВКТ с.826С>T (p. Arg288Trp/n) в экзоне 10).
Тактика лечения и наблюдения пациентов. После установления диагноза мальчики регулярно получают заместительную терапию иммуноглобуллином для внутривенного введения в дозе 0,4–0,5 г/кг массы 1 раз в 3–4 нед по жизненным показаниям, с целью профилактики пневмоцистных инфекций — внутрь противомикробный препарат триметоприм. Наблюдаются педиатром, иммунологом, отоларингологом по месту жительства. Проводится ежемесячный мониторинг предтрансфузионного уровня сывороточных иммуноглобулинов, показателей клинического анализа крови, биохимического анализа крови, общего анализа мочи. УЗИ органов брюшной полости, почек, лимфатических узлов, ЭКГ проводятся 1 раз в 3 мес, туберкулинодиагностика — ежегодно.
На фоне заместительной терапии состояние детей стабилизировалось, уменьшилось количество эпизодов заболевания респираторными инфекциями.
В связи с отсутствием препарата внутривенного иммуноглобулина у среднего брата развился синусит верхнечелюстной пазухи с затяжным течением. В настоящее время дети переведены на подкожное введение иммуноглобулина.
ЗАКЛЮЧЕНИЕ
Верифицирование диагноза наследственной АГГ имеет важное значение для определения генетического прогноза. Несмотря на возможность появления здоровых детей мужского пола в данной семье, все рожденные мальчики страдают ХLA с дефицитом В-клеток. Особенность клинического случая заключается в том, что описанные пациенты имеют нетипичное для болезни Брутона легкое течение.
Учитывая, что диагноз первичного иммунодефицита установлен в детском возрасте до формирования декомпенсированных состояний, при проведении адекватной пожизненной заместительной терапии иммуноглобулинами, регулярной профилактической противомикробной терапии, мониторинге иммунологических показателей, динамическом наблюдении прогноз жизни этих пациентов благоприятный.
Поступила: 05.06.2023
Принята к публикации: 06.10.2023








