Дифференциальная диагностика рекуррентных депрессий (РД) и биполярных депрессий (БД), т. е. депрессивных эпизодов при биполярном аффективном расстройстве, представляет определенные трудности в клинической и исследовательской практике. Многие авторы выделяют такие атипичные признаки БД, как гиперсомния и повышенный аппетит[1–6]. Относительно выраженной психомоторной заторможенности и, одновременно, повышенной эмоциональной реактивности мнения исследователей не столь однозначны, однако эти признаки атипии депрессивного синдрома выявляются далеко не во всех случаях. Между тем дифференциация рекуррентных (униполярных) и биполярных депрессий чрезвычайно важна для выбора терапии: антидепрессантов при РД или в первую очередь тимостабилизаторов при БД. При отсутствии надежных анамнестических данных важную дифференцирующую роль могут играть нейробиологические характеристики депрессивных состояний, хотя к настоящему времени успехи в исследованиях такого рода относительно скромны.
Одной из задач клинических нейрофизиологических исследований является поиск надежных маркеров, которые помогли бы в объективной диагностике заболеваний, в том числе в дифференциальной диагностике в ситуациях, когда наблюдаемые симптомы затруднительно однозначно отнести к определенному заболеванию. К настоящему моменту накоплены данные объективных исследований (нейрофизиологических и биохимических), на основе которых предлагаются биомаркеры как для униполярной[7], так и для биполярной депрессии[8]. Вопрос о схожести патогенетических механизмов, лежащих в основе разных видов депрессии, пока остается открытым.
Эмоциональные стимулы, в том числе эмоциональные лица, обрабатываются многими структурами мозга[9], при этом ключевыми являются миндалина и префронтальная кора. Эти же структуры чаще всего упоминаются, когда речь идет о нарушениях в обработке эмоциональной информации при депрессии[10]. По данным функциональной МРТ, при оценке эмоциональных лиц у пациентов с БД наблюдается бо’льшая активность в подкорковых отделах и в вентральной префронтальной коре по сравнению с пациентами с РД[11]. В другом исследовании авторам удалось показать более дифференцированные по типу эмоционального стимула различия в активности миндалины между этими группами пациентов[12]. Метаанализ исследований с эмоциональными лицами показал, что различия между уни- и биполярной депрессией наблюдаются в коре, таламусе и стриатуме, т. е. затрагивается обширная сеть структур мозга[13].
В нейрофизиологических исследованиях предполагается, что активность одной или нескольких структур у пациентов отличается от таковой у здорового контроля (ЗК) и зависит от диагноза, а выполнение когнитивного задания позволит этим различиям лучше проявиться. Использованная в нашем исследовании многоканальная запись ЭЭГ не позволяет локализовать активность в глубоких структурах, но имеет высокое временно’е разрешение, недоступное для метаболических методов (ПЭТ, МРТ), и достаточно высокое пространственное разрешение, в отличие от традиционной ЭЭГ.
В нашем исследовании была использована CNV-парадигма (англ. contingent negative variation — условная негативная волна) со зрительными стимулами: при таком дизайне эксперимента стимулы подаются парами с задержкой между ними, первый из них предупреждающий, а второй — пусковой, требующий какой-то реакции. Эта парадигма похожа на классическое (павловское) обусловливание, особенно если пусковой стимул является релевантным для испытуемого и может служить подкреплением. Испытуемые не были информированы о связи предупреждающего стимула (ключа) и определенной категории изображений, эта связь устанавливалась ими самими во время исследования неосознанно, имплицитно. Помимо нейтральных изображений людей и животных мы применяли угрожающие стимулы, которые имеют высокую релевантность и активируют защитные реакции мозга[14], что повышает вероятность образования ассоциации между ключом и изображением. Согласно литературным источникам ожидание стимулов может происходить без осознания и эффект сильнее проявляется при ожидании негативной лицевой экспрессии[15, 16]. Исследования неосознанных процессов могут быть перспективными при поиске нейрофизиологических маркеров психопатологических состояний, так как позволяют изучать когнитивные процессы, которые происходят с минимальным вмешательством сознания пациента.
Мы предполагали, что в результате данного исследования увидим различия в амплитудах компонентов зрительного ответа на ключ, т. е. эмоциональную модуляцию (ЭМ), вызванную ассоциацией этого ключа с нейтральными или эмоциональными стимулами. Предполагалось обнаружить различия в амплитуде или в топографии неосознанной ЭМ у пациентов в зависимости от того, проявляется ли депрессия в рамках РД или биполярного аффективного расстройства.
Целью данного исследования было изучение различий в активности мозга у пациентов с депрессивным эпизодом в рамках рекуррентной и биполярной депрессии.
МАТЕРИАЛЫ И МЕТОДЫ
Испытуемые
Исследование проведено на клинической базе отделения расстройств аффективного спектра Московского НИИ психиатрии с соблюдением стандартных предписаний по информированию пациентов и здоровых добровольцев. Критериями исключения были расстройства шизофренического спектра, депрессивные расстройства психотического уровня, наличие риска суицидального поведения, аддиктивные расстройства, эпилепсия и эпилептиформные синдромы, деменции, соматические и неврологические заболевания в стадии декомпенсации. Продолжительность за-
болевания от его клинической манифестации до обращения за помощью варьировала от 1 месяца до 2,5 года.
Запись ЭЭГ у пациентов выполняли до начала фармакотерапии клинически верифицированного депрессивного эпизода. В исследовании участвовали здоровые добровольцы — ЗК (16 человек, из них 9 женщин), пациенты с рекуррентным депрессивным расстройством — РД (16 человек, из них 10 женщин) и пациенты с депрессивным эпизодом в рамках биполярного аффективного расстройства — БД (16 человек, из них 8 женщин). Средний возраст испытуемых в контроле составлял 41 ± 10 лет, в группе РД — 41 ± 12 лет и в группе БД — 43 ± 12 лет. Возрастные границы обследуемых всех трех групп — от 23 до 60 лет. Статистически значимой разницы между группами по возрасту не было (F = 0,003, p = 0,99). Все участники были праворукими, с нормальным или скорректированным зрением.
Для психометрической оценки уровней тревоги и депрессии использовали Шкалу тревоги Гамильтона (англ. Hamilton Anxiety Rating Scale, HARS)[17] и Шкалу депрессии Гамильтона в варианте из 17 пунктов (англ. Hamilton Depression Rating Scale, HDRS-17)[18]. Средние значения по HARS для общей тревоги составляли 24,0 ± 6,4 балла в группе РД и 19,8 ± 8,9 балла в группе БД. Значения по HDRS-17 в группах РД и БД — 22,5 ± 5,8 и 22,6 ± 7,1 балла соответственно. В обеих группах пациентов показатель психической тревоги преобладал над выраженностью соматической тревоги: 13,5 ± 2,9 балла — психическая и 10,5 ± 4,1 балла — соматическая тревога для РД; 12,3 ± 4,2 балла — психическая и 7,4 ± 5,8 балла — соматическая тревога для БД. Разницы между группами по шкалам не было (p > 0,05).
Контрольная группа (здоровый контроль — ЗК) сформирована из большой группы здоровых добровольцев, которые выполняли ту же когнитивную задачу, что и пациенты основных групп. Выбор проводили по полу, возрасту и образовательному уровню. Поскольку пациенты основных групп сообщали, что не заметили связи между ключом и картинкой (см. пояснения ниже), в группу ЗК отбирали только тех добровольцев, которые тоже не заметили этой связи. Испытуемые контрольной группы не обращались за врачебной психиатрической помощью, не страдали неврологическими или тяжелыми соматическими заболеваниями. Для исключения недиагностированной аффективной патологии проводился скрининг с использованием Госпитальной шкалы тревоги и депрессии (англ. Hospital Anxiety and Depression Scale, HADS) в программе «Психотест» («Нейрософт», Россия). HADS состоит из двух подшкал, выявляющих признаки депрессии (HADS-D) и тревоги (HADS-A). У всех добровольцев значения обеих подшкал находились в пределах нормы.
Стимулы и общий план исследования
Всего было 160 изображений, выбранных в Интернете и обработанных в программе «Фотошоп». В качестве стимулов использовались черно-белые фотографии людей и животных, запечатленных анфас, со взглядом, направленным на смотрящего на снимок. Все стимулы принадлежали к одной из четырех категорий, по 40 фотографий в каждой: HN — нейтральные изображения людей; HE — эмоциональные изображения людей; AN — нейтральные изображения животных; AE — эмоциональные изображения животных. В качестве эмоциональных использовались фотографии, где объект проявлял злость, агрессию, угрозу. Стимулы из каждой категории предъявлялись в случайном порядке с равной вероятностью и без повторов в рамках одного исследования. Более подробно дизайн исследования описан в нашей работе[19].
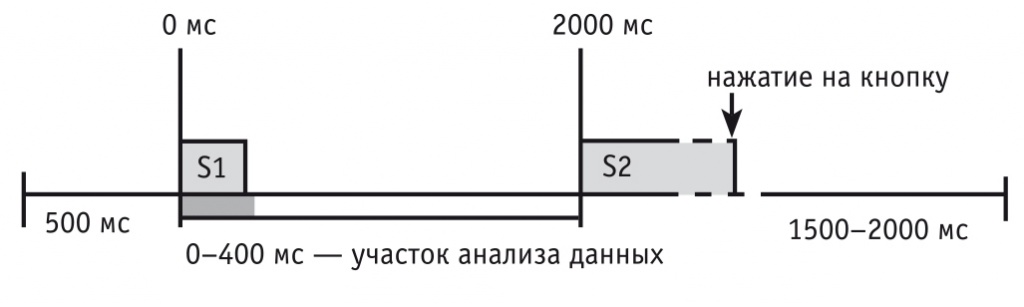
Согласно инструкции надо было нажимать на кнопку 1 при появлении изображений людей и кнопку 2 при появлении изображений животных. За 2 сек до предъявления фотографий подавался предупреждающий стимул (ключ), связь которого с фотографиями испытуемым не объяснялась. Каждой из четырех категорий соответствовал свой ключ: крест для людей и квадрат для животных, для эмоциональных стимулов эти фигуры были повернуты на 45 градусов. Фотография оставалась на экране до нажатия на кнопку, ожидание ответа составляло 5 сек, промежуток времени между единичными реализациями варьировал от 1500 до 2000 мс (рис. 1).
Рис. 1. Временны́е параметры единичной реализации.
Примечание. S1 — ключ (предупреждающий стимул) длительностью 17 мс; S2 — фотография человека или животного (пусковой стимул, требующий моторного ответа); темной полосой отмечен отрезок времени 0–400 мс после предъявления S1, для которого проводился анализ
После выполнения основного задания, где явного различения эмоций не требовалось, испытуемые дополнительно классифицировали те же стимулы как нейтральные или негативные (угрожающие). Стимулы предъявлялись с такими же временны́ми параметрами, как в основном задании. Аналогичное задание на явное, или эксплицитное, различение эмоций помимо участников данного исследования выполнялось большой группой здоровых добровольцев: база составляет 220 человек и продолжает пополняться. Для подачи стимулов использовалась программа E-Prime Professional, версия 2 (PST Inc., США).
Запись и анализ электроэнцефалограммы
ЭЭГ записывалась на оборудовании Net Station 4.4 (Electrical Geodesics Inc., США) от 128 каналов с частотой дискретизации 500 Гц в диапазоне частот 0–200 Гц. Запись ЭЭГ фильтровалась в диапазоне 0–30 Гц и сегментировалась относительно момента подачи ключа — 100 мс до и 2000 мс после. Этот участок включал зрительный ответ на ключ и медленную волну (CNV), вызванную ожиданием предъявления изображений людей и животных. Безартефактные единичные реализации усредняли для каждого испытуемого по четырем категориям только для правильных ответов. Исходный монтаж меняли на монтаж с усредненным референтом, что добавляло 129-й канал — вертекс, прежний референтный канал. Проводили коррекцию изолинии усредненных ответов и далее выполняли статистический анализ.
Были получены индивидуальные усредненные вызванные ответы для парных условий HN и HE (нейтральные
и угрожающие человеческие лица) и AN и AE (нейтральные и угрожающие изображения животных). Далее отдельно для каждой группы испытуемых из нейтрального условия вычитали эмоциональное условие в каждой паре условий, чтобы получить разностную волну (РВ). Эти волны сравнивали попарно между тремя группами испытуемых для изображений людей и для изображений животных.
Непараметрический тест для двух несвязанных выборок (тест Манна — Уитни) применяли для амплитуд синхронных точек РВ в каждом из 129 каналов отдельно с шагом 2 мс для отрезка 0–400 мс от начала ключа. Положительный результат определяли как наличие разницы при уровне значимости 0,05 (двухсторонний критерий). Проводили коррекцию результатов на повторные сравнения, а также не учитывали положительные результаты, если они наблюдались менее чем по трем соседним каналам. Компактные области статистически значимых различий по определенным каналам образовывали устойчивые топографические паттерны на поверхности скальпа в определенных временны́х окнах (рис. 2, 3). Выбранный участок анализа включал четыре основных хорошо выделявшихся компонента зрительного ответа мозга на ключ.
Рис. 2. Топокарты статистических различий между разностными волнами в группах для ключей перед изображениями людей.
Примечания к рис. 2, 3.
1. БД — биполярные депрессии; ЗК — здоровый контроль; РД — рекуррентные депрессии.
2. Компактные области статистически значимых различий показаны в виде затемненных участков на поверхности скальпа. Карты представлены для четырех временны́х окон со сходной топографией эмоциональной модуляции внутри каждого окна; лобные области сверху, правое полушарие справа
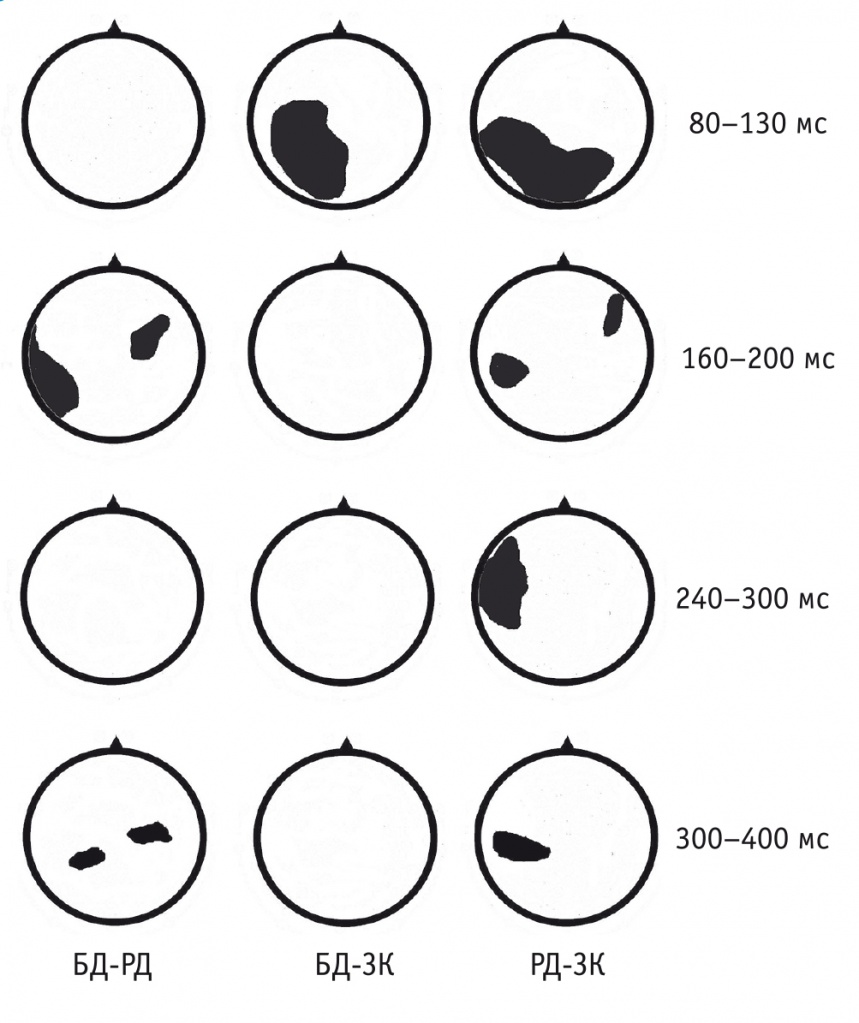
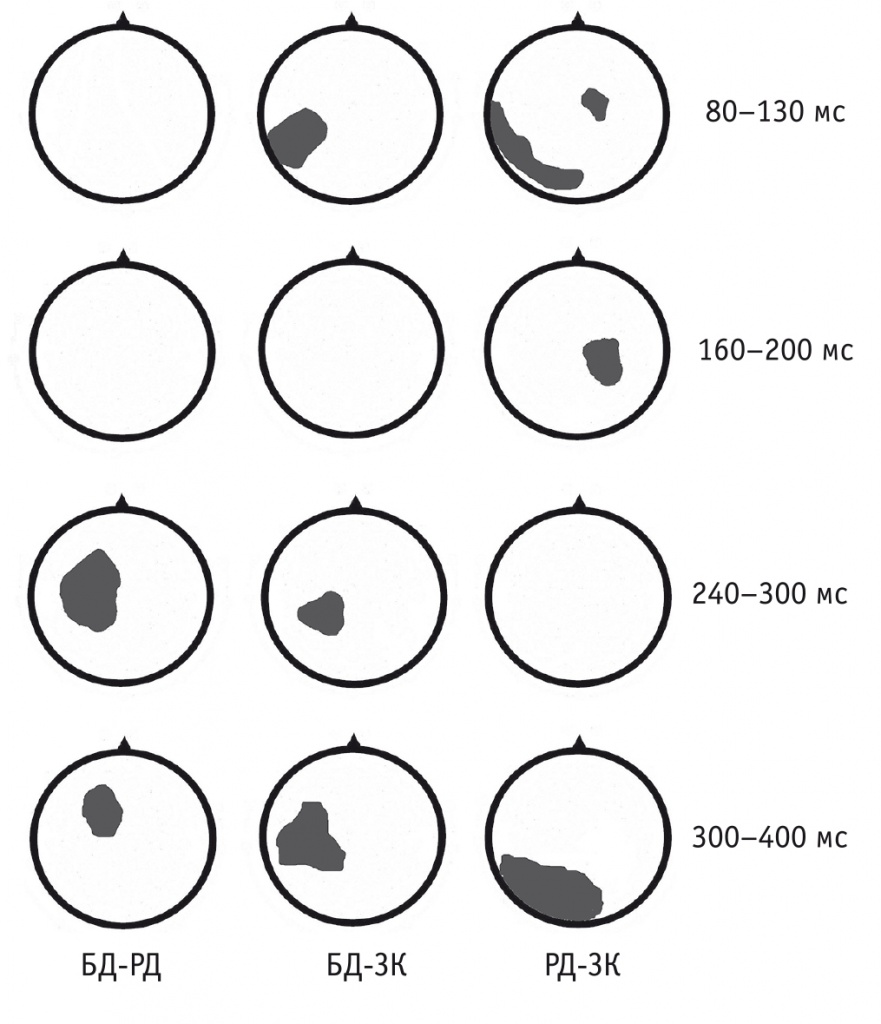
Рис. 3. Топокарты статистических различий между разностными волнами в группах для ключей перед изображениями животных
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Значение предупреждающего стимула (ключа) испытуемым в инструкции не объяснялось. Все они утверждали, что не заметили связи между ключом и определенной категорией стимулов, тем не менее в зрительном ответе на ключ произошли изменения, вызванные тем, что ключ ассоциировался с определенным типом стимулов в результате имплицитного обучения. Таким образом, был получен эффект неосознанной ЭМ зрительного ответа.
В данном пилотном исследовании мы ограничились прямым статистическим сравнением РВ между группами испытуемых. Такие волны представляют собой усредненные ответы, полученные при вычитании амплитуд в синхронных точках для двух связанных условий, отличающихся друг от друга предположительно по одному параметру. В представленном случае вычитание проводилось для эмоционального и нейтрального условий, отдельно для ключей, связанных с изображениями людей или животных. В каждой категории стимулов была получена ЭМ, т. е. прирост или редукция амплитуды, связанная с эмоциональностью стимула. Сравнение РВ между группами испытуемых дало статистически значимые различия амплитуд (p < 0,05), которые группировались по времени и в пространстве в компактные области (см. рис. 2, 3). На участке анализа 0–400 мс от начала стимула были выделены четыре временны́х окна, которые полностью или частично включали основные компоненты зрительного ответа на ключ — P100, N150, P220 и P380.
Окно 80–130 мс полностью включало компонент вызванной активности мозга, известный в литературе как Р100. Это позитивный в затылочных отведениях компонент с источником в зрительной коре. Латентность его может варьировать в промежутке от 80 до 120 мс, а полярность меняется на негативную в центральных и лобных областях. Предполагается, что Р100 отражает структурное кодирование зрительной информации и пространственное внимание. Для данных исследования пиковые латентности по задним височным и затылочным отведениям составляли 90 мс. ЭМ в этом компоненте для обоих типов стимулов различалась при сравнении между нормой и пациентами, но не между группами пациентов. В топографии различий ЭМ обнаружена некоторая специфика для РД и БД, но речь идет скорее о межиндивидуальных различиях, которые для зрительных вызванных ответов велики даже в норме. Для ключей перед изображениями людей ЭМ охватывала более обширные области, чем для ключей перед изображениями животных. Для обоих типов стимулов различия ЭМ были локализованы в основном в левом полушарии.
Следующий за Р100 компонент в задних областях имеет негативную полярность и пиковую латентность около 150 мс, по нашим данным. Компонент с латентностью, варьирующей от 130 до 200 мс в зависимости от условий записи, в литературе часто называют N170 и связывают со специфической чувствительностью к человеческим лицам. Он регистрируется и на другие зрительные объекты и предположительно отражает категоризацию зрительного стимула [20]. В норме этот компонент модулируется лицевой экспрессией[21], но есть основания предполагать, что его генератор в нижневисочной коре остается неизменным, а дополнительная активность, связанная с эмоциями, накладывается на этот компонент[22]. В описываемом исследовании ключи были простыми фигурами и не содержали изображений лиц, но они были ассоциированы с лицами благодаря обучению посредством классического обусловливания.
Второе окно (160–200 мс) частично попадает на этот негативный компонент с пиком на 150 мс (N150) и частично — на следующий позитивный компонент с пиковой латентностью около 220 мс (P220). Предполагается, что на латентностях около 250 мс происходят процесс различения стимула и выбор ответа, и в норме отмечено влияние избирательного внимания и эмоциональности стимула на компоненты этого диапазона[23]. Очевидно, что процессы обработки информации происходят в мозге не в одной временно́й точке, они не привязаны только к пикам компонентов, а также не имеют четких границ между стадиями. В окне 160–200 мс различия РВ между группами пациентов были обнаружены для ключей перед изображениями людей, но не животных. Различий между ЗК и БД не было найдено, а группа РД отличалась от нормы для обоих типов стимулов. В случае с ключами, связанными с лицами, различия РД–ЗК повторяли топографию различий РД–БД. Видимо, полученные результаты отражают тот факт, что ЭМ этого компонента вызванного ответа для БД ближе к норме, чем для РД.
Третье окно (240–300 мс) также попадает на промежуток между двумя хорошо выделяемыми пиками на усредненном вызванном ответе мозга. Это предыдущий компонент Р220, позитивный в затылочной и центрально-теменной областях, а также большой позитивный компонент с пиком около 380 мс, хорошо выделяемый в центральной области и в меньшей степени представленный в лобных областях. Согласно литературе на латентностях около 250 мс и более идут различение зрительного стимула и выбор ответа[23], работает избирательное внимание и возможна ЭМ. Видимо, наша позитивная волна Р380 — аналог компонента Р3а, т. е. разновидности Р300, которая имеет более ростральное расположение, чем Р3b, и связана с вниманием и ориентировкой к стимулу[24]. Возможно, ЭМ в этом окне отражает изменения уровня внимания, которые вызывают ключи, ассоциированные с ожиданием негативных стимулов (в описываемом исследовании — люди в гневе или агрессивные животные). А различия ЭМ между группами отражают разную заинтересованность участников из трех групп в эмоциональных стимулах и разный уровень модуляции внимания в группах. В этом окне различия между ЭМ для РД–ЗК наблюдались для ключей, связанных с лицами, но не с животными. Группа БД, напротив, отличалась от групп контроля и РД именно в случае с ключами, за которыми следовали изображения животных.
Последнее окно на участке анализа (300–400 мс) включает в себя пик Р380. Распределение данного компонента по скальпу в центральных и лобных областях свидетельствует о том, что это аналог волны Р3а, которую связывают с вниманием и реакцией на новизну стимула[24]. ЭМ рассматриваемого компонента для всех групп наблюдалась в основном в центральной области, а различия между группами в ЭМ локализовались в основном в центральной и теменной областях. Таких различий было больше для ключей, связанных с изображениями животных. Что довольно неожиданно, группа РД в окне 300–400 мс отличалась от нормы, топографически это были затылочные области и левый висок. Для компонентов с латентностью 300 мс и более в норме отмечается влияние эмоциональности стимула[23]. Как и в третьем окне, нами наблюдалась модуляция уровня внимания, вызванная тем, что эмоциональные стимулы в описываемом исследовании обладали высокими значениями такого показателя, как активация (англ. arousal).
ЗАКЛЮЧЕНИЕ
В представленном исследовании группы пациентов были небольшими (по 16 человек), но сопоставимыми по возрасту, соотношению полов и уровням тревоги и депрессии. Известно, что у пациентов некоторые компоненты вызванного ответа мозга могут быть редуцированы по сравнению с нормой уже на нейтральные изображения. Использование для анализа разностных волн между нейтральными и эмоциональными парными условиями позволило оценить относительные изменения, связанные именно с эмоциональной модуляцией (ЭМ).
Обнаружено, что ЭМ в компоненте Р100 может быть достаточно хорошим индикатором различий между нормой и депрессией, но, видимо, не позволяет различать разные виды депрессии. Следующие временны́е отрезки, на которых ЭМ различалась между группами, демонстрировали специфичность относительно группы и типа стимулов. Наблюдалось сходство ЭМ с нормой то для одной, то для другой группы пациентов. Вопрос требует дополнительного исследования, однако можно предположить, что биомаркером будет не модуляция отдельного компонента вызванной активности мозга, а, скорее, паттерн их изменений или отсутствия изменений при определенных условиях стимуляции.
Обнаруженные в данном исследовании статистически значимые различия неосознанной ЭМ между группами могут послужить заделом для дальнейшего поиска биомаркеров для разделения рекуррентной и биполярной депрессии. Увеличение групп испытуемых в дальнейших исследованиях покажет, были ли эти различия случайным эффектом, который нередко проявляется в небольших группах.








