ВВЕДЕНИЕ
Существующие методы раннего выявления лиц, употребляющих, а также склонных к употреблению психоактивных веществ, недостаточно информативны, так как устанавливают лишь факт их употребления и не позволяют проводить объективную оценку психического здоровья и определить прогноз заболевания[1, 2]. До последнего времени психиатрическая диагностика в рамках клинико-психопатологического метода базировалась в основном на описательных подходах. Поэтому крайне актуальны поиск и внедрение в психиатрию и наркологию объективизирующих лучевых методов диагностики, включая современные методы структурной нейровизуализации, такие как трактография, позволяющая уточнить тончайшие изменения связности корковых и подкорковых структур головного мозга (ГМ), которые не выявляются при рутинной МРТ[3].
В большинстве своем исследования, посвященные трактографии ГМ, проведены на малом количестве обследованных и не дают четкого понимания лучевой семиотики и функционально-микроорганического субстрата зависимостей[4]. При этом вопросы трактографии ГМ при аддиктивной патологии в отечественных научных публикациях практически не освещены и носят весьма противоречивый характер.
Встречающиеся исследования по микроструктурной патологии ГМ при синдроме зависимости от опиоидов (СЗО) и алкоголя (СЗА) оторваны от клинической практики, не могут использоваться в диагностическом процессе в силу своей изолированности и отсутствия комплексного подхода к решению данной проблемы[5]. Таким образом, из-за отсутствия единых технологических и методологических подходов в реальной практике внедрение магнитно-резонансной трактографии в современную наркологию в значительной степени затруднено.
Цель исследования — выявление с помощью магнитно-резонансной трактографии микроструктурных изменений ГМ у пациентов с СЗО и СЗА.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование отобраны 246 человек, из них 76 с СЗА (F10.2) и 170 с СЗО (F11.2), проходивших лечение в клиниках психиатрии и военно-полевой терапии Военно-медицинской академии им. С.М. Кирова в период с 2012 по 2019 г.
Средний возраст больных с СЗО составил 33,2 ± 6,24 года (20–45 лет), среди них было 119 мужчин (70%) и 51 женщина (30%). Средняя продолжительность зависимости от опиоидов — 8,2 ± 4,9 года, количество предыдущих курсов стационарного лечения — 4,7 ± 0,22.
У 158 (92,9%) больных имелся сопутствующий диагноз гепатита С. Гепатит В выявлен у 17 (10%) пациентов. При этом у 83 (48,8%) больных диагностирован ВИЧ.
Из числа других наркотических веществ, кроме опиоидов, 53 (31,2%) пациента эпизодически употребляли каннабиноиды, 42 (24,7%) — амфетамины и кокаин и 17 (10%) — седативные препараты (преимущественно бензодиазепины). Сопутствующее злоупотребление алкоголем наблюдалось у всех пациентов. При этом диагноз СЗА не устанавливался в связи с отсутствием достаточных критериев, приведенных в МКБ-10 для данной патологии.
В исследование также включены 76 пациентов с СЗА, средний возраст которых составил 35,1 ± 3,2 года, стаж алкоголизации — 6,3 ± 2,9 года. При этом все больные с СЗА находились в состоянии ремиссии (0,7 ± 0,5 месяца). Среднее количество ранее потребляемого алкоголя в пересчете на чистый этанол — 79,6 ± 8,96 г/день.
Всех участников осматривал психиатр-нарколог, который подтверждал наличие соответствующих критериев для включения в исследование.
В группу контроля вошли 150 здоровых людей без признаков зависимости от наркотических и психотропных веществ. Их средний возраст составил 28,2 ± 7,24 года.
Все обследуемые были проинформированы о проводимом исследовании и подписывали информированное добровольное согласие на участие. Критерии исключения: подтвержденное при МРТ наличие грубых морфологических изменений в ГМ и отказ от участия в исследовании, возраст (на момент обследования) менее 18 и более 45 лет, а также синдром зависимости от психоактивных веществ, не относящихся к классу опиоидов.
При проведении трактографических исследований все пациенты с синдромом зависимости вошли в две единые когорты по типу аддиктивной патологии. Такое распределение проведено исходя из необходимости подтверждения гипотезы об исходном присутствии микроструктурных изменений в сером и белом веществе ГМ при аддиктивной патологии разного типа.
Диффузионно-тензорная визуализация — методика МРТ, представляющая информацию о состоянии структур белого вещества ГМ и связях между этими структурами.
При выполнении исследования на магнитно-резонансном томографе с напряженностью магнитного поля 1,5 Тл использовалась импульсная последовательность DTI (DiffusionTensor Imaging) — одноимпульсная эхо-планарная томография без подавления сигнала от свободной жидкости с измерением в 12 направлениях коэффициента диффузивности. В дальнейшем получаемые последовательности использовались для преобразования и препроцессинга структурных данных с помощью трактографического модуля DSI Studio (http://dsi-studio.labsolver.org. DSI Studio является инструментом для анализа диффузионной МРТ с открытым исходным кодом, который отображает микроструктурные связи мозга и может сопоставлять результаты с нейропсихологическими данными.
Нами предпринята нестандартная попытка представить данные трактографии в аспекте понятия коннективности между структурами ГМ в норме и при патологии. Для анализа белого вещества мы создавали так называемые матрицы коннективности (МК). Для каждой исследуемой группы, исходя из современных представлений о составе аффективного круга Пейпеца, были составлены МК. Выбраны 28 регионов интереса, включающие зоны когнитивного контроля и возникновения аффективного заряда аддиктивной психопатологической симптоматики.
Получаемые данные накладывались на анатомический шаблон-маску, созданный в рамках проекта HCP (The Human Connectome Project) по данным трактографического обследования 1021 человека в возрасте от 25 до 35 лет без грубых органических изменений в ГМ.
РЕЗУЛЬТАТЫ
Оценка морфофункционального состояния ГМ по данным фракционной анизотропии проводилась с использованием МК, представляющих собой графическое отображение показателей связности между регионами интереса на основе коэффициента общей фракционной анизотропии (generalized fractional anisotropy, GFA), что дает представление о состоянии белого вещества — проводящих путей между корковыми и подкорковыми структурами. При анализе МК удалось констатировать различные показатели коннективности между выделенными структурами ГМ у людей, зависимых от опиоидов, у пациентов с СЗА и в группе контроля. На рисунке 1 представлены МК для групп пациентов с СЗО и здоровых людей при уровне порогового значения 0,1 ЕД GFA.
Рис. 1. Общий вид матриц коннективности структур головного мозга при наркозависимости (А) и в норме (Б) по атласу AAL (p < 0,05)
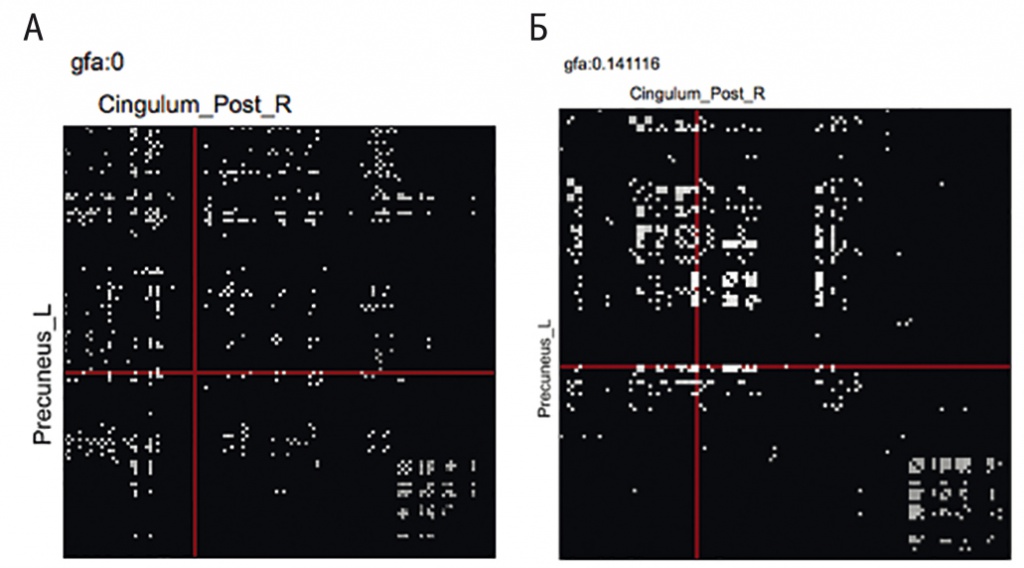
Для примера на перекресте линий обозначены коэффициенты коннективности между правой ободочной извилиной и предклиньем слева. В случае патологии такая связь между указанными структурами просто отсутствует (pFDR (False Discovery Rate) менее 0,05). Подобные зависимости хорошо визуализируются при графическом отображении коннективности ГМ по данным анализа графов у наркозависимых.
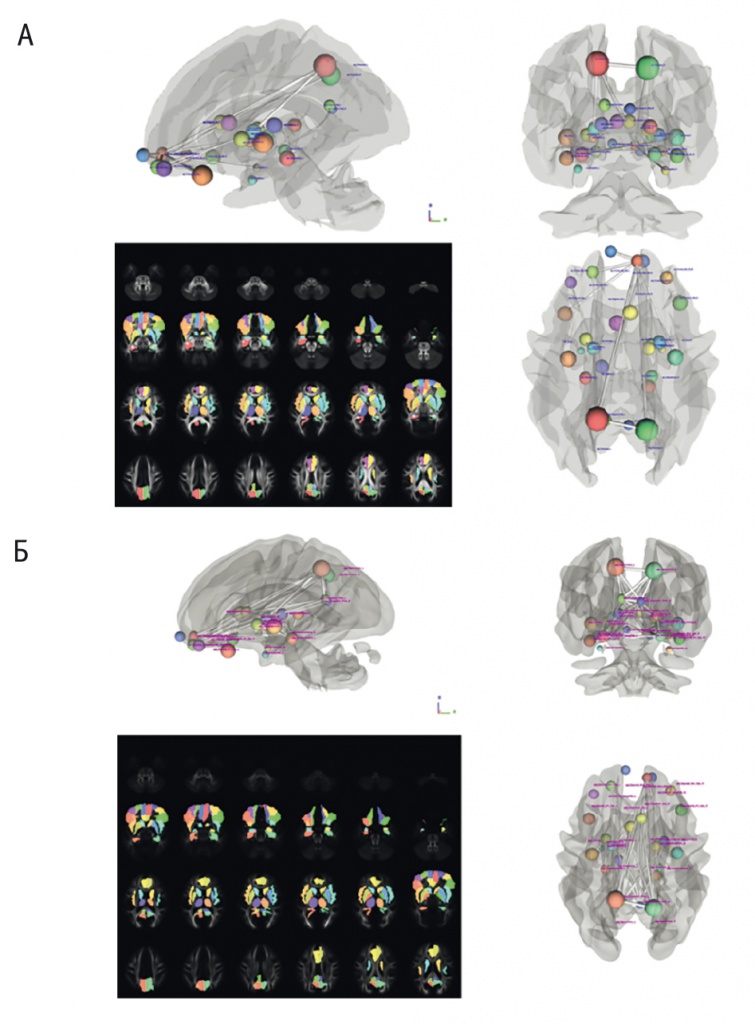
Так, на рисунке 2А отмечается разобщение нижних и средних отделов орбитофронтальной коры. Единственным участком орбитофронтальной коры, непосредственно связанным с субкортикальными структурами, остается верхний ее отдел. Взаимосвязи между ее различными отделами отсутствуют. Это хорошо видно на аксиальной проекции ГМ даже при визуальном сравнении на рисунке 2.
Рис. 2. Коннективность головного мозга при наркозависимости (А) и в норме (Б) на основе анализа графов (p < 0,05).
Примечание. Сферы символизируют корковые и подкорковые структуры, связи помечены линиями. Наблюдается значительное обеднение набора связей при наркозависимости
В таблице представлены общие свойства сконструированной нейросети из 28 мозговых структур по обозначенным в ней характеристикам.
Таблица
Характеристики артифициальной сети у пациентов с синдромом зависимости, усл. ед.
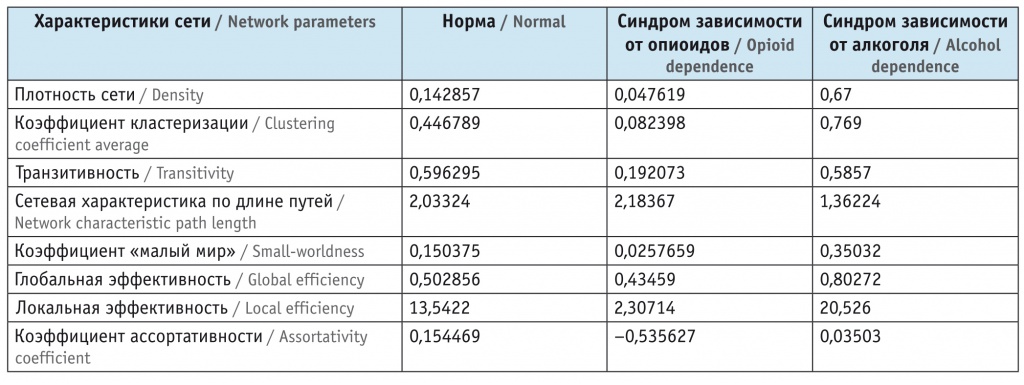
Плотность, демонстрирующая долю существующих соединений с возможными соединениями в спроектированной сети, в группе пациентов с СЗО была значительно снижена по сравнению с таковой в группе контроля и составляла 0,05 ЕД против 0,14 ЕД в норме.
Транзитивность — способность сети к пересечению связей ее узлов. Чем выше транзитивность, тем богаче и насыщеннее связность в ней. Этот показатель в группе наркозависимых также был значимо ниже по сравнению с нормой.
Коэффициент кластеризации — мера локальной связности внутри сети — обозначает количество связей, исходящих из одного узла, рассчитывается исходя из усредненных показателей без учета самого количества узлов. По нашему мнению, его уменьшение происходит при локальном обеднении функциональной значимости узлов сети, что должно коррелировать с данными функциональной МРТ (фМРТ). При анализе коэффициента кластеризации получены значимые различия с нормой, что свидетельствует об угнетении микроструктурной связности в сети.
Коэффициент ассортативности — коэффициент корреляции между всеми узлами сети на противоположных ее концах. Положительный коэффициент ассортативности показывает, что узлы имеют тенденцию связываться с другими узлами с такой же или сходной степенью. Отрицательный коэффициент свидетельствует о патологическом разобщении в сети и ее деградации, как в случае наркозависимости.
Сетевая характеристика по длине путей — характерная длина пути — это средняя кратчайшая длина пути в сети. Чем больше этот показатель, тем больше разобщенность в сети. Как видно из таблицы, у наркозависимых по сравнению с нормой этот показатель был выше.
Глобальная эффективность — средняя обратная длина кратчайшего пути в сети, она обратно пропорциональна характеристике длины пути. Локальная эффективность — глобальная эффективность, вычисляемая в окрестности узла, имеет связь с коэффициентом кластеризации. Условно говоря, эти две эффективности показывают эффективность работы исследуемой сети как бы по скорости распространения возбуждения в ней. Данные показатели у наркозависимых были значимо снижены.
Сеть «малого мира» — тип графа, в котором может быть достигнуто большинство узлов от каждого другого узла по наименьшему количеству связей. На примере большой компьютерной социальной сети это значит, что, например, какое-либо сообщество в ней и является сетью «малого мира». Чем больше этот показатель, тем более она насыщена управляющими центрами, состоящими не обязательно из каких-то объединенных структур, а напротив, из важных в функциональном плане, пусть и разобщенных локаций. Значительное снижение данного показателя также свидетельствует о дегенерации сети на микроструктурном уровне у наркозависимых, по-видимому, под влиянием воздействия наркотических препаратов.
У пациентов, зависимых от алкоголя, сетевые характеристики по параметрам плотности, кластеризации, глобальной и локальной эффективности были значительно выше нормы.
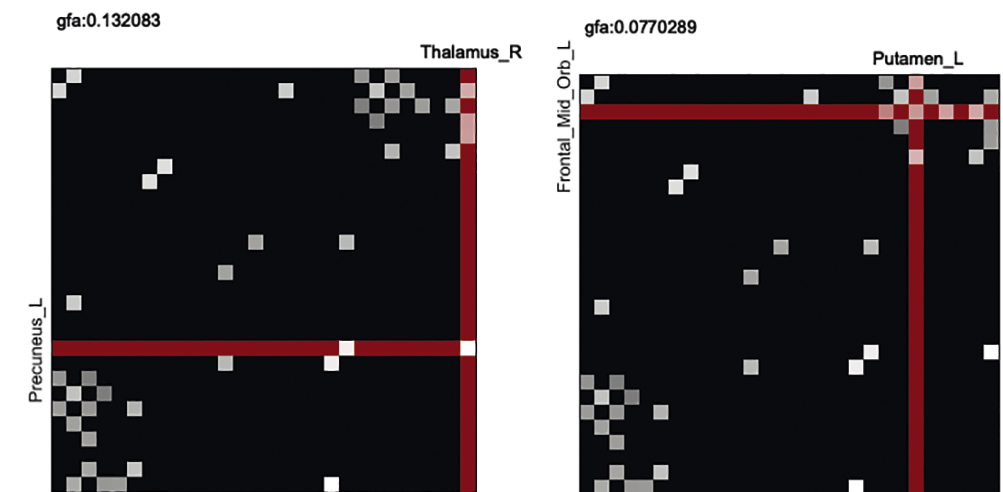
После анализа числовых характеристик сети проводился анализ коннективности между зонами интереса. Оценка связности структур осуществлялась по данным GFA в белом веществе. Из рисунка 3 видно, что наибольшие отличия выявлялись у наркозависимых пациентов. Наибольшее снижение коэффициентов GFA и, как следствие, связности между структурами отмечалось между подкорковыми и корковыми структурами при наркомании при относительной ее сохранности при алкоголизме.
Рис. 3. Различия матриц коннективности у пациентов с алкоголизмом (А), наркоманией (Б) и у участников группы контроля (В), p < 0,05

Из представленных на рисунке матриц коннективности хорошо видно, что у наркозависимых разобщена связность коры и подкорковых структур практически полностью, за исключением хвостатого ядра, таламуса и предклинья слева, а также уменьшен коэффициент GFA в этих структурных связях по сравнению с нормой. При этом у пациентов с алкоголизмом аналогичные связности не определялись вовсе.
По результатам сопоставления трактографических данных о ГМ в норме и у пациентов с алкоголизмом отмечается смещение коннективности в сторону подкорковых структур (рис. 4). Так, левый гиппокамп повышает связность с другими субкортикальными структурами (бледные шары, миндалина, хвостатые ядра и др.), образуя единый патологический конгломерат, а с медиальной орбитофронтальной корой связь утрачивается. Кроме того, при патологии миндалина выстраивает связи с обоими гиппокампами, создавая патологическое объединение хранилища эмоциональной памяти и тревоги у больных алкоголизмом.
Рис. 4. Матрицы микроструктурной коннективности. Патологический конгломерат связности подкорковых структур при алкоголизме (А) и норма (Б), по данным трактографии (p < 0,05)

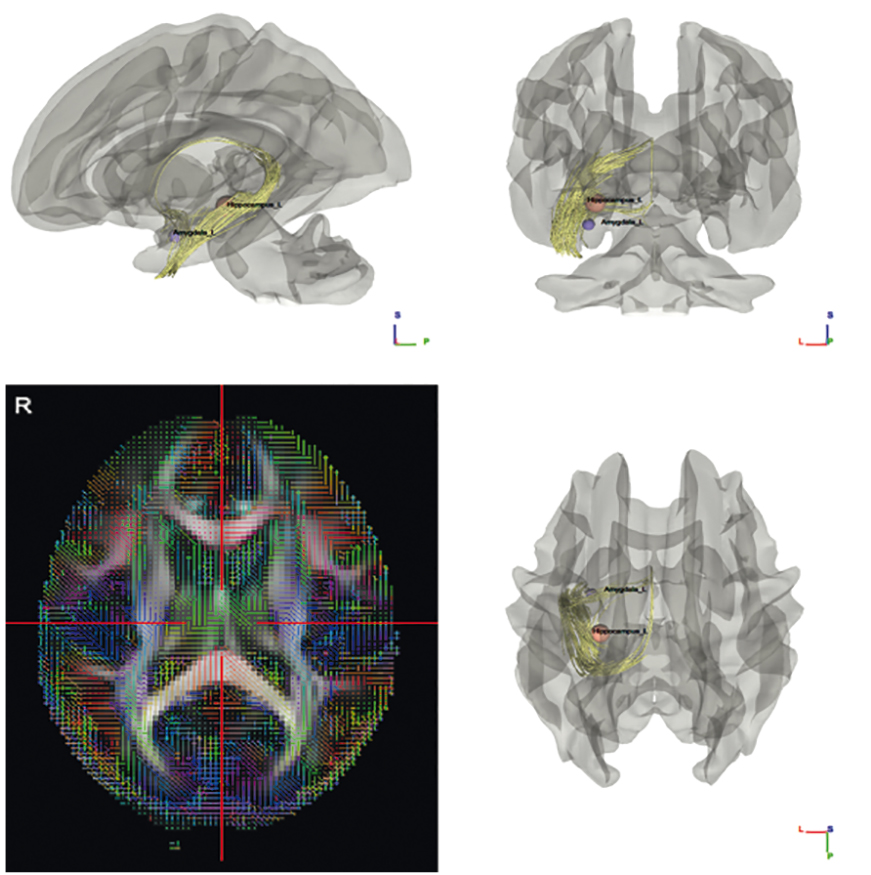
С целью анализа выявленного патологического взаимодействия смоделированы тракты, исходящие из этих двух структур (рис. 5).
Рис. 5. Моделирование взаимодействия миндалины и гиппокампа головного мозга при зависимости от алкоголя с использованием инструмента «файбертрекинг» программы DSI Studio (p < 0,05)
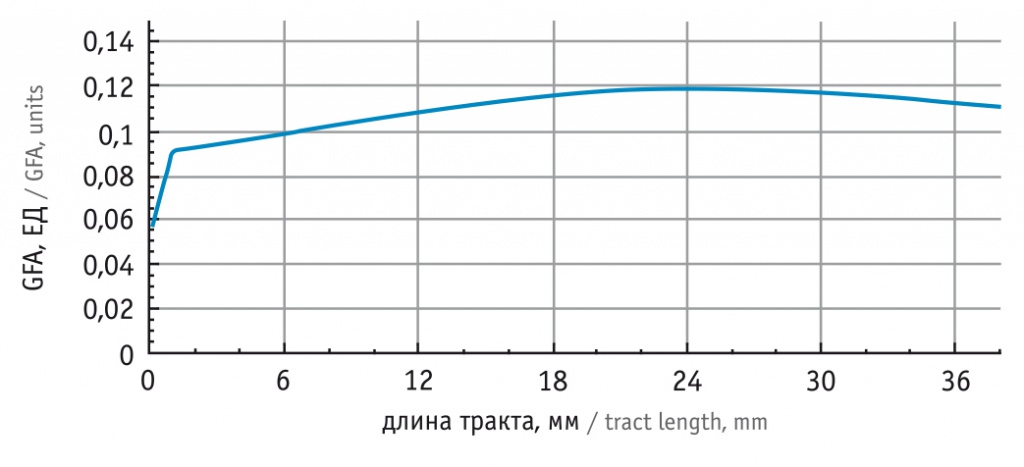
На рисунке 6 представлены соотношения длины трактов к коэффициенту GFA. Из рисунка 6 видно, что наибольшими показателями анизотропии обладали лишь короткие тракты с длиной не более 20 мм. По нашему мнению, состоятельность тракта определяется индексом GFA, а короткой длиной обладают либо молодые тракты, формирующиеся на основе текущей патологии, либо не сформировавшиеся в онтогенезе, что закладывает фундамент для расширения трактографических исследований в аспекте генетики и наследственности.
Рис. 6. График зависимости длины трактов амигдалярно-гиппокампального пучка от коэффициента общей фракционной анизотропии (GFA), p < 0,05
При СЗО, напротив, хвостатые ядра справа практически утрачивают свои связи (кроме связи с верхней орбитофронтальной корой), а доминировать по сравнению с нормой начинают левая скорлупа и таламусы (рис. 7), что является интересной особенностью микроструктурной организации ГМ при зависимости от опиоидов. Следует упомянуть, что все обследуемые были правшами.
Рис. 7. Разобщение корково-подкорковой микроструктурной организации головного мозга при наркомании (p < 0,05)
Самое наглядное визуальное сравнение проводится с помощью обработки полученных результатов по методике коннектометрии. На рисунке 8 продемонстрированы полные карты коннективности структур ГМ при групповом анализе для наркозависимых и при норме.
Рис. 8. Карты коннективности головного мозга при групповом анализе для наркозависимых (А) и в норме (Б), по данным трактографии (p < 0,05).
Примечание. При наркозависимости отмечается тотальное разобщение микроструктурных связей между медиальными лобными областями коры и подкорковыми структурами
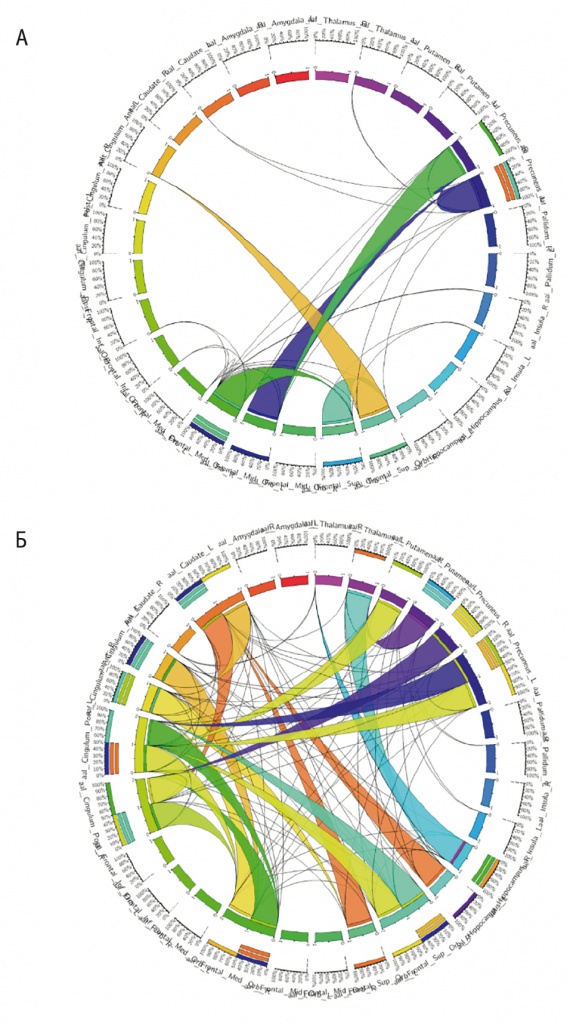
Как и в случае с функциональными результатами, наблюдается значительное обеднение коннектома при героиновой наркомании в виде практически тотального разобщения связей между медиальными лобными областями коры и подкорковыми структурами. Сохранность связности подкорковых структур с орбитофронтальной корой и предклиньем коррелирует с данными фМРТ. При этом следует отметить, что в группу обследованных наркозависимых входили пациенты как с длительными сроками ремиссии, так и находящиеся в активном употреблении.
Данные литературы[3, 6, 7] свидетельствуют о патологии поясной извилины при наркоманиях и алкоголизме. Стоит отметить, что последнее образование является составной частью эмоциональной системы мозга, одна из функций которой — обеспечение хранения, контроля и обработки данных архива эмоциональной памяти. При недостаточности контролирующей функции поясной извилины, по некоторым данным, и развивается патологическое возбуждение субкортикальных структур, провоцирующих поиск наркотика и зависимое поведение.
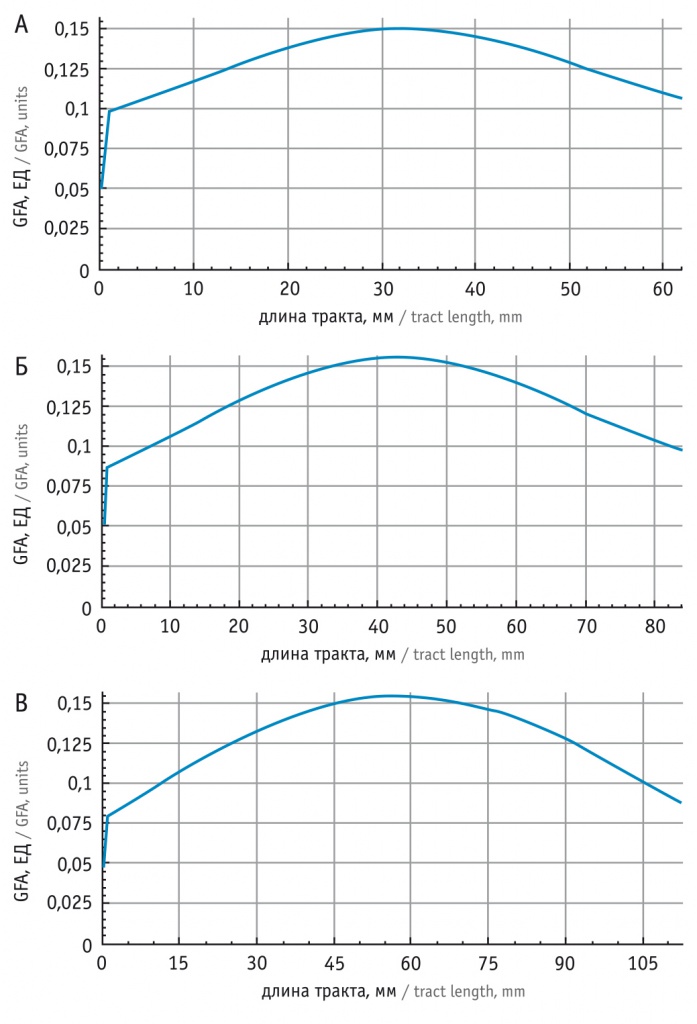
Для уточнения степени патологических изменений ободочной извилины оценивалось соотношение длины ее трактов и их характеристики по коэффициенту GFA. Как видно из графиков на рисунке 9, наибольшими длиной и показателем GFA обладали тракты поясной извилины ГМ пациентов из группы контроля. Так, наибольшие показатели (выше 0,15 ЕД) отмечались у трактов длиной от 55 до 65 мм. При алкоголизме аналогичные показатели GFA были только у трактов длиной от 35 до 45 мм, а при наркомании наблюдалось пропорциональное снижение GFA в трактах от 28 до 36 мм.
Рис. 9. Графики зависимости длины трактов в поясной извилине от коэффициента общей фракционной анизотропии (GFA) у наркозависимых (А), при алкоголизме (Б) и в норме (В) (при сравнении с нормой в обоих случаях p < 0,05)
Методика диффузионной магнитно-резонансной коннектометрии позволяет также выполнить межгрупповое сравнение состояния связности регионов интереса в общем у наркозависимых и в норме.
На рисунке 10 продемонстрированы тракты со значительным снижением коэффициента GFA, исходящие из мозолистого тела к поясной извилине и к структурам мозжечка.
Рис. 10. Снижение коэффициента общей фракционной анизотропии (GFA) в поясной извилине и мозжечке при наркомании (А) и его повышение при алкоголизме (Б), p < 0,05
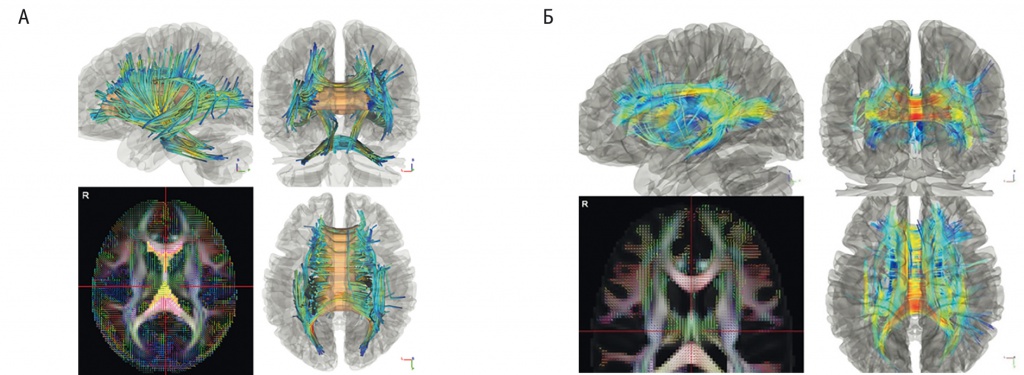
При аналогичном межгрупповом анализе пациентов с алкоголизмом и участников группы контроля выявлено уменьшение фракционной анизотропии в кортико-таламическом пучке справа и парадоксальное ее увеличение в мозолистом теле (FDR = 0,0763443), что говорит об особенностях микроструктурной организации между полушариями ГМ у больных с СЗА. Уменьшение коэффициента GFA в кортико-таламическом пучке, связывающем медиальную префронтальную кору с системой таламуса, свидетельствует о снижении контролирующего влияния коры на эмоциогенные структуры. Неоднозначным является повышение межполушарной коннективности при алкоголизме.
ОБСУЖДЕНИЕ
Результаты проведенного исследования подтверждают важность изучения микроструктурного состояния ГМ при различной психической патологии. Вместе с тем методика трактографии в психиатрической практике в настоящее время практически не используется. В основном она ограниченно применяется в нейрохирургии (в частности, лишь для визуальной оценки структур ГМ при планировании стереотаксических операций). При этом традиционно используются карты анизотропии, характеризующие степень патологических изменений белого вещества ГМ[8].
В нашем исследовании предпринята попытка провести анализ коннективности между структурами ГМ в норме и при патологии, основываясь на трактографических данных. При анализе МК удалось констатировать различные показатели коннективности между структурами ГМ обследуемых. У наркозависимых отмечалось разобщение нижних и средних отделов орбитофронтальной коры. Лишь верхний ее отдел оставался непосредственно связанным с подкорковыми структурами.
Полученные результаты сопоставимы с данными фМРТ[4, 9, 10], которые также свидетельствуют о разобщении корково-подкорковых структур у пациентов с синдромом зависимости от опиоидов. Вместе с тем в отличие от трактографии фМРТ показывала орбитофронтальную кору как единую статистически значимую область активности (исходя из атласа, заложенного в программу для обработки данных), тогда как трактография позволила определить специфические особенности связности конкретных отделов коры ГМ, задействованных в патогенезе зависимости от опиоидов.
Установлено, что коннективность коры и подкорковых структур у наркозависимых нарушена практически полностью, за исключением хвостатого ядра, таламуса и предклинья слева, что не совпадало с ранее полученными функциональными данными (фМРТ), где отмечалось снижение активности предклинья[11].
Достаточно информативными были трактографические данные и у пациентов с синдромом зависимости от алкоголя. В частности, наблюдалось отчетливое смещение коннективности в сторону подкорковых структур. При этом со стороны левого гиппокампа отмечено повышение связности с другими субкортикальными структурами (бледные шары, миндалина, хвостатые ядра и др.), образующими единый патологический конгломерат. Со стороны медиальной орбитофронтальной коры, напротив, связь утрачивалась.
В отличие от состояния у здоровых людей миндалина при данной патологии образовывала коннективность с обоими гиппокампами (появление «новой связности»), достигая своеобразного патологического объединения хранилища эмоциональной памяти и тревоги у больных алкоголизмом. Возможно, такое патологическое объединение в определенной степени может объяснять коморбидность алкоголизма с тревожными и депрессивными расстройствами, когда нередко алкоголь используется больным в качестве своеобразного анксиолитика[12], при этом алкогольная зависимость носит вторичный характер.
Согласно литературным данным, при недостаточности контролирующей функции поясной извилины развивается патологическое возбуждение подкорковых структур, во многом обусловливающее зависимое поведение[13]. Уменьшение GFA в кортико-таламическом пучке, вероятно, связано со снижением контролирующего влияния коры на эмоциогенные структуры.
При анализе сетевых характеристик нами найдены изменения по параметрам плотности, коэффициентам ассортативности и кластеризации, транзитивности, длине путей, локальной и глобальной эффективности (по сравнению с нормой), что свидетельствует о патологическом разобщении в нейросети и ее деградации у больных с СЗО. Значительное снижение этих показателей также говорит о дегенерации сети на микроструктурном уровне у наркозависимых (вероятно, под прямым токсическим воздействием наркотических препаратов или по механизмам нейропластичности).
У пациентов с СЗА сетевые характеристики по параметрам плотности, кластеризации, глобальной и локальной эффективности были значительно выше нормы, что остается пока недостаточно ясным и требует дальнейших исследований. Возможно, повышение этих показателей происходит за счет так называемого патологического конгломерата подкорковых структур ГМ.
ЗАКЛЮЧЕНИЕ
Выявленная с применением трактографии картина нарушения коннективности в белом веществе может служить определенным предиктором алкогольной и наркотической зависимости. Данный факт в перспективе возможно использовать и для прогноза риска возникновения аддиктивных расстройств.
Поступила: 06.02.2020
Принята к публикации: 03.03.2020








