ВВЕДЕНИЕ
Новая коронавирусная инфекция (COVID-19) — это острое респираторное заболевание с первичным поражением верхних и нижних дыхательных путей разной степени выраженности от бессимптомного носительства до клинически тяжелой формы вирусной пневмонии с развитием острой дыхательной недостаточности, острого респираторного дистресс-синдрома, а на поздней стадии — сепсиса и септического (инфекционного-токсического) шока[1, 2]. Учитывая тропность вируса к легочной ткани, он также поражает различные органы и системы организма человека, вызывает респираторные, сердечно-сосудистые, коагулопатические, почечные, гастроинтестинальные, печеночные, метаболические, двигательные, нейрокогнитивные, психические расстройства, приводя к развитию полиорганной недостаточности[3, 4].
В настоящее время Центр по контролю и профилактике заболеваний выделяет 5 штаммов коронавируса SARS-CoV-2[5].
Штамм альфа (линия PANGO B.1.1.7) был первоначально обнаружен в Великобритании в декабре 2020 г.[6]. Данный штамм обладает на 40–83% большей трансмиссивностью, чем штамм дикого типа B1, и приводит к более высокой вирусной нагрузке на носоглотку, вызывая более серьезные заболевания[5, 6]. Контагиозность штамма альфа в среднем выше на 60%, чем у штамма, первоначально выявленного в г. Ухань, уровень летальности выше на 59%. На сегодняшний день случаев данного варианта заболевания уже не отмечается[7, 8].
Штамм бета (линия PANGO В.1.351) был впервые обнаружен в Южно-Африканской Республике в мае 2020 г. и в то время стал преобладающим штаммом в регионе[9]. Предварительный анализ показал, что во второй волне COVID-19 был более высокий уровень смертности, хотя это могло быть связано с подавляющим воздействием на систему здравоохранения. C.A.B. Pearson и соавт. подтвердили, что штамм бета обладает повышенной трансмиссивностью и вирулентностью[10]. Исследования показали, что он чаще выявлялся у молодых и изначально здоровых людей[16].
Штамм гамма (линия PANGO B.1.1.248) был первоначально обнаружен у путешественников, прибывших из Бразилии в Японию 06.01.2021. Мутации штамма гамма позволяют избегать антител от предыдущих инфекций или от вакцинации, и, таким образом, многократно возрастает риск повторного инфицирования индивидуумов, которые ранее уже перенесли COVID-19. Данный вариант вируса приводит к летальному исходу в среднем на 50% чаще, чем «оригинальный» SARS-CoV-2[12].
Штамм дельта (линия PANGO В.1.617.2) впервые был обнаружен и выделен в Индии в октябре 2020 г. Эпидемиологические и геномные данные показали, что штамм дельта более трансмиссивен, чем исходный штамм, а также другие варианты[13, 14]. Передача вируса происходит в разных возрастных категориях. Инкубационный период сократился до 1–3 дней. Риск госпитализации — в 2 раза выше, чем у штамма альфа[15], при этом у госпитализированных пациентов, инфицированных штаммом дельта, отмечены осложненное течение заболевания и более высокий уровень госпитальной смертности[16]. По состоянию на декабрь 2021 г. на долю штамма дельта приходилось порядка 70% всех лабораторно подтвержденных случаев заболевания. Летальность штамма дельта достигала 82% по сравнению со штаммом альфа и 132% по сравнению с другими вариантами[17].
Штамм омикрон (линия PANGO B.1.1.529) впервые выявлен в ЮАР и Ботсване в ноябре 2021 г. На данный момент является наиболее сильно мутировавшим вариантом среди всех штаммов, что приводит к повышенной трансмиссивности и частичной устойчивости к иммунитету, индуцированному вакцинами против COVID-19. Однако случаев летального исхода от него пропорционально меньше, чем от других известных штаммов[18].
ПАТОФИЗИОЛОГИЧЕСКИЕ НАРУШЕНИЯ ДЫХАТЕЛЬНОЙ СИСТЕМЫ
Дыхание централизованно контролируется дыхательным центром в области продолговатого мозга и моста ствола мозга, которые контролируют «дыхательную активность», чтобы согласовать дыхание с метаболическими потребностями организма[19, 20]. Патофизиологические нарушения при COVID-19 могут объяснить несоответствие между тяжестью гипоксемии и относительно легким респираторным дискомфортом, о котором сообщают пациенты. Токсическое воздействие вируса на артериальные хеморецепторы ствола головного мозга, чувствительных к кислороду и являющихся сенсорами лактата, уровень которого может увеличиваться при патофизиологических состояниях, может приводить к такому явлению, как «немая гипоксия» или «счастливая гипоксия»[21]. Она развивается преимущественно в острый период заболевания, когда у многих пациентов в покое наблюдается заметный разрыв между глубокой гипоксемией без пропорциональных признаков дыхательной недостаточности и быстрым ухудшением состояния, следовательно, снижение сатурации не ощущается пациентом и не приводит к развитию вентиляционного ответа[22].
G. Lippi и соавт. установили, что при прогрессировании COVID-19 до тяжелой гипоксемии (SpO2 < 88%) до 30% пациентов нуждаются в той или иной формах респираторной поддержки, из них у 16–42% развивается острый респираторный дистресс-синдром[23 24]. Процент таких пациентов при хронической обструктивной болезни легких (ХОБЛ) возрастает в 5,97 раза[25]. ХОБЛ входит в число сопутствующих состояний, ассоциированных с высокой летальностью при COVID-19[26].
К настоящему времени предоставлено достаточно сведений о диагностике, клиническом течении заболевания и лечении, однако до сих пор идет накопление базы данных и профессиональной информации о проведении реабилитационных мероприятий пациентам с COVID-19 в рамках национальной трехэтапной системы медицинской реабилитации[27].
Первые рандомизированные исследования проведены в Китае и Италии. Остальные рекомендации различных стран в основном носят временный характер, т.к. основаны на мнении экспертных сообществ. Они постулируют, что медицинская реабилитация должна быть персонализированной, как и при других соматических патологиях, и организована в виде 3 этапов[28].
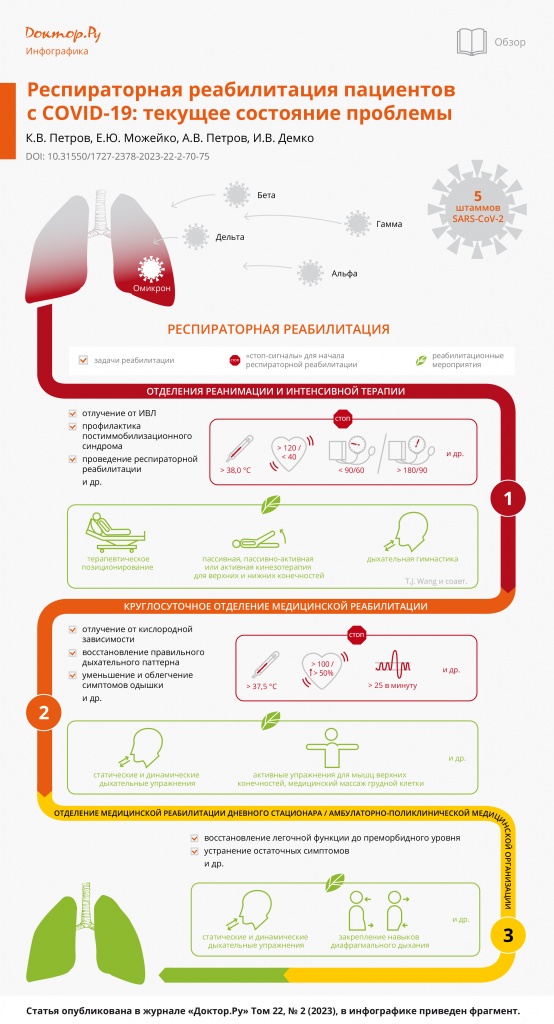
РЕСПИРАТОРНАЯ РЕАБИЛИТАЦИЯ
Определение респираторной реабилитации, адаптированное Американским торакальным обществом и Европейским респираторным обществом, представляет собой комплексное вмешательство, основанное на тщательном обследовании пациента, за которым следует индивидуально подобранная терапия, включающая, помимо прочего, физические упражнения, обучение и изменение поведения для улучшения физического состояния людей с респираторными заболеваниями[29].
Медицинская реабилитация на 1-м этапе
Медицинскую реабилитацию, в том числе респираторную, у пациентов с COVID-19 рекомендуется начинать в условиях отделений реанимации и интенсивной терапии (ОРИТ) при стабилизации витальных функций пациента[30–33].
Задачами медицинской реабилитации на 1-м этапе в условиях ОРИТ у пациентов с COVID-19 будет отлучение от ИВЛ, профилактика постиммобилизационного синдрома, проведение респираторной реабилитации, вертикализация пациента, повышение толерантности к физической нагрузке, нутритивная поддержка, восстановление эмоционального фона, улучшение повседневной активности пациента.
T.J. Wang и соавт. советуют подходить к респираторной реабилитации и активизации пациента в условиях ОРИТ с большой осторожностью, учитывая тяжесть основного состояния и нестабильность гемодинамических и вентиляционных показателей[34]. Исходя из этого методы реабилитации должны опираться на принципы 4S (Simple, Safe, Satisfy, Save) — простой, безопасный, успешный, спасающий жизнь[35].
Определены «стоп-сигналы» для начала респираторной реабилитации: температура тела > 38,0°C; срок от постановки первичного диагноза или появления первых симптомов ≤ 3 дней; первоначальное появление одышки ≤ 3 дней; прогрессирование клинической картины поражения легочной ткани по данным компьютерной томографии грудной клетки в течение 24–48 ч > 50%; SpO2 ≤ 90%; артериальное давление < 90/60 мм рт. ст. или > 180/90 мм рт. ст.; ЧДД > 40 раз/мин; ЧСС < 40 уд/мин или > 120 уд/мин; нарушение сердечного ритма или появление ишемических изменений миокарда или их нарастание по данным ЭКГ; изменение уровня сознания[35].
T.J. Wang и соавт. предложили программу реабилитационных мероприятий на 1-м этапе[34]:
1. Терапевтическое позиционирование для профилактики иммобилизационного синдрома, улучшения вентиляции легких (пассивное полувертикальное положение за счет подъема головного конца на 30 градусов, положение лежа на правом и левом боку, прон-позиция или полупрон-позиция, промежуточное между положением на боку и лежа на животе). Рекомендуется менять положение тела пациента каждые 2 ч для предупреждения развития пролежней и ателектазов в легких, использовать подушки и одеяла для поддержания позы и минимизации активной работы мышц пациента[36].
2. Пассивная, пассивно-активная или активная кинезотерапия для верхних и нижних конечностей в объеме физиологических движений в суставе с растягиванием мышц. При отсутствии противопоказаний выполнять каждые 3 ч (не менее 6 раз) по 5–7 движений в каждом суставе в медленном темпе продолжительностью 20 мин.
3. Дыхательная гимнастика (тренировка основных, вспомогательных и дополнительных мышц вдоха) 5–6 раз в сутки по 5–7 подходов при постоянном мониторинге сатурации крови кислородом и оценке одышки при физической нагрузке по шкале Борга для контактных пациентов. Шкала одышки Борга является простым и доступным инструментом для субъективной оценки пациентом самочувствия, переносимости физической нагрузки и интенсивности одышки[37].
A.P. Gautam и соавт. предложили алгоритм комплексной респираторной реабилитации[38]. Целью реабилитации у самых тяжелых пациентов, находящихся на ИВЛ, с несоответствием альвеолярной оксигенации/вентиляции от умеренной до тяжелой степени было улучшение оксигенации и предотвращение десатурации, возможное снижение летальности и отлучение от ИВЛ. Для таких пациентов предложено использование прон-позиции (положение лежа на животе) не менее 16 ч в сутки, метод постурального дренажа при осложнении полисегментарной пневмонией с последующей аспирацией мокроты; использование респираторной терапии и параметров респираторной поддержки аппарата ИВЛ согласно методическим рекомендациям анестезиологов и реаниматологов; проведение адекватной нутритивной поддержки с повышенной суточной дозировкой белка, цинка и других витаминов (энтеральный или парентеральный путь введения). Важной для данной группы пациентов является профилактика постиммобилизационного синдрома методом выполнения пассивных или активно-пассивных упражнений при постоянном мониторинге витальных функций, гемодинамики и сатурации крови кислородом[38].
Раннее начало реабилитационных мероприятий в условиях ОРИТ может улучшить клиническую картину течения заболевания, сократить сроки пребывания в отделении интенсивной терапии и ускорить выздоровление пациента. Реабилитационные вмешательства могут вселить в людей надежду и уверенность, что играет немаловажную роль на последующем этапе реабилитации, однако необходим индивидуальный подход и использование общепризнанных стандартов и клинических рекомендаций в условиях пандемии COVID-19.
Медицинская реабилитация на 2-м этапе
Медицинская реабилитация на 2-м этапе в условиях круглосуточного отделения медицинской реабилитации должна проводиться после стабилизации клинического состояния пациента и показателей гемодинамики, отлучения от ИВЛ, получения 2 отрицательных анализов на COVID-19 и перевода из «красной зоны»[40].
Противопоказания для проведения реабилитационных мероприятий пациентам с COVID-19 на 2-м этапе медицинской реабилитации: температура тела > 37,5°C; SpO2 ≤ 90% или десатурация на 4% от исходного уровня по данным пульсоксиметрии без кислородной поддержки, потребность в кислородной поддержке; ЧДД > 25 в минуту; cистолическое АД < 90 и > 180 мм рт. ст.; диастолическое АД > 110; или снижение от исходного систолического АД на ≥ 20 мм рт. ст., диастолического АД — на ≥ 10 мм рт. ст., среднего АД — на ≥ 15 мм рт. ст.; ЧСС > 100 уд/мин или повышение ЧСС > 50% от исходной величины или снижение ЧСС при нагрузке; нарушение сердечного ритма или появление ишемических изменений миокарда или их нарастание по данным ЭКГ; появление внешних признаков плохой переносимости нагрузки[33, 41].
Начальная интенсивность упражнений должна быть оценена при первичном осмотре и выполнении функциональных проб.
Задачами медицинской реабилитации на 2-м этапе являются отлучение пациента от кислородной зависимости, восстановление правильного дыхательного паттерна, уменьшение и облегчение симптомов одышки, улучшение вентиляции и эластичности легочной ткани, улучшение бронхиального клиренса, повышение толерантности к физической нагрузке, повышение качества жизни и скорейшее возвращение в общество[2].
Респираторная реабилитация включает статические и динамические дыхательные упражнения в различных исходных положениях (лежа, сидя, стоя) в зависимости от тяжести основного состояния пациента, насыщенности крови кислородом и переносимости физических нагрузок. Пациента обучают правильному дыхательному паттерну, правильной технике диафрагмального дыхания в положении лежа, сидя, стоя, самостоятельному восстановлению сатурации при ее снижении. Рекомендуются активные упражнения для мышц верхних конечностей, медицинский массаж грудной клетки, направленный на снижение тонуса дыхательной и вспомогательной мускулатуры для улучшения вдоха/выдоха, использование методов постурального и аутогенного дренажей (по показаниям)[38, 42], адекватная нутритивная поддержка с повышенной суточной дозировкой белка[43].
Физическая реабилитация: выполнение посуставной разминки и упражнений, активно-пассивная гимнастика — упражнения низкой интенсивности на мелкие и средние группы мышц, а также большие группы мышц при адекватной переносимости физической нагрузки (возможно, с легкими гантелями и/или эластической лентой) при постоянном мониторинге гемодинамики и сатурации крови кислородом. Циклические занятия на велотренажере и тредмиле низкой интенсивности. Дозированная ходьба в пределах палаты с дальнейшим расширением двигательного режима[40].
Психологические подходы в реабилитации в первую очередь касаются уменьшения уровня тревоги и депрессии, формирования позитивной мотивации на выздоровление и повышение вовлеченности в реабилитационный процесс[41].
Медицинская реабилитация на 3-м этапе
Остаточные явления после COVID-19 именуются постковидным синдромом. Утомляемость и одышка при выполнении рутинной бытовой и физической нагрузки часто возникают примерно через 30 дней после выписки из больницы и сопровождаются снижением качества жизни у 40% пациентов с COVID-19[44]. Поэтому пациентам, прошедшим 2-й этап стационарной медицинской реабилитации, рекомендуется продолжить дальнейшее реабилитационное долечивание (3-й этап) в условиях отделения медицинской реабилитации дневного стационара или амбулаторно-поликлинической медицинской организации[45], т.к. длительность заболевания и выраженное снижение функций всего организма значительно ограничивают повседневную активность и участие пациента в общественной жизни. Пациенты могут проходить реабилитацию на 3-м этапе при помощи телемедицины[46].
Задачи реабилитации на 3-м этапе: повышение толерантности к физической нагрузке и восстановление легочной функции до преморбидного уровня, устранение остаточных симптомов, восстановление мышечной силы, профилактика заболеваний сердечно-сосудистой системы, улучшение повседневной активности. Для решения данных задач предлагаются статические и динамические дыхательные упражнения в различных исходных положениях, закрепление навыков диафрагмального дыхания, применение восточных дыхательных техник полного дыхания (тай-чи, цигун, хатха-йога, бадуань цзинь), силовые упражнения (с сопротивлением «губы трубочкой» и др.)[47].
Для восстановления общей физической активности советуют выполнять активно-пассивную гимнастику — упражнения низкой и умеренной интенсивности на мелкие, средние и большие группы мышц, циклические занятия на велотренажере и тредмиле низкой интенсивности с увеличением нагрузки до умеренной, упражнения с отягощением (легкие гантели, эластические ленты) для мышц верхнего плечевого пояса, мышц спины, мышц нижних конечностей, дозированная ходьба на беговой дорожке, и в заключительной части упражнения на расслабление мышц. Кислородная поддержка, постоянный мониторинг гемодинамики и сатурации крови кислородом таким пациентам, как правило, не требуются[47].
ЭФФЕКТИВНОСТЬ РЕСПИРАТОРНОЙ РЕАБИЛИТАЦИИ
Учитывая, что у большинства пациентов с COVID-19, проходивших стационарное лечение, имеется поражение органов дыхания, встает вопрос, является ли респираторная реабилитация эффективным мероприятием у этих пациентов для улучшения исходов и снижения смертности.
K. Liu и соавт. изучили влияние 6-недельной респираторной реабилитации на дыхательную функцию, ежедневную активность и качество жизни у пациентов, перенесших COVID-19 в возрасте 65 лет и старше[48]. Тренинг включал 2 процедуры в неделю, 1 раз в день длительностью 10 мин. Программа состояла из тренировки дыхательных мышц с сопротивлением, упражнений активной эвакуации трахеобронхиального секрета (активные покашливания), диафрагмального дыхания с отягощением (груз весом 1–3 кг, помещенный на переднюю брюшную стенку), на растяжку мышц, участвующих в акте дыхания, под контролем специалиста и упражнений для самостоятельного выполнения в домашних условиях[48].
Данная программа показала улучшение дыхательной функции по данным спирометрии: объем форсированного выдоха за 1 с (ОФВ1) увеличился с 1,10 ± 0,08 до 1,44 ± 0,25 л, форсированная жизненная ёмкость лёгких (ФЖЕЛ) — с 1,79 ± 0,53 до 2,36 ± 0,49 л, ОФВ1/ФЖЕЛ — с 60,48 ± 6,39 до 68,19 ± 6,05%. Повысились ежедневная активность и толерантность к физической нагрузке по тесту 6-минутной ходьбы с 162,7 ± 72,0 м при поступлении до 212,3 ± 82,5 м перед выпиской. Уровень тревоги снизился как внутри группы исследуемых с 56,3 ± 8,1 до 47,4 ± 6,3 балла, так и в группе контроля — с 55,8 ± 7,4 до 54,9 ± 7,3 балла. Однако уровень депрессии не был статистически значимым внутри и между группами: 56,4 ± 7,9 балла при поступлении, 54,5 ± 5,9 — перед выпиской. Резюмируя проведенное исследование, авторы доказали значительное улучшение функции дыхания, активности и качества жизни у пожилых пациентов, прошедших 6-недельный курс респираторной реабилитации[48].
Для пациентов, прошедших стационарную и амбулаторную реабилитацию, которым была рекомендована самостоятельная работа на дому, существует компьютерная и телекоммуникационная технологии для обмена медицинской информацией[49]. Рекомендуется разработка индивидуальной реабилитационной программы, направленной на восстановление показателей дыхательной системы и толерантности к физической нагрузке в домашних условиях. Интенсивность аэробной нагрузки, упражнения и количество их повторов должны быть назначены с учетом состояния пациента и его физических возможностей. Пациенты должны быть обучены правильному паттерну дыхания, контролю эффективности и безопасности физических нагрузок в домашних условиях, знать «стоп-сигналы»[50]. Телемониторинг за основными жизненно важными показателями пациента (АД, ЧСС, ЧДД, SpO2) происходит до, во время и после занятия с использованием индивидуальных приборов регистрации. Дистанционное обучение подразумевает предоставление наглядного печатного, видеоматериала и также рекомендаций по индивидуальной программе реабилитации с возможностью своевременной ее корректировки[44].
ЗАКЛЮЧЕНИЕ
Респираторную реабилитацию следует проводить на протяжении всего процесса лечения COVID-19 независимо от того, находится пациент в стационаре или дома. Кроме того, реабилитационные мероприятия должны подразумевать персонализированный подход к каждому пациенту в зависимости от его соматического состояния. Пациенты, проходившие респираторную реабилитацию, оценили безопасность и эффективность данного метода как основополагающего после перенесенного COVID-19, он вселил надежду и уверенность в выздоровлении.
Будущие исследования должны помочь лучше понять траекторию развития легочной реабилитации после COVID-19 с целью повышения качества жизни пациентов, скорейшего восстановления их активности и участия в общественной жизни.
Поступила: 14.10.2022
Принята к публикации: 13.01.2023