С начала 1990х гг. в большинстве экономически развитых стран мира отмечается значительный рост заболеваемости микобактериозами, чему способствует и улучшение методов диагностики [4]. В своей клинической практике мы преимущественно сталкиваемся с микобактериозом легких.
Данные о заболеваемости микобактериозами и их распространенности в разных странах мира широко варьируют. Так, в США распространенность НТМБ составляет 1,8 случая на 100 тыс. населения, в Великобритании — 2,9 на 100 тыс., в Дании — 1,5 на 100 тыс., на Тайване — от 2,7 до 10,2 на 100 тыс.
В Российской Федерации официальный учет заболеваний, вызванных НТМБ, не ведется, отсутствуют нормативные документы и методические рекомендации, отражающие нормы современной лабораторной диагностики, не разработаны алгоритмы тактики и длительности лечения больных [5].
Наиболее часто микобактериоз можно наблюдать у лиц с иммунодефицитными состояниями (больные с ВИЧинфекцией, пациенты после трансплантации, химиотерапии и пр.). У пациентов с хроническими заболеваниями легких (ХОБЛ, бронхоэктатической болезнью, муковисцидозом, туберкулезом и др.) также высок риск развития микобактериоза. По некоторым данным, риск поражения НТМБ органов дыхания увеличивался в 16,5 раз у пациентов с любым типом хронических заболеваний дыхательных путей [6].
Наиболее частыми возбудителями микобактериоза легких становятся Mycobacterium avium complex, Mycobacterium kansasii, Mycobacterium xenopi, Mycobacterium fortuitum, Mycobacterium abscessus.
Клинические проявления микобактериоза легких неспецифичны и зависят от тяжести фонового заболевания и степени иммунодефицитного состояния. Пациенты жалуются на слабость, повышение температуры тела до субфебрильных цифр, малопродуктивный кашель. Достаточно часто НТМБинфекция может протекать бессимптомно и встречаться у пациентов без сопутствующих хронических заболеваний.
В соответствии с рекомендациями Американского общества инфекционных болезней и Американского торакального общества, критериями диагностики микобактериоза легких являются как минимум двукратное обнаружение НТМБ в различных биологических средах (мокроте, жидкости бронхоальвеолярного лаважа) в сочетании с соответствующими рентгенологическими изменениями в легких. При этом необходимо исключить туберкулез легких. Схожесть НТМБ с Mycobacterium tuberculosis, ограниченное применение современных молекулярногенетических методов диагностики, сходные рентгенологические изменения часто приводят к ошибочному диагнозу туберкулеза и длительному пребыванию пациентов в туберкулезных клиниках.
В то же время остаточные изменения туберкулеза легких могут приводить к значительной структурной перестройке легких и способствовать тем самым развитию микобактериоза, особенно у пожилых пациентов.
Лечение микобактериоза сопряжено с длительным приемом антибактериальных препаратов, который может вызывать тяжелые нежелательные явления (лейкемоидную реакцию, токсические гепатиты и пр.). Они серьезно ухудшают состояние больного, особенно пожилого пациента с сопутствующими заболеваниями, что требует отмены лечения. После отмены антибактериальной терапии не всегда происходит прогрессирование микобактериоза, однако в таких случаях требуются дополнительные клинические исследования.
Клинический случай. 86летний мужчина, житель г. Москвы, был госпитализирован в отделение дифференциальной диагностики туберкулеза легких ФГБНУ ЦНИИТ 5 ноября 2015 г. с жалобами на постоянный кашель с отделением большого количества слизистой мокроты, одышку при незначительной нагрузке, быструю утомляемость, плохой аппетит.
История заболевания. Туберкулез легких был выявлен у пациента в 1955 г. В результате длительного лечения было достигнуто клиническое излечение туберкулеза, после чего пациент наблюдался в противотуберкулезном диспансере до 1962 г., когда он был снят с учета. В последующем длительное время чувствовал себя удовлетворительно.
13.03.2013 г. с подозрением на рецидив туберкулеза был госпитализирован в противотуберкулезную клинику, где при обследовании в мокроте микроскопическим методом были выявлены кислотоустойчивые микобактерии (КУМ). Поставлен диагноз инфильтративного туберкулеза нижней доли правого легкого в фазе распада МБТ(+), и в течение 5 месяцев проводилась противотуберкулезная терапия по индивидуальной схеме (данные в медицинской документации не представлены) с удовлетворительной переносимостью (данные о чувствительности возбудителя отсутствуют). Была достигнута положительная клиническая и рентгенологическая динамика.
01.08.2014 г. пациент был переведен в урологическое отделение с острой задержкой мочеиспускания. В результате проведенного обследования выявлен рак предстательной железы, проведена экстренная аденэктомия.
В это же время при бронхологическом исследовании в промывных водах бронхов впервые обнаружили M. avium. Одновременно в мокроте был получен рост МБТ. Был установлен диагноз: Инфильтративный туберкулез верхней доли правого легкого, МБТ(+); микобактериоз легких, вызванный М. avium. Пациент был госпитализирован в туберкулезную клиническую больницу.
В течение 6 месяцев больной получал противотуберкулезную терапию, в результате которой была достигнута положительная клиническая и рентгенологическая динамика. В мокроте продолжала определяться М. avium, рост МБТ отсутствовал. С 13.10.2015 по 04.11.2015 г. пациент находился на лечении в туберкулезной клинической больнице с диагнозом: Диссеминированный туберкулез легких в фазе инфильтрации и распада, МБТ(+), микобактериоз легких, вызванный М. avium. К противотуберкулезной терапии был добавлен кларитромицин.
Стаж курения — 40 пачка/лет, последние 15 лет не курит. Диагноз ХОБЛ был установлен в 2014 г. С тех пор пациент постоянно получал ингаляции тиотропия бромидом. В 2013 г.диагностировали ИБС, атеросклеротический кардиосклероз, гипертоническую болезнь 2 стадии, высокого риска. Постоянно принимал ингаляции тиотропия бромидом и эпизодически спрей нитроглицерина.
При поступлении состояние средней тяжести. Кахексия, ИМТ — 18 кг/м2. Кожные покровы бледные с пепельным оттенком, акроцианоз. Дыхание через нос свободное. ЧДД — 22 в мин. Перкуторный звук с коробочным оттенком. Аускультативно дыхание жесткое, по всем полям выслушиваются сухие свистящие хрипы. Сатурация кислорода в крови в покое — 78%. Тоны сердца приглушены, ритм правильный. ЧСС — 110 в мин, АД — 150/90 мм рт. ст. Живот при пальпации мягкий, безболезненный. Нижний край печени у края реберной дуги. Симптом поколачивания по поясничной области безболезненный. Очаговой неврологической симптоматики нет.
Результаты обследования. Клинический анализ крови: гемоглобин — 113 г/л, эритроциты — 4,3 × 1012/л, тромбоциты — 301 × 109/л, лейкоциты — 15,2 × 109/л, нейтрофилы палочкоядерные — 9%, сегментоядерные — 72%, моноциты — 9%, лимфоциты — 10%, СОЭ — 75 мм/ч.
Биохимический анализ крови: общий белок — 78 г/л, общий билирубин — 7 мкмоль/л, АЛТ — 27 Е/л, АСТ — 32 Е/л, глюкоза — 3,8 ммоль/л.
Внутрикожная проба с Диаскинтестом отрицательная.
IgGантитела к МБТ — 2710 мкг/мл (резко повышенный уровень).
Анализ мокроты: мокрота слизистая, вязкая, серого цвета, значительные скопления нейтрофилов в слизи, многие в стадии деструкции, единичные макрофаги и спирали Куршмана. Обнаружены единичные КУМ.
Методом люминесцентной микроскопии мокроты шестикратно обнаружены КУМ. Методом посева многократно получен рост M. avium, чувствительных к рифабутину, кларитромицину и моксифлоксацину. ДНК МБТ методом ПЦР многократно не обнаружена.
Посев мокроты на неспецифическую микрофлору выявил сливной рост Proteus mirabilis, чувствительного только к комбинации имипенема и циластатина.
Общий анализ мочи: цвет соломенножелтый, относительная плотность — 1025, прозрачность неполная, белка и глюкозы нет. Микроскопия осадка: лейкоциты — до 500 в поле зрения, эритроциты — до 10 в поле зрения.
КТ органов грудной клетки от 01.11.2015 г.: распространенная центрилобулярная и панацинарная эмфизема. Бронхи деформированы, стенки их утолщены. Множественные варикозные и цилиндрические бронхоэктазы, некоторые из них заполнены секретом (рис. 1, 2). В обоих легких на всем протяжении определяются плотные очаги, часть в виде конгломератов, некоторые с плотными включениями (рис. 3). В верхних отделах с обеих сторон субплеврально — буллы размерами до 0,9–1,2 см. В бифуркационных и бронхопульмональных лимфатических узлах визуализируются кальцинаты. Жидкости в плевральных полостях нет. Аорта не расширена, стенки кальцинированы.
Рис. 1. Микобактериоз легких. Центрилобулярная и панацинарная эмфизема легких. Распространенные бронхоэктазы, некоторые из которых заполнены секретом. Здесь и далее в статье фото авторов
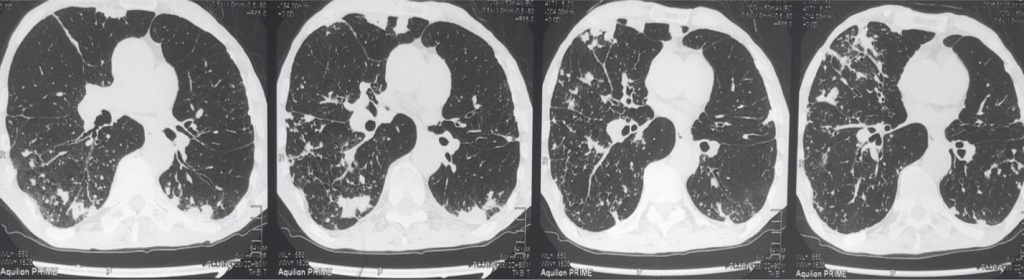
Рис. 2. Микобактериоз легких. Очаговые изменения в верхней доле левого легкого

Рис. 3. Микобактериоз легких. Буллезные изменения в верхних отделах легких. Очаговые изменения, часть из которых имеет сливной характер, в обоих легких
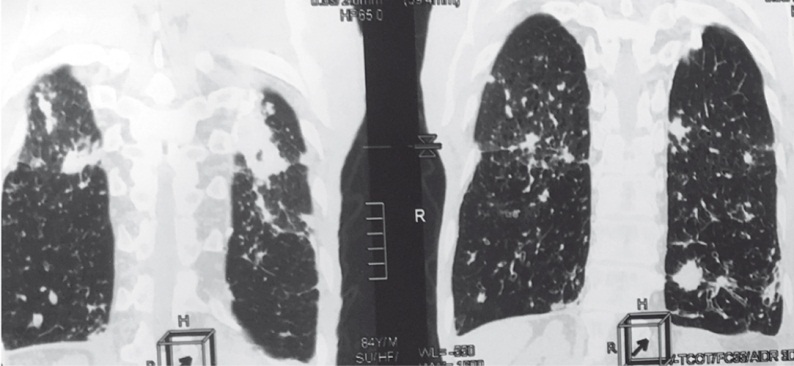
При исследовании ФВД определяется снижение вентиляционной способности легких по смешанному типу: жизненная емкость легких (ЖЕЛ) — 2,23 л (58,8%), ОФВ1 — 49,6%, индекс Тиффно — 82,9%. Бодиплетизмография: изменение структуры общей емкости легких (ОЕЛ) по обструктивному типу, гиперинфляция легких, умеренное увеличение ОЕЛ, значительное — остаточного объема легких и внутригрудного объема газа, снижение ЖЕЛ за счет снижения емкости вдоха.
Газы крови: парциальное напряжение кислорода в крови — 46 мм рт. ст., парциальное напряжение углекислоты — 40 мм рт. ст.
ЭКГ: ритм синусовый, ЧСС — 100 в мин. Отклонение электрической оси сердца влево. Блокада передней левой и неполная блокада правой ножки пучка Гиса. Гипертрофия обоих желудочков. Умеренные изменения миокарда высоких отделов боковой стенки ЛЖ.
ЭхоКГ: правые отделы сердца расширены (правый желудочек в парастернальной позиции — 3,6 см, в апикальной позиции — 4,2 см, правое предсердие в апикальной позиции — 4,4 см). Гипертрофия правого желудочка (толщина передней стенки — 0,8 см). Глобальная сократимость миокарда ЛЖ удовлетворительная. Аорта не расширена, стенки уплотнены. Створки аортального и митрального клапана уплотнены. Аортальная регургитация 2 степени, трикуспидальная регургитация 3 степени. Среднее систолическое давление в легочной артерии умеренно повышено — 28,5 мм рт. ст. Жидкости в полости перикарда нет.
В клинике установлен диагноз: Микобактериоз легких, вызванный М. avium. Остаточные изменения туберкулеза легких. ХОБЛ «D», обострение. Гипоксемическая дыхательная недостаточность 2 степени. Хроническое легочное сердце, декомпенсированное. ИБС. Атеросклеротический кардиосклероз. Стенокардия напряжения II функционального класса. Гипертоническая болезнь 2 стадии, АГ 2 степени, очень высокого риска. Недостаточность кровоснабжения 2Бстадии. Состояние после аденомэктомии по поводу рака предстательной железы 2014 г.
Было начато лечение: антибактериальная терапия с учетом лекарственной чувствительности М. avium: внутривенные инфузии комбинации имипенема и циластатина, моксифлоксацин 400 мг/день, кларитромицин 500 мг/день, рифабутин 150 мг/день, оксигенотерапия, ингаляции тиотропия бромидом.
На следующий день после начала приема рифабутина и моксифлоксацина пациент отметил усиление частоты и интенсивности болей в области сердца. На ЭКГ была зафиксирована полная атриовентрикулярная блокада. Антибактериальная терапия отменена, назначены инфузии калия и магния аспарагинатов, изосорбида мононитрат, клопидогрел, торасемид.
Через 2 недели на ЭКГ было отмечено улучшение состояния миокарда, отсутствие признаков атриовентрикулярной блокады. Повторная попытка возобновления терапии рифабутином и моксифлоксацином вновь привела к возникновению атриовентрикулярной блокады, в связи с чем антибактериальная терапия была отменена.
В период лечения в клинике у пациента возникли явления острого простатита, острого цистита, хронической задержки мочи, которые потребовали перевода его в урологическую клинику.
Таким образом, проведенная в клинике терапия позволила достигнуть ремиссии ХОБЛ. Попытки лечения микобактериоза приводили к развитию выраженных кардиотоксических побочных эффектов, в связи с чем антибактериальная терапия была вынужденно прекращена.
Заключение
Представленный случай демонстрирует сложность диагностики и лечения пожилого пациента с сочетанием туберкулеза, нетуберкулезного микобактериоза легких и ряда сопутствующих заболеваний. Антибактериальная терапия по поводу стойкого сохранения активности микобактериоза с упорным выделением нетуберкулезных микобактерий после клинического излечения туберкулеза была отменена в связи с возникновением жизнеугрожающих нежелательных эффектов.







