Папилломавирусная инфекция (ПВИ) широко распространена среди различных слоев населения. Инфицированность ВПЧ лиц молодого и среднего возраста составляет 20–60%[1, 8, 12]. В 50% случаев ВПЧ выводится из организма (спонтанная регрессия) в период от 1 года до 4 лет. Инфекция передается преимущественно половым путем при медицинских манипуляциях, вертикальным путем во время беременности, а также при прохождении новорожденного через инфицированные родовые пути матери[12, 15]. Инкубационный период — от 1 до 6 месяцев, максимальное содержание вируса в пораженных тканях обнаруживается на шестой месяц. Нередко результатом инфекции являются заболевания аногенитальной области: рак шейки матки (РШМ), рак вульвы, влагалища, перианальной области и генитальные кондиломы[8, 15, 16]. Считается, что 20% злокачественных опухолей у женщин и 10% у мужчин обусловлены ВПЧ. РШМ — второе по частоте злокачественное заболевание женщин: ежегодно в мире регистрируется более 500 тысяч случаев РШМ и более 300 тысяч больных женщин умирают[12, 16, 20]. ВПЧ — единственная группа вирусов, в отношении которых доказано, что они индуцируют образование опухолей у человека в естественных условиях.
Клональная экспансия инфицированных ВПЧ клеток базального слоя, прошедших первичную стадию дифференцировки, связана с их трансформацией и последующей иммортализацией, которые контролируются генами ВПЧ, кодирующими ранние (Е — early) белки Е6 и Е7 — онкопротеины[1, 12, 15]. Патогенетической основой вирусиндуцированного онкогенеза являются интеграция вирусной ДНК в хромосому инфицированных клеток с активным синтезом онкобелка Е7 и способность трансформированных клеток метаболизировать эстрадиол с образованием 16α-гидроксистерона — агрессивного метаболита, который активирует экспрессию гена Е7 (и способствует высокому устойчивому синтезу вирусного онкобелка Е7). Указанный метаболит обеспечивает пролиферативную активность формирующегося опухолевого клона за счет генетической нестабильности (мутаций (делеций) и эпигенетических модификаций), а также подавление системы иммунологического надзора (общего и местного иммунного статуса организма)[1]. Так, у женщин с цервикальной интраэпителиальной неоплазией (cervical intraepithelial neoplasia — CIN) I–II доказаны дисбаланс цитокиновой регуляции локального иммунного ответа со статистически значимым преобладанием противовоспалительных цитокинов (ИЛ-4, ИЛ-10) и резким снижением концентраций провоспалительных цитокинов (ИЛ-2, ИЛ-6, ФНО-α, а ИФН-γ — в 6,3 раза), а также другие нарушения иммунитета[18]. Все они являются важными факторами, поддерживающими персистенцию ВПЧ в эпителии шейки матки и способствующими развитию и прогрессированию CIN[17]. Высокая распространенность ПВИ и возможность ее исхода в рак указывают на важное медико-социальное значение этой инфекции для современного здравоохранения.
Цель исследования: оценка эффективности инозина пранобекс (Изопринозина) в комплексной терапии ПВИ.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено проспективное рандомизированное открытое несравнительное исследование. Под наблюдением в 2010–2012 гг. в поликлиниках НИИ экспериментальной медицины им. Пастера и Первого Санкт-Петербургского государственного медицинского университета им. акад. И. П. Павлова находились 90 женщин с аногенитальной ПВИ в возрасте от 19 до 50 лет (средний возраст составил 29,3 ± 2,1 года). Из них 50 пациенток (первая группа) получали инозин пранобекс (Изопринозин), 40 женщинам (вторая группа) проводился лишь вирусологический мониторинг в течение года.
ПВИ диагностировали на основании данных анамнеза, характерных клинических проявлений заболевания, результатов цитологического исследования мазков и иммунологического исследования крови, а также ПЦР с качественным
и количественным определением ВПЧ.
Критерии исключения:
- любая противовирусная терапия в течение 6 месяцев до начала исследования;
- серьезные сопутствующие заболевания;
- беременность и кормление грудью;
- интеллектуальные или другие нарушения, влияющие на способность осознанно дать согласие на исследование или адекватно следовать диагностическим и лечебным рекомендациям;
- аллергические реакции на любой ингредиент применяемых лекарственных препаратов;
- злокачественные новообразования в анамнезе.
У пациенток были исключены протозойные, бактериальные и вирусные заболевания урогенитального тракта помимо ПВИ.
Соскобы с измененных участков слизистых оболочек (отделяемого из уретры, цервикального канала и шейки матки) и из полости рта производили при помощи универсального пробозаборника («ИнтерЛабСервис», Швеция) и помещали в специальную транспортную среду. Выявление и количественное определение ДНК ВПЧ высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59-го типов) в клиническом материале осуществляли методом ПЦР с детекцией в режиме реального времени с использованием набора реагентов производства ООО «ИнтерЛабСервис» (Москва). Флуоресцентную детекцию продуктов амплификации делали на термоциклере Rotor-Gene 6000 (Corbett Research Pty Ltd, Австралия)[4–6].
Содержание металлопротеидов (трансферрина — ТФ, церулоплазмина — ЦП) в сыворотке крови пациенток изучали методом радиальной иммунодиффузии в агаровом геле по Манчини (1965) [18, 19]. Использовали антицерулоплазминовые (полученные В. В. Туркиным) и стандартные (Sevac, Прага) антитрансферриновые сыворотки[19]. Для оценки неферментативной антиоксидантной активности определяли коэффициент ТФ/ЦП. Металлоферменты ЦП и ТФ являются важными компонентами неспецифической защиты организма. Показана их клиническая значимость при вирусных заболеваниях[7], в том числе продемонстрирована роль коэффициента ТФ/ЦП: его повышение коррелирует с клиническим улучшением и, что важно, показывает степень восстановления иммунобиологической резистентности организма.
Для анализа субпопуляций иммунокомпетентных клеток периферической крови пациенток использовали метод непрямой иммунофлюоресценции с моноклональными антителами, полученными к дифференцировочным антигенам, локализованным на поверхности исследуемых клеток[17, 19]. Определяли уровни продукции ИФН-γ и ИФН-α/β (спонтанный и индуцированный) лейкоцитами периферической крови пациенток[6]. Содержание ИЛ-4 в сыворотке крови измеряли с помощью набора реагентов ProCon (ТОО «Протеиновый контур», Санкт-Петербург) методом твердофазного ИФА.
Схема терапии. Лечение проводили в два этапа. Сначала с помощью химической деструктивной терапии удаляли папилломатозные элементы: Солкодерм — 2 сеанса с интервалом 4–5 дней. На втором этапе у 50 пациенток проводили противорецидивный курс: инозин пранобекс — 2 таблетки 3 раза в день после еды в течение 10 дней. Одновременно на места бывших поражений наносили гель Алломедин 2–3 раза в день в течение 7–10 дней.
Для лечения использовали инозин пранобекс (Изопринозин, «ТЕВА», Израиль). Одна таблетка содержит 500 мг этого вещества. Химическая структура: комплекс инозина и диметиламино-2-пропанол р-ацетамидо-бензоата в соотношении 1 : 3. После приема препарата внутрь в дозе 1,5 г максимальная концентрация инозина достигается через час. Инозин пранобекс имеет широкий спектр действия. Он подавляет репликацию ДНК- и РНК-вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения, а также блокирует их репродукцию путем повреждения генетического аппарата. Оказывает иммуномодулирующее действие: стимулирует функции Т-лимфоцитов (в частности, Т-хелперов), NK-клеток. Увеличивает продукцию ИЛ, стимулирует фагоцитоз и синтез антител. Препарат обладает бифункциональными свойствами: доказанной противовирусной и иммуномодулирующей активностью.
Инозин пранобекс эффективен при лечении и профилактике вирусных инфекций у пациентов с нормальной и ослабленной иммунной системой: при гриппе и ОРВИ, кори, герпетической и цитомегаловирусной инфекции, инфицировании вирусом Эпштейна — Барр, ПВИ и др.[2, 3]. Дозу препарата определяют индивидуально в зависимости от характера течения и степени тяжести заболевания. Суточная доза составляет: взрослым — по 2 таблетки 3–4 раза в день; детям с 3 лет — 50–100 мг/кг в 3–4 приема. Курс лечения при ПВИ с учетом клинических проявлений — от 14 до 28 дней либо 3–4 повторных 10–14-дневных курса с интервалами 10 дней. Препарат применяется как в виде монотерапии, так и в комплексе с деструктивными методами с целью повышения их эффективности.
Математическую обработку полученных данных осуществляли с использованием компьютерных программ Excel (Microsoft Inc.), Statistica for Windows в версии 5.0 (StatSoft Inc., 1995) и с применением непарного двустороннего t-теста Стьюдента. Различия считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
В ходе исследования у пациенток второй группы (в том числе из слюны и в мазках из ротоглотки) ВПЧ-16 был выделен в 21 (52,5%) наблюдении, а ВПЧ-18 — в 11 (27,5%). Значительно реже — в пробах у 3 (7,5%) женщин — обнаруживали ВПЧ 31, 50, 59-го типов. ВПЧ-33 был обнаружен только у двух женщин. Следует отметить, что у 6 (15,0%) пациенток зарегистрировали несколько серотипов вируса одновременно: в двух пробах были выделены ВПЧ 16-го и 18-го типов, в трех — ВПЧ 16-го и 50-го типов, в одной пробе — ВПЧ 16, 31 и 39-го типов. У большинства пациенток ВПЧ выделяли в течение года[4, 8, 9]. Полученные данные указывают на существенную роль орально-генитальных контактов в распространении ПВИ, в том числе вирусов высокого канцерогенного риска, а также могут косвенно свидетельствовать о повышении риска развития злокачественных заболеваний полости рта и гортани у женщин, практикующих орально-генитальные контакты[4, 8].
По результатам ПЦР-анализа у 5 (10%) женщин основной группы не удалось установить генотип ВПЧ. У 45 пациенток при определении типа ВПЧ получили следующие результаты: 18 (40,0%) участниц имели ВПЧ-11; 5 (11,1%) — ВПЧ-16; 3 (6,7%) — ВПЧ-18; 19 (42,2%) — ВПЧ 2, 7, 31 и 33-го типов. Клинически регистрировали формы ПВИ: остроконечные кондиломы (по МКБ-10: А63.0 — аногенитальные (венерические) бородавки) у 22 женщин и плоские бородавки (по МКБ-10: В07 — вирусные бородавки) — у 28.
На фоне терапии инозином пранобекс после деструкции отмечено заживление раневой поверхности в течение 8,8 ± 0,6 дня. У пациенток первой группы также статистически значимо повышались показатели неспецифической резистентности организма — уровни CD4+, NK-клеток, ТФ, синтеза эндогенных ИФН (табл.). ВПЧ методом ПЦР через 30–35 дней после окончания курса лечения в этой группе выявляли статистически значимо реже: у 6 (12%) женщин против 45 (90%) пациенток перед началом лечения (р < 0,05). Использование инозина пранобекс в комплексной терапии ПВИ позволило снизить частоту рецидивов ПВИ с 49 до 14% в течение 6 месяцев после курса терапии.
Таблица
Иммунологические показатели у пациенток первой группы до и после лечения
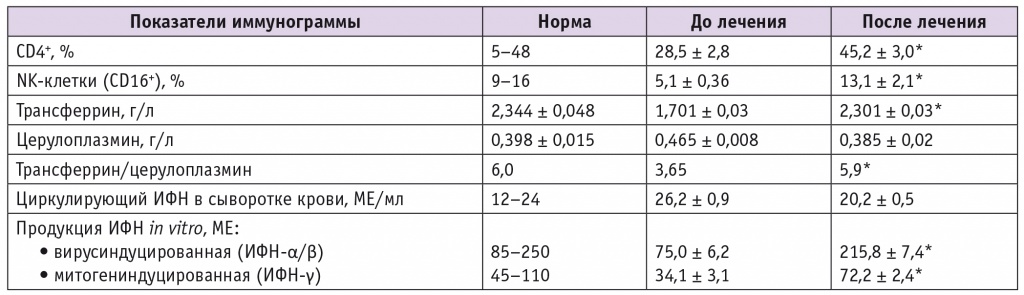
* Различия с показателями до лечения статистически значимы (р < 0,05).
Примечание: ИФН — интерферон.
ОБСУЖДЕНИЕ
Лечение больных с различными формами ПВИ не позволяет избежать рецидивов заболевания в 20–50% случаев[2, 4, 12, 20]. Поскольку полного излечения достичь трудно, считают, что целью терапии должна быть не элиминация возбудителя, а устойчивая ремиссия (клиническое выздоровление). В связи с этим предлагается разрушение папилломатозных очагов (деструктивные методы) с последующей противорецидивной терапией противовирусными (инозин пранобекс, индолкарбинол) и патогенетическими (системная энзимотерапия, антиоксиданты, про- и пребиотики) средствами[3, 4, 8, 12, 14].
Локальная деструкция очагов при клиническом и субклиническом течении ПВИ, направленная на удаление поверхностного слоя эпидермиса без санации клеток базального слоя, позволяет излечить только участок эпителия, где произошла манифестация инфекции. В окружающих тканях остается резервуар ВПЧ в неактивном состоянии или недиагностированной субклинической форме, который может быть причиной рецидивов болезни. В ходе пятилетнего наблюдения за пациентками с инфекционным поражением шейки матки, обусловленным ВПЧ, в 21,4% случаев нами отмечена прогрессия латентной стадии ПВИ в клиническую или субклиническую форму, причем клиническая манифестация инфекции происходила у женщин с персистенцией ВПЧ на фоне дисбаланса показателей иммунитета. Важно отметить, что в случае использования ВПЧ-тестирования в постоперационном мониторинге, в частности у пациенток с CIN2+, выявление вируса даже с низкой нагрузкой может быть ранним маркером рецидива[10]. Адекватная иммунотерапия инозином пранобекс способствует эрадикации ВПЧ из организма, снижая частоту рецидивов и уменьшая риск развития предраковых состояний и РШМ у пациенток с латентной ПВИ.
В литературе имеются данные об успешном применении инозина пранобекс при лечении остроконечных кондилом, генитального герпеса, ПВИ шейки матки, CIN и РШМ[3, 11, 13, 15]. Следует отметить, что доза препарата 50–100 мг/кг (взрослым по 2 таблетки 3–4 раза в день) является лечебной, а дозу 20–50 мг/кг (взрослым по 1 таблетке 2 раза в день) мы используем в течение 2–4 месяцев для профилактики рецидивов. При остроконечных кондиломах проводится лечение обоих партнеров. Рекомендуется воздерживаться от половых контактов в период приема лекарств и использовать барьерную контрацепцию в течение 6 месяцев после завершения терапии.
Известно, что ВПЧ угнетает синтез ИФН, а инфицирование вызывает слабый иммунный ответ[1, 12]. Доказано развитие иммунодефицитных состояний, обусловленных недостаточностью различных звеньев иммунной системы, поэтому для повышения эффективности комплексного лечения назначают ИФН и различные иммуномодуляторы[3, 8, 12, 15]. Однако ИФН-терапия не приводит к стойкой клинической ремиссии. Эффективность лечения напрямую зависит от уровня синтеза онкобелка Е7, который нейтрализует противовирусную активность ИФН, блокируя большинство генов, индуцируемых ИФН. Кроме того, Е7 внутриклеточно инактивирует фактор регуляции ИФН, включающий транскрипцию генов, кодирующих синтез противовирусных белков.
ЗАКЛЮЧЕНИЕ
Полученные результаты позволяют считать обоснованным и перспективным использование препарата инозин пранобекс в комплексной терапии пациентов с различными формами папилломавирусной инфекции (ПВИ) как в острый период болезни, так и для последующей продолжительной профилактики.
Приходится констатировать, что ни один из методов лечения ПВИ не является безупречным, так как при использовании любого из них возможно рецидивирование инфекционного процесса[8, 9, 15, 16]. По-видимому, в ряде случаев (при профилактике рака шейки матки) более эффективной может быть вакцинация. Однако придется найти ответы на многие вопросы, прежде чем новые технологии будут разработаны и внедрены в клиническую практику.








